文档内容
第6课时 必备知识——氧化还原反应的基本概念
[基本概念]①氧化还原反应;②氧化反应和还原反应;③氧化剂和还原剂;④
氧化性和还原性;⑤氧化产物和还原产物。
知识清单
[基本规律]①氧化还原反应中电子转移的表示;②氧化还原反应与四种基本
反应类型的关系
知识点1 氧化还原反应的概念
1.氧化还原反应的本质和特征
2.氧化还原反应的相关概念及其关系
上述关系概括为“升失氧、降得还,剂性一致、其他相反”。
一种元素由化合态变为游离态时,该元素可能被氧化,也可能被还原。例如,电
解的反应2HO=====2H↑+O↑中,氢元素被还原,氧元素被氧化。
2 2 2
3.氧化还原反应中电子转移的表示方法
双线桥法 单线桥法
表示
方法
①箭头指向反应前后有元素化合价变化的 ①箭头从失电子元素的原子指向
同种元素的原子,且需注明“得”或 得电子元素的原子。
注意
“失”。 ②不标“得到”或“失去”,只标
事项
②箭头的方向不代表电子转移的方向,仅表 明电子转移的总数。
示电子转移前后的变化。 ③线桥只出现在反应物中。应用
举例
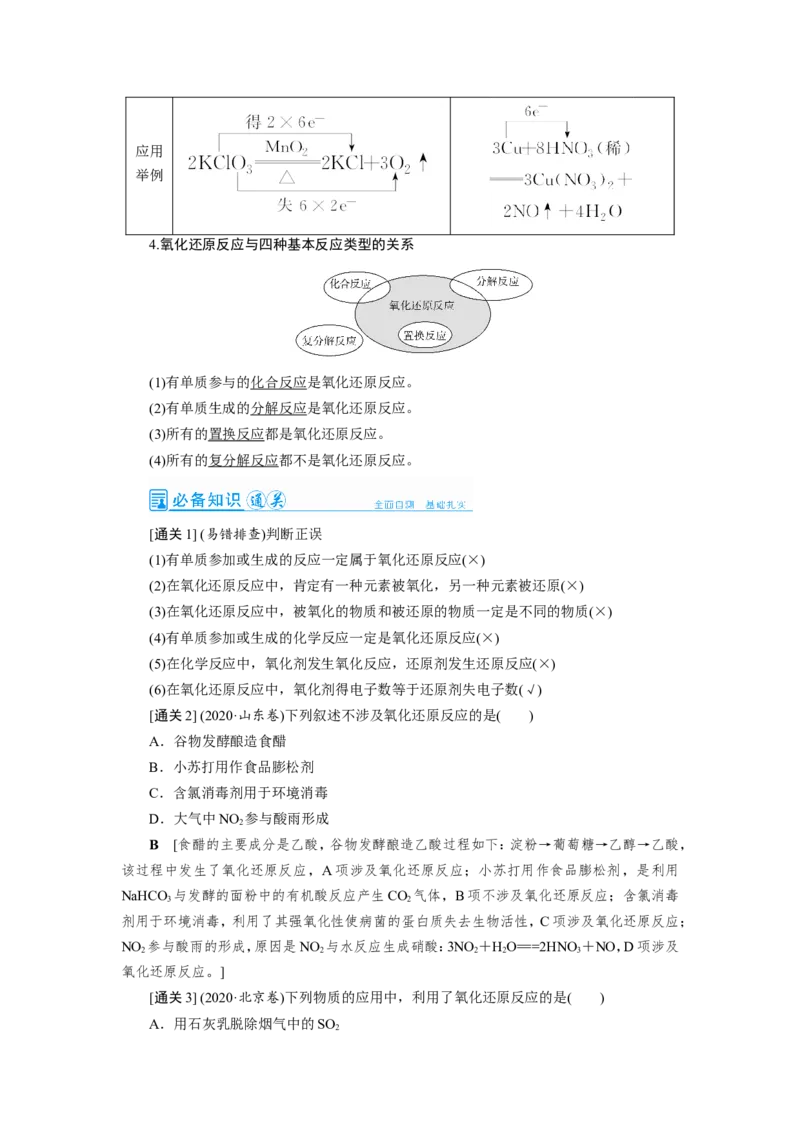
4.氧化还原反应与四种基本反应类型的关系
(1)有单质参与的化合反应是氧化还原反应。
(2)有单质生成的分解反应是氧化还原反应。
(3)所有的置换反应都是氧化还原反应。
(4)所有的复分解反应都不是氧化还原反应。
[通关1] (易错排查)判断正误
(1)有单质参加或生成的反应一定属于氧化还原反应(×)
(2)在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原(×)
(3)在氧化还原反应中,被氧化的物质和被还原的物质一定是不同的物质(×)
(4)有单质参加或生成的化学反应一定是氧化还原反应(×)
(5)在化学反应中,氧化剂发生氧化反应,还原剂发生还原反应(×)
(6)在氧化还原反应中,氧化剂得电子数等于还原剂失电子数(√)
[通关2] (2020·山东卷)下列叙述不涉及氧化还原反应的是( )
A.谷物发酵酿造食醋
B.小苏打用作食品膨松剂
C.含氯消毒剂用于环境消毒
D.大气中NO 参与酸雨形成
2
B [食醋的主要成分是乙酸,谷物发酵酿造乙酸过程如下:淀粉→葡萄糖→乙醇→乙酸,
该过程中发生了氧化还原反应,A项涉及氧化还原反应;小苏打用作食品膨松剂,是利用
NaHCO 与发酵的面粉中的有机酸反应产生CO 气体,B项不涉及氧化还原反应;含氯消毒
3 2
剂用于环境消毒,利用了其强氧化性使病菌的蛋白质失去生物活性,C项涉及氧化还原反应;
NO 参与酸雨的形成,原因是NO 与水反应生成硝酸:3NO +HO===2HNO +NO,D项涉及
2 2 2 2 3
氧化还原反应。]
[通关3] (2020·北京卷)下列物质的应用中,利用了氧化还原反应的是( )
A.用石灰乳脱除烟气中的SO
2B.用明矾[KAl(SO)·12H O]处理污水
4 2 2
C.用盐酸去除铁锈(主要成分Fe O·xHO)
2 3 2
D.用84消毒液(有效成分NaClO)杀灭细菌
D [SO 是酸性氧化物,可与碱反应,用石灰乳脱除烟气中的SO 时,SO 与氢氧化钙反
2 2 2
应生成亚硫酸钙或亚硫酸氢钙,不涉及氧化还原反应,A项错误;用明矾[KAl(SO )·12HO]
4 2 2
溶于水中,电离出的Al3+发生水解生成氢氧化铝胶体,利用胶体的吸附性可吸附污水中的固
体颗粒物,该过程利用胶体的吸附性,不涉及氧化还原反应,B项错误;用盐酸去除铁锈(主要
成分Fe O·xHO),发生的主要反应为:6HCl+Fe O===2FeCl +3HO,反应中没有元素化
2 3 2 2 3 3 2
合价的变化,不涉及氧化还原反应,C项错误;用84消毒液有效成分NaClO,具有强氧化性,
能使蛋白质发生变性从而杀死细菌病毒,杀菌消毒的过程利用了氧化还原反应,D项正确。]
[通关4] (2020.1·浙江选考)反应MnO +4HCl(浓)=====MnCl +Cl↑+2HO中,氧化产
2 2 2 2
物是( )
A.MnO B.HCl
2
C.MnCl D.Cl
2 2
D [该反应中,部分Cl元素由-1价升高到0价,则HCl发生氧化反应,生成的Cl 是氧
2
化产物。]
[通关5] (深度思考)实验室利用MnO 固体与浓盐酸加热制取Cl ,反应原理为MnO +
2 2 2
4HCl(浓)=====MnCl +Cl↑+2HO。
2 2 2
(1)该反应中,MnO 发生______________反应,HCl发生____________反应。
2
(2)生成1 mol Cl 时转移电子数目为__________,被氧化的HCl的物质的量是______
2
mol。
(3)该反应中,盐酸表现出的性质是__________性和________性。
(4)用双线桥法标出该反应电子转移的方向和数目:
________________________________________________________________________。
答案 (1)还原 氧化 (2)2N 2 (3)还原 酸
A
(4)MnO +4HCl(浓)=====M得2e-nCl+C失2×e-l↑+2HO
2 2 2 2知识点2 氧化剂和还原剂
1.氧化剂和还原剂
(1)常见的氧化剂
常见氧化剂包括某些非金属单质、含有高价态元素的化合物、过氧化物等。例如:
①在水溶液中,O 的还原产物与酸碱性有关,在酸性条件下是HO,在中性、碱
2 2
性条件下是OH-。
②硝酸与金属反应的还原产物与浓度有关,浓硝酸的还原产物是NO ,稀HNO 的还原
2 3
产物是NO。
(2)常见的还原剂
常见还原剂包括活泼的金属单质、非金属离子及低价态化合物、低价金属阳离子、非金
属单质及其氢化物等。例如:
单质铁的氧化产物与氧化剂的氧化能力有关,与Cl、Br 反应时氧化产物是Fe3
2 2
+,与S反应时氧化产物是Fe2+。
2.氧化性和还原性(1)氧化性
氧化剂在反应中表现出来的性质,是指氧化剂得到电子的性质(或能力)。例如,在反应
Fe+CuSO ===FeSO+Cu中,CuSO 作氧化剂,表现出氧化性。
4 4 4
(2)还原性
还原剂在反应中表现出来的性质,是指还原剂失去电子的性质(或能力)。例如,在反应
3Cu+8HNO(稀)===3Cu(NO )+2NO↑+4HO中,Cu 作还原剂,表现出还原性。
3 3 2 2
(3)性质与元素价态的关系
元素化合价处于中间价态的物质既有氧化性,又有还原性:
①同一种氧化剂(或还原剂)所对应的还原产物(或氧化产物)可能不同,与还原剂
(或氧化剂)的性质、反应条件、反应物的浓度、溶液的酸碱性等有关。例如,在酸性溶液中,
KMnO 的还原产物一般是Mn2+,而在中性或碱性溶液中,其还原产物一般是MnO 等。②物
4 2
质所含元素的化合价处于中间价态,既有氧化性又有还原性,但以其一为主。例如,Fe2+、SO
主要表现还原性,HO 主要表现氧化性。
2 2
[通关1] (易错排查)判断正误
(1)阳离子只有氧化性,阴离子只有还原性(×)
(2)在氧化还原反应中,一种物质是氧化剂,另一种物质必定是还原剂(×)
(3)在反应3NO +HO===2HNO +NO中,NO 既表现氧化性又表现还原性(√)
2 2 3 2
(4)(山东卷)2NaO+2HO===4NaOH+O↑、Cl+HO===HCl+HClO均为水作还原剂
2 2 2 2 2 2
的氧化还原反应(×)
(5)(2019·江苏卷)向3 mL KI溶液中滴加几滴溴水,振荡,再滴加1 mL 淀粉溶液,溶液显
蓝色,Br 的氧化性比I 的强(√)
2 2
(6)(2020·江苏卷)向0.1 mol·L-1 HO 溶液中滴加0.01 mol·L-1 KMnO 溶液,溶液褪色,
2 2 4
则HO 具有氧化性(×)
2 2
[通关2] (2020·北京卷)水与下列物质反应时,水表现出氧化性的是( )
A.Na B.Cl
2
C.NO D.NaO
2 2
A [Na与水反应生成NaOH和H,H元素被还原,HO作氧化剂,表现出氧化性,A项
2 2
正确;Cl、NO 与水反应时,HO既不是氧化剂又不是还原剂,B、C项均错误;NaO与水反应
2 2 2 2
生成NaOH,不是氧化还原反应,D项错误。][通关3] (2020.7·浙江选考)反应MnO +4HCl(浓)=====MnCl +Cl↑+2HO中,氧化产
2 2 2 2
物与还原产物的物质的量之比是( )
A.1∶2 B.1∶1
C.2∶1 D.4∶1
B [Cl 是氧化产物,MnCl 为还原产物,二者物质的量之比为1∶1,B项正确。]
2 2
[通关4] (新教材链接)(人教必修第一册,9题改编)氢化钠(NaH)可在野外用作生氢剂,其
中氢元素为-1价。NaH用作生氢剂时的化学反应原理为:NaH+HO===NaOH+H↑。下列
2 2
有关该反应的说法中,正确的是( )
A.该反应属于置换反应
B.该反应中,NaH表现氧化性
C.该反应中,HO发生氧化反应
2
D.该反应中,H 既是氧化产物又是还原产物
2
D [H O中+1价H元素化合价降低,NaH中-1价H元素化合价升高,H 既是氧化产
2 2
物又是还原产物,D项正确;NaH作还原剂,表现还原性,B项正确;HO作氧化剂,发生还原
2
反应,C项错误。]
[通关5] (深度思考)氧化还原是一类重要的反应,在工农业生产、日常生活中有着广泛的
应用。
(1)火药是中国的四大发明之一,黑火药在发生爆炸时,发生反应:2KNO +3C+
3
S===K S+N↑+3CO↑,其中被氧化的元素是________,氧化剂是__________。
2 2 2
(2)用FeCl 溶液腐蚀印刷铜质线路板的反应为Cu+2Fe3+===Cu2++2Fe2+,该反应中还
3
原剂是________,氧化性:Fe3+________Cu2+(填“<”或“>”)。
(3)过氧化钠常用作呼吸面具里的供氧剂,发生反应2NaO+2CO===2Na CO+O,该
2 2 2 2 3 2
反应中,氧化剂与还原剂的物质的量之比为__________,若转移3 mol电子,则所产生的氧气
在标准状况下的体积为______L。
(4)在xR2++yH++O===mR3++nHO的离子方程式中,对系数m和R2+、R3+判断正确
2 2
的是________。
A.m=y,R3+是还原剂 B.m=2y,R2+被氧化
C.m=2,R3+是氧化剂 D.m=4,R2+是还原剂
解析 (2)已知反应中Cu化合价升高,被氧化,为还原剂,由反应可知氧化性:Fe3+>Cu2
+。(3)在已知反应中,只有NaO 中O元素的化合价发生变化,分别由-1价变化为0价和-2
2 2
价,所以2 mol Na O 发生反应转移电子数为2e-,则转移3 mol电子,有3 mol Na O 发生反
2 2 2 2
应,产生的氧气为1.5 mol,标况下体积为1.5 mol×22.4 L·mol-1=33.6 L。(4)根据氧原子守恒
可得,n=2;根据氢原子守恒可得,y=4;根据R原子守恒可得,x=m;根据电荷守恒则2x+y
=3m,则x=y=m。在反应中,R的化合价升高,R2+是还原剂,所以R3+是氧化产物,氧元素
化合价降低,则HO是还原产物。
2
答案 (1)C(或碳) KNO、S (2)Cu > (3)1∶1 33.6 (4)D
3训练(九) 氧化还原反应的基本概念
1.(2020·北京房山区二模)下列水处理方法涉及氧化还原反应的是( )
A.用明矾处理水中的悬浮物
B.用NaS处理水中的Cu2+、Hg2+等重金属离子
2
C.用FeSO 处理含Cr O的酸性废水,再调节pH除去Cr3+
4 2
D.用NaOH处理含高浓度NH的废水并回收利用氨
C [用明矾处理水中的悬浮物,Al3+发生水解生成Al(OH) 胶体,不涉及氧化还原反应,
3
A项错误;用NaS处理水中Cu2+、Hg2+等重金属离子,产生CuS、HgS等沉淀,不涉及氧化还
2
原反应,B项错误;用FeSO 处理含Cr O的酸性废水,调节pH除去Cr3+,说明Cr O被还原
4 2 2
为Cr3+,Fe2+被氧化为Fe3+,C项正确;用NaOH处理含高浓度NH的废水并回收利用氨,发
生反应:NH+OH-===NH↑+HO,不涉及氧化还原反应,D项错误。]
3 2
2.(2021·湖南浏阳六校联考)下列反应中,水只作氧化剂的是( )
①氟气通入水中 ②水蒸气通过灼热的焦炭 ③钠块投入水中 ④铁与水蒸气反应
⑤氯气通入水中
A.只有①④ B.只有①⑤
C.只有②③ D.只有②③④
D [①F 与水反应生成HF和O,HO作还原剂,被氧化生成O;②水蒸气与灼热焦炭
2 2 2 2
反应生成H 和CO,HO作氧化剂,被还原生成H;③Na与水反应生成NaOH和H,HO作
2 2 2 2 2氧化剂,被还原生成H;④Fe与水蒸气反应生成Fe O 和H,HO作氧化剂,被还原生成H;
2 3 4 2 2 2
⑤Cl 与水反应生成HCl和HClO,HO既不是氧化剂又不是还原剂。]
2 2
3.(2021·北京朝阳区一模)下列物质的用途与其体现的性质对应关系不合理的是( )
物质 用途 体现的性质
A SO 生产硫酸 还原性
2
B NH 生产碳酸氢铵 还原性
3
C SiO 制取硅单质 氧化性
2
D Fe O 冶炼金属铁 氧化性
2 3
B [SO 被氧化为SO ,SO 与水化合生成HSO ,体现SO 的还原性,A项正确;NH 生
2 3 3 2 4 2 3
产NH HCO 过程中,发生非氧化还原反应,B项错误;利用焦炭还原SiO 制得粗硅,体现
4 3 2
SiO 的氧化性,C项正确;冶炼金属铁时,Fe O 被还原为Fe,体现Fe O 的氧化性,D项正
2 2 3 2 3
确。]
4.(2021·北京第八中学一模)下列变化中,气体反应物既被氧化又被还原的是( )
A.金属钠露置在空气中迅速变暗
B.充满二氧化氮的试管倒扣在水槽中,试管内液面上升
C.露置在空气中的过氧化钠固体变白
D.将氨气与氯化氢混合,产生大量白烟
B [钠露置在空气中迅速变暗,Na与O 反应生成NaO,O 被还原,A项错误;充满NO
2 2 2 2
的试管倒扣在水槽中,发生反应:3NO +HO===2HNO +NO,N元素由+4价变为+5价和
2 2 3
+2价,则NO 既被氧化又被还原,B项正确;露置在空气中的NaO 固体变白,是由于吸收
2 2 2
了空气中CO 和HO(g),NaO 既是氧化剂又是还原剂,则气体既不被氧化又不被还原,C项
2 2 2 2
错误;NH 和HCl混合发生反应生成NH Cl固体,产生大量白烟,该反应是非氧化还原反应,
3 4
D项错误。]
5.(2021·广东韶关一模)在酸性介质中,往MnSO 溶液中滴加(NH )SO(过二硫酸铵)溶
4 4 2 2 8
液会发生反应:Mn2++SO+HO―→ MnO+SO+H+。下列说法不正确的是( )
2 2
A.可以利用该反应检验Mn2+
B.氧化性:SO > MnO
2
C.该反应可用盐酸作为酸性介质
D.若有0.1 mol氧化产物生成,则转移0.5 mol电子
C [酸性条件下,Mn2+能被SO氧化生成MnO,溶液由无色变为紫红色,故可以用该反
2
应检验Mn2+,A项正确;该反应中,SO为氧化剂,Mn2+为还原剂,MnO为氧化产物,氧化剂
2
的氧化性大于氧化产物的氧化性,则氧化性比较:SO>MnO,B项正确;盐酸为强还原性酸,
2
能被SO氧化生成氯气,故不能用盐酸作酸性介质,C项错误;MnO是氧化产物,Mn元素由
2
+2价升高到+7价,故有0.1 mol氧化产物生成,则转移电子为0.5 mol,D项正确。]
6.(2021·北京海淀区一模)I-具有还原性,含碘食盐中的碘元素主要以KIO 的形式存在,
3I-、I、IO在一定条件下可发生如图转化关系。下列说法不正确的是( )
2
A.用淀粉KI试纸和食醋可检验食盐是否加碘
B.由图可知氧化性的强弱顺序为Cl>IO>I
2 2
C.生产等量的碘,途径Ⅰ和途径Ⅱ转移电子数目之比为5∶2
D.途径Ⅲ反应的离子方程式:3Cl
2
+I-+3H
2
O⇌6Cl-+IO+6H+
C [加碘食盐中含KIO ,在酸性条件下可与I-发生氧化还原反应生成I,淀粉遇I 显蓝
3 2 2
色,A项正确。I-被适量Cl 氧化成I,被足量Cl 氧化成IO,则氧化性:Cl>I,Cl>IO;途径
2 2 2 2 2 2
Ⅱ中IO被NaHSO 还原为I,IO是氧化剂,则氧化性:IO>I ,故氧化性:Cl>IO>I ,B项正确。
3 2 2 2 2
生产1 mol I ,途径Ⅰ转移2 mol电子,途径Ⅱ转移10 mol电子,则途径Ⅰ和途径Ⅱ转移电子
2
数目之比为 2∶5,C项错误。途径Ⅲ中I-被足量Cl 氧化生成 IO,反应为3Cl +I-+
2 2
3H
2
O⇌6Cl-+IO+6H+,D项正确。]
7.(2021·广东湛江调研)将SO 分别通入无氧、有氧的浓度均为0.1 mol·L-1的 BaCl 溶
2 2
液和Ba(NO ) 溶液中进行四组实验,探究体系中微粒间的相互作用,测得溶液pH变化如图
3 2
所示。实验现象中观察到:实验a中不产生白色沉淀;实验b、c、d中均产生白色沉淀。下列说
法中不正确的是( )
A.实验a中溶液pH降低的原因是SO 与HO反应生成HSO
2 2 2 3
B.实验a和c相比,实验c所表示的过程中O 是氧化SO 的主要微粒
2 2
C.与实验a、b、c相比,可知实验d所表示的过程中NO是氧化SO 的主要微粒
2
D.依据该实验预测0.2 mol·L-1的KNO 溶液(无氧)也可以氧化SO
3 2
C [实验a中SO 通入BaCl 溶液(无氧),无较强的氧化性物质存在,不发生氧化还原反
2 2
应,溶液pH降低的原因是SO 与HO反应生成HSO ,A项正确;实验a和c相比,c中BaCl
2 2 2 3 2
溶液有氧,溶液的pH变化较大,且所需时间短,说明实验c所表示的过程中O 将SO 氧化生
2 2
成HSO ,B项正确;实验d与c相比,都有氧环境,两溶液的pH变化相差较小,不能说明实
2 4
验d过程中NO将SO 氧化,C项错误;对比实验a和b,在无氧条件下,实验b中溶液pH变
2
化比a大,且变化快,说明NO能氧化SO ,D项正确。]
2
8.(2021·河北武邑模拟)锑(Sb)广泛用于生产各种阻燃剂、陶瓷、半导体元件、医药等。以
辉锑矿为原料制备金属锑,其一种工艺流程如下:已知部分信息如下:
①辉锑矿(主要成分为Sb S,还含有As S、PbS、CuO和SiO 等);
2 3 2 5 2
②浸出液主要含盐酸和SbCl ,还含SbCl 、CuCl 、AsCl 和PbCl 等杂质;
3 5 2 3 2
③常温下,K (CuS)=1.0×10-36,K (PbS)=9.0×10-29。
sp sp
回答下列问题:
(1)NaH PO 中P的化合价为________。
2 2
(2)“酸浸”过程中SbCl 和Sb S 反应有S生成,该反应的还原产物是____________(填
5 2 3
化学式)。
(3)写出“还原”反应的化学方程式,并用双线桥标出电子转移的方向和数目:
________________________________________________________________________
________________________________________________________________________。
(4)已知:浸出液中c(Cu2+)=0.01 mol·L-1、c(Pb2+)=0.1 mol·L-1。在沉淀铜、铅过程中,
缓慢滴加极稀的NaS溶液,先产生的沉淀是_________(填化学式)。
2
(5)在“除砷”过程中,氧化产物为HPO 。该反应中氧化剂与还原剂的物质的量之比为
3 4
________ 。 常 温 下 , SbCl 溶 液 的 pH<7 , 用 离 子 方 程 式 表 示 其 原 因 :
3
________________________________________________________________________
________________________________________________________________________。
解析 (1)NaH PO 中,Na和H元素显+1价,O元素显-2价,根据化合物中各元素的
2 2
代数和为0可得,P元素的化合价为+1。
(2)“酸浸”过程中SbCl 和Sb S 反应有S生成,结合信息②“浸出液主要含盐酸和
5 2 3
SbCl ,还含SbCl 、CuCl 、AsCl 和PbCl 等杂质”推知,该反应的还原产物是SbCl 。
5 3 2 3 2 3
(3)浸出液主要含盐酸和SbCl ,“还原”过程中加入适量Sb,与SbCl 发生氧化还原反
5 5
应生成SbCl ,化学方程式为3SbCl +2Sb===5SbCl 。
3 5 3
(4)浸出液中c(Cu2+)=0.01 mol·L-1、c(Pb2+)=0.1 mol·L-1,Cu2+开始沉淀时,c(S2-)=
K (CuS)/c(Cu2+)=(1.0×10-36)/ 0.01 mol·L-1=1.0×10-34 mol·L-1;Pb2+开始沉淀时,c(S2-)
sp
=K (PbS)/c(Pb2+)=(9.0×10-29)/ 0.1 mol·L-1=9.0×10-28 mol·L-1,显然Cu2+优于Pb2+先沉
sp
淀,故先产生的沉淀是CuS。
(5)“除砷”过程中,加入NaH PO ,氧化产物为HPO ,同时生成As,其中P元素由+1
2 2 3 4
价升高到+5价,As元素由+3价降低到0价,则AsCl 是氧化剂,NaH PO 是还原剂,据得失
3 2 2
电子守恒可知,氧化剂与还原剂的物质的量之比为4∶3。SbCl 是强酸弱碱盐,常温下SbCl
3 3
溶液的pH<7,其原因是Sb3+发生水解反应:Sb3++3H
2
O⇌Sb(OH)
3
+3H+。答案 (1)+1 (2)SbCl
3
(3)3SbCl +2Sb===5S得3×2e-失2×3e-bCl (4)CuS
5 3
(5)4∶3 Sb3++3H
2
O⇌Sb(OH)
3
+3H+