文档内容
第 6 讲 钠及其化合物
【练基础】
1.氯化钾灼烧时火焰呈
A.红色 B.紫色 C.绿色 D.黄色
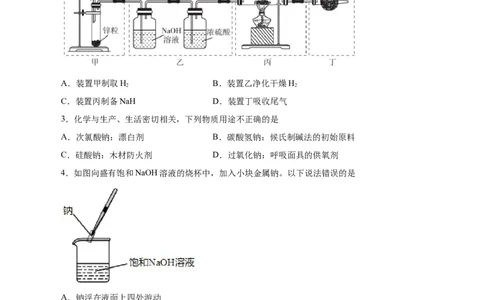
2.实验室用Na与H 反应制备氢化钠(NaH)。下列实验装置和原理不能达到实验目的的是
2
A.装置甲制取H B.装置乙净化干燥H
2 2
C.装置丙制备NaH D.装置丁吸收尾气
3.化学与生产、生活密切相关,下列物质用途不正确的是
A.次氯酸钠:漂白剂 B.碳酸氢钠:候氏制碱法的初始原料
C.硅酸钠:木材防火剂 D.过氧化钠:呼吸面具的供氧剂
4.如图向盛有饱和NaOH溶液的烧杯中,加入小块金属钠。以下说法错误的是
A.钠浮在液面上四处游动
B.钠熔化成一个光亮的小球
C.恢复到室温时,溶液中的Na+数目减小
D.恢复到室温时,NaOH溶液的浓度增大
5.化学与生产、生活密切相关。下列关于物质用途的说法错误的是
A.NH C1溶液用作除锈剂 B.还原铁粉用作抗氧化剂
4
C.NaHCO 用作糕点膨松剂 D.干冰用作Na着火时的灭火剂
3
6.不能正确表示下列反应的离子方程式是 ( )A.钠与水反应:2Na+2HO=2Na++2OH-+H↑
2 2
B.钠与CuSO 溶液反应:2Na+Cu2+=Cu+2Na+
4
C.钠与盐酸反应:2Na+2H+=2Na++H↑
2
D.钠与氯化钾溶液反应:2Na+2HO=2Na++2OH-+H↑
2 2
7.测定一定质量小苏打中NaHCO 的含量(杂质为NaCl),下列实验方案不可行的是
3
A.加热至恒重,称量剩余固体质量
B.加入足量稀硫酸,测定生成气体的体积
C.溶解后以甲基橙为指示剂,用标准盐酸溶液滴定
D.溶解后加入足量CaCl 溶液,过滤、洗涤、干燥后称量沉淀质量
2
8.中国科学家以二氧化碳为碳源,在470℃、80Mpa下与金属钠反应合成出金刚石。下列说法不正确
的是
A.金属钠在反应中作还原剂
B.反应中生成的氧化产物为NaO
2 2
C.二氧化碳转变为金刚石发生的是还原反应
D.钠被氧化最终生成碳酸钠
【练提升】
9.下列对焰色试验的实验操作注意事项的说法正确的是
①钾的焰色要透过蓝色钴玻璃观察
②先将铂丝灼烧至无色,再蘸取被检验的物质
③每次实验后,要将铂丝用稀盐酸洗净
④实验时最好选择本身颜色较浅的火焰
⑤没有铂丝时,也可以用光洁无锈的铁丝代替
A.①②④⑤ B.①②③⑤ C.①②③④ D.①②③④⑤
10.在无色溶液中加入适量过氧化钠后仍能大量共存的离子组是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
11.将金属钠放入盛有下列溶液的小烧杯中,既有气体产生,又有白色沉淀产生的是(不考虑溶液温度
变化)( )
①MgSO 溶液②稀NaSO 溶液③饱和澄清石灰水④CuSO 溶液⑤饱和NaCl溶液⑥FeCl 溶液
4 2 4 4 3
A.①④⑥ B.②④⑤ C.③④⑥ D.①③⑤12.下列说法正确的是
A.向NaCO 溶液中通入CO 一定析出NaHCO 晶体
2 3 2 3
B.用饱和NaCO 溶液除去CO 气体中的HCl气体
2 3 2
C.等质量的NaCO 和NaHCO 分别与足量稀盐酸反应,后者放出CO 多
2 3 3 2
D.等质量的NaCO 和NaHCO 分别与足量稀盐酸反应,后者消耗盐酸多
2 3 3
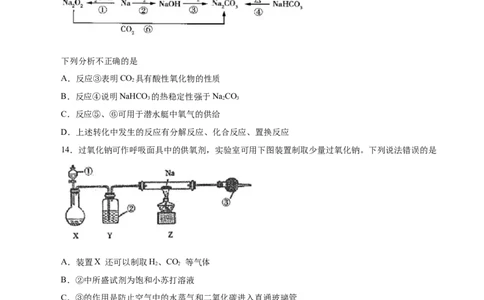
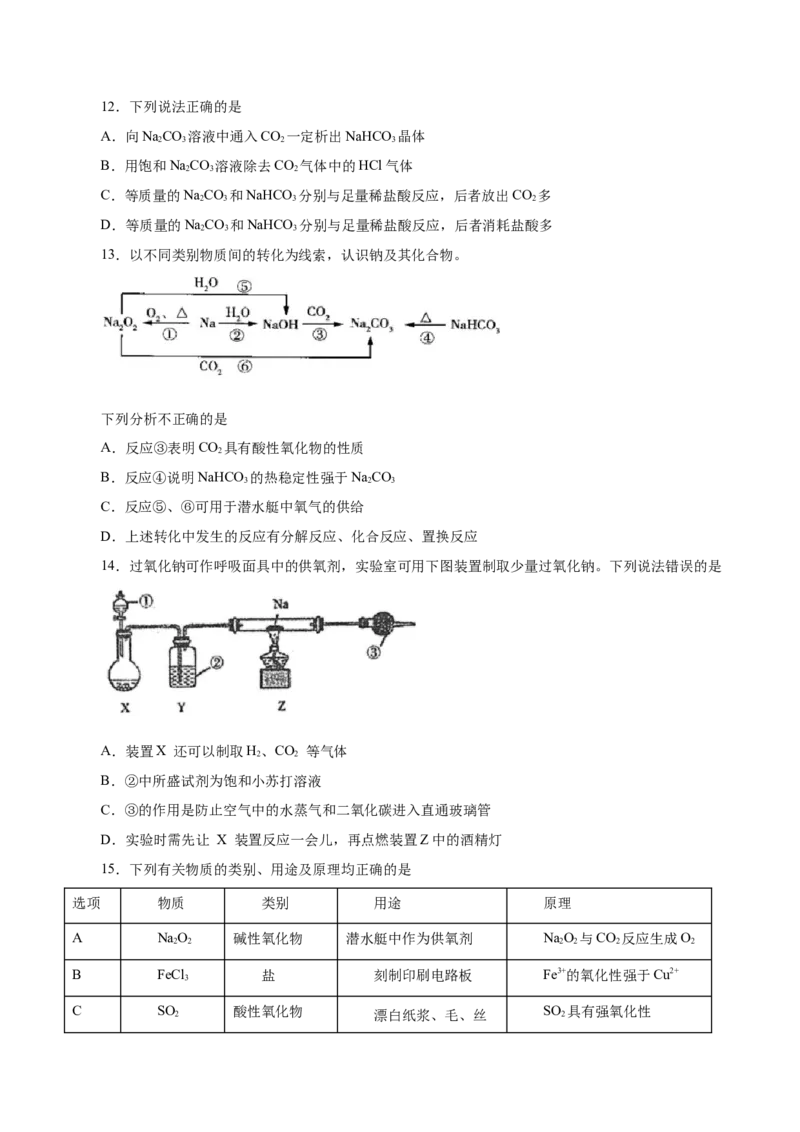
13.以不同类别物质间的转化为线索,认识钠及其化合物。
下列分析不正确的是
A.反应③表明CO 具有酸性氧化物的性质
2
B.反应④说明NaHCO 的热稳定性强于NaCO
3 2 3
C.反应⑤、⑥可用于潜水艇中氧气的供给
D.上述转化中发生的反应有分解反应、化合反应、置换反应
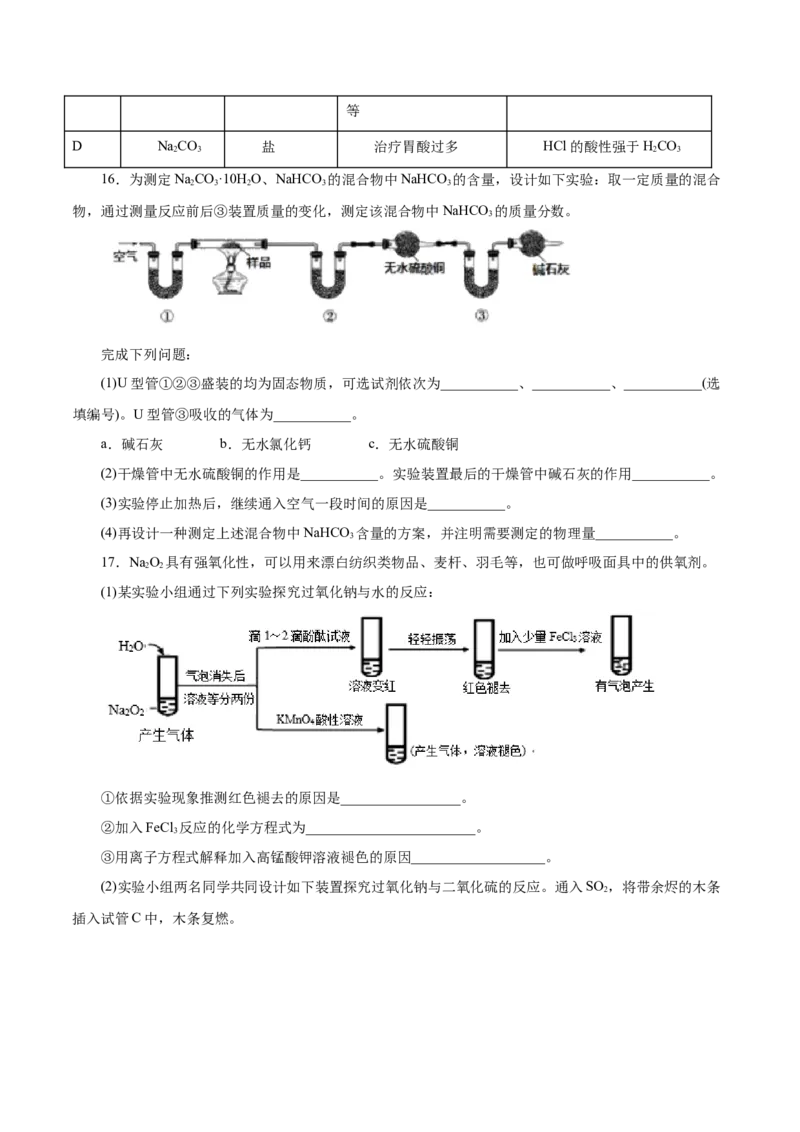
14.过氧化钠可作呼吸面具中的供氧剂,实验室可用下图装置制取少量过氧化钠。下列说法错误的是
A.装置X 还可以制取H、CO 等气体
2 2
B.②中所盛试剂为饱和小苏打溶液
C.③的作用是防止空气中的水蒸气和二氧化碳进入直通玻璃管
D.实验时需先让 X 装置反应一会儿,再点燃装置Z中的酒精灯
15.下列有关物质的类别、用途及原理均正确的是
选项 物质 类别 用途 原理
A NaO 碱性氧化物 潜水艇中作为供氧剂 NaO 与CO 反应生成O
2 2 2 2 2 2
B FeCl 盐 刻制印刷电路板 Fe3+的氧化性强于Cu2+
3
C SO 2 酸性氧化物 漂白纸浆、毛、丝 SO 2 具有强氧化性等
D NaCO 盐 治疗胃酸过多 HCl的酸性强于HCO
2 3 2 3
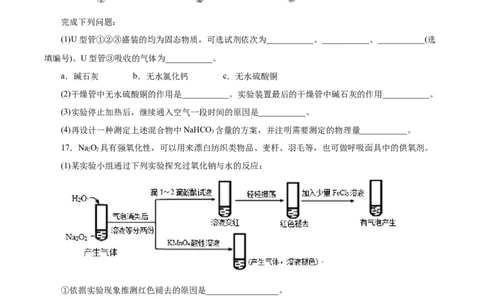
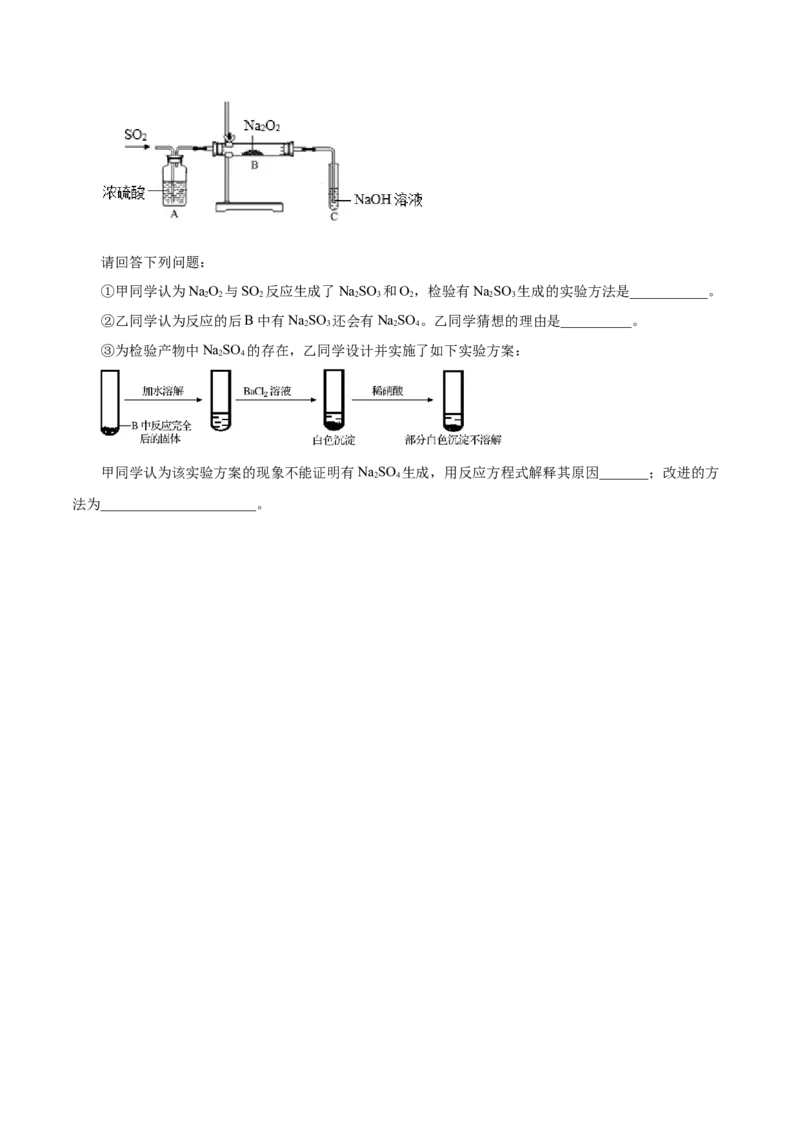
16.为测定NaCO·10H O、NaHCO 的混合物中NaHCO 的含量,设计如下实验:取一定质量的混合
2 3 2 3 3
物,通过测量反应前后③装置质量的变化,测定该混合物中NaHCO 的质量分数。
3
完成下列问题:
(1)U型管①②③盛装的均为固态物质,可选试剂依次为___________、___________、___________(选
填编号)。U型管③吸收的气体为___________。
a.碱石灰 b.无水氯化钙 c.无水硫酸铜
(2)干燥管中无水硫酸铜的作用是___________。实验装置最后的干燥管中碱石灰的作用___________。
(3)实验停止加热后,继续通入空气一段时间的原因是___________。
(4)再设计一种测定上述混合物中NaHCO 含量的方案,并注明需要测定的物理量___________。
3
17.NaO 具有强氧化性,可以用来漂白纺织类物品、麦杆、羽毛等,也可做呼吸面具中的供氧剂。
2 2
(1)某实验小组通过下列实验探究过氧化钠与水的反应:
①依据实验现象推测红色褪去的原因是_________________。
②加入FeCl 反应的化学方程式为________________________。
3
③用离子方程式解释加入高锰酸钾溶液褪色的原因___________________。
(2)实验小组两名同学共同设计如下装置探究过氧化钠与二氧化硫的反应。通入SO ,将带余烬的木条
2
插入试管C中,木条复燃。请回答下列问题:
①甲同学认为NaO 与SO 反应生成了NaSO 和O,检验有NaSO 生成的实验方法是___________。
2 2 2 2 3 2 2 3
②乙同学认为反应的后B中有NaSO 还会有NaSO 。乙同学猜想的理由是__________。
2 3 2 4
③为检验产物中NaSO 的存在,乙同学设计并实施了如下实验方案:
2 4
甲同学认为该实验方案的现象不能证明有NaSO 生成,用反应方程式解释其原因_______;改进的方
2 4
法为______________________。