文档内容
第八、九讲 钠及其化合物、焰色反应
【基础巩固】
1.(2022·全国·统考高考真题)生活中处处有化学,下列叙述正确的是
A.HB铅笔芯的成分为二氧化铅 B.碳酸氢钠可做食品膨松剂
C.青铜和黄铜是不同结构的单质铜 D.焰火中红色来源于钠盐灼烧
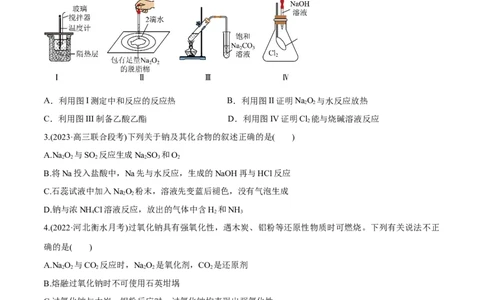
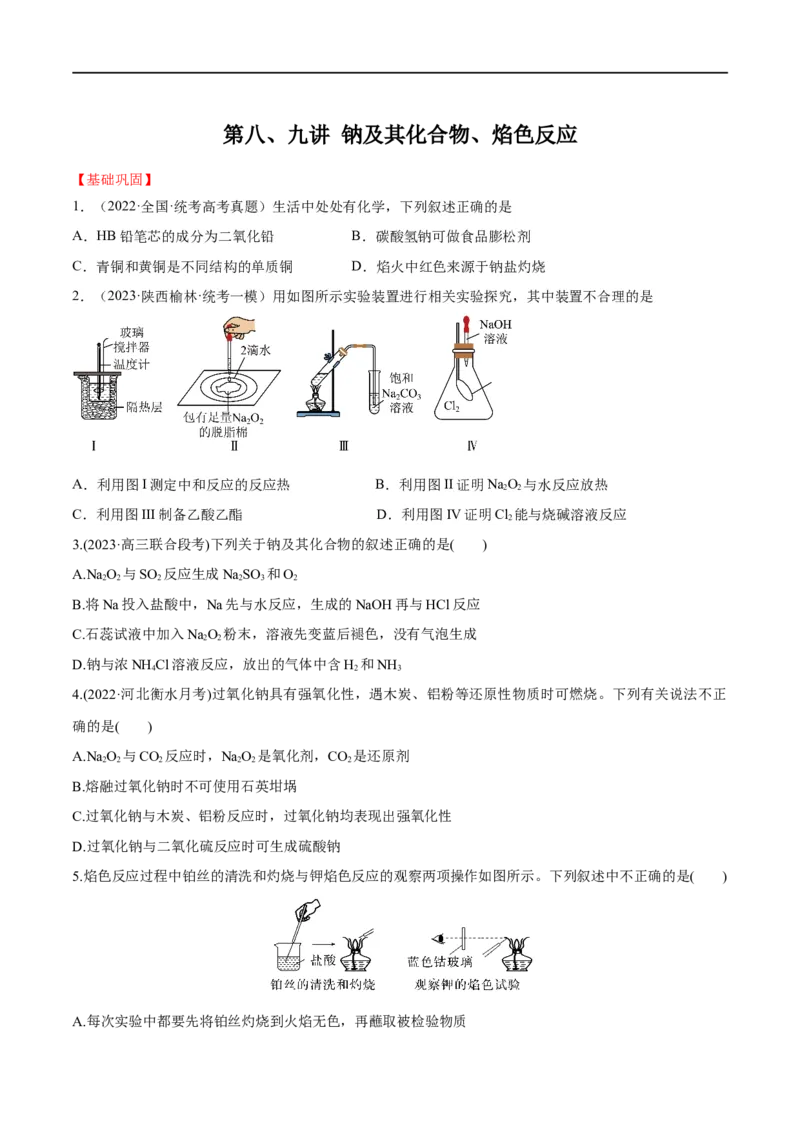
2.(2023·陕西榆林·统考一模)用如图所示实验装置进行相关实验探究,其中装置不合理的是
A.利用图I测定中和反应的反应热 B.利用图II证明NaO 与水反应放热
2 2
C.利用图III制备乙酸乙酯 D.利用图IV证明Cl 能与烧碱溶液反应
2
3.(2023·高三联合段考)下列关于钠及其化合物的叙述正确的是( )
A.Na O 与SO 反应生成NaSO 和O
2 2 2 2 3 2
B.将Na投入盐酸中,Na先与水反应,生成的NaOH再与HCl反应
C.石蕊试液中加入NaO 粉末,溶液先变蓝后褪色,没有气泡生成
2 2
D.钠与浓NH Cl溶液反应,放出的气体中含H 和NH
4 2 3
4.(2022·河北衡水月考)过氧化钠具有强氧化性,遇木炭、铝粉等还原性物质时可燃烧。下列有关说法不正
确的是( )
A.Na O 与CO 反应时,NaO 是氧化剂,CO 是还原剂
2 2 2 2 2 2
B.熔融过氧化钠时不可使用石英坩埚
C.过氧化钠与木炭、铝粉反应时,过氧化钠均表现出强氧化性
D.过氧化钠与二氧化硫反应时可生成硫酸钠
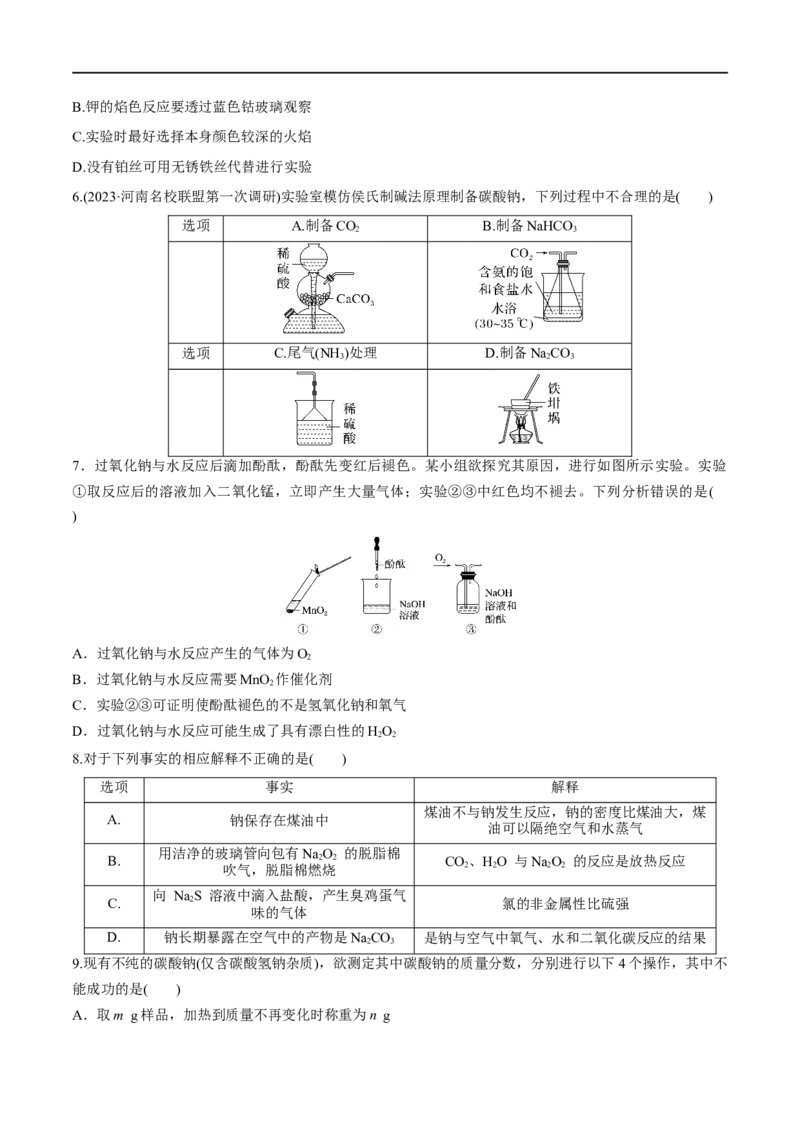
5.焰色反应过程中铂丝的清洗和灼烧与钾焰色反应的观察两项操作如图所示。下列叙述中不正确的是( )
A.每次实验中都要先将铂丝灼烧到火焰无色,再蘸取被检验物质B.钾的焰色反应要透过蓝色钴玻璃观察
C.实验时最好选择本身颜色较深的火焰
D.没有铂丝可用无锈铁丝代替进行实验
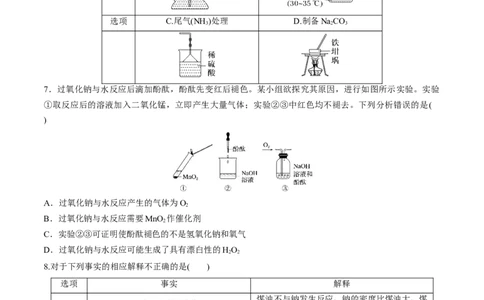
6.(2023·河南名校联盟第一次调研)实验室模仿侯氏制碱法原理制备碳酸钠,下列过程中不合理的是( )
选项 A.制备CO B.制备NaHCO
2 3
选项 C.尾气(NH )处理 D.制备NaCO
3 2 3
7.过氧化钠与水反应后滴加酚酞,酚酞先变红后褪色。某小组欲探究其原因,进行如图所示实验。实验
①取反应后的溶液加入二氧化锰,立即产生大量气体;实验②③中红色均不褪去。下列分析错误的是(
)
A.过氧化钠与水反应产生的气体为O
2
B.过氧化钠与水反应需要MnO 作催化剂
2
C.实验②③可证明使酚酞褪色的不是氢氧化钠和氧气
D.过氧化钠与水反应可能生成了具有漂白性的HO
2 2
8.对于下列事实的相应解释不正确的是( )
选项 事实 解释
煤油不与钠发生反应,钠的密度比煤油大,煤
A. 钠保存在煤油中
油可以隔绝空气和水蒸气
用洁净的玻璃管向包有NaO 的脱脂棉
B. 2 2 CO、HO 与NaO 的反应是放热反应
吹气,脱脂棉燃烧 2 2 2 2
向 NaS 溶液中滴入盐酸,产生臭鸡蛋气
C. 2 氯的非金属性比硫强
味的气体
D. 钠长期暴露在空气中的产物是NaCO 是钠与空气中氧气、水和二氧化碳反应的结果
2 3
9.现有不纯的碳酸钠(仅含碳酸氢钠杂质),欲测定其中碳酸钠的质量分数,分别进行以下4个操作,其中不
能成功的是( )
A.取m g样品,加热到质量不再变化时称重为n gB.取m g样品,加入过量的稀盐酸,再将所得溶液加热蒸发、结晶、灼烧,余下物质质量为n g
C.取m g样品,溶于水,向所得溶液中加入过量的CaCl 溶液,将所得沉淀过滤、洗涤、烘干后称重为n
2
g
D.取m g样品,加入过量的稀硫酸,再将所逸出的气体用碱石灰吸收,碱石灰增重n g
10.(2023春·河南洛阳·高三孟津县第一高级中学校考阶段练习)元素的价类二维图是我们学习元素及其化
合物、化合价相关知识的重要模型和工具,如图为铁元素的价类二维图,图中甲至庚均含铁元素。下列说
法正确的是( )
A.在空气中加热丁,可实现丁→乙的转化
B.甲高温下与水蒸气的反应可实现甲乙的转化
C.己溶液是否含有Fe2+,不能选用KSCN和新制的氯水检验
D.高铁酸根离子(FeO 2-)具有氧化性,可用于消毒,FeO2-与水反应最终可生成胶体,还可用作净水剂
4 4
11.某小组通过实验探究NaHCO 和NaCO 的性质。
3 2 3
实验一:探究NaHCO 和NaCO 的溶解性和水溶液的酸碱性。
3 2 3
观察到的实验现象
步骤 实验操作
NaCO NaHCO
2 3 3
在2支试管里分别加入1 g NaHCO 和NaCO, 全部溶解,得到透 部分溶解,试管底部
① 3 2 3
各加入10 mL水,振荡 明溶液 有少许固体
将步骤①的试管中溶液分别分成两份,其中1份
② 溶液变红色 溶液变浅红色
溶液中各滴加2滴酚酞溶液
在步骤②的另两份溶液中各滴加2滴10%盐酸,
③ 没有气泡产生 产生少量气泡
振荡
根据上述实验现象,回答下列问题:
(1)常温下,NaHCO 的溶解度________(填“大于”“小于”或“等于”) Na CO 的溶解度。
3 2 3
(2)下列推断正确的是________(填字母)。
A.碳酸钠溶液呈碱性,碳酸氢钠溶液呈酸性
B.碳酸钠溶液、碳酸氢钠溶液都呈碱性
C.碳酸钠溶液、碳酸氢钠溶液都呈酸性
D.碳酸钠溶液呈碱性,碳酸氢钠溶液呈中性
(3)Na CO 溶液和少量盐酸反应生成NaHCO ,离子方程式为___________________________________。
2 3 3实验二:探究NaHCO 和NaCO 的热稳定性。
3 2 3
观察到的实验现象如下表所示:
物质 装置B中现象 装置C中现象
NaCO 无明显变化 开始断断续续产生气泡,一会儿后,没有气泡,溶液保持澄清
2 3
NaHCO 白色粉末变蓝色 开始断断续续产生气泡,一会儿后,产生连续气泡,溶液变浑浊
3
根据上述实验现象,回答下列问题:
(4) 加 热 NaCO 时 , 装 置 C 中 产 生 气 泡 的 原 因 是
2 3
____________________________________________________。
(5)实验结论是_________________________________________________________。
(6)加热NaHCO 发生反应的化学方程式为________________________________________________________。
3
【拔高练习】
1.(2022·西安模拟)《本草述钩元》中“石碱”条目下写道:“采蒿蓼之属,……晒干烧灰,以原水淋汁,
……久则凝淀如石,……浣衣发面,……亦去垢发面。”这里的“石碱”是指( )
A.KOH B.KAl(SO ) C.KHCO D .KCO
4 2 3 2 3
答案 D
解析 “采蒿蓼之属,……晒干烧灰”,说明“石碱”为蒿蓼烧成的灰中的成分;“以原水淋汁”,说明
“石碱”易溶于水;“浣衣发面,……亦去垢发面”,说明“石碱”能去油污、作发酵剂;且植物烧成的
灰中的主要成分一般为碳酸盐,故“石碱”为KCO,D项符合题意。
2 3
2.(2023春·河南·高三专题练习)化学与社会、生活、技术密切相关,下列说法正确的是
A.北宋科学家沈括在《梦溪笔谈•器用》中记载“以剂钢为刃,柔铁为茎干,不尔则断折。剑之钢者,刃
多毁缺,巨阙是也,故不可纯用剂钢”,其描述的铁合金的硬度和熔点比纯铁高
B.我国化学家侯德榜创立的“侯氏制碱法”原理为:以食盐、氨、二氧化碳为原料,直接生成纯碱
C.节日燃放的五彩缤纷的烟花,是锂、钠、钾、锶、钡等金属化合物发生化学反应时呈现的各种艳丽的
色彩
D.将废铁屑加入FeCl 溶液中,可用于除去工业废气中的Cl
2 2
3.(2023·浙江·校联考三模)探究钠及其化合物的性质,下列方案设计、现象及结论都正确的是( )
方案设计 现象 结论向露置在空气中的NaO 固体中加入稀盐
A 2 2 溶液中产生气泡 NaO 固体已经变质
酸 2 2
将一小块金属钠在燃烧匙中点燃,伸入盛 钠的还原性强,与二氧化碳发生
B 产生黑、白两种固体
有CO 的集气瓶中 了置换反应
2
向2mL 2mol/L Na CO 溶液中滴加2滴 该NaCO 溶液中混有NaHCO 杂
C 2 3 溶液中产生气泡 2 3 3
4mol/L 稀盐酸 质
向插有温度计的10mL 0.1mol/L NH Cl 有刺激性气味产生, 反应NH ++OH-=NH↑+H O为放
D 4 4 3 2
溶液中加入一定量NaOH固体 温度计示数增大 热反应
A.A B.B C.C D.D
4.(2023秋·河北唐山·高三统考期末)碘及其化合物广泛用于医药、染料等方面, 的一种制备方法如下
图:
下列说法正确的是
A.“转化”步骤反应的离子方程式: 3AgI + Fe =3Ag + Fe2++3I-
B.为提高 的产率,氯气的用量越多越好
C.所得沉淀与硝酸反应后的某种生成物可以循环使用
D.流程中过滤时玻璃仪器只需烧杯和漏斗
5.(2023·河南·统考模拟预测)某无色溶液中可能含有 K+、Ag+、Ba2+、 Fe3+、Cl-、OH-、 中的几
种,对其进行如下实验操作:
①取少量溶液,用pH计测得pH=13.3;
②另取少量溶液,加入足量BaCl 溶液,产生白色沉淀;
2
③将②所得混合物过滤,向滤液中加入AgNO 溶液,有白色沉淀生成。
3
下列对该溶液的说法正确的是
A.要确定是否含有K+,需做焰色反应实验
B.一定含有K+、OH-、CO2-
3
C.含有Ag+、Ba2+、Fe3+三种离子中的一种
D.原溶液中一定含有Cl-
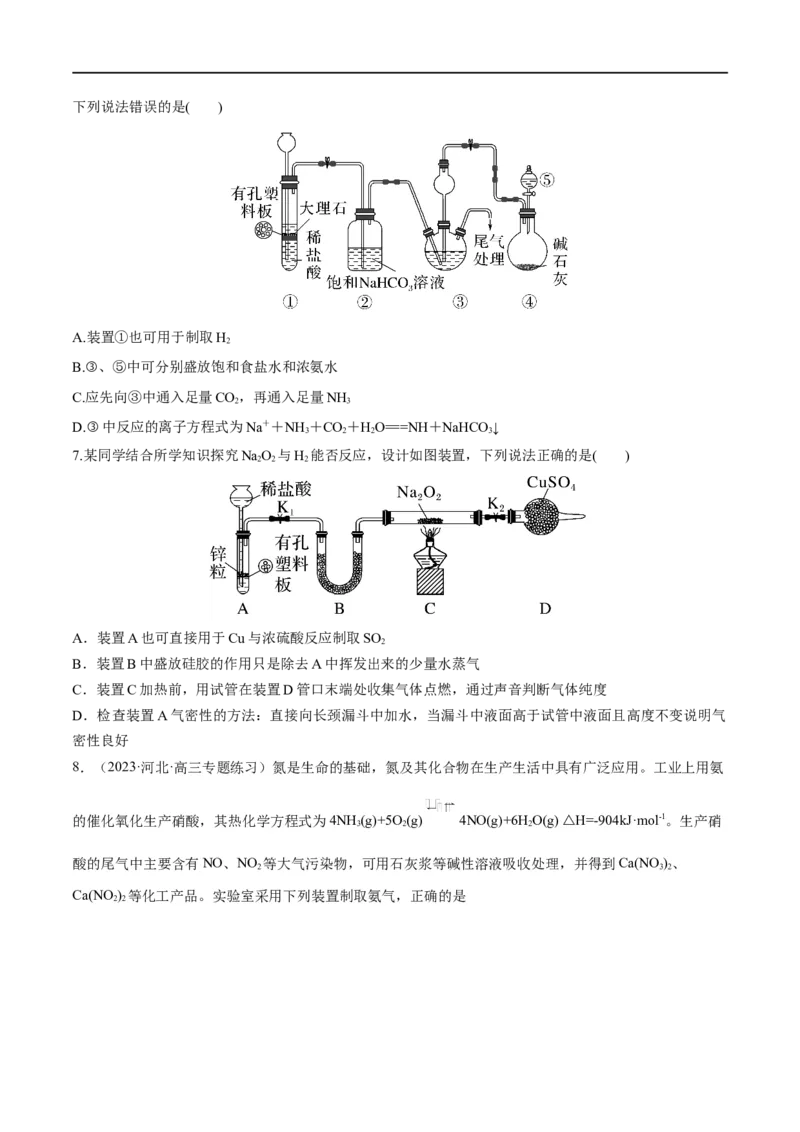
6.(2022·永州模拟)某小组设计如图所示装置(夹持装置略去),在实验室模拟侯氏制碱工艺中NaHCO 的制备。
3下列说法错误的是( )
A.装置①也可用于制取H
2
B.③、⑤中可分别盛放饱和食盐水和浓氨水
C.应先向③中通入足量CO,再通入足量NH
2 3
D.③中反应的离子方程式为Na++NH +CO+HO===NH+NaHCO ↓
3 2 2 3
7.某同学结合所学知识探究NaO 与H 能否反应,设计如图装置,下列说法正确的是( )
2 2 2
A.装置A也可直接用于Cu与浓硫酸反应制取SO
2
B.装置B中盛放硅胶的作用只是除去A中挥发出来的少量水蒸气
C.装置C加热前,用试管在装置D管口末端处收集气体点燃,通过声音判断气体纯度
D.检查装置A气密性的方法:直接向长颈漏斗中加水,当漏斗中液面高于试管中液面且高度不变说明气
密性良好
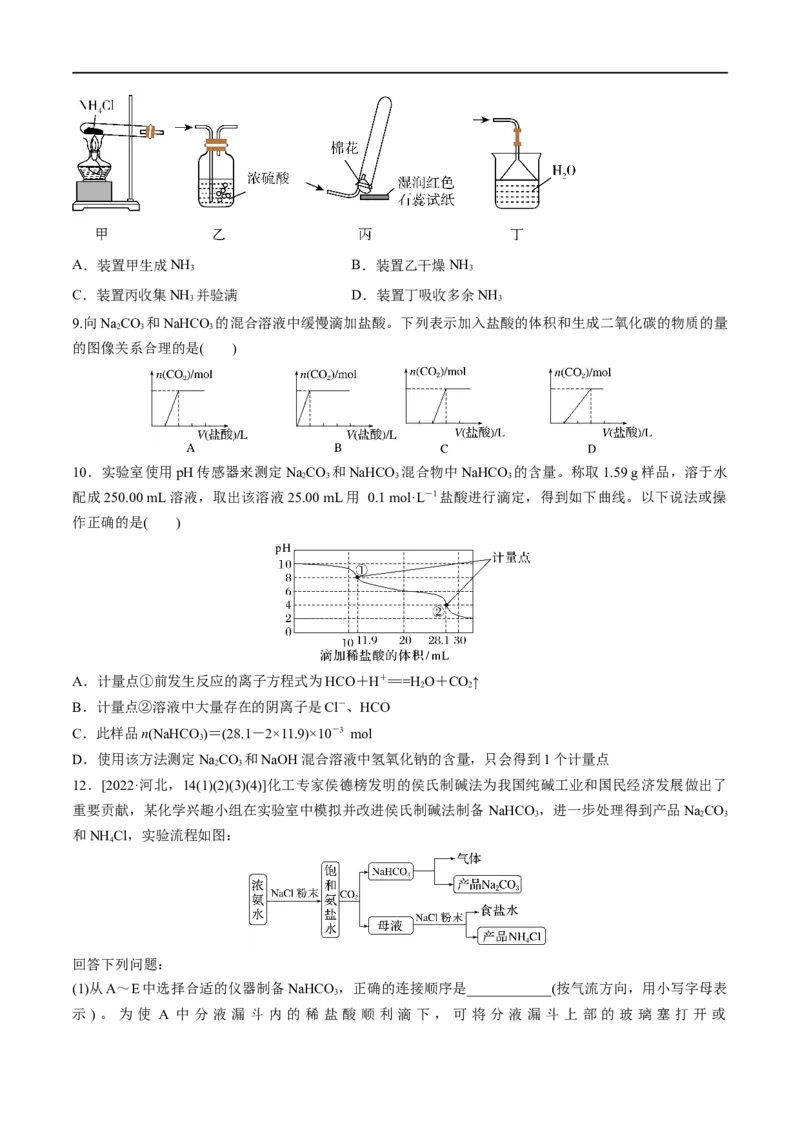
8.(2023·河北·高三专题练习)氮是生命的基础,氮及其化合物在生产生活中具有广泛应用。工业上用氨
的催化氧化生产硝酸,其热化学方程式为4NH (g)+5O(g) 4NO(g)+6H O(g) △H=-904kJ·mol-1。生产硝
3 2 2
酸的尾气中主要含有NO、NO 等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO )、
2 3 2
Ca(NO ) 等化工产品。实验室采用下列装置制取氨气,正确的是
2 2A.装置甲生成NH B.装置乙干燥NH
3 3
C.装置丙收集NH 并验满 D.装置丁吸收多余NH
3 3
9.向NaCO 和NaHCO 的混合溶液中缓慢滴加盐酸。下列表示加入盐酸的体积和生成二氧化碳的物质的量
2 3 3
的图像关系合理的是( )
10.实验室使用pH传感器来测定NaCO 和NaHCO 混合物中NaHCO 的含量。称取1.59 g样品,溶于水
2 3 3 3
配成250.00 mL溶液,取出该溶液25.00 mL用 0.1 mol·L-1盐酸进行滴定,得到如下曲线。以下说法或操
作正确的是( )
A.计量点①前发生反应的离子方程式为HCO+H+===H O+CO↑
2 2
B.计量点②溶液中大量存在的阴离子是Cl-、HCO
C.此样品n(NaHCO )=(28.1-2×11.9)×10-3 mol
3
D.使用该方法测定NaCO 和NaOH混合溶液中氢氧化钠的含量,只会得到1个计量点
2 3
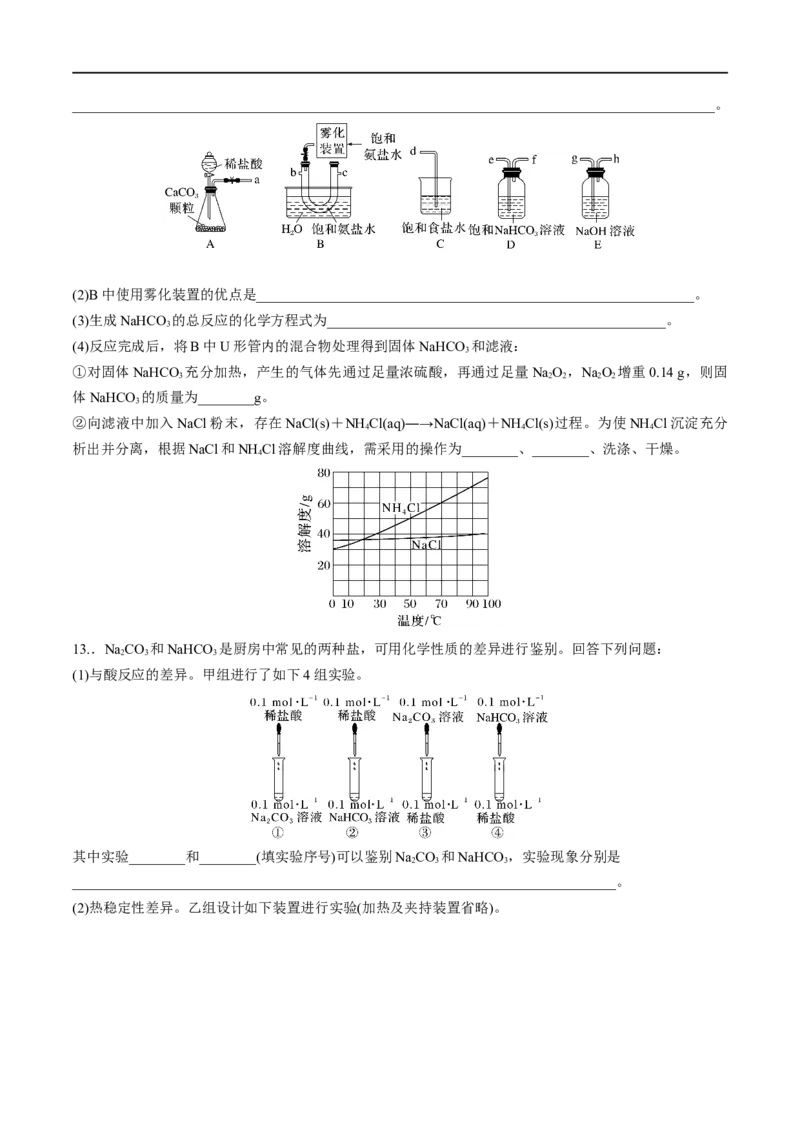
12.[2022·河北,14(1)(2)(3)(4)]化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了
重要贡献,某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备 NaHCO ,进一步处理得到产品NaCO
3 2 3
和NH Cl,实验流程如图:
4
回答下列问题:
(1)从A~E中选择合适的仪器制备NaHCO ,正确的连接顺序是____________(按气流方向,用小写字母表
3
示 ) 。 为 使 A 中 分 液 漏 斗 内 的 稀 盐 酸 顺 利 滴 下 , 可 将 分 液 漏 斗 上 部 的 玻 璃 塞 打 开 或___________________________________________________________________________________________。
(2)B中使用雾化装置的优点是______________________________________________________________。
(3)生成NaHCO 的总反应的化学方程式为________________________________________________。
3
(4)反应完成后,将B中U形管内的混合物处理得到固体NaHCO 和滤液:
3
①对固体NaHCO 充分加热,产生的气体先通过足量浓硫酸,再通过足量NaO ,NaO 增重0.14 g,则固
3 2 2 2 2
体NaHCO 的质量为________g。
3
②向滤液中加入NaCl粉末,存在NaCl(s)+NH Cl(aq)―→NaCl(aq)+NH Cl(s)过程。为使NH Cl沉淀充分
4 4 4
析出并分离,根据NaCl和NH Cl溶解度曲线,需采用的操作为________、________、洗涤、干燥。
4
13..NaCO 和NaHCO 是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:
2 3 3
(1)与酸反应的差异。甲组进行了如下4组实验。
其中实验________和________(填实验序号)可以鉴别NaCO 和NaHCO ,实验现象分别是
2 3 3
_____________________________________________________________________________。
(2)热稳定性差异。乙组设计如下装置进行实验(加热及夹持装置省略)。①将分别装有 NaCO 和 NaHCO 的试管同时放入甘油浴加热(甘油沸点为 290 ℃),目的是
2 3 3
________________________________________________________________________。
②该实验用饱和碳酸钠溶液检验反应的产物,a、b试管中的实验现象分别为
______________________________、________________________。
③b试管中发生反应的化学方程式为______________________________________________________。
(3)与盐溶液反应的差异。丙组设计如下实验,探究NaCO 和NaHCO 溶液与CaCl 溶液反应的差异。
2 3 3 2
反应物 现象
实
验 气泡情况
浓度/ CaCl 浓度/
2
组 物质 是否有沉淀(室温)
(mol·L-1) (mol·L-1) 室温 60 ℃水浴
号
A NaHCO 0.05 0.05 有少量白色沉淀 无 无
3
B NaCO 0.05 0.05 有较多白色沉淀 无 无
2 3
C NaHCO 0.5 0.5 有大量白色沉淀 无 有明显气泡
3
D NaCO 0.5 0.5 有大量白色沉淀 无 无
2 3
① 丙 组 由 此 得 出 “ 能 用 CaCl 鉴 别 同 浓 度 的 NaCO 和 NaHCO 溶 液 ” 的 结 论 , 理 由 是
2 2 3 3
_____________________________________________________________________________。
②请写出C组中60 ℃时,NaHCO 与CaCl 溶液反应的离子方程式:____________。
3 2