文档内容
第 7 讲 铁及其化合物
【学科核心素养】
1.宏观辨识与微观探析:认识铁及其化合物的性质及应用,能以“铁三角”转化关系理解变价元素的
转化条件。
2.科学态度与社会责任:利用铁及其化合物的性质,科学认识铁及其化合物的提纯和制备工艺流程,
形成严谨求实的科学态度和崇尚真理的意识。
3.科学探究与创新意识:能提出有价值的氢氧化亚铁及其他铁的化合物的制备方案,并进行实验探
究。
【核心素养发展目标】
1.能从物质类别和铁元素化合价的角度认识铁及其化合物的性质,理清铁元素不同价态之间的转化关
系,增强证据推理与模型认知的能力。
2.会设计实验制备氢氧化亚铁,检验Fe3+,探究Fe3+、Fe2+的氧化性与还原性,增强科学探究与创新
意识。
【知识点解读】
知识点一 铁及其重要化合物的性质
1.铁
铁位于元素周期表中第4周期Ⅷ族,是一种应用最广泛的过渡金属元素;铁元素是一种典型的变价金
属元素。
(1)结构
(2)铁的物理性质
银白色固体,熔点较高,具有良好的导热、导电、延展性,能被磁铁吸引。
(3)铁的化学性质
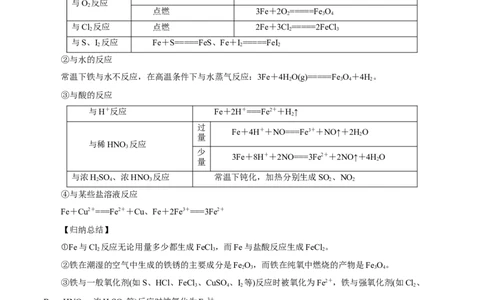
铁元素性质活泼,有较强的还原性,主要化合价为+2价和+3价。①与非金属单质的反应
常温 铁锈(成分为Fe O·xHO)
2 3 2
与O 反应
2
点燃 3Fe+2O=====Fe O
2 3 4
与Cl 反应 点燃 2Fe+3Cl=====2FeCl
2 2 3
与S、I 反应 Fe+S=====FeS、Fe+I=====FeI
2 2 2
②与水的反应
常温下铁与水不反应,在高温条件下与水蒸气反应:3Fe+4HO(g)=====Fe O+4H。
2 3 4 2
③与酸的反应
与H+反应 Fe+2H+===Fe2++H↑
2
过
Fe+4H++NO===Fe3++NO↑+2HO
量 2
与稀HNO 反应
3
少
3Fe+8H++2NO===3Fe2++2NO↑+4HO
量 2
与浓HSO 、浓HNO 反应 常温下钝化,加热分别生成SO 、NO
2 4 3 2 2
④与某些盐溶液反应
Fe+Cu2+===Fe2++Cu、Fe+2Fe3+===3Fe2+
【归纳总结】
①Fe与Cl 反应无论用量多少都生成FeCl ,而Fe与盐酸反应生成FeCl 。
2 3 2
②铁在潮湿的空气中生成的铁锈的主要成分是Fe O,而铁在纯氧中燃烧的产物是Fe O。
2 3 3 4
③铁与一般氧化剂(如S、HCl、FeCl 、CuSO 、I 等)反应时被氧化为Fe2+,铁与强氧化剂(如Cl、
3 4 2 2
Br 、HNO、浓HSO 等)反应时被氧化为Fe3+。
2 3 2 4
④在电化学中铁作负极时电极反应式为Fe-2e-===Fe2+。
(3)铁的冶炼
冶炼原理:Fe O+3CO=====2Fe+3CO
2 3 2
2.铁的氧化物
化学式 FeO Fe O Fe O
2 3 3 4
俗名 铁红 磁性氧化铁
颜色状态 黑色粉末 红棕色粉末 黑色晶体(有磁性)溶解性 难溶于水 难溶于水 难溶于水
铁的化合价 +2 +3 +2,+3
稳定性 不稳定 稳定 稳定
与H+反应的 FeO+2H+=== Fe 2 O 3 +6H+=== Fe O+8H+===Fe2+
3 4
离子方程式 Fe2++HO 2Fe3++3HO +2Fe3++4H 2 O
2 2
3.铁的氢氧化物
(1)Fe(OH) 是白色絮状物,易被空气中的氧气氧化生成Fe(OH) ,颜色由白色变为灰绿色,最后变为红
2 3
褐色,方程式为4Fe(OH) +O+2HO===4Fe(OH) 。
2 2 2 3
(2)Fe(OH) 是红褐色、难溶于水的固体,在空气中久置会部分失水生成铁锈(Fe O·xHO),受热易分
3 2 3 2
解,方程式为2Fe(OH) =====Fe O+3HO;制取Fe(OH) 用可溶性铁盐与碱反应,离子方程式:Fe3++
3 2 3 2 3
3OH-===Fe(OH) ↓。
3
4.亚铁盐
(1)Fe2+的氧化性和还原性
含有Fe2+的溶液呈浅绿色,Fe2+处于铁的中间价态,既有氧化性,又有还原性,其中以还原性为主,
如:遇Br 、Cl、HO、NO(H+)等均表现为还原性。
2 2 2 2
Fe2+的酸性溶液与HO 反应的离子方程式:2Fe2++HO+2H+===2Fe3++2HO。
2 2 2 2 2
(2)可水解
Fe(OH) 是弱碱,含Fe2+的盐(如硫酸亚铁)溶液呈酸性。配制硫酸亚铁溶液时常加少量硫酸抑制Fe2+的
2
水解,加少量铁屑防止Fe2+被氧化。
5.铁盐的性质及应用
(1)氧化性:含有Fe3+的溶液呈棕黄色,Fe3+处于铁的高价态,遇Fe、Cu、HI、HS等均表现为氧化
2
性。
①Fe3+与S2-、I-、HS-、SO等具有较强还原性的离子不能大量共存。
②Fe3+可腐蚀印刷电路板上的铜箔,反应的离子方程式为2Fe3++Cu===Cu2++2Fe2+。
(2)易水解:Fe(OH) 是很弱的碱,且溶度积很小,因而Fe3+极易水解,只能存在于酸性较强的溶液
3
中。
①利用Fe3+易水解的性质,实验室可用FeCl 滴入沸水中制取氢氧化铁胶体,反应的化学方程式:
3
FeCl +3HO=====Fe(OH) (胶体)+3HCl。
3 2 3
②利用Fe3+易水解的性质,工业上常用调节pH方法除去溶液中的铁离子。
③利用Fe3+易水解的性质,实验室配制氯化铁溶液,通常将氯化铁固体先溶于较浓的盐酸中,然后再
稀释至所需浓度。
④Fe3+与HCO、[Al(OH) ]-、CO、ClO-等水解呈碱性的离子不能大量共存。
4知识点二 Fe2+和Fe3+的检验
1.亚铁盐
(1)Fe2+的氧化性和还原性
含有Fe2+的溶液呈浅绿色,Fe2+处于铁的中间价态,既有氧化性,又有还原性,其中以还原性为主,
如遇Br 、Cl、HO、NO(H+)、MnO(H+)等均表现为还原性。
2 2 2 2
Fe2+的酸性溶液与HO 反应的离子方程式:2Fe2++2H++HO===2Fe3++2HO
2 2 2 2 2
向FeCl 溶液中滴加酸性KMnO 溶液,溶液褪色。反应的离子方程式:MnO+5Fe2++8H+===5Fe3++
2 4
Mn2++4HO。
2
(2)可水解
Fe2+的盐(如硫酸亚铁)溶液因水解呈酸性。
2.铁盐
(1)氧化性:含有Fe3+的溶液呈黄色,Fe3+处于铁的高价态,遇Fe、Cu、HI、HS等均表现为氧化性。
2
如用FeCl 溶液腐蚀印刷电路板上的铜箔,反应的离子方程式2Fe3++Cu===2Fe3++Cu2+。
3
(2)易水解:Fe3+极易水解,只能存在于酸性较强的溶液中。
3.Fe2+、Fe3+的检验方法
(1)Fe2+的检验
方法1 ―――――――→无现象―――――――→溶液变红色,证明含有Fe2+
――――――――→产生白色絮状沉淀,迅速变成灰绿色,最终变为红褐色,证
方法2
明含有Fe2+
方法3 ―――――――――→生成蓝色沉淀,证明含有Fe2+
(2)Fe3+的检验
方法1 ――――――――→溶液变红色,证明含有Fe3+
方法2 ―――――――→产生红褐色沉淀,证明含有Fe3+
(3)混合溶液中Fe3+、Fe2+的检验
①Fe3+的检验
a.――→溶液变血红色,说明含有Fe3+
b.――→试纸变蓝色,说明含有Fe3+
②Fe2+的检验
a.――→KMnO 溶液褪色,说明含有Fe2+
4
b.――→溴水褪色,说明含有Fe2+
c.――→生成蓝色沉淀,说明含有Fe2+
4.亚铁盐、铁盐性质应用(1)盐溶液的配制与保存
(2)物质的制备
(3)判断离子能否共存
Fe2+NO(H+)、ClO-、MnO(H+)
Fe3+S2-、I-、SO
Fe3+HCO、CO等水解相互促进的离子
【典例剖析】
高频考点一 铁及其化合物的性质
例1.(高考组合题)下列有关物质性质的叙述错误的是( )
A. (2021·浙江卷)铁粉与氧化铝发生的铝热反应可用于焊接铁轨
B.(2019·天津卷)将废铁屑加入FeCl 溶液中,可用于除去工业废气中的Cl
2 2
C.(2020·江苏卷)室温下,Fe与浓HSO 反应生成FeSO
2 4 4
D. (2018·江苏卷)Cu与FeCl 溶液反应可生成CuCl
3 2
【答案】AC
【解析】铝粉与氧化铁发生铝热反应时放出大量的热,因此,生成的铁是液态的,其可以将两段铁轨
焊接在一起,故其可用于焊接铁轨,但是,铁粉与氧化铝不能发生铝热反应,A错误;铁和亚铁能将氯气
还原为氯离子,从而除去工业废气中的氯气,B正确;室温下,铁在浓硫酸中发生钝化,C错误; Cu与
FeCl 溶液反应生成CuCl 和FeCl ,反应的化学方程式为Cu+2FeCl =CuCl +2FeCl ,D正确。
3 2 2 3 2 2
【变式探究】(高考组合题)下列观点的叙述正确的是( )
A.(2021·浙江卷)将生铁进一步炼制减少含碳量,能得到耐腐蚀的钢
Cl 2 N aO H( aq)
B.(2017·江苏卷)Fe 点燃 FeCl Fe(OH)
2 2
C.(2018·江苏卷)D.(2017·新课标II卷)向2 mL 0.1 mol·L-1的FeCl 溶液中加足量铁粉,振荡,加1滴KSCN溶液,黄
3
色逐渐消失,加KSCN溶液颜色不变,说明还原性:Fe>Fe2+
【答案】AD
【解析】将生铁进一步炼制可以减少碳含量,在使用这种钢材时可以减少电化学腐蚀过程,这样的钢
材更耐腐蚀,A正确;铁与氯气反应只能生成氯化铁,B错误;Al与Fe O 高温发生铝热反应生成Al O 和
2 3 2 3
Fe,Fe与HCl反应生成FeCl 和H,第二步反应不能实现,C错误;加入过量的铁粉,黄色消失,加入
2 2
KSCN溶液,溶液不变色,说明Fe3+完全被消耗,即Fe+2Fe3+=3Fe2+,根据氧化还原反应规律,还原剂的
还原性大于还原产物得还原性,Fe元素化合价升高,Fe为还原剂,Fe2+即使还原产物又是氧化产物,因此
还原性Fe>Fe2+,D正确。
高频考点二 铁及其化合物的转化与计算
例2.在给定条件下,下列物质间的转化不能实现的是( )
A.Fe――→FeCl B.Fe――→FeSO
3 4
C.Fe――→Fe O D.Fe――→FeCl
3 4 2
【答案】B
【解析】Fe和Cl 在加热条件下发生反应生成FeCl :2Fe+3Cl=====2FeCl ,物质间的转化能实现,
2 3 2 3
故A不符合;常温下Fe在浓硫酸中发生钝化不能继续反应,物质间的转化不能实现,故B符合;Fe和
HO(g)在高温条件下发生反应生成Fe O 和H :3Fe+4HO(g)=====Fe O +4H ,物质间的转化能实现,故
2 3 4 2 2 3 4 2
C不符合;Fe和FeCl 溶液反应生成FeCl :Fe+2Fe3+===3Fe2+,物质间的转化能实现,故D不符合。
3 2
【变式探究】含有agHNO 的稀硝酸与bg铁恰好反应,铁全部溶解,生成NO。已知有gHNO 被还
3 3
原,则a∶b不可能是( )
A.3∶1 B.3∶2 C.4∶1 D.9∶2
【答案】B
【解析】若生成硝酸亚铁:
3Fe+8HNO===3Fe(NO)+2NO↑+4HO
3 3 2 2
168 2×63=126
b
=
a∶b=3∶1
若生成硝酸铁:
Fe+4HNO===Fe(NO)+NO↑+2HO
3 3 3 2
56 63b
=
a∶b=9∶2
还可能生成硝酸铁和硝酸亚铁的混合物,所以3∶1≤a∶b≤9∶2之间,不符合题意的只有B项。
【方法技巧】数轴法分析铁与稀硝酸反应的产物
一是明确哪种物质过量,二是根据两种物质的量分析讨论判断。根据化学方程式:
HNO 过量:Fe+4HNO(稀)===Fe(NO)+NO↑+2HO;
3 3 3 3 2
Fe过量:Fe+2Fe(NO )===3Fe(NO);
3 3 3 2
两者相加得总方程式:3Fe+8HNO(稀)===3Fe(NO)+2NO↑+4HO;
3 3 2 2
可以用数轴表示:
解题时需注意量的范围:
①≤,产物仅有Fe(NO ),稀HNO 可能有剩余;②≥,产物仅有Fe(NO ),Fe可能有剩余;③<
3 3 3 3 2
<,产物为Fe(NO ) 和Fe(NO ),Fe和稀HNO 都完全反应。
3 3 3 2 3
高频考点三、铁及其化合物的实验探究
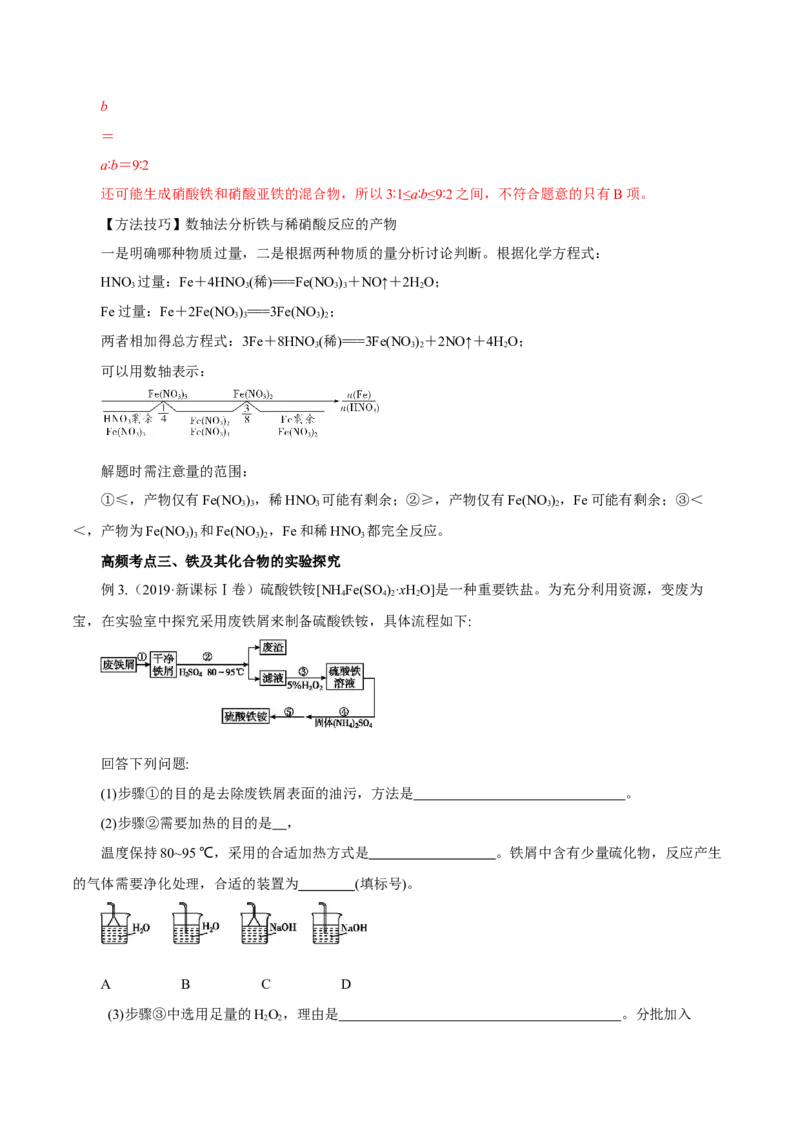
例3.(2019·新课标Ⅰ卷)硫酸铁铵[NH Fe(SO )·xHO]是一种重要铁盐。为充分利用资源,变废为
4 4 2 2
宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:
回答下列问题:
(1)步骤①的目的是去除废铁屑表面的油污,方法是 。
(2)步骤②需要加热的目的是 ,
温度保持80~95 ℃,采用的合适加热方式是 。铁屑中含有少量硫化物,反应产生
的气体需要净化处理,合适的装置为 (填标号)。
A B C D
(3)步骤③中选用足量的HO,理由是 。分批加入
2 2HO,同时为了 , 溶液要保持pH小于0.5。
2 2
(4)步骤⑤的具体实验操作有 ,经干燥得到硫酸铁铵晶体样品。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时失掉1.5个结晶水,
失重5.6%。硫酸铁铵晶体的化学式为 。
【解析】 (1)油污在热的碱性条件下易水解,故去除废铁屑表面的油污的方法是碱煮水洗。(2)适当加
热可加快反应速率。加热温度为80~95 ℃,低于100 ℃,可用热水浴加热。铁屑中含有少量硫化物,与
HSO 反应生成HS气体,HS易与NaOH溶液反应,为防倒吸,故选C装置。(3)足量的HO 可充分将
2 4 2 2 2 2
Fe2+氧化为Fe3+,且不会引入新的杂质。Fe3+易水解,故溶液应保持一定的pH,防止Fe3+水解。(4)在过程④
后溶液中存在大量的Fe3+、NH+、SO2-,从溶液中提取晶体的操作有蒸发浓缩、冷却结晶、过滤、洗涤、
4 4
1.5×18
干燥等。(5)硫酸铁铵[NH Fe(SO )·xHO]晶体失去1.5个结晶水,失重5.6%,可知
4 4 2 2 266+18x
×100%=5.6%,解得x=12,硫酸铁铵晶体的化学式为NH Fe(SO )·12HO。
4 4 2 2
【答案】(1)碱煮水洗
(2)加快反应 热水浴 C
(3)将Fe2+全部氧化为Fe3+;不引入杂质 防止Fe3+水解
(4)加热浓缩、冷却结晶、过滤(洗涤)
(5)NH Fe(SO )·12HO
4 4 2 2
【变式探究】(2018·北京卷)实验小组制备高铁酸钾(KFeO)并探究其性质。
2 4
资料:KFeO 为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O,在
2 4 2
碱性溶液中较稳定。
(1)制备KFeO(夹持装置略)
2 4
①A为氯气发生装置。A中反应方程式是________________(锰被还原为Mn2+)。
②将除杂装置B补充完整并标明所用试剂。
③C中得到紫色固体和溶液。C中Cl 发生的反应有3Cl+2Fe(OH) +10KOH===2KFeO+6KCl+8H O,
2 2 3 2 4 2
另外还有________________。(2)探究KFeO 的性质
2 4
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl。为证明是否
2
KFeO 氧化了Cl-而产生Cl,设计以下方案:
2 4 2
方案Ⅰ 取少量a,滴加KSCN溶液至过量,溶液呈红色。
用KOH溶液充分洗涤C中所得固体,再用KOH溶液将KFeO 溶出,得到紫色溶液
方案Ⅱ 2 4
b。取少量b,滴加盐酸,有Cl 产生。
2
Ⅰ.由方案Ⅰ中溶液变红可知a中含有______离子,但该离子的产生不能判断一定是KFeO 将Cl-氧
2 4
化,还可能由________________产生(用方程式表示)。
Ⅱ.方案Ⅱ可证明KFeO 氧化了Cl-。用KOH溶液洗涤的目的是________________。
2 4
②根据KFeO 的制备实验得出:氧化性Cl________ (填“>”或“<”),而方案Ⅱ实验表
2 4 2 FeO2−
4
明,Cl 和 的氧化性强弱关系相反,原因是________________。
2 FeO2−
4
③资料表明,酸性溶液中的氧化性 > ,验证实验如下:将溶液b滴入MnSO 和足量HSO
FeO2− MnO− 4 2 4
4 4
的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性 > 。若能,请说明理由;若不
FeO2− MnO−
4 4
能,进一步设计实验方案。理由或方案:________________。
【解析】(1)①A为氯气发生装置,KMnO 与浓盐酸反应时,锰被还原为Mn2+,浓盐酸被氧化成
4
Cl,KMnO 与浓盐酸反应生成KCl、MnCl 、Cl 和HO,根据得失电子守恒和原子守恒,反应的化学方程
2 4 2 2 2
式为2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8H O,离子方程式2MnO -+10Cl-+16H+=2Mn2+
4 2 2 2 4
+5Cl↑+8H O。
2 2
②由于盐酸具有挥发性,所得Cl 中混有HCl和HO(g),HCl会消耗Fe(OH)、KOH,用饱和食
2 2 3
盐水除去HCl,除杂装置B为 。
③ C中Cl 发生的反应有3Cl+2Fe(OH)+10KOH=2K FeO+6KCl+8H O,还有Cl 与KOH的反应,
2 2 3 2 4 2 2
Cl 与KOH反应的化学方程式为Cl+2KOH=KCl+KClO+H O,反应的离子方程式为Cl+2OH-=Cl-+ClO-
2 2 2 2
+H O。
2(2)①根据上述制备反应,C的紫色溶液中含有KFeO、KCl,还可能含有KClO等。
2 4
I.方案I加入KSCN溶液,溶液变红说明a中含Fe3+。但Fe3+的产生不能判断KFeO 与Cl-发生了反
2 4
应,根据题意KFeO 在酸性或中性溶液中快速产生O,自身被还原成Fe3+,根据得失电子守恒、原子守恒
2 4 2
和电荷守恒,可能的反应为4FeO2-+20H+=3O ↑+4Fe3++10H O。
4 2 2
II.产生Cl 还可能是ClO-+Cl-+2H+=Cl↑+H O,即KClO的存在干扰判断;KFeO 微溶于KOH溶液,用
2 2 2 2 4
KOH溶液洗涤的目的是除去KClO、排除ClO-的干扰,同时保持KFeO 稳定存在。
2 4
②制备KFeO 的原理为3Cl+2Fe(OH)+10KOH=2K FeO+6KCl+8H O,在该反应中Cl元素的化合
2 4 2 3 2 4 2
价由0价降至-1价,Cl 是氧化剂,Fe元素的化合价由+3价升至+6价,Fe(OH) 是还原剂,KFeO 为氧
2 3 2 4
化产物,根据同一反应中,氧化性:氧化剂>氧化产物,得出氧化性Cl>FeO2-;方案II的反应为2FeO2-
2 4 4
+6Cl-+16H+=2Fe3++3Cl↑+8H O,实验表明,Cl 和FeO2-氧化性强弱关系相反;对比两个反应的条件,制备
2 2 2 4
KFeO 在碱性条件下,方案II在酸性条件下;说明溶液的酸碱性的不同影响物质氧化性的强弱。
2 4
③该小题为开放性试题。若能,根据题意KFeO 在足量HSO 溶液中会转化为Fe3+和O,最后溶液中
2 4 2 4 2
不存在FeO2-,溶液振荡后呈浅紫色一定是MnO -的颜色,说明FeO2-将Mn2+氧化成MnO -,所以该实验方
4 4 4 4
案能证明氧化性FeO2->MnO -。(或不能,因为溶液b呈紫色,溶液b滴入MnSO 和HSO 的混合溶液
4 4 4 2 4
中,c(FeO2-)变小,溶液的紫色也会变浅;则设计一个空白对比的实验方案,方案为:向紫色溶液b中
4
滴加过量稀HSO ,观察溶液紫色快速褪去还是显浅紫色)。
2 4
【答案 (1)2KMnO+16HCl==2MnCl +2KCl +5Cl ↑+8H O
4 2 2 2
Cl +2OH−==Cl−+ClO−+H O (2)Ⅰ. Fe3+ 4FeO2−+20H+==4Fe3++3O ↑+10H O Ⅱ.排除ClO−的
2 2 4 2 2
干扰 > 溶液的酸碱性不同 若能,理由:FeO2−在过量酸的作用下完全转化为Fe3+和O,溶液
4 2
浅紫色一定是MnO −的颜色(若不能,方案:向紫色溶液b中滴加过量稀HSO ,观察溶液紫色快速褪去
4 2 4
还是显浅紫色)
高频考点四 氢氧化亚铁制备方法的实验创新改进
例4.下列各图示中能较长时间看到Fe(OH) 白色沉淀的是 (填序号)。
2【答案】①②③⑤
【解析】Fe(OH) 在空气中很容易被氧化为红褐色的Fe(OH),即发生反应:4Fe(OH)+O+
2 3 2 2
2HO===4Fe(OH)。因此要较长时间看到Fe(OH) 白色沉淀,就要排除装置中的氧气或空气。①②原
2 3 2
理一样,都是先用铁与稀硫酸反应产生的氢气将装置中的空气排尽,并使生成的Fe(OH) 处在氢气的保
2
护中;③的原理为铁做阳极产生Fe2+,与阴极产生的OH-结合生成Fe(OH),且液面用汽油保护,能防
2
止空气进入;⑤中液面加苯阻止了空气进入;④由于空气中的氧气能迅速将Fe(OH) 氧化,因而不能较
2
长时间看到白色沉淀。
【方法技巧】制备Fe(OH) 常用的三种方法
2
(1)有机层覆盖法
将吸有NaOH溶液的胶头滴管插到液面以下,并在液面上覆盖一层苯或煤油(不能用CCl ),以防止
4
空气与Fe(OH) 接触发生反应,如图1所示。
2
(2)还原性气体保护法
用H 将装置内的空气排尽后,再将亚铁盐与NaOH溶液混合,这样可较长时间观察到白色沉淀,如图
2
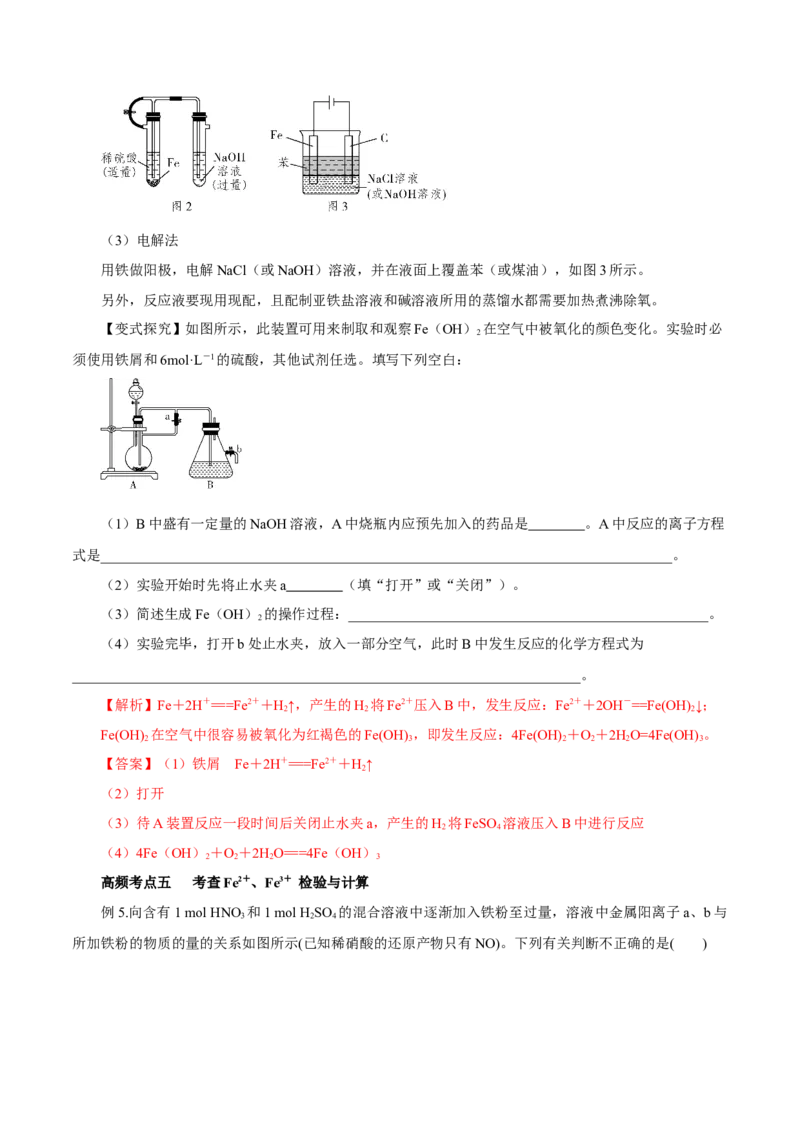
2所示。(3)电解法
用铁做阳极,电解NaCl(或NaOH)溶液,并在液面上覆盖苯(或煤油),如图3所示。
另外,反应液要现用现配,且配制亚铁盐溶液和碱溶液所用的蒸馏水都需要加热煮沸除氧。
【变式探究】如图所示,此装置可用来制取和观察Fe(OH) 在空气中被氧化的颜色变化。实验时必
2
须使用铁屑和6mol·L-1的硫酸,其他试剂任选。填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中烧瓶内应预先加入的药品是 。A中反应的离子方程
式是_________________________________________________________________________________。
(2)实验开始时先将止水夹a (填“打开”或“关闭”)。
(3)简述生成Fe(OH) 的操作过程:___________________________________________________。
2
(4)实验完毕,打开b处止水夹,放入一部分空气,此时B中发生反应的化学方程式为
________________________________________________________________________。
【解析】Fe+2H+===Fe2++H↑,产生的H 将Fe2+压入B中,发生反应:Fe2++2OH-==Fe(OH) ↓;
2 2 2
Fe(OH) 在空气中很容易被氧化为红褐色的Fe(OH) ,即发生反应:4Fe(OH) +O+2HO=4Fe(OH) 。
2 3 2 2 2 3
【答案】(1)铁屑 Fe+2H+===Fe2++H↑
2
(2)打开
(3)待A装置反应一段时间后关闭止水夹a,产生的H 将FeSO 溶液压入B中进行反应
2 4
(4)4Fe(OH)+O+2HO===4Fe(OH)
2 2 2 3
高频考点五 考查Fe2+、Fe3+ 检验与计算
例5.向含有1 mol HNO 和1 mol H SO 的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与
3 2 4
所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。下列有关判断不正确的是( )A.a表示Fe3+的关系曲线
B.n=0.75
1
C.P点时,n(Fe2+)=0.562 5 mol
D.向P点溶液中加入铜粉,最多可溶解12.2 g
【答案】CD
【解析】该反应可以看作两步:①Fe+4H++NO===Fe3++NO↑+2HO,NO过量,H+不足;②2Fe3
2
++Fe===3Fe2+。a表示Fe3+的关系曲线,A正确;溶液中共有3 mol H+参加反应,消耗铁为 0.75 mol,B
正确;P点n(Fe2+)=n(Fe3+),二者均为0.45 mol,C错误;P点剩余0.45 mol Fe3+,消耗0.225 mol铜,质
量为14.4 g,D错误。
【举一反三】某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L 的溶液。在FeCl 溶液中需加入少量铁
2
屑,其目的是___________________________________________。
(2)甲组同学取2 mL FeCl 溶液,加入几滴氯水,再加入1滴 KSCN溶液,溶液变红,说明Cl 可将Fe2
2 2
+氧化。FeCl 溶液与氯水反应的离子方程式为_____________________。
2
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl 溶液中先加入0.5 mL煤油,再于液面下
2
依 次 加 入 几 滴 氯 水 和 1 滴 KSCN 溶 液 , 溶 液 变 红 , 煤 油 的 作 用 是
_____________________________________。
(4)丙组同学取10 mL 0.1 mol/L KI溶液,加入6 mL 0.1 mol/L FeCl 溶液混合。分别取2 mL此溶液于3
3
支试管中进行如下实验:
①第一支试管中加入1 mL CCl 充分振荡、静置,CCl 层显紫色;
4 4
②第二支试管中加入1滴K[Fe(CN) ] 溶液,生成蓝色沉淀;
3 6
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是________(填离子符号);实验①和③说明:在I-过量的情况下,溶液中仍含有
______(填离子符号),由此可以证明该氧化还原反应为____________________。
【解析】(1)Fe2+具有还原性,FeCl 溶液易被氧化而变质,配制FeCl 溶液时加入少量铁屑,目的是防
2 2
止Fe2+被氧化。(2)溶液变红,说明有Fe3+生成,则FeCl 溶液与氯水反应生成FeCl ,离子方程式为2Fe2+
2 3+Cl===2Fe3++2Cl-。(3)甲组实验中,FeCl 易被空气中的O 氧化生成FeCl ,因此实验不够严谨。加入
2 2 2 3
煤油,煤油的密度比水小,可以起到隔绝空气的作用,从而排除氧气对实验的影响。(4)实验②中
K[Fe(CN) ]溶液的作用是检验Fe2+。根据实验①,CCl 层显紫色,说明有I 生成,根据实验②,生成蓝色
3 6 4 2
沉淀,说明有Fe2+生成,根据实验③,溶液变红,说明有Fe3+剩余,在I-过量的情况下,溶液中仍含有
Fe3+,由此可以证明该反应为可逆反应。
【答案】(1)防止Fe2+被氧化
(2)2Fe2++Cl===2Fe3++2Cl-
2
(3)隔绝空气(排除氧气对实验的影响)
(4)Fe2+ Fe3+ 可逆反应
【方法技巧】检验Fe2+和Fe3+时的注意事项
(1)检验Fe2+时不能先加氯水后加KSCN溶液,也不能将加KSCN后的混合溶液加入足量的新制氯
水中(新制氯水可以氧化SCN-)。
(2)当溶液浓度较稀时,利用观察法或加NaOH溶液的方法都不宜检验Fe2+和Fe3+的存在。
(3)Fe3+、Fe2+、Cl-同时存在时不能用酸性KMnO 溶液检验Fe2+(Cl-能还原酸性KMnO ,有干
4 4
扰)。
(4)检验Fe2+、Fe3+的其他方法
①检验Fe2+最好、最灵敏的试剂是铁氰化钾K[Fe(CN)]。
3 6
②检验Fe3+也可用苯酚(C HOH),在FeCl 溶液中滴加苯酚,溶液显紫色。
6 5 3
【变式探究】要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时,最佳顺序为( )
①加入足量氯水 ②加入足量酸性KMnO 溶液 ③加入少量NH SCN溶液
4 4
A.①③ B.③②
C.③① D.①②③
【答案】C
【解析】在该溶液中先加入少量NH SCN溶液,溶液不变红色,证明无Fe3+存在,再加入氯水,将
4
Fe2+氧化成Fe3+,溶液变为红色。KMnO 溶液呈紫红色,溶液颜色变化不明显,所以不能用酸性KMnO
4 4
溶液代替氯水检验。
高频考点六 铁及其化合物的转化
例6.(2021·广东高考真题)部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是A. 可与 反应生成
B. 既可被氧化,也可被还原
C.可将 加入浓碱液中制得 的胶体
D.可存在 的循环转化关系
【答案】C
【解析】图中所示铁元素不同化合价的物质:a为Fe,b为FeCl 、FeSO 、Fe(NO ) 等Fe(II)的盐类物
2 4 3 2
质,c为Fe(OH) ,e为FeCl 、Fe (SO )、Fe(NO ) 等Fe(III)的盐类物质,d为Fe(OH) 。Fe与Fe(III)的盐类
2 3 2 4 3 3 3 3
物质可发生反应生成Fe(II)的盐类物质,如Fe+2FeCl =3FeCl ,故A不选;Fe(II)为铁元素的中间价态,既
3 2
有还原性也有氧化性,因此既可被氧化,也可被还原,故B不选;Fe(III)的盐类物质与浓碱液反应生成
Fe(OH) 沉淀,制备Fe(OH) 胶体操作为:向沸水中滴加饱和FeCl 溶液,继续煮沸至溶液呈红褐色,停止
3 3 3
加热,故C选; 转化如
,故D不选;综上所述,答案为C。
【举一反三】(2018·高考全国卷Ⅰ)磷酸亚铁锂(LiFePO )电池是新能源汽车的动力电池之一。采
4
用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如图所示:
下列叙述错误的是( )
A.合理处理废旧电池有利于保护环境和资源再利用
B.从“正极片”中可回收的金属元素Al、Fe、Li
C.“沉淀”反应的金属离子为Fe3+
D.上述流程中可用硫酸钠代替碳酸钠
【答案】D
【解析】废旧电池中含有的金属、电解质溶液会对水体和土壤等造成污染,处理废旧电池有利于资源再利用,同时能够降低环境污染,保护环境,A项正确;从流程图看出,正极材料涉及了铝、铁、锂等金
属,B项正确;因流程中加入的有HNO,故在含Li、P、Fe等滤液中加碱液,发生“沉淀”反应的金属离
3
子为Fe3+,C项正确;因为锂及其化合物的性质与镁相似,由硫酸镁易溶于水推知,硫酸锂易溶于水,由
碳酸镁微溶于水推知,碳酸锂微溶于水,所以不能用硫酸钠代替碳酸钠,D项错误。
【变式探究】(2019·全国卷Ⅰ)硫酸铁铵[NH Fe(SO )·xHO]是一种重要铁盐。为充分利用资源,
4 4 2 2
变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:
回答下列问题:
(1)步骤①的目的是去除废铁屑表面的油污,方法是 。
(2)步骤②需要加热的目的是 ,温度保持80~95℃,采用的合适加热方式是
。铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为 (填标号)。
(3)步骤③中选用足量的HO,理由是______________________________________
2 2
________________________________________________________________________。
分批加入HO,同时为了 ,溶液要保持pH小于0.5。
2 2
(4)步骤⑤的具体实验操作有______________________________________________,
经干燥得到硫酸铁铵晶体样品。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150℃时失掉1.5个结晶
水,失重5.6%。硫酸铁铵晶体的化学式为 。
【解析】(1)除去铁屑表面油污的方法是用热纯碱溶液清洗铁屑,再用水洗。(2)铁与稀硫酸反应
时加热,可提高反应速率。温度低于水的沸点,可以用热水浴加热,受热均匀且便于控制。含少量硫化物
的铁屑与稀硫酸反应有硫化氢生成。氢气不与碱溶液反应,而硫化氢能与碱溶液反应,硫化氢在水中溶解
度小,故氢气中混有的硫化氢用烧碱溶液除去,又因为硫化氢与碱反应较快,容易引起倒吸,C装置倒置
漏斗能防倒吸。故宜选择C装置吸收硫化氢。(3)铁与稀硫酸反应生成硫酸亚铁和氢气,加入足量双氧
水的目的是将Fe2+全部氧化为Fe3+,发生反应为2Fe2++HO+2H+===2Fe3++2HO,从生成物看,又不
2 2 2
引入杂质。铁离子对双氧水分解起催化作用,分批加入双氧水,避免反应过快、放出热量较多,减少双氧
水分解,以免造成氧化剂损失;铁离子易水解,保持溶液呈强酸性,避免铁离子发生水解反应生成氢氧化铁。(4)步骤⑤是要从溶液中得到硫酸铁铵晶体,故实验操作有加热浓缩、冷却结晶、过滤(洗涤)。
(5)失重5.6%是质量分数,设结晶水合物的化学式为NH Fe(SO )·xHO,由题意知=,解得x=12。
4 4 2 2
【答案】(1)碱煮水洗
(2)加快反应 热水浴 C
(3)将Fe2+全部氧化为Fe3+;不引入杂质 防止Fe3+水解
(4)加热浓缩、冷却结晶、过滤(洗涤)
(5)NH Fe(SO )·12H O
4 4 2 2