文档内容
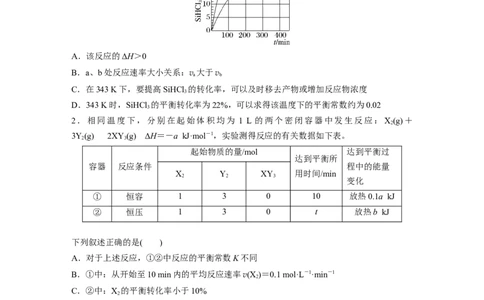
1.对于反应2SiHCl (g)SiHCl(g)+SiCl (g),采用大孔弱碱性阴离子交换树脂催化剂在
3 2 2 4
323 K和343 K时SiHCl 的转化率随时间变化的结果如图所示。下列说法不正确的是( )
3
A.该反应的ΔH>0
B.a、b处反应速率大小关系:v 大于v
a b
C.在343 K下,要提高SiHCl 的转化率,可以及时移去产物或增加反应物浓度
3
D.343 K时,SiHCl 的平衡转化率为22%,可以求得该温度下的平衡常数约为0.02
3
2.相同温度下,分别在起始体积均为 1 L 的两个密闭容器中发生反应:X(g)+
2
3Y(g)2XY (g) ΔH=-a kJ·mol-1,实验测得反应的有关数据如下表。
2 3
起始物质的量/mol 达到平衡过
达到平衡所
容器 反应条件 程中的能量
X Y XY 用时间/min
2 2 3
变化
① 恒容 1 3 0 10 放热0.1a kJ
② 恒压 1 3 0 t 放热b kJ
下列叙述正确的是( )
A.对于上述反应,①②中反应的平衡常数K不同
B.①中:从开始至10 min内的平均反应速率v(X )=0.1 mol·L-1·min-1
2
C.②中:X 的平衡转化率小于10%
2
D.b>0.1a
3.已知:2CrO+2H+Cr O+HO。25 ℃时,调节初始浓度为1.0 mol·L-1的NaCrO 溶
2 2 2 4
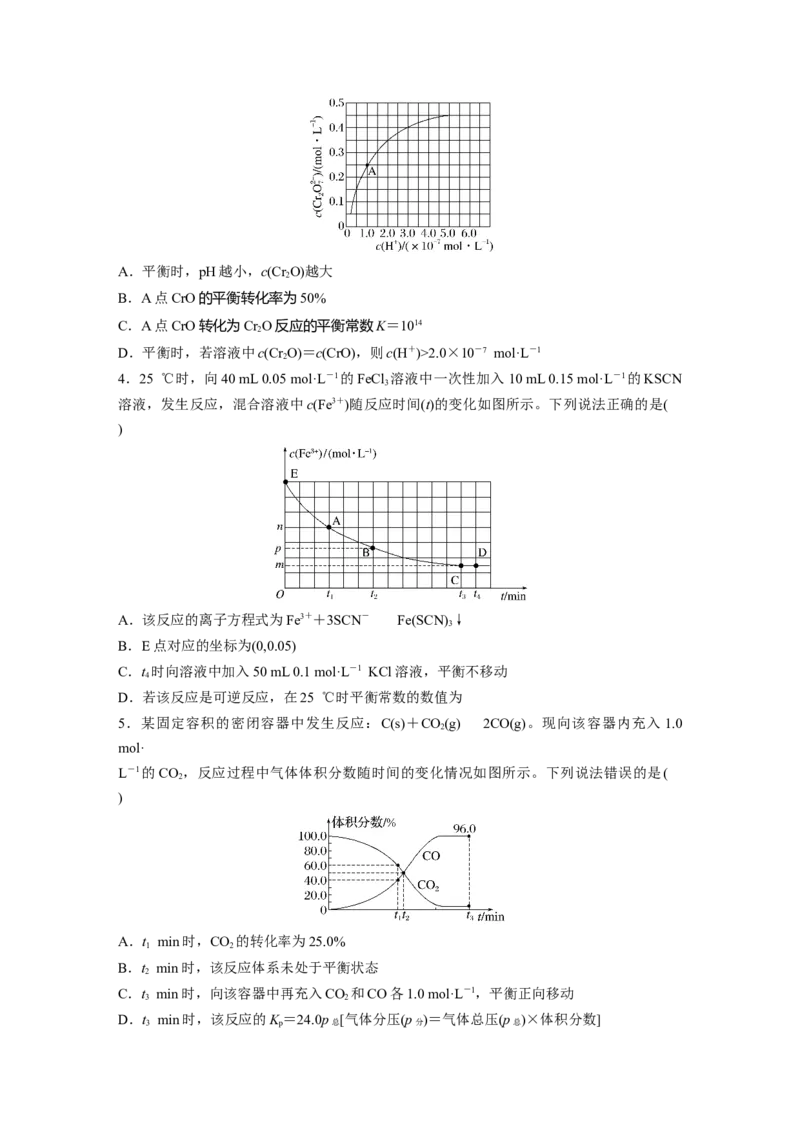
液的pH,测定平衡时溶液中c(CrO)和c(H+),获得如图所示的曲线。下列说法不正确的是(
2
)A.平衡时,pH越小,c(CrO)越大
2
B.A点CrO的平衡转化率为50%
C.A点CrO转化为Cr O反应的平衡常数K=1014
2
D.平衡时,若溶液中c(CrO)=c(CrO),则c(H+)>2.0×10-7 mol·L-1
2
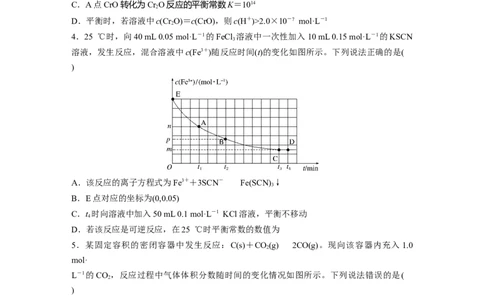
4.25 ℃时,向40 mL 0.05 mol·L-1的FeCl 溶液中一次性加入10 mL 0.15 mol·L-1的KSCN
3
溶液,发生反应,混合溶液中c(Fe3+)随反应时间(t)的变化如图所示。下列说法正确的是(
)
A.该反应的离子方程式为Fe3++3SCN-Fe(SCN) ↓
3
B.E点对应的坐标为(0,0.05)
C.t 时向溶液中加入50 mL 0.1 mol·L-1 KCl溶液,平衡不移动
4
D.若该反应是可逆反应,在25 ℃时平衡常数的数值为
5.某固定容积的密闭容器中发生反应:C(s)+CO(g)2CO(g)。现向该容器内充入1.0
2
mol·
L-1的CO ,反应过程中气体体积分数随时间的变化情况如图所示。下列说法错误的是(
2
)
A.t min时,CO 的转化率为25.0%
1 2
B.t min时,该反应体系未处于平衡状态
2
C.t min时,向该容器中再充入CO 和CO各1.0 mol·L-1,平衡正向移动
3 2
D.t min时,该反应的K =24.0p [气体分压(p )=气体总压(p )×体积分数]
3 p 总 分 总6.在容积恒为2 L的密闭容器中充入2 mol CH OH(g)和2 mol CO(g),在一定温度下发生反
3
应:CHOH(g)+CO(g)HCOOCH (g),测得容器内的压强随时间的变化如下表所示。
3 3
t/min 0 2 4 6 8 10 12 14
p/kPa p - 0.8p - - 0.7p 0.7p 0.7p
0 0 0 0 0
在此条件,0~4 min的v(CHOH)=______kPa·min-1,该反应的平衡常数K =______kPa-
3 p
1(以分压表示,分压=总压×物质的量分数)。
7 . 1 mol CH CHOH 和 1 mol H O 充 入 恒 容 密 闭 容 器 中 发 生 反 应 : 2CO(g) +
3 2 2
4H(g)CHCHOH(g)+HO(g),在550 K时,气体混合物中H 的物质的量分数x(H )与反
2 3 2 2 2 2
应时间t的关系如表所示。
t/min 0 20 40 60 80 100
x(H )/% 0 15 29 40 48 48
2
上 述 反 应 中 , 正 反 应 速 率 v 正 = k 正 ·x2(CO)·x4(H 2 ) , 逆 反 应 速 率 v 逆 = k
·x(CHCHOH)·x(H O),其中k 、k 为速率常数,则k =______________(以K 和k 表
逆 3 2 2 正 逆 逆 x 正
示,其中K 为用物质的量分数表示的平衡常数),若k =75 mol·L-1·min-1,在t=80 min时
x 逆
v逆 =______________。
8.乙烷在一定条件下可脱氢制得乙烯:C H(g)C H(g)+H(g) ΔH>0。
2 6 2 4 2
(1)提高乙烷平衡转化率的措施有________________________________、______________。
(2)一定温度下,向恒容密闭容器中通入等物质的量的 C H 和H ,初始压强为100 kPa,发
2 6 2
生上述反应,乙烷的平衡转化率为20%。平衡时体系的压强为________kPa,该反应的平衡
常数K =________kPa (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
p
9.已知:NO(g)2NO (g) ΔH>0。298 K时,将一定量NO 气体充入恒容的密闭容器
2 4 2 2 4
中发生反应。t 时刻反应达到平衡,混合气体平衡总压强为 p,NO 气体的平衡转化率为
1 2 4
25%,则NO 的分压为________(分压=总压×物质的量分数),反应NO(g)2NO (g)的平
2 2 4 2
衡常数K =________[对于气相反应,用某组分B的物质的量分数x(B)代替物质的量浓度
x
c(B)也可表示平衡常数,记作K]。
x
10.亚硝酰氯(NOCl)是有机合成中的重要试剂,可由 NO和Cl 反应得到,化学方程式为
2
2NO(g)+Cl(g)2NOCl(g)。
2
(1)在1 L恒容密闭容器中充入2 mol NO(g)和1 mol Cl (g),在不同温度下测得c(NOCl)与时
2
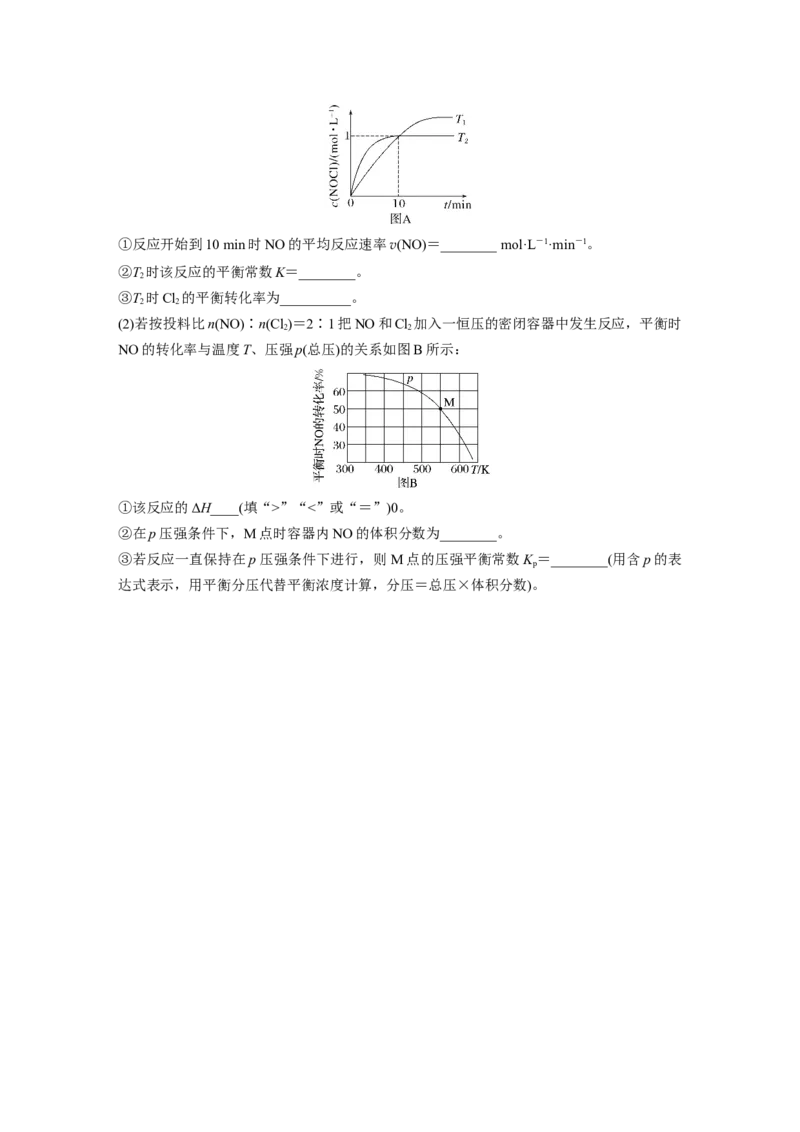
间t的关系如图A所示:①反应开始到10 min时NO的平均反应速率v(NO)=________ mol·L-1·min-1。
②T 时该反应的平衡常数K=________。
2
③T 时Cl 的平衡转化率为__________。
2 2
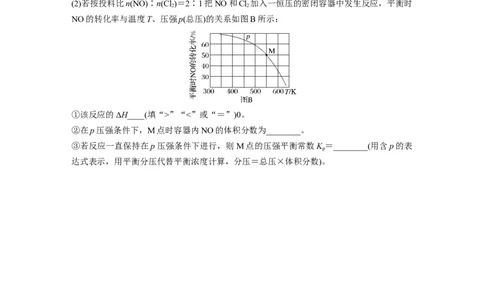
(2)若按投料比n(NO)∶n(Cl )=2∶1把NO和Cl 加入一恒压的密闭容器中发生反应,平衡时
2 2
NO的转化率与温度T、压强p(总压)的关系如图B所示:
①该反应的ΔH____(填“>”“<”或“=”)0。
②在p压强条件下,M点时容器内NO的体积分数为________。
③若反应一直保持在p压强条件下进行,则M点的压强平衡常数K =________(用含p的表
p
达式表示,用平衡分压代替平衡浓度计算,分压=总压×体积分数)。