文档内容
第 47 讲 化学平衡常数的计算
[复习目标] 1.掌握平衡常数和平衡转化率计算的一般方法。2.了解速率常数与化学平衡常
数的关系并能进行有关计算。
考点一 化学平衡常数与平衡转化率的计算
1.常用的四个公式
公式 备注
反应物的转化率 ×100%=×100%
①平衡量可以是物质的量、
生成物的产率 ×100%
气体的体积;
平衡时混合物组分
×100% ②某组分的体积分数,也可
的百分含量
以是物质的量分数
某组分的体积分数 ×100%
2.平衡常数的计算步骤
(1)写出有关可逆反应的化学方程式,写出平衡常数表达式。
(2)利用“三段式”(见化学反应速率及影响因素),确定各物质的起始浓度、转化浓度、平衡
浓度。
(3)将平衡浓度代入平衡常数表达式。
(4)注意单位的统一。
3.压强平衡常数
(1)以aA(g)+bB(g)cC(g)+dD(g)为例,
K =[p(X):X在平衡体系中物质的量分数(或体积分数)×总压强]。
p
(2)计算方法
①根据“三段式”法计算平衡体系中各物质的物质的量或物质的量浓度。
②计算各气体组分的物质的量分数或体积分数。
③根据分压计算公式求出各气体物质的分压,某气体的分压=气体总压强×该气体的体积分
数(或物质的量分数)。
④根据平衡常数计算公式代入计算。
例 一定温度和催化剂条件下,将1 mol N 和3 mol H 充入压强为p 的恒压容器中,测得平
2 2 0
衡时N 的转化率为50%,计算该温度下的压强平衡常数(K )。
2 p
________________________________________________________________________________________________________________________________________________
一、平衡常数与转化率的相关计算
1.已知在密闭容器中发生可逆反应:M(g)+N(g)P(g)+Q(g) ΔH>0。某温度下,反应
物的起始浓度分别为c(M)=1 mol·L-1,c(N)=2.4 mol·L-1。
思考并解答下列问题:
(1)若达到平衡后,M的转化率为60%,列出“三段式”,计算此时N的平衡浓度是多少?
平衡常数K是多少?
_______________________________________________________________________________
(2)若反应温度不变,反应物的起始浓度分别为 c(M)=4 mol·L-1,c(N)=a mol·L-1;达到
平 衡 后 , c(P) = 2 mol·L - 1 , 则 M 的 转 化 率 为
____________________________________________,
N的起始浓度为________。
2.(2021·重庆1月适应性测试,17)内酯在化工、医药、农林等领域有广泛的应用。内酯可
以通过有机羧酸异构化制得。某羧酸A在0.2 mol·L-1盐酸中转化为内酯B的反应可表示为
A(aq)B(aq),忽略反应前后溶液体积变化。一定温度下,当A的起始浓度为a mol·L-1时,
A的转化率随时间的变化如下表所示:
t/min 0 21 36 50 65 80 100 ∞
A的转化率/% 0 13.3 20.0 27.8 33.3 40.0 45.0 75.0
(1)反应进行到100 min时,B的浓度为________ mol·L-1。
(2)v正 (t=50 min)________(填“>”“<”或“=”)v逆 (t=∞ min)。
(3)增加A的起始浓度,A在t=∞ min时转化率将________(填“增大”“减小”或“不
变”)。
(4)该温度下,平衡常数K=________;在相同条件下,若反应开始时只加入B,B的起始浓
度也为a mol·L-1,平衡时B的转化率为________。
(5)研究发现,其他条件不变时,减小盐酸的浓度,反应速率减慢,但平衡时B的含量不变,
原因是_______________________________________________________________________。
二、压强平衡常数
3.设K为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替
浓度。气体的相对分压等于其分压(单位为kPa)除以p(p =100 kPa)。在某温度下,原料组
0 0
成n(CO)∶n(NO)=1∶1,发生反应:2CO(g)+2NO(g)N(g)+2CO(g),初始总压为100
2 2
kPa的恒容密闭容器中进行上述反应,体系达到平衡时N 的分压为20 kPa,则该反应的相对
2
压力平衡常数K=________。
4.在一刚性密闭容器中,CH 和CO 的分压分别为20 kPa、25 kPa,加入Ni/α-Al O 催化剂
4 2 2 3并加热至1 123 K使其发生反应:CH(g)+CO(g)2CO(g)+2H(g)。达到平衡后测得体系
4 2 2
压强是起始时的1.8倍,则该反应的平衡常数的计算式为 K =____________ kPa2(用各物质
p
的分压代替物质的量浓度计算)。
考点二 化学平衡常数与速率常数的关系
正、逆反应的速率常数与平衡常数的关系
对于基元反应aA(g)+bB(g)cC(g)+dD(g),v正 =k
正
·ca(A)·cb(B),v逆 =k
逆
·cc(C)·cd(D),平
衡常数K==,反应达到平衡时v正 =v逆 ,故K=。
例 温度为 T ,在三个容积均为 1 L 的恒容密闭容器中仅发生反应:CH(g)+
1 4
H 2 O(g)CO(g)+3H 2 (g) ΔH=+206.3 kJ·mol-1,该反应中,正反应速率为 v 正 =k
正
·c(CH
4
)·c(H
2
O),逆反应速率为v逆 =k
逆
·c(CO)·c3(H
2
),k
正
、k
逆
为速率常数,受温度影响。
已知T 时,k =k ,则该温度下,平衡常数K =________;当温度改变为T 时,若k =
1 正 逆 1 2 正
1.5k ,则T________(填“>”“=”或“<”)T。
逆 2 1
1.利用NH 的还原性可以消除氮氧化物的污染,其中除去NO的主要反应如下:
3
4NH (g)+6NO(g)5N(g)+6HO(l) ΔH<0
3 2 2
已知该反应速率v正 =k
正
·c4(NH
3
)·c6 (NO),v逆 =k
逆
·cx(N
2
)·cy(H
2
O) (k
正
、k
逆
分别是正、逆反
应速率常数),该反应的平衡常数K=,则x=________,y=________。
2.乙烯气相直接水合法过程中会发生乙醇的异构化反应:C HOH(g)CHOCH (g) ΔH
2 5 3 3
=+50.7 kJ·mol-1,该反应的速率方程可表示为 v 正 =k 正 ·c(C 2 H 5 OH)和 v 逆 =k
·c(CHOCH ),k 和k 只与温度有关。该反应的活化能 E ________(填“>”“=”或
逆 3 3 正 逆 a(正)
“<”)E ,已知:T ℃时,k =0.006 s-1,k =0.002 s-1,该温度下向某恒容密闭容器中
a(逆) 正 逆
充入1.5 mol乙醇和
4 mol甲醚,此时反应________(填“正向”或“逆向”)进行。
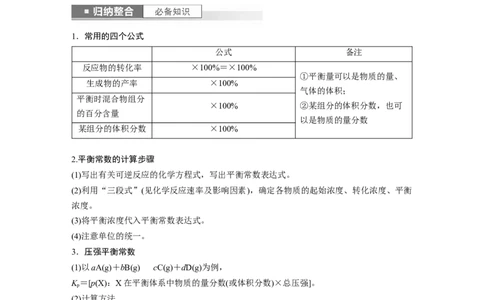
3.肌肉中的肌红蛋白(Mb)与 O 结合生成 MbO ,其反应原理可表示为 Mb(aq)+
2 2
O(g)MbO (aq),该反应的平衡常数可表示为K=。在37 ℃条件下达到平衡时,测得肌
2 2
红蛋白的结合度(α)与 p(O 2 )的关系如图所示[α=×100%]。研究表明正反应速率 v 正 =k
正
·c(Mb) · p(O
2
),逆反应速率v逆 =k
逆
·c(MbO
2
)(其中k
正
和k
逆
分别表示正反应和逆反应的速
率常数)。(1)试写出平衡常数K与速率常数k 、k 之间的关系式为K=________(用含有k 、k 的式
正 逆 正 逆
子表示)。
(2)试求出图中c点时,上述反应的平衡常数K=________ kPa-1。已知k =60 s-1,则速率
逆
常数k =______s-1·kPa-1。
正
4.(2022·青岛高三模拟)乙烯、环氧乙烷是重要的化工原料,用途广泛。
实验测得 2CH
2
===CH
2
(g)+O
2
(g)2 (g) ΔH<0 中,v
逆
=k
逆
·c2( ),v
正
=k
·c2(CH===CH)·c(O )(k 、k 为速率常数,只与温度有关)。
正 2 2 2 正 逆
(1)反应达到平衡后,仅降低温度,下列说法正确的是________(填字母)。
A.k 、k 均增大,且k 增大的倍数更多
正 逆 正
B.k 、k 均减小,且k 减小的倍数更少
正 逆 正
C.k 增大、k 减小,平衡正向移动
正 逆
D.k 、k 均减小,且k 减小的倍数更少
正 逆 逆
(2)若在1 L的密闭容器中充入1 mol CH ===CH(g)和1 mol O (g),在一定温度下只发生上述
2 2 2
反应,经过10 min反应达到平衡,体系的压强变为原来的0.875倍,则0~10 min内v(O )=
2
____________,=________。
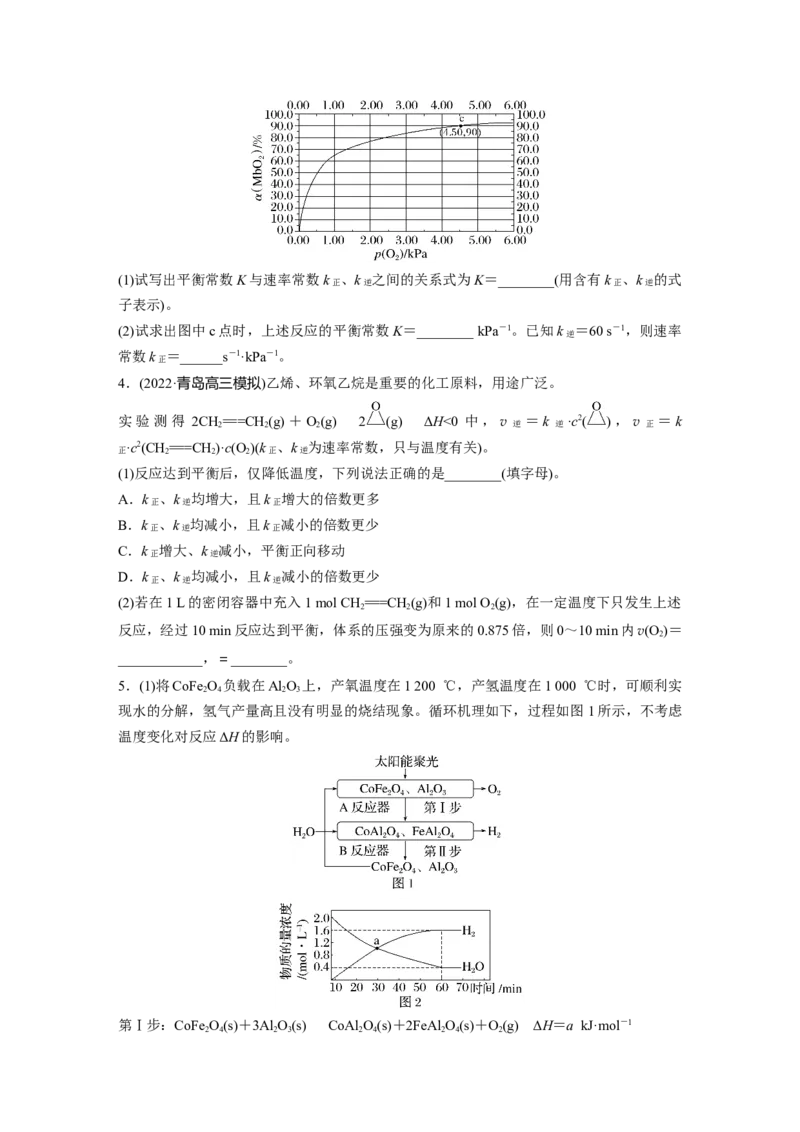
5.(1)将CoFe O 负载在Al O 上,产氧温度在1 200 ℃,产氢温度在1 000 ℃时,可顺利实
2 4 2 3
现水的分解,氢气产量高且没有明显的烧结现象。循环机理如下,过程如图1所示,不考虑
温度变化对反应ΔH的影响。
第Ⅰ步:CoFe O(s)+3Al O(s)CoAl O(s)+2FeAl O(s)+O(g) ΔH=a kJ·mol-1
2 4 2 3 2 4 2 4 2第Ⅱ步:CoAl O(s)+2FeAl O(s)+HO(g)CoFe O(s)+3Al O(s)+H(g) ΔH=b kJ·
2 4 2 4 2 2 4 2 3 2
mol-1
第Ⅱ步反应的v正 =k
正
·c(H
2
O),v逆 =k
逆
·c(H
2
),k
正
、k
逆
分别为正、逆反应速率常数,仅与
温度有关。1 000 ℃时,在体积为1 L的B反应器中加入2 mol H O发生上述反应,测得
2
HO(g)和 H 物质的量浓度随时间的变化如图 2 所示,则 60 min 内,v(CoFe O)=
2 2 2 4
________g·min-1(结果保留2位小数)。a点时,v正 ∶v逆 =________(填最简整数比)。
(2)在T K、1.0×104 kPa下,等物质的量的CO与CH 混合气体发生如下反应:CO(g)+
2 4
CH
4
(g)CH
3
CHO(g)。反应速率v正 -v逆 =k
正
·p(CO)·p(CH
4
)-k
逆
·p(CH
3
CHO),k
正
、k
逆
分
别为正、逆反应速率常数,p为气体的分压(气体分压p=气体总压p ×体积分数)。用气体
总
分压表示的平衡常数K =4.5×10-5 kPa-1,则CO的转化率为20%时,=________。
p
1.(2017·全国卷Ⅰ,28节选)HS与CO 在高温下发生反应:HS(g)+CO(g)COS(g)+
2 2 2 2
HO(g)。在610 K时,将0.10 mol CO 与0.40 mol H S充入2.5 L的空钢瓶中,反应平衡后水
2 2 2
的物质的量分数为0.02。
(1)H S的平衡转化率α=________%,反应平衡常数K=________(保留三位有效数字)。
2 1
(2)在620 K时重复实验,平衡后水的物质的量分数为0.03,HS的转化率α______(填“>”
2 2
“<”或“=”,下同)α,该反应的ΔH______0。
1
2.[2019·全国卷Ⅱ,27(2)节选]某温度下,等物质的量的碘和环戊烯( )在刚性容器内发
生反应: (g)+I(g) (g)+2HI(g) ΔH>0,起始总压为105 Pa,平衡时总压增加
2
了20%,环戊烯的转化率为________________,该反应的平衡常数K =____________Pa。
p
3.(2022·全国甲卷,28节选)(1)TiO 转化为TiCl 有直接氯化法和碳氯化法。在1 000 ℃时
2 4
反应的热化学方程式及其平衡常数如下:
(ⅰ)直接氯化:TiO(s)+2Cl(g)===TiCl (g)+O(g) ΔH=+172 kJ·mol-1,K =1.0×10-2
2 2 4 2 1 p1
(ⅱ)碳氯化:TiO(s)+2Cl(g)+2C(s)===TiCl (g)+2CO(g) ΔH =-51 kJ·mol-1,K =
2 2 4 2 p2
1.2×1012Pa
反应2C(s)+O(g)===2CO(g)的ΔH为________kJ·mol-1,K =__________Pa。
2 p
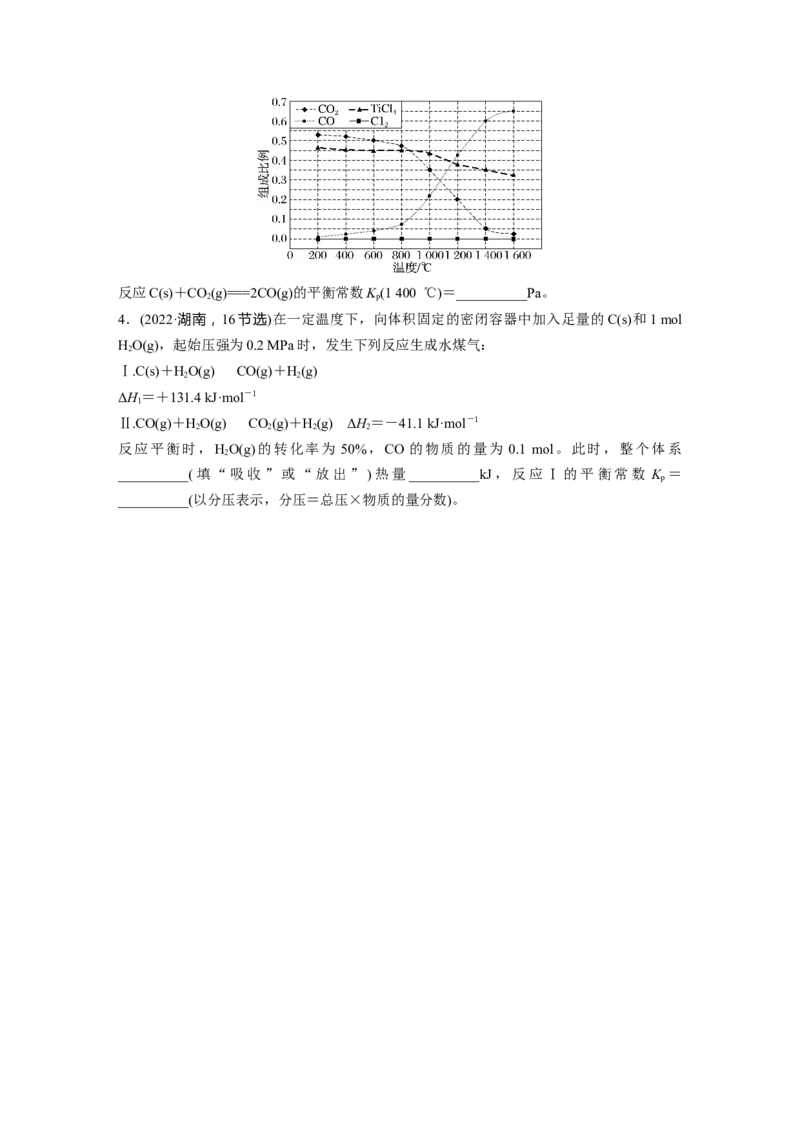
(2)在1.0×105 Pa,将TiO 、C、Cl 以物质的量比1∶2.2∶2进行反应。体系中气体平衡组
2 2
成比例(物质的量分数)随温度变化的理论计算结果如图所示。反应C(s)+CO(g)===2CO(g)的平衡常数K (1 400 ℃)=__________Pa。
2 p
4.(2022·湖南,16节选)在一定温度下,向体积固定的密闭容器中加入足量的C(s)和1 mol
HO(g),起始压强为0.2 MPa时,发生下列反应生成水煤气:
2
Ⅰ.C(s)+HO(g)CO(g)+H(g)
2 2
ΔH=+131.4 kJ·mol-1
1
Ⅱ.CO(g)+HO(g)CO(g)+H(g) ΔH=-41.1 kJ·mol-1
2 2 2 2
反应平衡时,HO(g)的转化率为 50%,CO 的物质的量为 0.1 mol。此时,整个体系
2
__________(填“吸收”或“放出”)热量__________kJ,反应Ⅰ的平衡常数 K =
p
__________(以分压表示,分压=总压×物质的量分数)。