文档内容
第 48 讲 影响化学平衡的因素
[复习目标] 1.掌握外界条件改变对化学平衡的影响和勒夏特列原理。2.掌握新旧平衡状态
比较的一般方法和思路。
考点一 化学平衡的移动
1.含义
在一定条件下,当可逆反应达到化学平衡状态后,如果改变影响平衡的条件(如____、
______、______等),化学平衡状态被破坏(正、逆反应速率不再相等),平衡体系的物质组
成也会随着改变,直至正、逆反应速率再次______,在新的条件下达到新的化学平衡状态。
这种由原有的平衡状态达到新的平衡状态的过程叫做化学平衡的移动,简称平衡移动。
2.平衡移动方向的判断
(1)根据速率判断
①若v正 ____v逆 ,则平衡向正反应方向移动。
②若v正 ____v逆 ,则平衡不移动。
③若v正 ____v逆 ,则平衡向逆反应方向移动。
(2)根据体系中各组分含量的变化判断
平衡移动的结果,如果是使体系中产物含量(如物质的量、浓度或百分含量等)______,则
平衡正向移动;反之则逆向移动。
3.外界因素对化学平衡的影响
条件的改变(其他条件不变) 化学平衡的移动
增大反应物浓度或减小生成物浓度 向________方向移动
浓度
减小反应物浓度或增大生成物浓度 向________方向移动
向________________的
增大压强
压强(对有 反应前后气体分子数 方向移动
气体参加 改变 向________________的
减小压强
的反应) 方向移动
反应前后气体分子数 改变压强不变
升高温度 向______反应方向移动
温度
降低温度 向______反应方向移动
催化剂 使用催化剂
4.充入与反应无关的气体与平衡移动的关系
5.勒夏特列原理
如果改变影响平衡的一个因素(如浓度、压强或温度),平衡就向着能够______这种改变的
方向移动,这就是勒夏特列原理,也称化学平衡移动原理。
1.升高温度,平衡向吸热反应方向移动,此时v 减小,v 增大( )
放 吸
2.化学平衡正向移动,反应物的转化率一定增大( )
3.向平衡体系FeCl +3KSCNFe(SCN) +3KCl中加入适量KCl固体,平衡逆向移动,
3 3
溶液的颜色变浅( )
4.对于2NO (g)NO(g)的平衡体系,压缩体积,增大压强,平衡正向移动,混合气体
2 2 4
的颜色变浅( )
5.C(s)+CO(g)2CO(g) ΔH>0,其他条件不变时,升高温度,反应速率v(CO)和CO
2 2 2
的平衡转化率均增大( )
6.只要v 增大,平衡一定正向移动( )
正
1.COCl (g)CO(g)+Cl(g) ΔH>0,当反应达到平衡时,下列措施:①升温、②恒容通
2 2
入惰性气体、③增加CO的浓度、④减压、⑤加催化剂、⑥恒压通入惰性气体,能提高
COCl 转化率的是( )
2
A.①②④ B.①④⑥ C.②③⑤ D.③⑤⑥
2.(2022·浦东新区模拟)可逆反应mA(g)+nB(?)pC(g)+qD(?)中A和C都是无色气体,
当达到平衡后,下列叙述正确的是( )
A.若改变条件后,平衡正向移动,D的百分含量一定增大
B.若升高温度,A的浓度增大,说明正反应是吸热反应C.若增大压强,平衡不移动,说明m+n一定等于p+q
D.若增加B的量,平衡移动后体系颜色加深,说明B必是气体
3.在压强为0.1 MPa、温度为300 ℃条件下,a mol CO与3a mol H 的混合气体在催化剂
2
作用下发生反应生成甲醇:CO(g)+2H(g)CHOH(g) ΔH<0。
2 3
(1)平衡后将容器的容积压缩到原来的一半,其他条件不变,对平衡体系产生的影响是
________(填字母,下同)。
A.c(H )减小
2
B.正反应速率加快,逆反应速率减慢
C.反应物转化率增大
D.重新达到平衡时减小
(2)若容器容积不变,下列措施可增大甲醇产率的是________。
A.升高温度
B.将CHOH从体系中分离
3
C.充入He,使体系总压强增大
考点二 平衡移动方向与转化率的判断
反应aA(g)+bB(g)cC(g)+dD(g)的转化率分析
(1)若反应物起始物质的量之比等于化学计量数之比,达到平衡后,它们的转化率相等。
(2)若只增加A的量,平衡正向移动,B的转化率增大,A的转化率减小。
(3)若按原比例同倍数地增加(或降低)A、B的浓度,等效于压缩(或扩大)容器体积,气体反
应物的转化率与化学计量数有关。
同倍数增大c(A)和c(B)
应用举例
对于以下三个反应,从反应开始进行到达到平衡后,保持温度、体积不变,按要求回答下
列问题。
(1)PCl (g)PCl (g)+Cl(g)
5 3 2
再充入 PCl (g),平衡向________方向移动,达到平衡后,PCl (g)的转化率________,
5 5
PCl (g)的百分含量______。
5
(2)2HI(g)I(g)+H(g)
2 2
再充入HI(g),平衡向________方向移动,达到平衡后,HI(g)的分解率__________,HI(g)
的百分含量________。
(3)2NO (g)NO(g)
2 2 4再充入 NO (g),平衡向________方向移动,达到平衡后,NO (g)的转化率________,
2 2
NO (g)的百分含量________。
2
(4)mA(g)+nB(g)pC(g)
同等倍数的加入A(g)和B(g),平衡________移动,达到平衡后,①m+n>p,A、B的转化
率都________,体积分数都________;②m+n=p,A、B的转化率、体积分数都________;
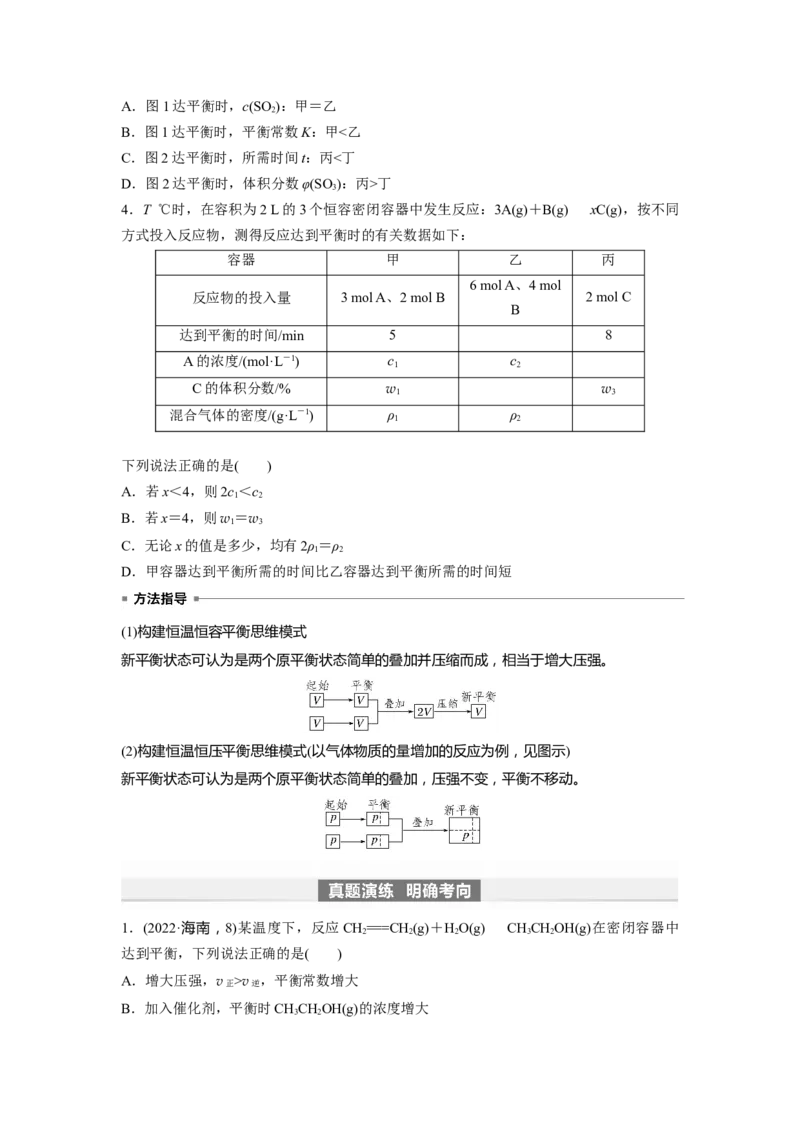
③m+n丁
3
4.T ℃时,在容积为2 L的3个恒容密闭容器中发生反应:3A(g)+B(g)xC(g),按不同
方式投入反应物,测得反应达到平衡时的有关数据如下:
容器 甲 乙 丙
6 mol A、4 mol
反应物的投入量 3 mol A、2 mol B 2 mol C
B
达到平衡的时间/min 5 8
A的浓度/(mol·L-1) c c
1 2
C的体积分数/% w w
1 3
混合气体的密度/(g·L-1) ρ ρ
1 2
下列说法正确的是( )
A.若x<4,则2c<c
1 2
B.若x=4,则w=w
1 3
C.无论x的值是多少,均有2ρ=ρ
1 2
D.甲容器达到平衡所需的时间比乙容器达到平衡所需的时间短
(1)构建恒温恒容平衡思维模式
新平衡状态可认为是两个原平衡状态简单的叠加并压缩而成,相当于增大压强。
(2)构建恒温恒压平衡思维模式(以气体物质的量增加的反应为例,见图示)
新平衡状态可认为是两个原平衡状态简单的叠加,压强不变,平衡不移动。
1.(2022·海南,8)某温度下,反应CH===CH(g)+HO(g)CHCHOH(g)在密闭容器中
2 2 2 3 2
达到平衡,下列说法正确的是( )
A.增大压强,v正 >v逆 ,平衡常数增大
B.加入催化剂,平衡时CHCHOH(g)的浓度增大
3 2C.恒容下,充入一定量的HO(g),平衡向正反应方向移动
2
D.恒容下,充入一定量的CH===CH(g),CH===CH(g)的平衡转化率增大
2 2 2 2
2.(2020·浙江7月选考,20)一定条件下:2NO (g)NO(g) ΔH<0。在测定NO 的相对
2 2 4 2
分子质量时,下列条件中,测定结果误差最小的是( )
A.温度0 ℃、压强50 kPa
B.温度130 ℃、压强300 kPa
C.温度25 ℃、压强100 kPa
D.温度130 ℃、压强50 kPa
3.[2022·河北,16(2)①]工业上常用甲烷、水蒸气重整制备氢气,体系中发生如下反应。
Ⅰ.CH (g)+HO(g)CO(g)+3H(g)
4 2 2
Ⅱ.CO(g)+HO(g)CO(g)+H(g)
2 2 2
下列操作中,能提高CH(g)平衡转化率的是_________(填字母)。
4
A.增加CH(g)用量 B.恒温恒压下通入惰性气体
4
C.移除CO(g) D.加入催化剂
4.[2022·湖南,16(1)①]在一定温度下,向体积固定的密闭容器中加入足量的C(s)和1 mol
HO(g),起始压强为0.2 MPa时,发生下列反应生成水煤气:
2
Ⅰ.C(s)+HO(g)CO(g)+H(g) ΔH=+131.4 kJ·mol-1
2 2 1
Ⅱ.CO(g)+HO(g)CO(g)+H(g) ΔH=-41.1 kJ·mol-1
2 2 2 2
下列说法正确的是__________。
A.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
B.混合气体的密度保持不变时,说明反应体系已达到平衡
C.平衡时H 的体积分数可能大于
2
D.将炭块粉碎,可加快反应速率