文档内容
1.下列事实不能用勒夏特列原理解释的是( )
A.溴水中有下列平衡:Br +HOHBr+HBrO,当加入少量AgNO 溶液后,溶液的颜
2 2 3
色变浅
B.对于反应:2HI(g)H(g)+I(g),缩小容器的容积可使平衡体系的颜色变深
2 2
C.反应:CO(g)+NO (g)CO(g)+NO(g) ΔH<0,升高温度可使平衡向逆反应方向移动
2 2
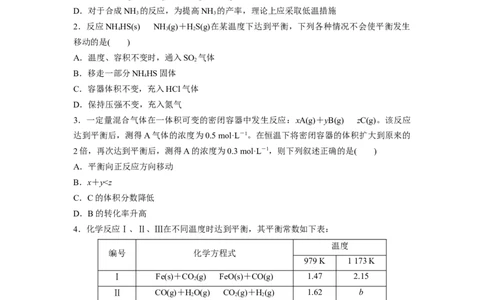
D.对于合成NH 的反应,为提高NH 的产率,理论上应采取低温措施
3 3
2.反应NH HS(s)NH (g)+HS(g)在某温度下达到平衡,下列各种情况不会使平衡发生
4 3 2
移动的是( )
A.温度、容积不变时,通入SO 气体
2
B.移走一部分NH HS固体
4
C.容器体积不变,充入HCl气体
D.保持压强不变,充入氮气
3.一定量混合气体在一体积可变的密闭容器中发生反应:xA(g)+yB(g)zC(g)。该反应
达到平衡后,测得A气体的浓度为0.5 mol·L-1。在恒温下将密闭容器的体积扩大到原来的
2倍,再次达到平衡后,测得A的浓度为0.3 mol·L-1,则下列叙述正确的是( )
A.平衡向正反应方向移动
B.x+y-197 kJ·mol-1
3 1 1
8.如图所示,向A中充入1 mol X和1 mol Y,向B中充入2 mol X和2 mol Y,起始V =
A
V =a L,在相同温度和有催化剂的条件下,两容器中各自发生下列反应:X(g)+
B
Y(g)2Z(g)+W(g) ΔH>0;达到平衡时,V =1.2a L,则下列说法不正确的是( )
A
A.反应开始时,B容器中化学反应速率快B.A容器比B容器中X的转化率大
C.打开K一段时间达平衡时,A的体积为2.4a L(连通管中气体体积不计)
D.打开K达新平衡后,升高B容器温度,A容器体积会增大
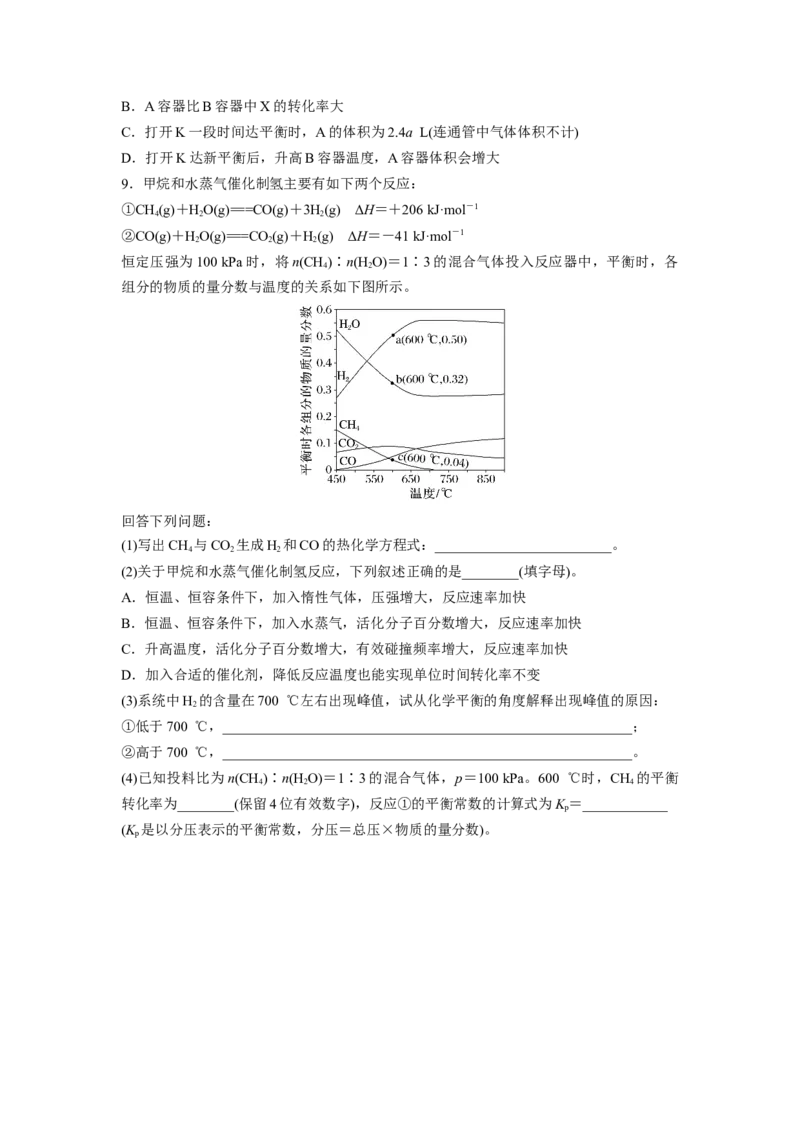
9.甲烷和水蒸气催化制氢主要有如下两个反应:
①CH(g)+HO(g)===CO(g)+3H(g) ΔH=+206 kJ·mol-1
4 2 2
②CO(g)+HO(g)===CO(g)+H(g) ΔH=-41 kJ·mol-1
2 2 2
恒定压强为100 kPa时,将n(CH)∶n(H O)=1∶3的混合气体投入反应器中,平衡时,各
4 2
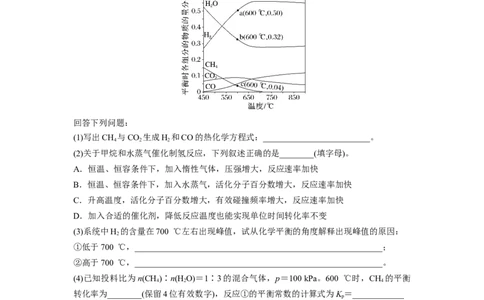
组分的物质的量分数与温度的关系如下图所示。
回答下列问题:
(1)写出CH 与CO 生成H 和CO的热化学方程式:_________________________。
4 2 2
(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是________(填字母)。
A.恒温、恒容条件下,加入惰性气体,压强增大,反应速率加快
B.恒温、恒容条件下,加入水蒸气,活化分子百分数增大,反应速率加快
C.升高温度,活化分子百分数增大,有效碰撞频率增大,反应速率加快
D.加入合适的催化剂,降低反应温度也能实现单位时间转化率不变
(3)系统中H 的含量在700 ℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
2
①低于700 ℃,__________________________________________________________;
②高于700 ℃,__________________________________________________________。
(4)已知投料比为n(CH)∶n(H O)=1∶3的混合气体,p=100 kPa。600 ℃时,CH 的平衡
4 2 4
转化率为________(保留4位有效数字),反应①的平衡常数的计算式为K =____________
p
(K 是以分压表示的平衡常数,分压=总压×物质的量分数)。
p