文档内容
第二章 化学物质及其变化
测试卷
时间:90分钟 分值:100分
可能用到的相对原子质量:H 1 C 12 N 14 O16 Na 23 S 32 K 39 Ca 40 Ag 108
一、选择题(每小题只有一个正确选项,共16*3分)
1.(2022·天津南开·二模)下列离子方程式书写正确的是
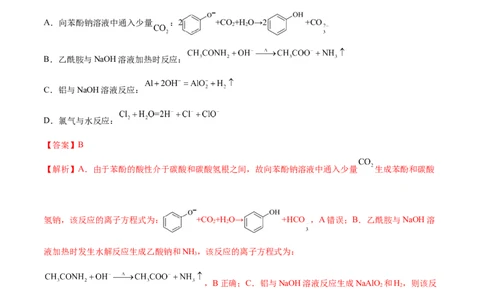
A.向苯酚钠溶液中通入少量 :2 +CO +H O→2 +CO
2 2
B.乙酰胺与NaOH溶液加热时反应:
C.铝与NaOH溶液反应:
D.氯气与水反应:
【答案】B
【解析】A.由于苯酚的酸性介于碳酸和碳酸氢根之间,故向苯酚钠溶液中通入少量 生成苯酚和碳酸
氢钠,该反应的离子方程式为: +CO +H O→ +HCO ,A错误;B.乙酰胺与NaOH溶
2 2
液加热时发生水解反应生成乙酸钠和NH ,该反应的离子方程式为:
3
,B正确;C.铝与NaOH溶液反应生成NaAlO 和H,则该反
2 2
应的离子方程式为: ,C错误;D.已知HClO为弱酸,离子方程式书
写时不能拆,且氯气与水反应是一个可逆反应,故该反应的离子方程式为: ,
D错误;故答案为:B。
2.(2022·上海虹口·模拟预测)侯德榜先生于1943年创立了“侯氏制碱法”。该工艺中一般不涉及的离
子反应是A. B.
C. D.
【答案】D
【解析】A.原理分析可知,侯德榜制碱法,得到碳酸氢钠晶体,涉及Na++HCO →NaHCO ,A不符合题
3
意;B.制备过程中氨气生成碳酸氢铵,最后反应得到氯化铵和碳酸钠,涉及NH + HCO →NH +CO ,
3
B不符合题意;C.向氨化的饱和氯化钠溶液中通入二氧化碳发生反应,涉及NH + H O +CO →HCO +
3 2 2
NH ↑,C不符合题意;D.反应过程中不涉及NH +OH-→NH ↑+H O,D符合题意;故选D。
3 3 2
3.(2022·四川成都·三模)中华诗词中蕴含着丰富的化学知识。下列关于诗词的分析错误的是
A.“ 蜡烛有心还惜别,替人垂泪到天明”,句中蜡烛变化过程只涉及物理变化
B.“梨花院落溶溶月, 柳絮池塘淡淡风”,句中柳絮的主要成分属于糖类
C.“遍身罗绮者,不是养蚕人”,句中的罗绮不可用沸水浸泡
D.“炉火照天地,红星乱紫烟”,句中情境描述了金属的冶炼过程
【答案】A
【解析】A. “ 蜡烛有心还惜别,替人垂泪到天明”,句中蜡烛变化过程中有二氧化碳生成涉及了化学
变化,故A错误;B. “梨花院落溶溶月, 柳絮池塘淡淡风”,句中柳絮的主要成分是纤维素,纤维素
属于糖类,故B正确;C. “遍身罗绮者,不是养蚕人”,句中的罗绮指的是丝绸,它的主要成分是蛋白
质,不可用沸水浸泡,故C错误;D. “炉火照天地,红星乱紫烟”,诗句意思是炉火熊熊燃烧,红星四
溅,紫烟蒸腾,句中情境描述了金属的冶炼过程,故D正确;故答案为:A。
4.(2022·全国·模拟预测)次磷酸( )是一种精细磷化工产品,有强还原性,可冶炼金属。已知:①
,② 。下列推断错
误的是A. 的结构式为
B. 具有强还原性,可使重金属离子变为金属单质
C. 是正盐
D.每消耗2mol ,反应①中转移12mol电子
【答案】D
【解析】A.根据反应②可知 是一元酸,只有—OH中的H原子能够电离,因此 的结构式为
,故A正确;B.由于P元素的最高化合价是+5,而在 中P元素化合价为+1,说
明该物质具有强还原性,可将重金属离子还原为金属单质,故B正确;C.根据A选项可知 是一元
酸,所以 是正盐,故C正确;D.反应①中转移情况为:
可知在反应①中转移电子数是6,说明每有2mol 参加反应,转移6mol电子,故D错误。
故选D。
5.(2022·浙江温州·三模)关于反应2Cu O+Cu S 6Cu+SO↑,下列说法不正确的是
2 2 2
A.Cu O被Cu S还原
2 2
B.Cu S既是氧化剂,又是还原剂
2
C.还原产物与氧化产物的物质的量之比为1∶6D.生成1molSO 时,转移了6mol电子
2
【答案】C
【解析】反应2Cu O+Cu S 6Cu+SO↑中,Cu O中Cu由+1价降低到0价的Cu,发生还原反应;Cu S
2 2 2 2 2
中Cu由+1价降低到0价的Cu,发生还原反应,S由-2价升高到+4价的SO ,发生氧化反应。A.根据分
2
析可知,Cu O被Cu S还原,故A正确;B.根据分析可知,Cu S既发生氧化反应又发生还原反应,故既
2 2 2
是氧化剂,又是还原剂,故B正确;C.还原产物为Cu,氧化产物为SO ,故还原产物与氧化产物的物质
2
的量之比为6∶1,故C错误;D.S由-2价升高到+4价的SO ,故生成1molSO 时,转移了6mol电子,故
2 2
D正确;故选C。
6.(2022·上海·格致中学模拟预测)汞(熔点-39℃, 沸点356℃)是制造电池、电极的重要原料,历史上曾
用“灼烧辰砂法”制取汞,另一主要产物为SO ,目前工业上制粗汞的一种流程图如下:
2
下列分析正确的是
A.洗涤粗汞可用5%的盐酸代替5%的硝酸
B.辰砂与氧化钙加热反应时,CaSO 为还原产物
4
C.“灼烧辰砂法”过程中若2molHgS参加反应转移电子数为6N
A
D.减压蒸馏的目的是降低汞的沸点,提高分离效率
【答案】D
【解析】A.粗汞中含有的金属铜可以和硝酸之间反应,但是和盐酸之间不反应,所以洗涤粗汞不可用5%
的盐酸代替5%的硝酸,故A项错误;B.辰砂与氧化钙加热反应时,化合价升高的是HgS中的S元素,
所以CaSO 是氧化产物,故B项错误;C.“灼烧辰砂法”发生反应方程式:HgS+O Hg+SO ,化学反应
4 2 2
中化合价的升高的元素是S ,从-2价升高到+4价,降低的元素是Hg和O ,化合价升高数=化合价降低数
值=转移电子数=6,故2molHgS参加反应转移电子数为12N ,故C项错误;D.实验目的是获得纯汞,
A
最后一步根据汞的熔点-39°C ,沸点356°C,可以减压蒸馏降低汞的沸点,提高分离效率,故D项正确;
故答案选D。
7.(2022·上海虹口·模拟预测)天然 晶体称为水晶,是古代重要宝石品种。有关 的说法错误的是
A.属于原子晶体 B.属于非电解质 C.属于酸性氧化物 D.含有 键
【答案】D
【解析】A.SiO 属于原子晶体,A正确;B.SiO 难溶于水,在熔融状态下也不能导电,属于非电解质,
2 2
B正确;C.SiO 属于酸性氧化物,能和强碱反应生成硅酸盐和水,C正确;D.SiO 晶体中只含有Si-O键,
2 2
不含Si=O键,D错误;故选D。
8.(2022·上海·格致中学模拟预测)某KCO 样品中含有NaCO、KNO 和Ba(NO ) 三种杂质中的一种或
2 3 2 3 3 3 2
两种,现将13.8g样品加入足量水,样品全部溶解,再加入过量的CaCl 溶液,得到9g沉淀,对样品所含
2
杂质的正确判断是
A.肯定有KNO,没有NaCO
3 2 3
B.肯定没有NaCO 和Ba(NO )
2 3 3 2
C.肯定没有Ba(NO ),可能有KNO
3 2 3
D.肯定有KNO,可能还会有NaCO
3 2 3
【答案】D
【解析】取样品加入水中,样品全部溶解,则不可能存在硝酸钡,加入氯化钙能产生沉淀,然后根据沉淀
的质量利用极值法进一步确定碳酸钠和硝酸钾的存在。假设13.8g全为碳酸钾,根据方程式
可知,产生沉淀为10g,假设13.8g全为碳酸钠,根据方程式
,可知,产生沉淀13g,但是目前产生沉淀9g,说明不可能
仅为碳酸钾或者碳酸钾和碳酸钠的混合物,因此杂质中一定存在硝酸钾,如果只存在一种杂质,则样品中
只有硝酸钾,如果存在两种杂质,则样品中含有硝酸钾和碳酸钠,以上两种情况均有可能。A.肯定存在
硝酸钾,可能存在碳酸钠,A错误;B.肯定没有硝酸钡,但是可能存在碳酸钠,B错误;C.肯定没有硝
酸钡,但是一定存在硝酸钾,C错误;D.肯定存在硝酸钾,可能存在碳酸钠,D正确;故答案选D。
9.(2022·河南开封·模拟预测)下列各组离子在相应条件下一定能大量共存的是
A.pH=14的溶液:K+、Na+、Cl-、ClO-
B.能使甲基橙变红的溶液:K+、Na+、CI-、SO
2C.能使KI淀粉试纸变蓝的溶液:Na+、NH 、S2-、SO
D.能与金属铝反应生成H 的溶液:K+、Ca2+、NO 、HCO
2
【答案】A
【解析】A.pH=14的溶液呈碱性,碱性条件下K+、Na+、Cl-、ClO-相互之间不反应,能大量共存,故选
A;B.能使甲基橙变红的溶液呈酸性,酸性条件下SO 发生歧化反应生成S和二氧化硫,故不选B;
2
C.能使KI淀粉试纸变蓝的溶液具有氧化性,S2-具有还原性,S2-能被氧化,故不选C;D.能与金属铝反
应生成H 的溶液呈酸性或碱性,酸性条件下,硝酸根具有氧化性,与Al反应不放氢气,HCO 与H+反应
2
放出二氧化碳;碱性条件下,HCO 与OH-反应生成 ,故不选D;选A。
10.(2022·黑龙江·哈尔滨三中三模)古诗词是我国传统文化的瑰宝。下列诗词解读不正确的是
A.“朝坛雾卷,曙岭烟沉”,雾有丁达尔现象是因为胶体粒子对光有散射作用
B.“千淘万漉虽辛苦,吹尽黄沙始到金”,利用金和泥沙密度不同而进行淘洗分离
C.“章山之铜,所谓丹阳铜也。今有白铜,盖点化为之,非其本质”,纯铜比白铜硬度大,熔点低
D.“错把陈醋当成墨,写尽半生纸上酸”,陈醋里的醋酸是弱电解质
【答案】C
【解析】A.雾有丁达尔现象是因为胶体粒子对光有散射作用,形成光亮的通路,A正确;B.淘金利用的
是金的密度比较大,B正确;C.白铜为合金,合金比纯铜的硬度大,熔点低,C错误;D.醋酸是弱电解
质,D正确;故选C。
11.(2022·陕西·西安中学模拟预测)自2019年12月份以来,由武汉引发的一场重大疫情席卷中国大地,
专家发现了一种新型冠状肺炎病毒,其形状呈圆形或椭圆形,直径约为60~140nm。下列有关病毒说法不
正确的是
A.病毒携带者打喷嚏或者咳嗽时可能会带出病毒飞沫,其在空气中可以形成胶体
B.用紫外线照射或加热至56℃以上30分钟能有效灭活病毒,原理是使蛋白质变性
C.用含氯消毒剂、过氧乙酸均可有效灭活病毒,原理是运用了消毒剂的强氧化性
D.75%乙醇可以杀灭活病毒,因此可以采用饮用高度白酒的方法消灭病毒
【答案】D
【解析】A.病毒直径约为60~140nm,其在空气中可以形成胶体,故A正确;B.紫外线照射或加热可以使蛋白质变性,故B正确;C.含氯消毒剂、过氧乙酸够具有强氧化性,所以含氯消毒剂、过氧乙酸均可
有效灭活病毒,故C正确;D.高度白酒达不到75%,且高度白酒对人体有伤害,不宜采用饮用高度白酒
的方法消灭病毒,故D错误;选D。
12.(2022·上海·格致中学模拟预测)从硫化物中提取单质锑(Sb)是先在高温下将硫化物转化为氧化物,再
用碳还原:
①2Sb S+3O +6Fe→Sb O + 6FeS
2 3 2 4 6
②Sb O+6C→4Sb +6CO↑
4 6
关于反应①、②的说法正确的是
A.反应①②中的氧化剂分别是Sb S、Sb O
2 3 4 6
B.反应①中每生成3 mol FeS时,共转移6 mol电子
C.反应②说明高温下Sb的还原性比C强
D.每生成4mol Sb时,反应①与反应②中还原剂的物质的量之比为4∶3
【答案】B
【解析】反应①中Fe元素的化合价由0价升至+2价,Fe为还原剂,O元素的化合价由0价降至-2价,O
2
为氧化剂,Sb S 中Sb、S元素的化合价在反应前后都没有改变,Sb S 既不是氧化剂、也不是还原剂;反
2 3 2 3
应②中C元素的化合价由0价升至+2价,C为还原剂,Sb元素的化合价由+3价降至0价,Sb O 为氧化剂。
4 6
A.反应①中Fe元素的化合价由0价升至+2价,Fe为还原剂,O元素的化合价由0价降至-2价,O 为氧
2
化剂,Sb S 中Sb、S元素的化合价在反应前后都没有改变,Sb S 既不是氧化剂、也不是还原剂;反应②
2 3 2 3
中C元素的化合价由0价升至+2价,C为还原剂,Sb元素的化合价由+3价降至0价,Sb O 为氧化剂,A
4 6
项错误;B.反应①中Fe元素的化合价由0价升至+2价,Fe为还原剂,O元素的化合价由0价降至-2价,
O 为氧化剂,反应中每生成6molFeS转移12mol电子,则每生成3molFeS转移6mol电子,B项正确;C.
2
反应②中C元素的化合价由0价升至+2价,C为还原剂,Sb元素的化合价由+3价降至0价,Sb O 为氧化
4 6
剂,Sb为还原产物,则高温下Sb的还原性比C弱,C项错误;D.每生成4molSb,反应②消耗
1molSb O、6molC;反应①生成1molSb O 消耗6molFe,反应①与反应②中还原剂的物质的量之比为
4 6 4 6
6∶6=1∶1,D项错误;答案选B。
13.(2022·浙江绍兴·模拟预测)亚氨基锂(Li NH)是一种安全性好的固体储氢材料,其储氢原理可表示为:
2
。下列有关说法正确的是
A.LiNH中N的化合价是-1 B.该反应中 既是氧化剂又是还原剂
2
C. 和 的离子半径相等 D.此法储氢和钢瓶储氢的原理相同【答案】B
【解析】A.LiNH中H元素为+1价,根据化合物化合价代数和为0,可得氮元素化合价为-3价,A错误;
2
B.反应物H 中H元素化合价为0,产物中LiNH 中H元素为+1价,LiH中H元素为-1价,所以H 既是氧
2 2 2
化剂又是还原剂,B正确;C.Li+有一个电子层,H+核外没有电子层,两者半径不相等,C错误;D.钢瓶
储氢为物理过程,此法储氢为化学变化,两者原理不同,D错误;故答案选B。
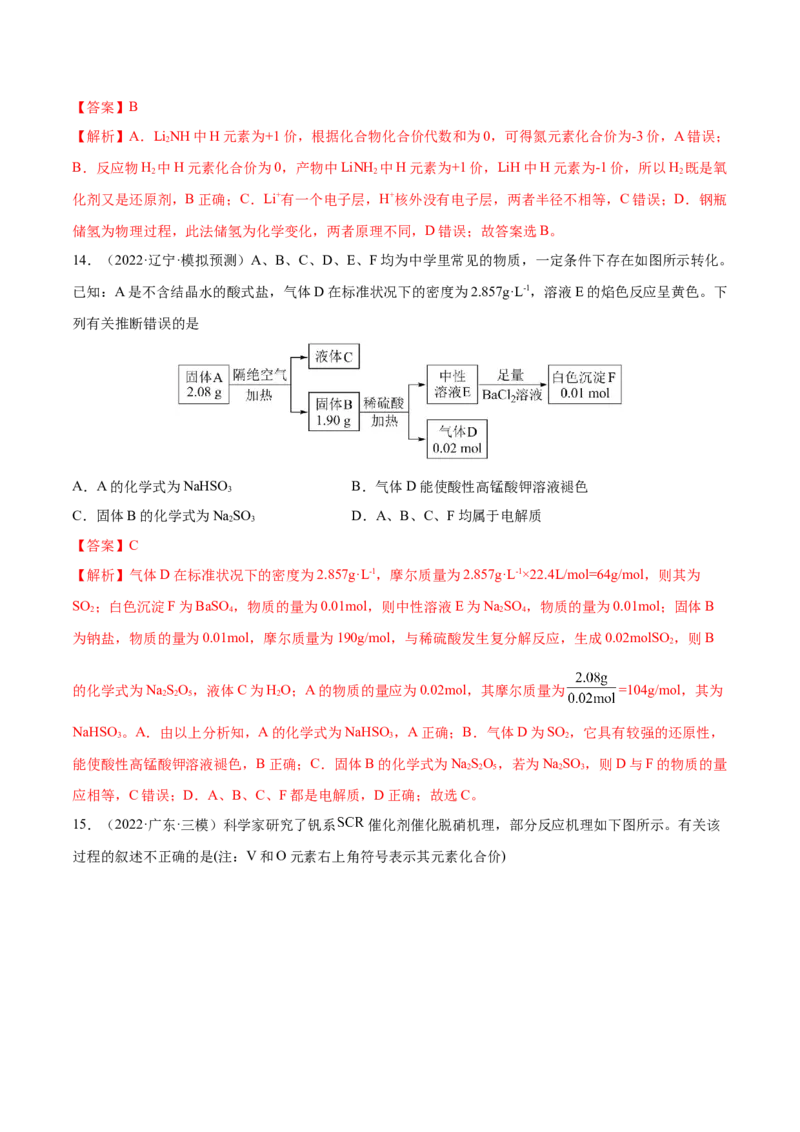
14.(2022·辽宁·模拟预测)A、B、C、D、E、F均为中学里常见的物质,一定条件下存在如图所示转化。
已知:A是不含结晶水的酸式盐,气体D在标准状况下的密度为2.857g·L-1,溶液E的焰色反应呈黄色。下
列有关推断错误的是
A.A的化学式为NaHSO B.气体D能使酸性高锰酸钾溶液褪色
3
C.固体B的化学式为NaSO D.A、B、C、F均属于电解质
2 3
【答案】C
【解析】气体D在标准状况下的密度为2.857g·L-1,摩尔质量为2.857g·L-1×22.4L/mol=64g/mol,则其为
SO ;白色沉淀F为BaSO,物质的量为0.01mol,则中性溶液E为NaSO ,物质的量为0.01mol;固体B
2 4 2 4
为钠盐,物质的量为0.01mol,摩尔质量为190g/mol,与稀硫酸发生复分解反应,生成0.02molSO ,则B
2
的化学式为NaSO,液体C为HO;A的物质的量应为0.02mol,其摩尔质量为 =104g/mol,其为
2 2 5 2
NaHSO。A.由以上分析知,A的化学式为NaHSO,A正确;B.气体D为SO ,它具有较强的还原性,
3 3 2
能使酸性高锰酸钾溶液褪色,B正确;C.固体B的化学式为NaSO,若为NaSO ,则D与F的物质的量
2 2 5 2 3
应相等,C错误;D.A、B、C、F都是电解质,D正确;故选C。
15.(2022·广东·三模)科学家研究了钒系 催化剂催化脱硝机理,部分反应机理如下图所示。有关该
过程的叙述不正确的是(注:V和O元素右上角符号表示其元素化合价)A. 是反应中间体 B.反应过程中V的成键数目发生变化
C.反应过程中 被还原 D.脱硝反应为:
【答案】D
【解析】A.由转化示意图可知, 是反应中间体,故A正确;B. 中V为双键,H-O-
V4+中V为单键,故B正确;C.反应过程中 中V由+5价降低到+4价,故被还原,故C正确;D.
由转化示意图可知,在催化剂作用下脱硝反应为: ,故D错误;故选D。
16.(2022·内蒙古赤峰·模拟预测)三氧化二铬(CrO) 是一种深绿色的固体,熔点很高,难溶于水,其化
2 3
学性质类似于Al O,水溶液中Cr(+3)具有还原性。下列关于Cr O 的说法错误的是
2 3 2 3
A.与稀硫酸反应: Cr O+ 3H SO = Cr(SO )+ 3H O
2 3 2 4 2 4 3 2
B.与NaOH溶液反应: Cr O+ 4OH- = 2 +2H O
2 3 2
C.碱性条件下被HO 氧化为Cr(+6): Cr O+ 3H O+ 4OH- =2 + 5H O
2 2 2 3 2 2 2
D.由于金属性铝强于铬,且铬的熔点较高,故可用铝热法还原Cr O 制取金属铬
2 3
【答案】B
【解析】A.Cr O 呈碱性氧化物的性质,与酸反应生成盐Cr O +3H SO =Cr (SO )+3H O,A项正确;
2 3 2 3 2 4 2 4 3 2
B.Cr O 与碱反应呈现出酸性氧化物,反应产生 ,方程式为 ,题目中B项
2 3
方程式未配平,B项错误;C.与HO 发生氧化还原反应,Cr O 碱性条件下氧化为 ,而HO 还原为
2 2 2 3 2 2HO,离子方程为 ,C项正确;D.较活泼的金属可用热还原法制备金
2
属单质,同时Al活泼性强于Cr可以制备,D项正确;故选B。
二、主观题(共5小题,共52分)
17.(2021·北京丰台区·高三二模)(10分)银及其化合物在制造钱币、电子工业、医药等方面具有广泛
用途。
Ⅰ.银的冶炼及性质
(1)热分解法是金属冶炼方法之一。以Ag O为原料冶炼银的化学方程式为__。
2
(2)电解精炼银的工作原理如图所示,___(填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体
生成,则生成该气体的电极反应式为___。
Ⅱ.银的化合物的性质
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式__。
(4)在光照条件下,AgNO 可分解为Ag、O 和某种氮的氧化物。称取34g AgNO 固体,充分光照使其完全
3 2 3
分解,测得反应后生成O 的体积(折合成标准状况)为2.24L,反应过程中转移电子的物质的量为__。
2
(5)纳米硫化(Ag S)应用广泛。Ag S溶于浓HNO 后,产生淡黄色固体及无色气体,该气体遇空气迅速变为
2 2 3
红棕色。写出反应的化学方程式__。
【答案】(除标注外,每空2分)(1)2Ag O 4Ag+O↑
2 2
(2)a(1分) NO +e-+2H+=NO +H O
2 2
(3) AgCl+Br-=AgBr+Cl-(1分)
(4)0.4mol
(5)3Ag S+8HNO (浓)=6AgNO+3S↓+2NO↑+4H O
2 3 3 2
【解析】(1)Ag的金属活泼性比较弱,用热分解法冶炼金属Ag。以Ag O为原料冶炼银的化学方程式为
2
2Ag O 4Ag+O↑;答案为:2Ag O 4Ag+O↑;
2 2 2 2
(2)由图可知,电极a与电源正极相连,作阳极。电极b与电源负极相连,作阴极。根据电解原理,可知粗银作阳极,即a极为含有杂质的粗银。红棕色气体为NO 气体,b极有该气体生成,说明NO 得到电子发
2
生还原反应,电极反应式为:NO +e-+2H+=NO +H O;答案为:a;NO +e-+2H+=NO +H O;
2 2 2 2
(3)AgBr为淡黄色沉淀,说明反应中AgCl转化为AgBr,反应的离子方程式为:AgCl+Br-=AgBr+Cl-;答案
为:AgCl+Br-=AgBr+Cl-;
(4)34gAgNO 的物质的量= ,生成的O 的物质的量= ,NO 中O
3 2
元素的化合价由-2价变为0价,每生成1molO 转移4mol电子,则生成0.1molO 转移0.4mol电子。答案为:
2 2
0.4mol;
(5)由题可知,Ag S溶于浓HNO 后,生成S单质和NO气体,根据电子转移以及原子守恒等规律,可知反
2 3
应方程式为:3Ag S+8HNO (浓)=6AgNO+3S↓+2NO↑+4H O;答案为:3Ag S+8HNO (浓)=
2 3 3 2 2 3
6AgNO+3S↓+2NO↑+4H O。
3 2
18.(2020·大连市一0三中学高三一模)(10分)亚硝酸钠易溶于水,水溶液显碱性,有氧化性,也有还
原性。由于NaNO 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才
2
能排放。处理方法之一如下:
___NaNO +___KI+_____→___NO↑+___I +___K SO +___Na SO +______
2 2 2 4 2 4
(1)请完成该化学方程式并配平。
(2)将上述反应方程式改写为离子反应方程式:______________________;
(3)用上述反应来处理NaNO 并不是最佳方法,其原因是______________________。从环保角度来讲,
2
要处理NaNO ,所用的物质的______(填“氧化性”或“还原性”)应该比KI更________(填“强”或
2
“弱”)。
(4)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式并用单线桥表示
其电子转移的方向和数目_____________________________。
【答案】(除标注外,每空2分)(1)2 2 2H SO 2 1 1 1 2H O
2 4 2
(2)2 +2I-+4H+ = 2NO↑ +I +2H O
2 2
(3)生成物中含有大气污染物NO 还原性(1分) 强(1分)
(4)
【解析】(1)在反应___NaNO +___KI+_____→___NO↑+___I +___K SO +___Na SO +______中,NaNO 中N
2 2 2 4 2 4 2元素化合价降低,NaNO 是氧化剂,KI中I元素化合价升高,KI是还原剂,依据得失电子守恒和原子守恒,
2
确定方程式为2NaNO +2KI+ 2H SO =2NO↑+I +K SO +Na SO +2H O;
2 2 4 2 2 4 2 4 2
(2)将化学方程式2NaNO +2KI+ 2H SO =2NO↑+I +K SO +Na SO +2H O中的NaNO 、HSO 、KSO 、
2 2 4 2 2 4 2 4 2 2 2 4 2 4
NaSO 改写成离子形式,并删去方程式两边相同数目的相同离子,得上述反应的离子反应方程式为2
2 4
+2I-+4H+ = 2NO↑ +I +2H O;
2 2
(3)在上述反应中,生成物中含有大气污染物NO,所以用此法来处理NaNO 并不是最佳方法;从环保角度
2
来讲,要处理NaNO ,所用的物质的还原性应该比KI更强;
2
(4)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,该反应的化学方程式为:
NaNO +NHCl=NaCl+N ↑+2H O,用单线桥表示电子转移的方向和数目时,箭头应从NH Cl中的N元素指
2 4 2 2 4
向NaNO 中的N元素,数目为转移电子总数(3e-),表示为: 。
2
19.(2022·江苏扬州·模拟预测)(11分)硫化氢的转化是资源利用和环境保护的重要研究课题。
(1)工业上利用克劳斯法将 转化为硫单质回收。该法首先将部分 燃烧转化为 ,然后再将 与
剩余的 混合。为实现硫的最大回收,用于燃烧的 和剩余的 的物质的量之比为_______。
(2) 化学反应循环制氢的原理如题图所示,按图示方法制氢,理论上, 可制得_______ 。
(3)活性炭 (多孔性活性炭为载体的 )是一种高效、可再生的脱硫剂。可用于脱除 气体。活
性炭 ,脱除 后所得的含硫产物为 、 和 。其脱除原理如下:
① ;
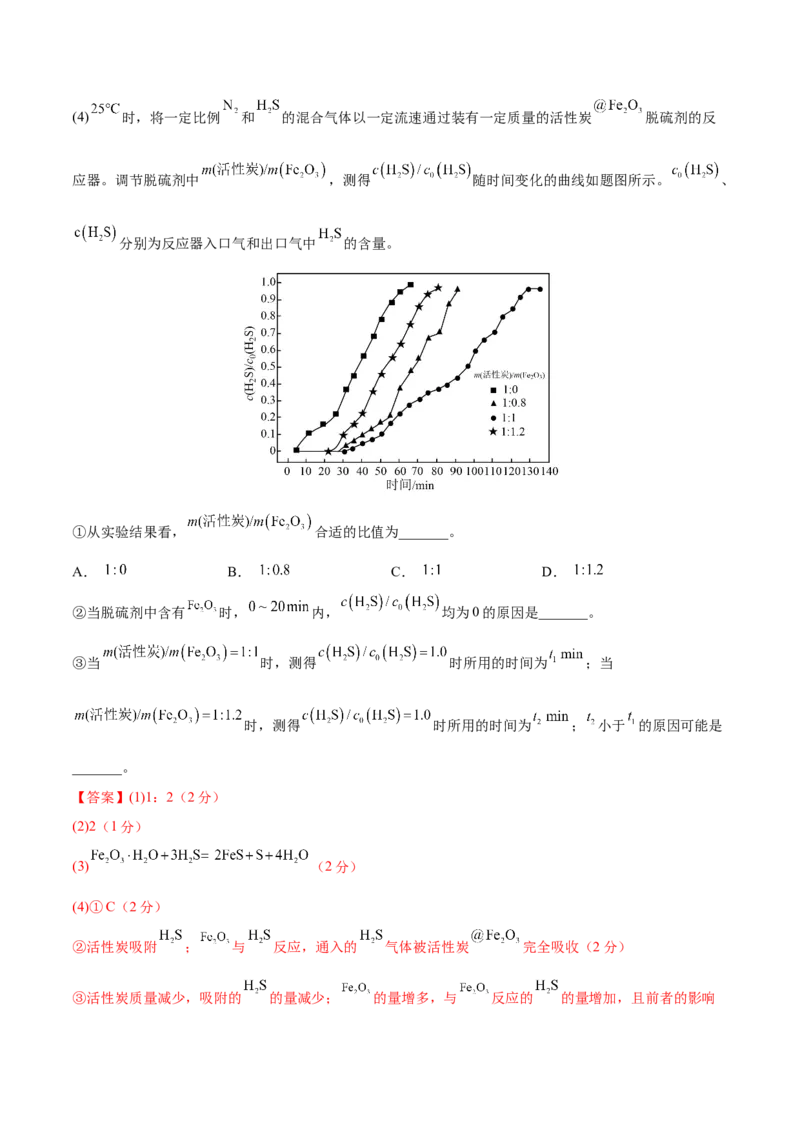
② 和 反应生成 的化学方程式为_______。(4) 时,将一定比例 和 的混合气体以一定流速通过装有一定质量的活性炭 脱硫剂的反
应器。调节脱硫剂中 ,测得 随时间变化的曲线如题图所示。 、
分别为反应器入口气和出口气中 的含量。
①从实验结果看, 合适的比值为_______。
A. B. C. D.
②当脱硫剂中含有 时, 内, 均为0的原因是_______。
③当 时,测得 时所用的时间为 ;当
时,测得 时所用的时间为 ; 小于 的原因可能是
_______。
【答案】(1)1:2(2分)
(2)2(1分)
(3) (2分)
(4)①C(2分)
②活性炭吸附 ; 与 反应,通入的 气体被活性炭 完全吸收(2分)
③活性炭质量减少,吸附的 的量减少; 的量增多,与 反应的 的量增加,且前者的影响大于后者。与 反应的 的量增加,导致生成的 、 、 的质量增多,覆盖在脱硫剂表
面,影响反应的进一步进行,也影响活性炭的吸附性能。(“堵塞活性炭的管道,降低了活性炭的吸附能
力”也可)(2分)
【解析】(1)根据反应2HS+3O 2SO +2H O,2HS+SO=3S+2H O,假设第一反应生成二氧化硫为2mol,
2 2 2 2 2 2 2
则在第二反应中消耗硫化氢4mol,故整个过程第一反应消耗硫化氢为2mol,即燃烧消耗2mol,剩余
4mol,物质的量之比为1:2,故答案为1:2;
(2)根据流程中总反应为HS+O+2H O==2H +H SO ,故每消耗1mol硫化氢生成氢气是2mol,故答案为
2 2 2 2 2 4
2;
(3)根据元素原子守恒及元素化合价升降守恒配平得: ;
(4)①在反应30分钟后, 的比值为1:1时,出来的硫化氢与进入的硫化氢比值最小,故
选择C。
②当脱硫剂中含有 时, 内,活性炭吸附 ; 与 反应,通入的 气体被活性炭
完全吸收,故答案为:活性炭吸附 ; 与 反应,通入的 气体被活性炭 完
全吸收;
③ 变为 时,活性炭质量减少,吸附的 的量减少;
的量增多,与 反应的 的量增加,且前者的影响大于后者。与 反应的 的量增加,导
致生成的 、 、 的质量增多,覆盖在脱硫剂表面,影响反应的进一步进行,也影响活性炭
的吸附性能,故答案为:活性炭质量减少,吸附的 的量减少; 的量增多,与 反应的 的
量增加,且前者的影响大于后者。与 反应的 的量增加,导致生成的 、 、 的质量
增多,覆盖在脱硫剂表面,影响反应的进一步进行,也影响活性炭的吸附性能。
20.(2021·江苏盐城市·高三二模)(10分)氧化还原法、沉淀法等是常用于治理水体污染的重要化学方法。
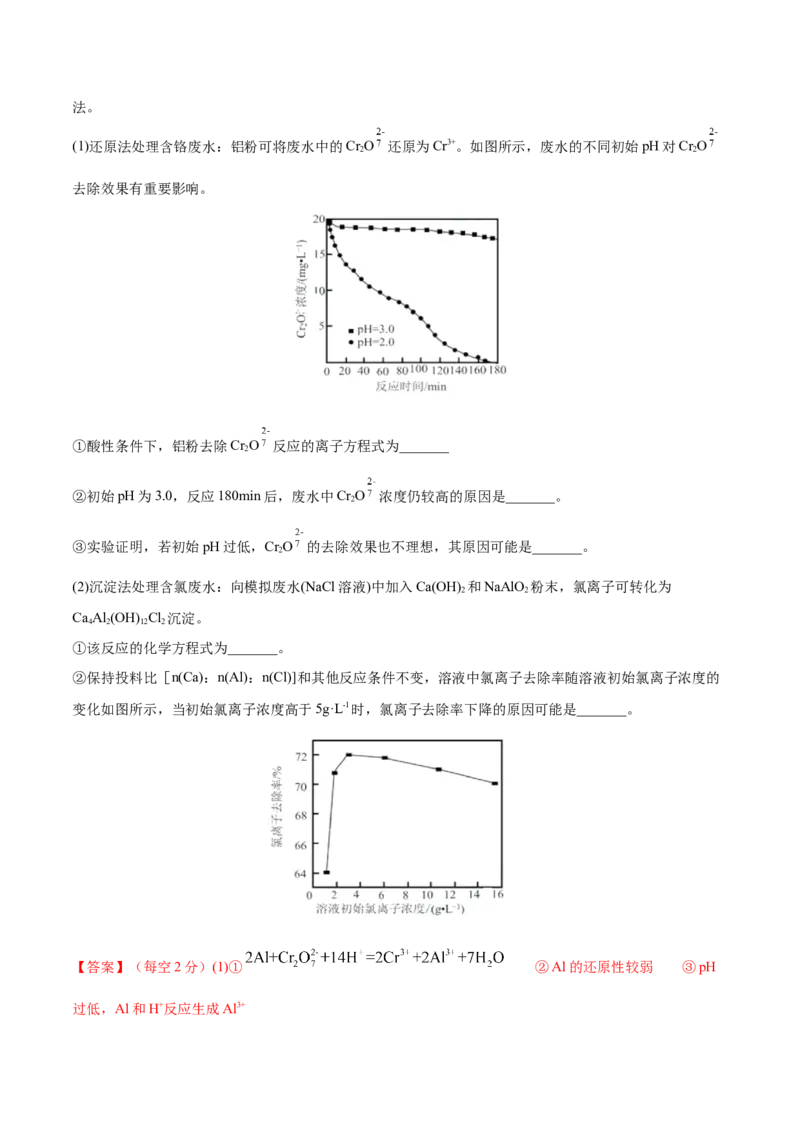
(1)还原法处理含铬废水:铝粉可将废水中的Cr O 还原为Cr3+。如图所示,废水的不同初始pH对Cr O
2 2
去除效果有重要影响。
①酸性条件下,铝粉去除Cr O 反应的离子方程式为_______
2
②初始pH为3.0,反应180min后,废水中Cr O 浓度仍较高的原因是_______。
2
③实验证明,若初始pH过低,Cr O 的去除效果也不理想,其原因可能是_______。
2
(2)沉淀法处理含氯废水:向模拟废水(NaCl溶液)中加入Ca(OH) 和NaAlO 粉末,氯离子可转化为
2 2
Ca Al (OH) Cl 沉淀。
4 2 12 2
①该反应的化学方程式为_______。
②保持投料比[n(Ca):n(Al):n(Cl)]和其他反应条件不变,溶液中氯离子去除率随溶液初始氯离子浓度的
变化如图所示,当初始氯离子浓度高于5g·L-1时,氯离子去除率下降的原因可能是_______。
【答案】(每空2分)(1)① ②Al的还原性较弱 ③pH
过低,Al和H+反应生成Al3+(2)① ② Cl-浓度较高时,使得OH-浓
度较高,Ca2+、 在溶液中浓度降低,导致氯离子去除率下降
【解析】(1)①酸性条件下,铝粉可将废水中的Cr O 还原为Cr3+,化学方程式为:
2
;
②pH为3.0,Al的还原性较弱;
③pH过低,溶液中H+含量较高,Al和H+反应生成Al3+,导致Cr O 的去除效果不理想;
2
(2)①NaCl溶液、Ca(OH) 和NaAlO 反应生成Ca Al (OH) Cl 沉淀,化学方程式为:
2 2 4 2 12 2
;
②保持投料比[n(Ca):n(Al):n(Cl)] 和其他反应条件不变,当初始氯离子浓度高于5g·L-1时,
,Cl-浓度较高时,使得OH-浓度较高,
Ca2+、 在溶液中浓度降低,导致氯离子去除率下降。
21.(2021·山东潍坊市·高三一模)(11分)硫氰酸钾(KSCN),是一种用途广泛的化学药品,常用于合成
树脂、杀虫杀菌剂等。某化学小组用下图实验装置模拟工业制备硫氰酸钾,并进行相关实验探究。
已知:① 不溶于 和 不溶于水且密度比水大;
②D中三颈烧瓶内盛放 、水和催化剂,发生反应 ,该反应比较缓慢且 在高于170℃时易分解, 在高于25℃时即分解。
回答下列问题:
(1)试剂a是_________,装置D中盛装KOH溶液的仪器名称是_______。
(2)制备KSCN溶液:将D中反应混合液加热至105℃,打开K 通入氨气。
1
①反应一段时间后,关闭K,此时装置C中观察到的现象是保持三颈烧瓶内反应混合液温度为105℃一段
1
时间,这样操作的目的是__________________。
②打开K,缓缓滴入适量的KOH溶液,继续保持反应混合液温度为105℃。
2
(3)装置E中发生氧化还原反应的离子方程式是__________________。
(4)制备硫氰酸钾晶体:先滤去三颈烧瓶中的固体催化剂,再经________(填操作名称)、减压蒸发浓缩、冷
却结晶、过滤、洗涤、干燥,得到硫氰酸钾晶体。
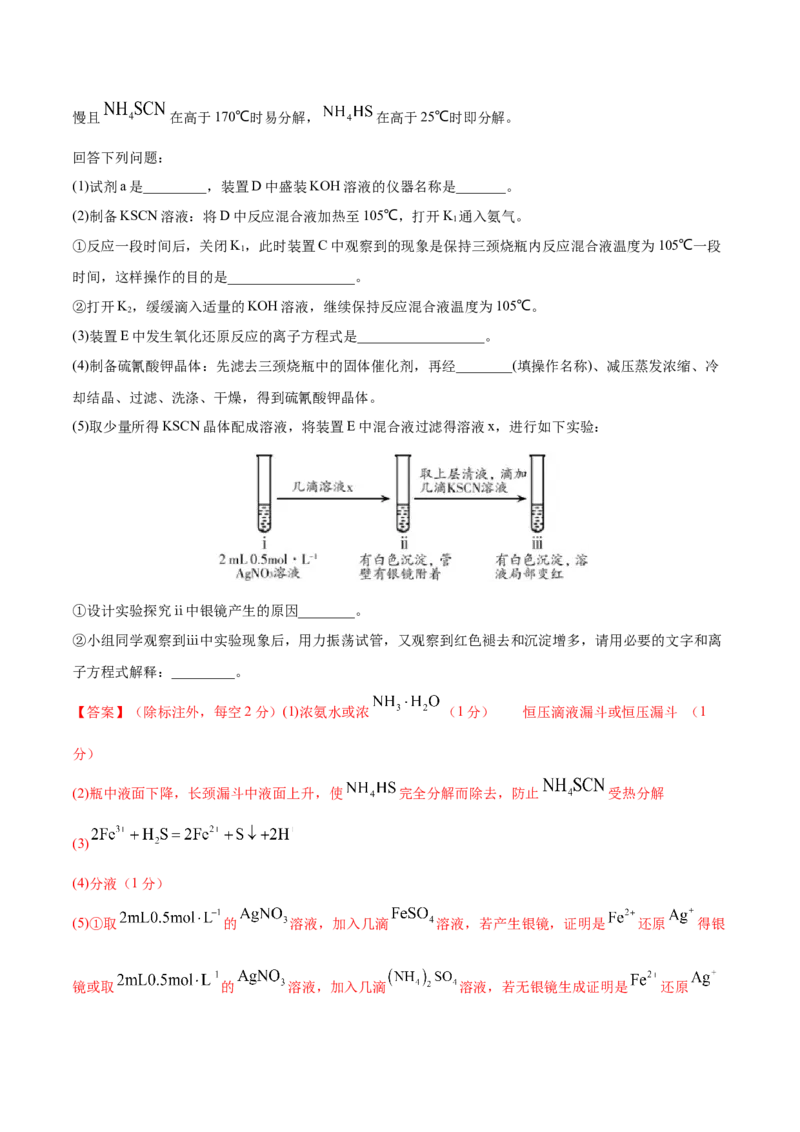
(5)取少量所得KSCN晶体配成溶液,将装置E中混合液过滤得溶液x,进行如下实验:
①设计实验探究ⅱ中银镜产生的原因________。
②小组同学观察到ⅲ中实验现象后,用力振荡试管,又观察到红色褪去和沉淀增多,请用必要的文字和离
子方程式解释:_________。
【答案】(除标注外,每空2分)(1)浓氨水或浓 (1分) 恒压滴液漏斗或恒压漏斗 (1
分)
(2)瓶中液面下降,长颈漏斗中液面上升,使 完全分解而除去,防止 受热分解
(3)
(4)分液(1分)
(5)①取 的 溶液,加入几滴 溶液,若产生银镜,证明是 还原 得银
镜或取 的 溶液,加入几滴 溶液,若无银镜生成证明是 还原得银镜
②红色溶液存在平衡 ,用力振荡,发生反应 ,
沉淀增多,平衡逆向移动,红色褪去
【解析】将浓氨水与生石灰发生反应,利用球型干燥器除水干燥后,通入到四氯化碳中,产生的氨气,与
D中的 、水和催化剂发生反应生成NH SCN以及NH HS,并且通过已给的条件得知,该反应比较缓慢
4 4
且 在高于170℃时易分解, 在高于25℃时即分解,生成的产物与氢氧化钾发生反应,
生成KSCN,未反应的氢氧化钾及氨气可以用过尾气处理与酸性的硫酸铁溶液进行反应。
(1)判断依据为,①给出的条件都提到了NH 和N元素,②反应中出现了NH ;由此可以判断A装置是制取
3 3
氨气,故填浓 ;
(2)关闭K,A装置依旧产生气泡,故可以看到此时装置C中有气泡,题中给出了关于温度的条件,故判断
1
目的是防止 受热分解;
(3)氧化还原反应,故写出三价铁离子与硫化氢气体的离子方程式为 ;
(4)过滤除去固体催化剂后,应该除去未反应完的CS,故操作为分液;
2
(5)①产生银镜反应的原因是溶液中银离子有氧化性,亚铁离子有还原性,两者发生反应,故可设计实验为:
取 的 溶液,加入几滴 溶液,若产生银镜,证明是 还原 得银镜或
取 的 溶液,加入几滴 溶液,若无银镜生成证明是 还原 得银
镜;②用力振荡,发生反应 ,沉淀增多,使 平
衡逆向移动,红色褪去。