文档内容
第八章 水溶液中的离子反应与平衡
测试卷
时间:75分钟 分值:100分
可能用到的相对原子质量:H 1 C 12 N 14 O16 Na 23 Al 27 S 32 Cl 35.5 K 39 Ca 40 Fe 56
Cu 64 Ag 108 Ba 137
一、选择题(每小题只有一个正确选项,共15×3分)
1.(2024·陕西省榆林市高三模拟)常温下,取pH均等于2的HCl和CHCOOH各 分别稀释2倍
3
后,再分别加入 锌粉,在相同条件下充分反应。下列有关说法正确的是( )
A.与Zn反应速率:HCl<CHCOOH
3
B.稀释后溶液的pH:HCl<CHCOOH
3
C.稀释2倍后,水的电离程度:HCl<CHCOOH
3
D.与Zn充分反应放出H 的质量: HCl>CHCOOH
2 3
2.(2023·浙江省金华外国语学校质检)为探究浓度对醋酸电离程度的影响,用 计测定 时不同浓
度醋酸的 结果如下,下列说法正确的是( )
浓度/ 0.0010 0.010 0.020 0.10 0.20
3.88 3.38 3.23 2.88 2.83
A.实验过程中可以改用广泛 试纸
B. 溶液稀释过程中,醋酸电离程度及溶液导电性都增大
C. 时,电离常数K(CH COOH)的数量级为10-5
3
D.CHCOOH溶液稀释过程中不可能出现c(H+)>c(OH―)>c(CHCOO-)
3 3
3.室温下,将0.05 mol Na CO 固体溶于水配成100 mL溶液,向溶液中加入下列物质,有关结论正确
2 3
的是( )
加入的物质 结论
A.50 mL 1 mol·L-1 HSO 反应结束后,c(Na+)=c(SO)
2 4
B.0.05 mol CaO 溶液中增大
C.50 mL H O 由水电离出的c(H+)·c(OH-)不变
2
D.0.1 mol NaHSO 固体 反应完全后,溶液pH减小,c(Na+)不变
4
4.(2024·辽宁省丹东市高三二模)室温下,探究0.1mol·L-1NaHSO 溶液的性质,下列实验方案能达到
3
探究目的的是( )
(已知HSO :K =1.4×10-2,K =6.0×10-8;HCO:K =4.5×10-7,K =4.7×10-11)
2 3 a1 a2 2 3 a1 a2
选项 探究目的 实验方案
A 溶液中是否含有 用玻璃棒蘸取少量NaHSO 溶液,在酒精灯火焰上灼
3Na+ 烧,观察火焰颜色变化
溶液中HSO -是否 向2mL NaHSO 溶液中滴加几滴等浓度的酸性KMnO
3 3 4
B
具有还原性 溶液,观察溶液颜色变化
溶液中HSO -是否 向2mL NaHSO 溶液中滴加 滴酚酞,观察溶液颜
3 3
C
水解 色变化
溶液中HSO -是否 向2mL0.1mol·L-1NaCO 溶液中滴加几滴等浓度的
3 2 3
D
显酸性 NaHSO 溶液,观察气泡产生的情况
3
5.(2024·天津市部分区高三二模)常温下,一种解释乙酰水杨酸(用HA表示, )药物在人
体吸收模式如下:
假设离子不会穿过组织薄膜,而未电离的HA分子则可自由穿过该膜且达到平衡。下列说法正确的是(
)
A.血浆中c(HA)大于胃中c(HA) B.取胃中液体,加水稀释100倍后,pH=3.0
C.在血浆中, D.在血浆和胃中,HA电离程度相同
6.(2024·上海市洋泾中学高三模拟)H C O 为二元弱酸,K (H C O)=5.4×10-2,K (H C O)=5.4×10-5,
2 2 4 a1 2 2 4 a2 2 2 4
NaHC O 溶液显酸性。设HC O 溶液中c(总)=c(H C O)+c(HC O-)+c(C O2-)。室温下用NaOH溶液滴定
2 4 2 2 4 2 2 4 2 4 2 4
25.00mL0.1000mol·L-1HC O 溶液至终点。滴定过程得到的下列溶液中微粒的物质的量浓度关系一定正确的
2 2 4
是( )
A.0.1000mol·L-1HC O 溶液:c(H+)=0.1000mol·L-1+c(C O2-)+c(OH-)+c(H C O)
2 2 4 2 4 2 2 4
B.c(Na+)=c(总)的溶液:c(Na+)>c(H C O)>c(H+)>c(C O2-)
2 2 4 2 4
C.pH=7的溶液:c(Na+)=0.1000mol·L-1+c(C O2-)-c(HC O)
2 4 2 2 4
D.c(Na+)=2c(总)的溶液:c(OH-)-c(H+)=2c(H C O)+c(HC O-)
2 2 4 2 4
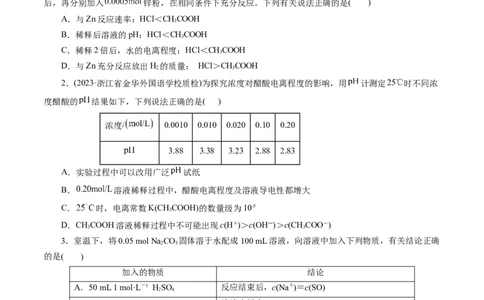
7.某温度下,水溶液中CO、HCO、HCO -和CO2-的物质的量分数随 变化如图所示。下列说法
2 2 3 3 3
不正确的是( )A.碳酸的电离方程式为:HCO H++HCO -,HCO - H++CO2-
2 3 3 3 3
B.该温度下,HCO H++HCO - K >1×10-8
2 3 3 a1
C.该温度下,HCO H++CO2- K =1×10-b
3 3 a2
D.NaCO 溶液中,2c(Na+)+c(H+)=c(HCO -)+c(OH―)+ c(CO2-)
2 3 3 3
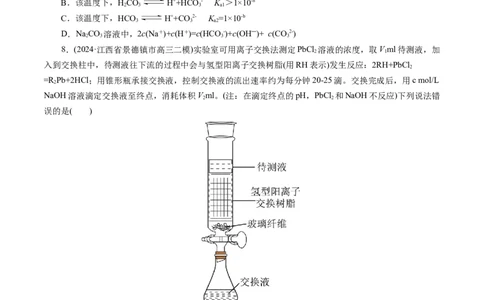
8.(2024·江西省景德镇市高三二模)实验室可用离子交换法测定PbCl 溶液的浓度,取Vml待测液,加
2 1
入到交换柱中,待测液往下流的过程中会与氢型阳离子交换树脂(用RH表示)发生反应:2RH+PbCl
2
=R Pb+2HCl;用锥形瓶承接交换液,控制交换液的流出速率约为每分钟20-25滴。交换完成后,用c mol/L
2
NaOH溶液滴定交换液至终点,消耗体积Vml。(注:在滴定终点的pH,PbCl 和NaOH不反应)下列说法错
2 2
误的是( )
A.滴定时可选择酚酞作指示剂
B. 溶液的浓度为 mol/L
C.若交换液的流出速率过快,可能导致测得PbCl 溶液的浓度偏小
2
D.利用该方法可以准确测定 溶液的浓度
9.一种测定水样中溴离子浓度的实验步骤如下:
①向锥形瓶中加入处理后的水样25.00mL,加入几滴NH Fe(SO ) 溶液。
4 4 2
②加入V mL c mol∙L−1AgNO 溶液(过量),充分摇匀。
1 1 3③用c mol∙L−1KSCN标准溶液进行滴定,至终点时消耗标准溶液VmL 。
2 2
已知:K (AgBr)=7.7×10−13,Ag++SCN-= AgSCN(白色)↓,K (AgSCN)=1×10−12,下列说法不正确的是(
sp sp
)
A.滴定终点时,溶液变为红色
B.该水样中溴离子浓度为:c(Br-)= mol∙L−1
C.AgBr(s)+SCN-(aq) AgSCN(s)+Br-(aq)的平衡常数K=0.77
D.该实验需要严格控制水样的pH,若pH过高则测定结果将偏高
10.(2024·山东省临沂市二模)[Co(NH )Cl]Cl (M=250.5g/mol)是一种易溶于热水,难溶于乙醇的紫红色
3 5 2
晶体。
(1)制备步骤:将适量氯化铵溶于浓氨水中,边搅拌边分批次加入ag研细的CoCl ·6H O(M=238g/
2 2
mol),得到[Co(NH )]Cl 沉淀。边搅拌边慢慢滴入足量30%H O 溶液,得到[Co(NH )HO]Cl 溶液。慢慢
3 6 2 2 2 3 5 2 3
注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到bg
产品。
(2)钴的测定:取5.0g样品于锥形瓶中,加入NaOH溶液并加热使钴(Ⅲ)完全沉淀,后加入HSO 和
2 4
HO 将其还原为钴(Ⅱ),再加入VmLcmol/LEDTA,用cmol/LZnCl 标准溶液滴定过量的EDTA,消耗
2 2 1 1 2 2
ZnCl 溶液平均体积为VmL(EDTA与金属阳离子1:1反应)。
2 2
下列有关计算正确的是( )
A.[Co(NH )Cl]Cl 的产率为
3 5 2
B.[Co(NH )Cl]Cl 的产率为
3 5 2
C.样品中钴的质量分数为
D.样品中钴的质量分数为
11.(2024·浙江省七彩阳光新高考研究联盟三联考)常温下,某研究小组设计如下流程探究粗盐中的硫
酸钠杂质的转化:
已知:溶液混合时体积变化忽略不计,K (BaSO)= 1×10-10,K (BaCO)= 1×10-9。下列说法不正确的
sp 4 sp 3
是( )
A.在A中有白色沉淀生成
B.在B溶液中:c(SO 2-)<c(CO2-)+c(HCO -)·+c(H CO)
4 3 3 2 3
C.A→B的过程中BaSO 全部转化为BaCO
4 3
D.B→C的过程中BaCO 全部溶解,沉淀消失
3
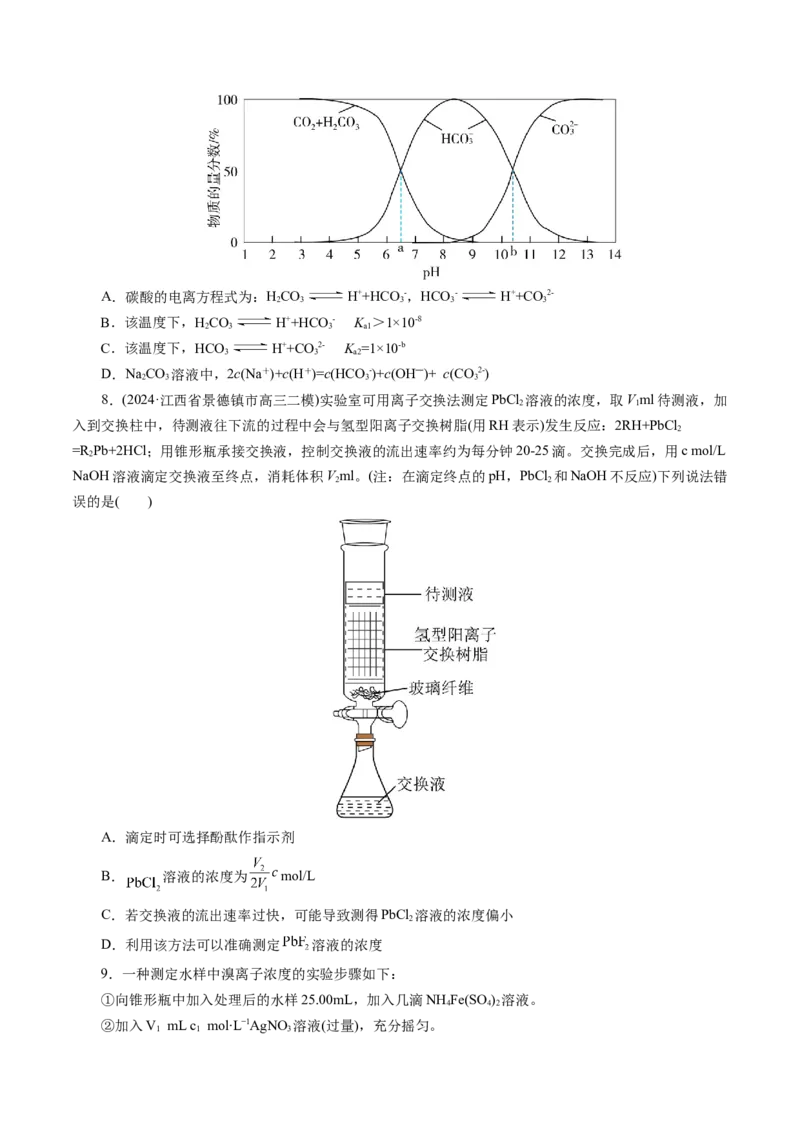
12.(2024·福建省福州市高三三模)向敞口容器中加入一定体积pH=13的84消毒液(NaClO的浓度约为1mol·L-1,不断搅拌,逐滴加入0.1mol·L-1FeSO 溶液,溶液pH变化曲线如图1所示(AB段pH快速下降的
4
原因之一是Fe2++2OH-=Fe(OH) ↓)。图2表示NaClO溶液中含氯微粒的物质的量分数与pH的关系。
2
关于上述滴定过程,下列说法正确的是( )
A.原84消毒液中,HClO的含量约为
B.AB段Fe2+被氧化的反应5ClO-+2Fe2++5H O=2Fe(OH) ↓+Cl-+4HClO
2 3
C.CD段较BC段pH下降快的主要原因是HClO的氧化性强于ClO⁻
D.400s后反应几乎停止
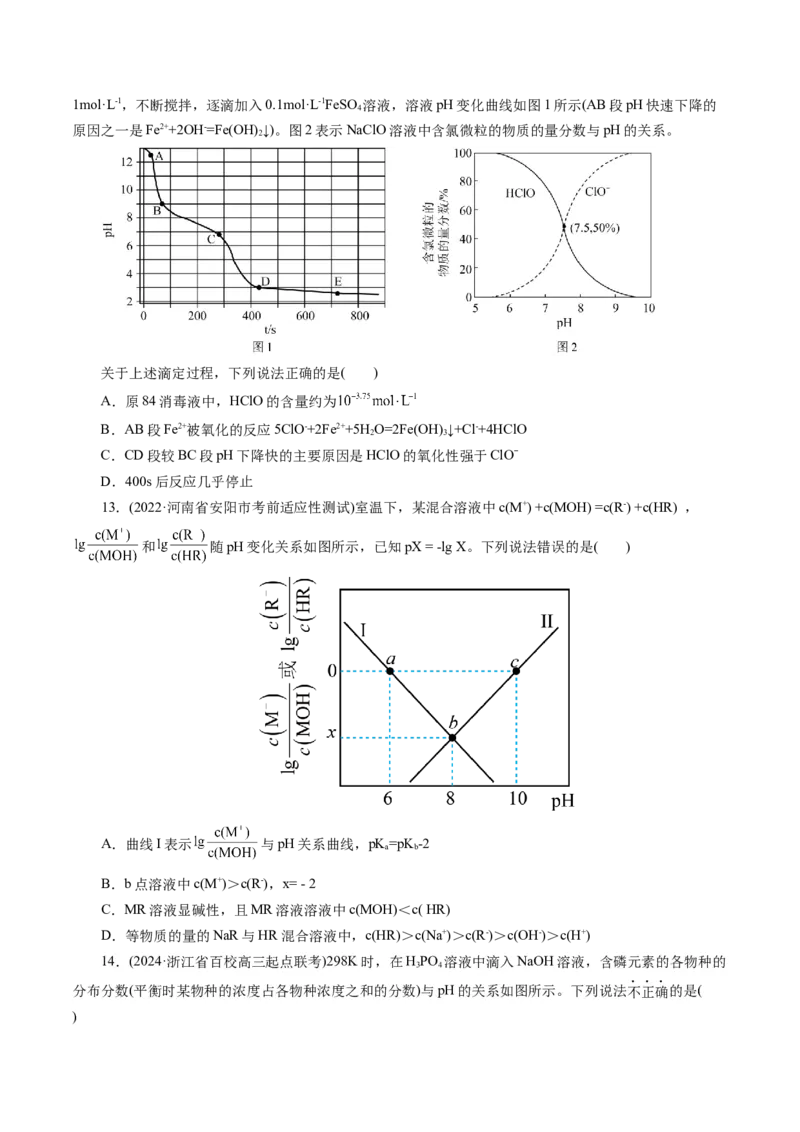
13.(2022·河南省安阳市考前适应性测试)室温下,某混合溶液中c(M+) +c(MOH) =c(R-) +c(HR) ,
和 随pH变化关系如图所示,已知pX = -lg X。下列说法错误的是( )
A.曲线I表示 与pH关系曲线,pK=pK -2
a b
B.b点溶液中c(M+)>c(R-),x= - 2
C.MR溶液显碱性,且MR溶液溶液中c(MOH)<c( HR)
D.等物质的量的NaR与HR混合溶液中,c(HR)>c(Na+)>c(R-)>c(OH-)>c(H+)
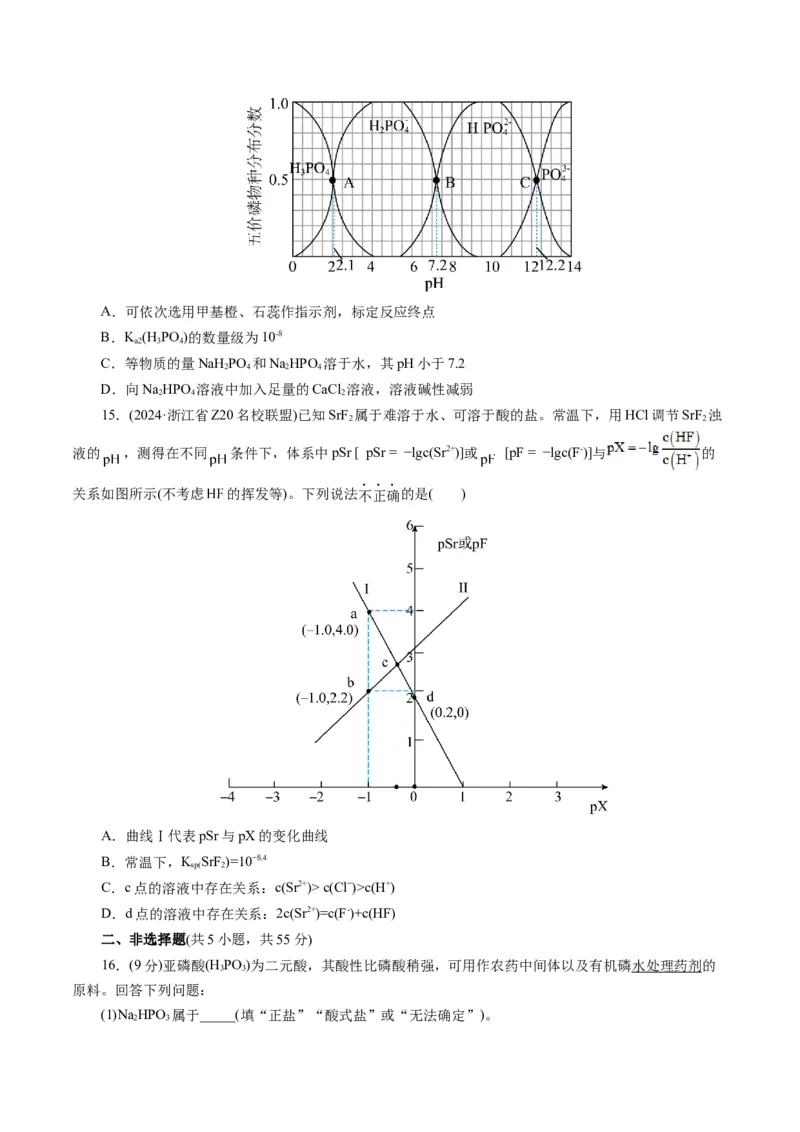
14.(2024·浙江省百校高三起点联考)298K时,在HPO 溶液中滴入NaOH溶液,含磷元素的各物种的
3 4
分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。下列说法不正确的是(
)A.可依次选用甲基橙、石蕊作指示剂,标定反应终点
B.K (H PO )的数量级为10-8
a2 3 4
C.等物质的量NaH PO 和NaHPO 溶于水,其pH小于7.2
2 4 2 4
D.向NaHPO 溶液中加入足量的CaCl 溶液,溶液碱性减弱
2 4 2
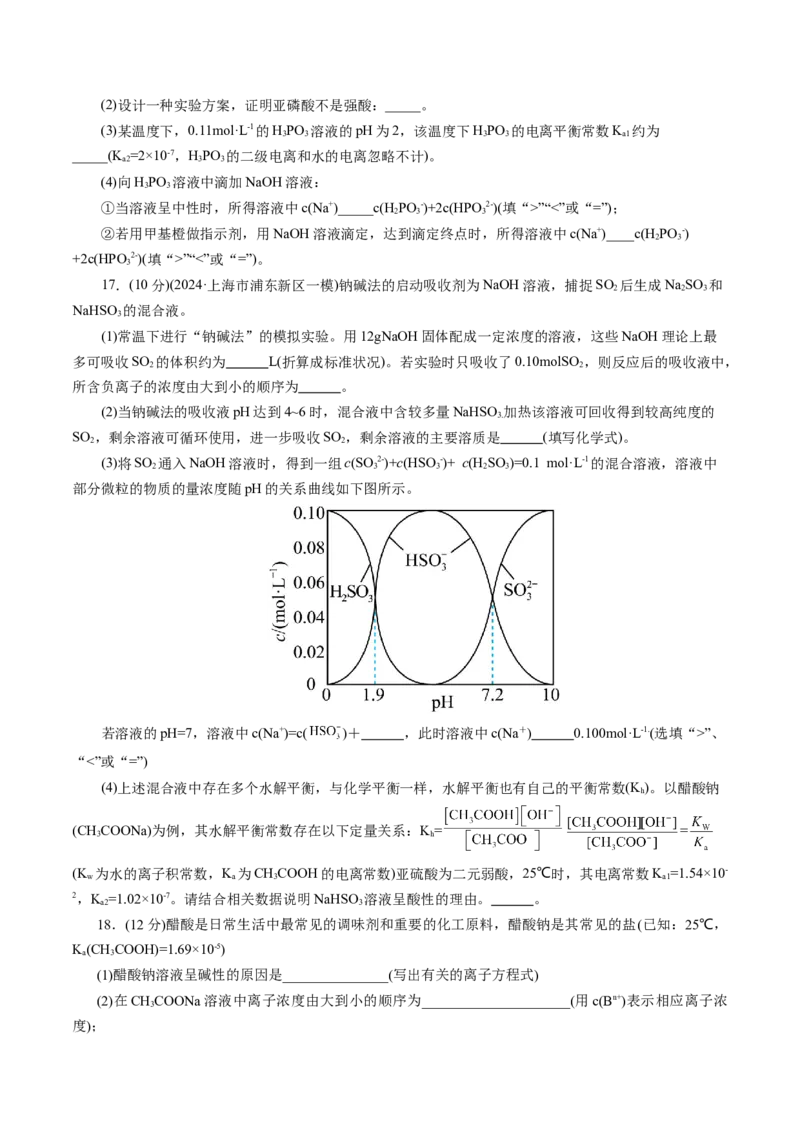
15.(2024·浙江省Z20名校联盟)已知SrF 属于难溶于水、可溶于酸的盐。常温下,用HCl调节SrF 浊
2 2
液的 ,测得在不同 条件下,体系中pSr [ pSr = −lgc(Sr2+)]或 [pF = −lgc(F-)]与 的
关系如图所示(不考虑 的挥发等)。下列说法不正确的是( )
A.曲线Ⅰ代表pSr与pX的变化曲线
B.常温下,K SrF )=10−8.4
sp( 2
C.c点的溶液中存在关系:c(Sr2+)> c(Cl−)>c(H+)
D.d点的溶液中存在关系:2c(Sr2+)=c(F-)+c(HF)
二、非选择题(共5小题,共55分)
16.(9分)亚磷酸(H PO )为二元酸,其酸性比磷酸稍强,可用作农药中间体以及有机磷水处理药剂的
3 3
原料。回答下列问题:
(1)Na HPO 属于_____(填“正盐”“酸式盐”或“无法确定”)。
2 3(2)设计一种实验方案,证明亚磷酸不是强酸:_____。
(3)某温度下,0.11mol·L-1的HPO 溶液的pH为2,该温度下HPO 的电离平衡常数K 约为
3 3 3 3 a1
_____(K =2×10-7,HPO 的二级电离和水的电离忽略不计)。
a2 3 3
(4)向HPO 溶液中滴加NaOH溶液:
3 3
①当溶液呈中性时,所得溶液中c(Na+)_____c(HPO -)+2c(HPO 2-)(填“>”“<”或“=”);
2 3 3
②若用甲基橙做指示剂,用NaOH溶液滴定,达到滴定终点时,所得溶液中c(Na+)____c(HPO -)
2 3
+2c(HPO2-)(填“>”“<”或“=”)。
3
17.(10分)(2024·上海市浦东新区一模)钠碱法的启动吸收剂为NaOH溶液,捕捉SO 后生成NaSO 和
2 2 3
NaHSO 的混合液。
3
(1)常温下进行“钠碱法”的模拟实验。用12gNaOH固体配成一定浓度的溶液,这些NaOH理论上最
多可吸收SO 的体积约为 L(折算成标准状况)。若实验时只吸收了0.10molSO ,则反应后的吸收液中,
2 2
所含负离子的浓度由大到小的顺序为 。
(2)当钠碱法的吸收液pH达到4~6时,混合液中含较多量NaHSO 加热该溶液可回收得到较高纯度的
3.
SO ,剩余溶液可循环使用,进一步吸收SO ,剩余溶液的主要溶质是 (填写化学式)。
2 2
(3)将SO 通入NaOH溶液时,得到一组c(SO 2-)+c(HSO -)+ c(H SO )=0.1 mol·L-1的混合溶液,溶液中
2 3 3 2 3
部分微粒的物质的量浓度随pH的关系曲线如下图所示。
若溶液的pH=7,溶液中c(Na+)=c( )+ ,此时溶液中c(Na+) 0.100mol·L-1.(选填“>”、
“<”或“=”)
(4)上述混合液中存在多个水解平衡,与化学平衡一样,水解平衡也有自己的平衡常数(K )。以醋酸钠
h
(CHCOONa)为例,其水解平衡常数存在以下定量关系:K= =
3 h
(K 为水的离子积常数,K 为CHCOOH的电离常数)亚硫酸为二元弱酸,25℃时,其电离常数K =1.54×10-
w a 3 a1
2,K =1.02×10-7。请结合相关数据说明NaHSO 溶液呈酸性的理由。 。
a2 3
18.(12分)醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钠是其常见的盐(已知:25℃,
K(CHCOOH)=1.69×10-5)
a 3
(1)醋酸钠溶液呈碱性的原因是_______________(写出有关的离子方程式)
(2)在CHCOONa溶液中离子浓度由大到小的顺序为_____________________(用c(Bn+)表示相应离子浓
3
度);(3)25℃时,0.10mol/L的醋酸溶液的pH约为___________( 已知:lg1.3=0.114);
(4)对于醋酸溶液和醋酸钠溶液的下列说法正确的是____________;
A.稀释醋酸溶液,醋酸的电离程度增大,而稀释醋酸钠溶液则醋酸钠的水解程度减小.
B.升高温度可以促进醋酸电离,也可以促进醋酸钠水解.
C.醋酸和醋酸钠混合液中,醋酸抑制醋酸钠的水解、醋酸钠也抑制醋酸的电离.
D.醋酸和醋酸钠混合液中,醋酸促进醋酸钠的水解、醋酸钠也促进醋酸的电离.
(5)物质的量浓度均为0.1mol/L的CHCOONa和CHCOOH溶液等体积混合(注:混合前后溶液体积变
3 3
化忽略不计),混合液中的下列关系式正确的是_______;
A.c(CHCOOH)+2c(H+)=c(CH COO-)+2c(OH-)
3 3
B.c(Na+)+c(H+)=c(CH COO-)+c(OH-)
3
C.c(CHCOO-)+c(CH COOH)=0.1mol/L
3 3
(6)常温时,有以下3种溶液,其中pH最小的是____________;
A.0.02mol•L-1CHCOOH与0.02mol•L-1NaOH溶液等体积混合液
3
B.0.03mol•L-1CHCOOH与0.01mol•L-1NaOH溶液等体积混合液
3
C.pH=2的CHCOOH与pH=12的NaOH溶液等体积混合液
3
(7)用 pH 试纸在常温下分别测定 0.10mol/L 的醋酸钠溶液和 0.10mol/L 的碳酸钠溶液,则
pH(CH COONa)_______ pH(Na CO) (填:“>”、“<”或“=”)
3 2 3
19.(12分)(2024·陕西省西安市二模)EDTA(乙二胺四乙酸)是一种重要的络合剂,其结构简式为
(可简写为HY)。某实验小组以一氯乙酸(ClCH COOH)和乙二胺
4 2
(H NCH CHNH )等为原料合成EDTA并测定饮用水的硬度。步骤如下:
2 2 2 2
步骤Ⅰ:称取一氯乙酸94.50g于一定规格的三颈烧瓶中,慢慢加入50%NaCO 溶液至不再产生气泡
2 3
为止。
步骤Ⅱ:向三颈烧瓶中继续加入15.60g乙二胺,摇匀,放置片刻,加入 溶液90mL,
加水至总体积为400mL左右,装上空气冷却回流装置,于50℃水浴上保温2h,再于沸水浴上保温回流
4h。
步骤Ⅲ:取下三颈烧瓶,将混合物冷却后倒入烧杯中,加入活性炭,搅拌、过滤。
步骤Ⅳ:用浓盐酸调节pH至1.2,有白色沉淀生成,抽滤得EDTA粗品。
请回答下列问题:
(1)三颈烧瓶最适宜的规格为 (填“500mL”或“1000mL”)。
(2)写出步骤Ⅰ中反应的化学方程式: 。
(3)步骤Ⅱ中需要配制 溶液,下列操作中正确的是 (填字母);加入
NaOH溶液的作用是 。操作
选项 a b c d
(4)使用活性炭的作用是脱色,一般加入活性炭的量为粗产品质量的1%~5%,加入量过多造成的影响
是 。
(5)步骤Ⅳ中若选用试纸控制pH,应选用 (填“精密”或“广泛”)pH试纸。
(6)用NaHY溶液测定饮用水的总硬度。取饮用水样品250mL,加入掩蔽剂排除干扰、调节pH等预
2 2
处理后,用0.0100 mol·L-1NaHY标准溶液进行测定。测定中涉及的反应有:M2++HIn2-(蓝色) MIn-
2 2
(酒红色)+H+、MIn-(酒红色)H Y2- MY2-+ HIn2-(蓝色)+H+、M2++ H Y2- MY2-+2H+[M2+代表
2 2
Ca2+、Mg2+;铬黑T(HIn2-)为指示剂]。
①确认达到滴定终点的标志是 。
②平行实验三次,滴定终点时共消耗NaHY溶液的平均值为20.00mL,则该饮用水的硬度=
2 2
度(水硬度的表示方法是将水中的Ca2+和Mg2+都看作Ca2+,并将其折算成CaO的质量,通常把1L水中含有
10mgCaO称为1度)。
20.(12分) (2024·江苏省南通市高三统考)制备锂离子电池的正极材料的前体FePO 的一种流程如下:
4
资料:i.磷灰石的主要成分是Ca (PO )F
5 4 3
ii.Ca(HPO ) 可溶于水,CaSO·2H O微溶于水
2 4 2 4 2
iii.K (FePO )=1.3×10-22
sp 4
(1)酸浸制粗HPO
3 4
用HPO 溶液、HSO 溶液浸取磷灰石生成HF、CaSO·2H O和HPO 。
3 4 2 4 4 2 3 4
①加入HPO 溶液、HSO 溶液的顺序为 。
3 4 2 4
②写出该反应的化学方程式: 。
③“酸浸”时能否要浓盐酸代替硫酸? (判断并说明理由)。
(2)纯化制备HPO
3 4
已知纯磷酸(熔点为42℃,沸点261℃),高于100℃时会脱水生成焦磷酸。则由85%的粗磷酸纯化制纯
磷酸的实验操作为 。
(3)制备FePO
4
①已知25℃时HPO 电离平衡常数K =6.9×10-3,K =6.2×10-8,K =4.8×10-13,则NaHPO 水解平衡常
3 4 a1 a2 a3 2 4
数为 (保留2位有效数字)。
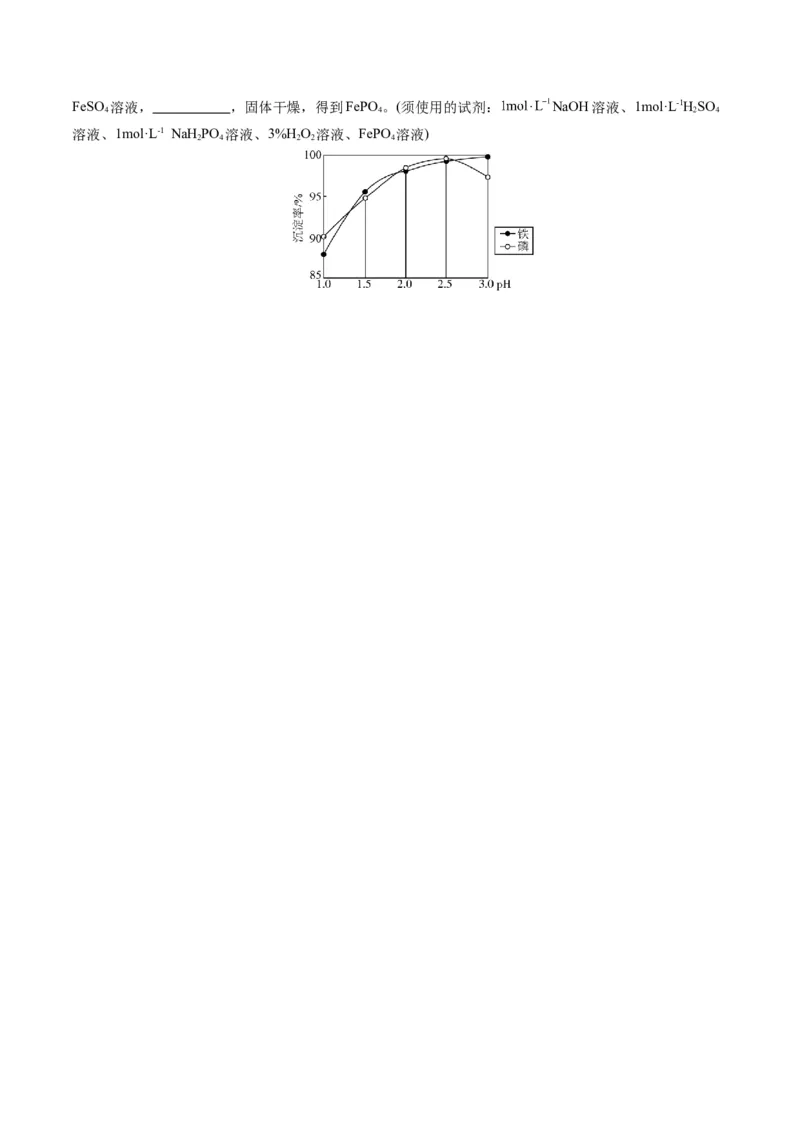
②已知:制备FePO 反应原理为Fe (SO )+ 2 NaH PO =2FePO ↓+2Na SO + H SO ,不同pH对磷酸铁沉
4 2 4 3 2 4 4 2 4 2 4
淀的影响如图所示。请补充以酸性FeSO (含少量 )的溶液制备较纯净的FePO 的实验方案:取一定量
4 4FeSO 溶液, ,固体干燥,得到FePO 。(须使用的试剂: NaOH溶液、1mol·L-1HSO
4 4 2 4
溶液、1mol·L-1 NaH PO 溶液、3%H O 溶液、FePO 溶液)
2 4 2 2 4