文档内容
1.下列说法错误的是 ( )
A.卤化氢中,HF的沸点最高,是由于HF分子间存在氢键
B.邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点低
C.HO的沸点比HF的沸点高,是由于水中氢键键能大
2
D.氨气极易溶于水与氨气分子和水分子间形成氢键有关
2. (2023·山东日照模拟)下列不能用氢键相关知识解释的是( )
A.羊毛衫水洗后变形 B.氨容易液化
C.HO比HS更稳定 D.冰浮在水面上
2 2
3.(2021·山东,9)关于CHOH、NH 和(CH)NNH 的结构与性质,下列说法错误的是(
3 2 4 3 2 2
)
A.CHOH为极性分子
3
B.NH 空间结构为平面形
2 4
C.NH 的沸点高于(CH)NNH
2 4 3 2 2
D.CHOH和(CH)NNH 中C、O、N杂化方式均相同
3 3 2 2
4.下列化合物中含有2个手性碳原子的是( )
A.
B.
C.
D.
5.(2021·湖北,9)下列有关N、P及其化合物的说法错误的是( )
A.N的电负性比P的大,可推断NCl 分子的极性比PCl 的大
3 3
B.N与N的π键比P与P的强,可推断N≡N的稳定性比P≡P的高
C.NH 的成键电子对间排斥力较大,可推断NH 的键角比PH 的大
3 3 3D.HNO 的分子间作用力较小,可推断HNO 的熔点比HPO 的低
3 3 3 4
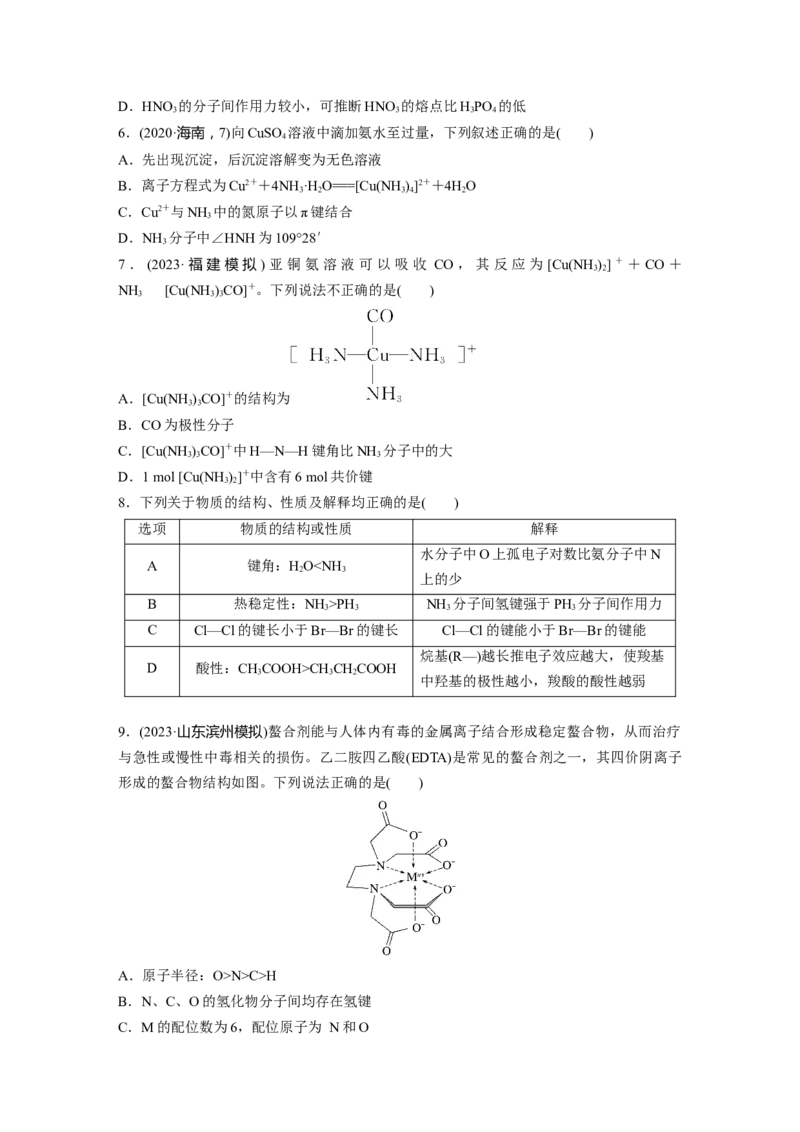
6.(2020·海南,7)向CuSO 溶液中滴加氨水至过量,下列叙述正确的是( )
4
A.先出现沉淀,后沉淀溶解变为无色溶液
B.离子方程式为Cu2++4NH ·H O===[Cu(NH)]2++4HO
3 2 3 4 2
C.Cu2+与NH 中的氮原子以π键结合
3
D.NH 分子中∠HNH为109°28′
3
7.(2023·福建模拟)亚铜氨溶液可以吸收 CO,其反应为[Cu(NH )]++CO+
3 2
NH [Cu(NH )CO]+。下列说法不正确的是( )
3 3 3
A.[Cu(NH )CO]+的结构为
3 3
B.CO为极性分子
C.[Cu(NH )CO]+中H—N—H键角比NH 分子中的大
3 3 3
D.1 mol [Cu(NH)]+中含有6 mol共价键
3 2
8.下列关于物质的结构、性质及解释均正确的是( )
选项 物质的结构或性质 解释
水分子中O上孤电子对数比氨分子中N
A 键角:HOPH NH 分子间氢键强于PH 分子间作用力
3 3 3 3
C Cl—Cl的键长小于Br—Br的键长 Cl—Cl的键能小于Br—Br的键能
烷基(R—)越长推电子效应越大,使羧基
D 酸性:CHCOOH>CH CHCOOH
3 3 2
中羟基的极性越小,羧酸的酸性越弱
9.(2023·山东滨州模拟)螯合剂能与人体内有毒的金属离子结合形成稳定螯合物,从而治疗
与急性或慢性中毒相关的损伤。乙二胺四乙酸(EDTA)是常见的螯合剂之一,其四价阴离子
形成的螯合物结构如图。下列说法正确的是( )
A.原子半径:O>N>C>H
B.N、C、O的氢化物分子间均存在氢键
C.M的配位数为6,配位原子为 N和OD.螯合物中每两个氮碳键(N—C)的夹角均为107°
10.吡啶( )含有与苯环类似的大π键,下列说法或实验操作不正确的是( )
A.吡啶中N原子的价层孤电子对占据了一个未参与杂化的p轨道
B.吡啶是极性分子且能与水形成氢键,故吡啶在水中的溶解度比苯大
C.除去苯中含有的少量吡啶:用盐酸洗涤、分液、干燥有机层
D. 、 的碱性随N原子电子云密度的增大而增强,故 碱性较强
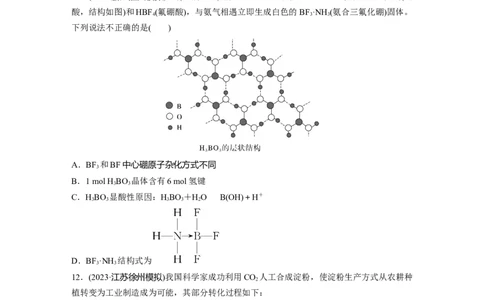
11.(2023·浙江嘉兴模拟)BF(三氟化硼)熔点-127 ℃,沸点-100 ℃,水解生成HBO(硼
3 3 3
酸,结构如图)和HBF (氟硼酸),与氨气相遇立即生成白色的BF·NH (氨合三氟化硼)固体。
4 3 3
下列说法不正确的是( )
A.BF 和BF中心硼原子杂化方式不同
3
B.1 mol H BO 晶体含有6 mol氢键
3 3
C.HBO 显酸性原因:HBO+HOB(OH)+H+
3 3 3 3 2
D.BF·NH 结构式为
3 3
12.(2023·江苏徐州模拟)我国科学家成功利用CO 人工合成淀粉,使淀粉生产方式从农耕种
2
植转变为工业制造成为可能,其部分转化过程如下:
已知:ZnO是两性氧化物;ZrCl 水解可制得ZrO。
4 2
下列有关物质的说法正确的是( )
A.H 和HCHO均属于非极性分子
2
B.CO 的空间结构为V形
2C.HO 和HO中均含极性键和非极性键
2 2 2
D.CHOH的熔点高于HCHO
3
13.(1)CO为配合物中常见的配体。CO作配体时,提供孤电子对的通常是C原子而不是O
原子,其原因是________________________________________________________________
______________________________________________________________________________。
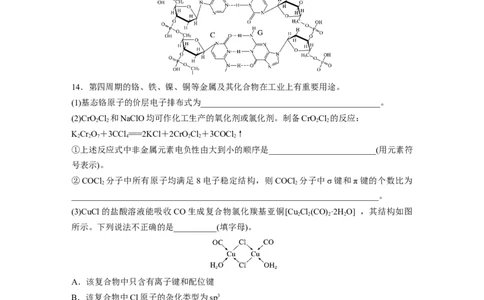
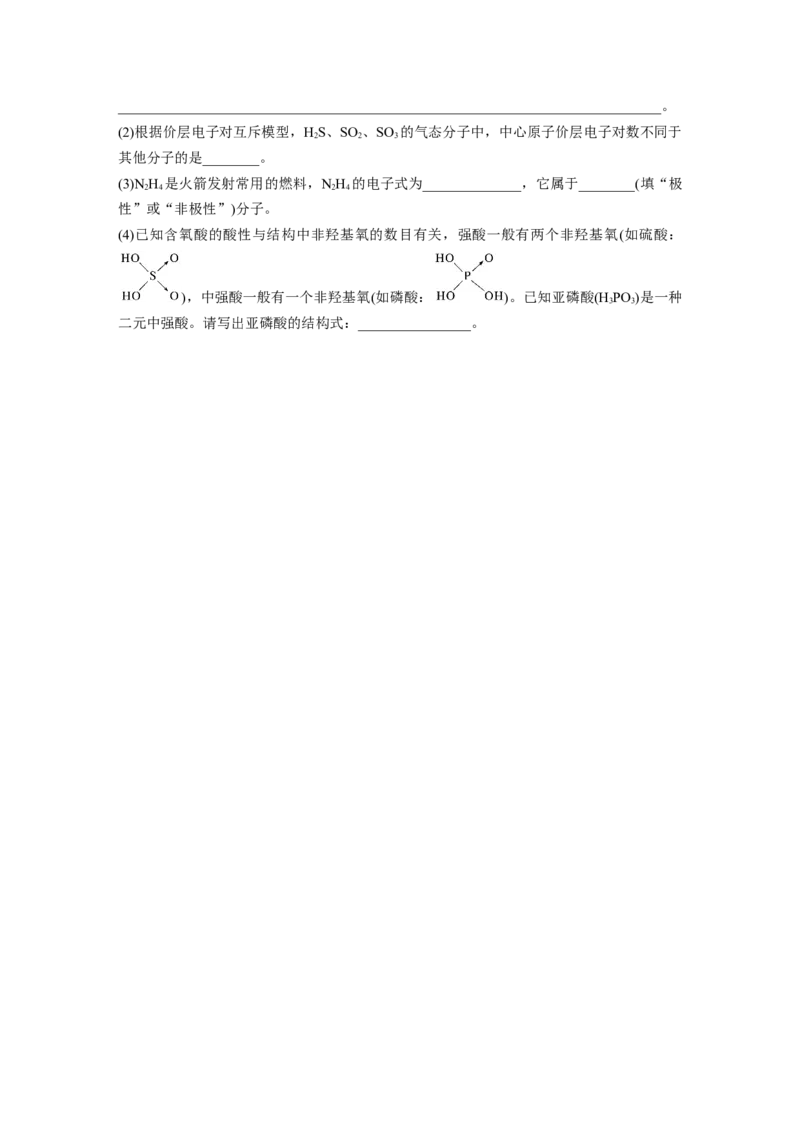
(2)如图为DNA结构局部图。DNA双螺旋是通过氢键使它们的碱基(A和T、C和G)相互配
对形成的,请写出图中存在的两种氢键的表示式:______________、______________。
14.第四周期的铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)基态铬原子的价层电子排布式为__________________________________________。
(2)CrO Cl 和NaClO均可作化工生产的氧化剂或氯化剂。制备CrOCl 的反应:
2 2 2 2
KCr O+3CCl ===2KCl+2CrOCl+3COCl ↑
2 2 7 4 2 2 2
①上述反应式中非金属元素电负性由大到小的顺序是_________________________(用元素符
号表示)。
②COCl 分子中所有原子均满足8电子稳定结构,则COCl 分子中σ键和π键的个数比为
2 2
________________________________________________________________________。
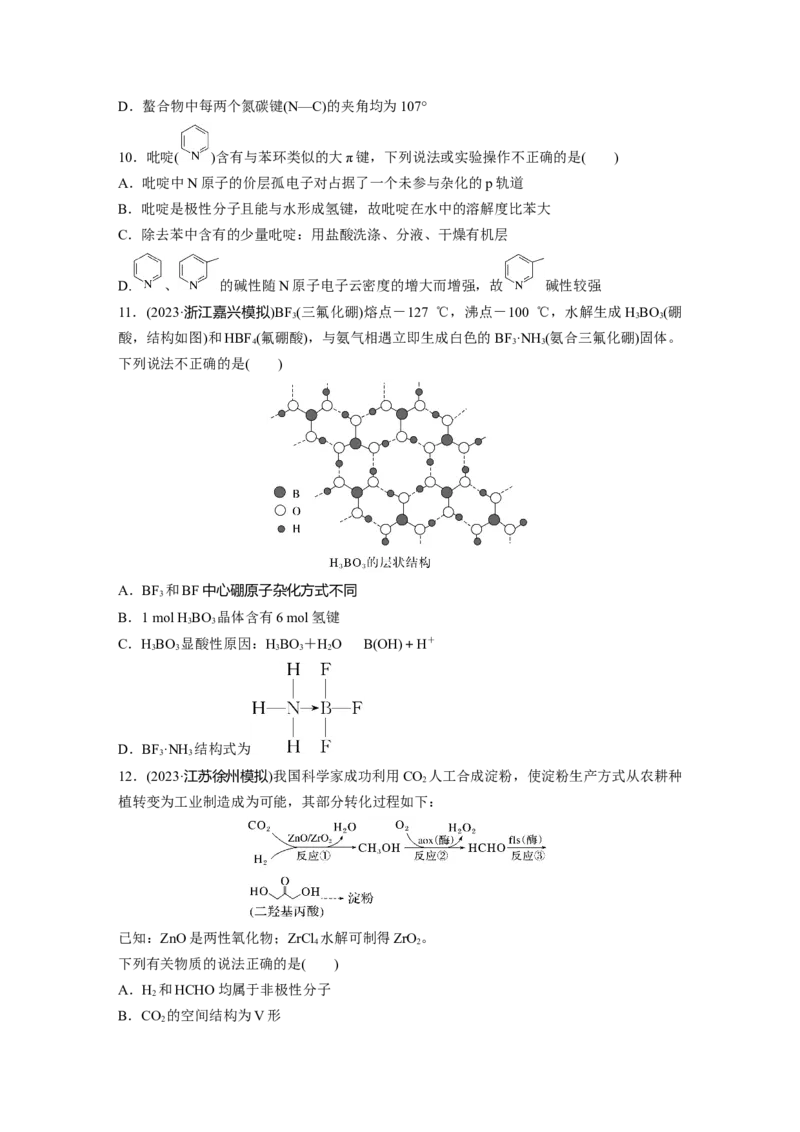
(3)CuCl的盐酸溶液能吸收CO生成复合物氯化羰基亚铜[Cu Cl(CO) ·2H O] ,其结构如图
2 2 2 2
所示。下列说法不正确的是__________(填字母)。
A.该复合物中只含有离子键和配位键
B.该复合物中Cl原子的杂化类型为sp3
C.该复合物中只有CO和HO作为配体
2
D.CO与N 的价层电子总数相同,其结构为C≡O
2
15.氮族、氧族元素及其化合物种类繁多,有许多用途,部分物质的熔、沸点如下表所示:
HO HS S SO SO HSO NH
2 2 8 2 3 2 4 2 4
熔点/°C 0 -85.5 115.2 -75.5 16.8 10.3 1.4
沸点/°C 100 -60.3 444.6 -10.0 45.0 337.0 113.5
(1)H O、NH 的熔、沸点要比HS的熔、沸点高很多,主要原因为___________________
2 2 4 2_____________________________________________________________________________。
(2)根据价层电子对互斥模型,HS、SO 、SO 的气态分子中,中心原子价层电子对数不同于
2 2 3
其他分子的是________。
(3)N H 是火箭发射常用的燃料,NH 的电子式为______________,它属于________(填“极
2 4 2 4
性”或“非极性”)分子。
(4)已知含氧酸的酸性与结构中非羟基氧的数目有关,强酸一般有两个非羟基氧(如硫酸:
),中强酸一般有一个非羟基氧(如磷酸: )。已知亚磷酸(H PO )是一种
3 3
二元中强酸。请写出亚磷酸的结构式:________________。