文档内容
考点 03 物质的量浓度及溶液配制
(好题冲关)
【基础过关】
1.配制100mL2.0mol•L-1NaOH溶液时,不需要用到的仪器是( )
A. 烧杯 B. 玻璃棒 C. 容量瓶 D. 集气瓶
2.实验中需用1.0mol·L-1的CuSO 溶液950mL,配制时选用容量瓶的规格和称取药品的质量分别为(
4
)
A B C D
容量瓶规格 1000mL 950mL 1000mL 500mL
3.下列叙述正确的是( )
A.将5.85 g NaCl晶体溶入100 mL水中,制得1 mol·L-1NaCl溶液
B.将1体积c mol·L-1硫酸用水稀释为5体积,得到0.2c mol·L-1硫酸
C.将25 g无水CuSO 溶于水配制成100 mL溶液,其浓度为1 mol·L-1
4
D.将w g a% NaCl溶液蒸发掉w/2 g水,得到4a% NaCl溶液
4.下列关于0.2 mol/L Ba(NO ) 溶液的说法中,正确的是( )
3 2
A.溶液中含有的阴、阳离子总数为0.6 mol
B.在0.5 L该溶液中,Ba2+的浓度为0.1 mol/L
C.在500 mL该溶液中,含有0.2 mol NO
D.取1 L该溶液稀释到10 L时,NO的浓度为0.02 mol/L
5.下列溶液Cl-物质的量浓度与200mL1mol·L-1AlCl 溶液中Cl-物质的量浓度相等的是( )
3
A.150mL3mol·L-1NaClO溶液 B.75mL3mol·L-1CaCl 溶液
2
C.150mL3mol·L-1KCl溶液 D.150mL2mol·L-1MgCl 溶液
2
6.下列说法正确的是( )
A.将44.8 L的HCl气体溶于水配成1 L溶液,溶液的浓度为2 mol/L
B.将40 g NaOH固体溶解在1 L水中,所得溶液的浓度恰好是1 mol/L
C.2 L0.2 mol/L的NaCl溶液与5 L0.4 mol/L的NaCl溶液的Cl-浓度之比为1:2
D.从100 mL硫酸溶液中取出10 mL,则这10 mL硫酸溶液的物质的量浓度是原溶液的
7.下列操作所得溶液的溶质的物质的量浓度为1 的是( )
资料收集整理【淘宝店铺:向阳百分百】A.将9.5g MgCl 溶于蒸馏水,配成100mL溶液
2
B.将4gNaOH固体溶于100mL蒸馏水
C.将50mL2 NaCl溶液与50mL蒸馏水混合
D.将3.36L氯化氢气体溶于水,配成150mL溶液
8.下列溶液中,溶质的物质的量浓度不是1 mol·L-1的是( )
A.10 g NaOH固体溶解在水中配成250 mL溶液
B.将80 g SO 溶于水并配成1 L的溶液
3
C.将0.5 mol·L-1的NaNO 溶液100 mL加热蒸发掉50 g水的溶液
3
D.标况下,将22.4 L氯化氢气体溶于水配成1 L溶液
9.(2023·上海市高三模拟)室温下,甲同学配制5%的 溶液100g,乙同学配制 的
溶液100mL( 的溶解度为 水),下列说法正确的是( )
A.所需溶质的质量相同 B.所需仪器均包括100mL容量瓶
C.所配溶液均为不饱和溶液 D.所配溶液质量相同
10.用质量分数为98%的浓硫酸(ρ=1.84 g·cm-3)配制240 mL 1.84 mol·L-1稀硫酸,下列操作正确的是
( )
A.将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B.必需的定量仪器有50 mL量筒、250 mL容量瓶和托盘天平
C.量取浓硫酸的体积为25.0 mL
D.先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容
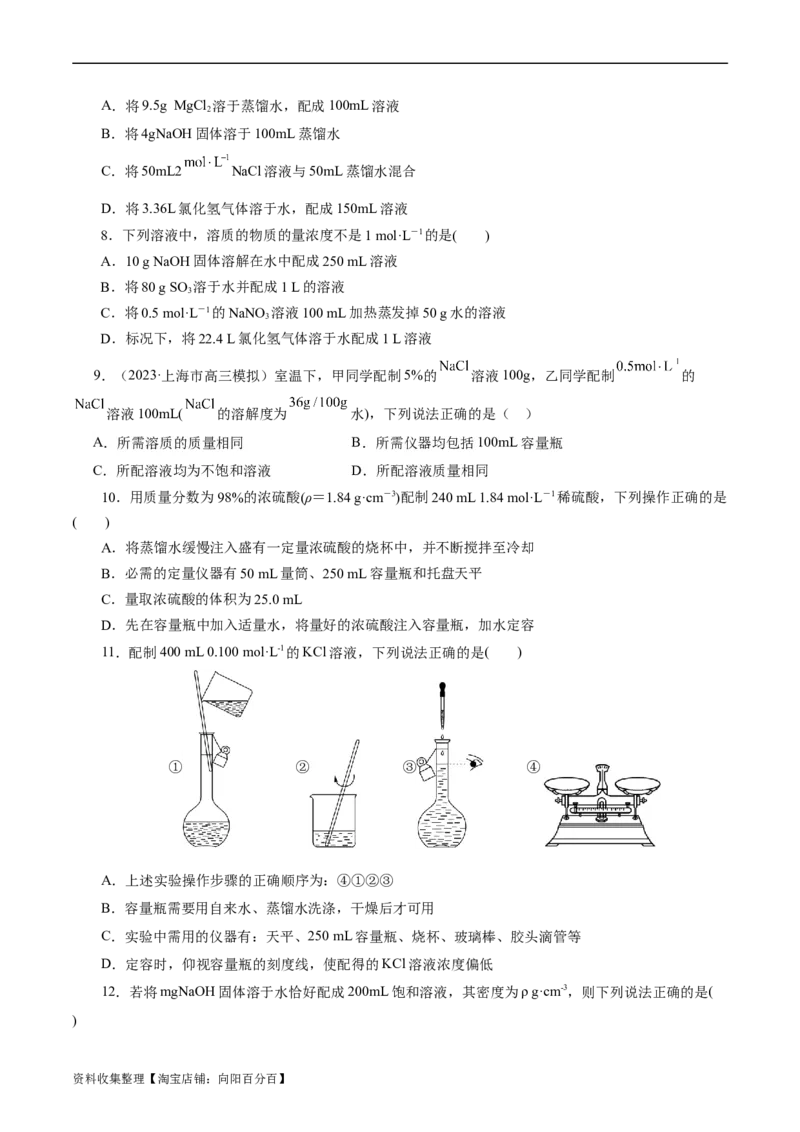
11.配制400 mL 0.100 mol·L-1的KCl溶液,下列说法正确的是( )
① ② ③ ④
A.上述实验操作步骤的正确顺序为:④①②③
B.容量瓶需要用自来水、蒸馏水洗涤,干燥后才可用
C.实验中需用的仪器有:天平、250 mL容量瓶、烧杯、玻璃棒、胶头滴管等
D.定容时,仰视容量瓶的刻度线,使配得的KCl溶液浓度偏低
12.若将mgNaOH固体溶于水恰好配成200mL饱和溶液,其密度为ρ g·cm-3,则下列说法正确的是(
)
资料收集整理【淘宝店铺:向阳百分百】A.溶质的质量分数为
B.溶质的物质的量浓度为 mol·L-1
C.溶质和溶剂的物质的量之比为 :
D.从该溶液中取出50 mL,含NaOH的物质的量为 mol
13.用密度为 质量分数是 的浓盐酸,与水配制成体积比为1:4的稀盐酸,密度为 ,
则所配制稀盐酸的物质的量浓度( )
A. B. C. D.
14.体积为VmL,密度为的ρg/cm3含有相对分子质量为M的某种物质的溶液,其中溶质为mg,其物
质的量浓度为cmol/L,溶质的质量分数为w%,则下列表示正确的是( )
A. B. C.c= D.
15.将溶质的质量分数为a%的NaOH溶液蒸发掉mg水后,变成溶质质量分数为2a%的NaOH不饱和
溶液VmL,所得溶液的物质的量浓度是( )
A. mol•L-1 B. mol•L-1 C. mol•L-1 D. mol•L-1
16.实验室用氢氧化钠固体配制 氢氧化钠溶液,得到的溶液浓度偏高,原因可能是(
)
A.氢氧化钠固体已变质 B.固体溶解后立即转移入容量瓶
C.定容时,仰视刻度线 D.容量瓶洗净后未干燥
17.标准状况下,用一定量的水吸收氨气后制得溶液(密度为0.915 g·cm-3)。该溶液中氨水的物质的量
浓度为12.0 mol·L-1,试计算:
(1)该氨水中NH 的质量分数约为 。
3
(2)1体积水需吸收 体积氨气(标准状况)可制得上述氨水。
a
(3)取 mL的上述氨水,稀释到5a mL,所得溶液中氨水的物质的量浓度为 mol·L-1。(本题
5
资料收集整理【淘宝店铺:向阳百分百】中氨水稀释过程中的其他变化忽略不计,水的密度为1.00 g·cm-3)
18.在标准状况下,将224 L HCl气体溶于635 mL水中,所得盐酸的密度为1.18 g·cm-3。试计算:
(1)所得盐酸的质量分数和物质的量浓度分别是________、________。
(2)取这种盐酸100 mL,稀释至1.18 L,所得稀盐酸的物质的量浓度是________。
(3)在40.0 mL 0.065 mol·L-1NaCO 溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不
2 3
产生CO 气体,加入稀盐酸的体积最多不超过________mL。
2
(4)将不纯的NaOH样品1 g(样品含少量NaCO 和水),放入50 mL 2 mol·L-1的盐酸中,充分反应后,
2 3
溶液呈酸性,中和多余的酸又用去 40 mL 1 mol·L-1的 NaOH 溶液。蒸发中和后的溶液,最终得到
________g固体。
19.如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题:
(1)该浓硫酸的物质的量浓度为_______mol/L。
(2)取用任意体积的该硫酸溶液时,下列物理量中不随所取体积的多少而变化的是_______。
A.溶液中HSO 的物质的量 B.溶液的浓度
2 4
C.溶液中SO 2-的数目 D.溶液的密度
4
(3)某学生欲用上述浓硫酸和蒸馏水配制480mL物质的量浓度为0.2mol/L稀硫酸。
①该学生需要量取_______mL上述浓硫酸进行配制。
②配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)_______;
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓硫酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中,用玻璃棒慢
慢搅动,使其混合均匀
C.将已冷却的硫酸沿玻璃棒注入一定体积的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
③在配制过程中,下列实验操作使所配制的稀硫酸的物质的量浓度偏高的是_______
A.用量筒量取浓硫酸时仰视观察凹液面
B.稀释用的烧杯和玻璃棒未洗涤
C.洗净的容量瓶未经干燥就用于配制溶液
D.溶液注入容量瓶前没有恢复到室温就进行定容
资料收集整理【淘宝店铺:向阳百分百】E.定容时俯视观察凹液面
F.加水超过刻度线后,用胶头滴管吸出多余的液体
(4)现将100mL该硫酸与300mL 0.4mol/LCuSO 溶液混合,体积变化忽略不计,所得溶液中SO 2-的物
4 4
质的量浓度是_______mol/L。
【能力提升】
20.某儿童检验报告单的部分数据如表所示
××医院检验报告单
名称 检测结果 单位 参考值(儿童)
锌( ) 115.92 73~180
铁( ) 36.95↓ 40~160
钙( ) 1.48 1.1~1.6
…
下列叙述错误的是( )
A.报告单中“μmol⋅L−1”、“mmol⋅L−1”均是物质的量浓度的单位
B.该儿童易患铁缺乏症
C.服用维生素C可使食物中的 在人体内转化为 ,体现了维生素C的还原性
D.检验某补铁口服液中铁元素的价态,可向口服液中先加少量氯水,再加过量硫氰酸钾溶液
21.有BaCl 和NaCl的混合溶液aL, 将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀, 消
2
耗xmolH SO ;另一份滴加AgNO 溶液,使Cl-离子完全沉淀,消耗ymol AgNO 。则原混合溶液中的
2 4 3 3
c(Na+)( )
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
22.在标准状况下,将VLA气体(摩尔质量是Mg/mol)溶于0.1L水中,所得溶液的密度为dg/cm3,则
此溶液的物质的量浓度为( )
A. B. C. D.
23.实验室配制浓度为1.0mol·L-1NaOH溶液100mL,下面有关操作及说法正确的是( )
A.称量NaOH固体时,应在托盘天平两盘上各放一张大小相同的纸片
资料收集整理【淘宝店铺:向阳百分百】B.若所称量NaOH固体中有少量NaO杂质,则造成所配溶液浓度偏低
2
C.若用10mol·L-1NaOH溶液来配制,用量筒量取10mLNaOH浓溶液倒入烧杯后,应该用同一量筒取
一定量蒸馏水倒入烧杯中
D.定容后将容量瓶反复上下颠倒摇匀,静置发现液面低于刻度线,无需再滴加蒸馏水至刻线
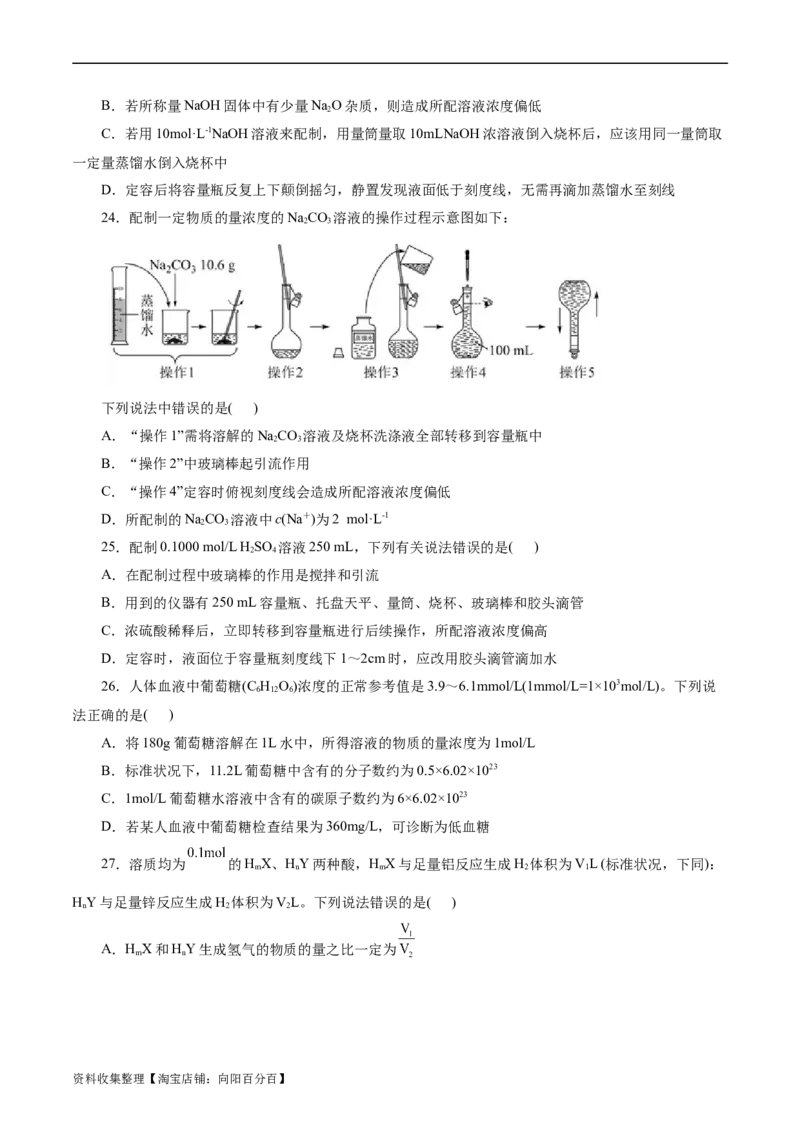
24.配制一定物质的量浓度的NaCO 溶液的操作过程示意图如下:
2 3
下列说法中错误的是( )
A.“操作1”需将溶解的NaCO 溶液及烧杯洗涤液全部转移到容量瓶中
2 3
B.“操作2”中玻璃棒起引流作用
C.“操作4”定容时俯视刻度线会造成所配溶液浓度偏低
D.所配制的NaCO 溶液中c(Na+)为2 mol·L-1
2 3
25.配制0.1000 mol/L H SO 溶液250 mL,下列有关说法错误的是( )
2 4
A.在配制过程中玻璃棒的作用是搅拌和引流
B.用到的仪器有250 mL容量瓶、托盘天平、量筒、烧杯、玻璃棒和胶头滴管
C.浓硫酸稀释后,立即转移到容量瓶进行后续操作,所配溶液浓度偏高
D.定容时,液面位于容量瓶刻度线下1~2cm时,应改用胶头滴管滴加水
26.人体血液中葡萄糖(C H O)浓度的正常参考值是3.9~6.1mmol/L(1mmol/L=1×103mol/L)。下列说
6 12 6
法正确的是( )
A.将180g葡萄糖溶解在1L水中,所得溶液的物质的量浓度为1mol/L
B.标准状况下,11.2L葡萄糖中含有的分子数约为0.5×6.02×1023
C.1mol/L葡萄糖水溶液中含有的碳原子数约为6×6.02×1023
D.若某人血液中葡萄糖检查结果为360mg/L,可诊断为低血糖
27.溶质均为 的H X、HY两种酸,H X与足量铝反应生成H 体积为VL (标准状况,下同):
m n m 2 1
HY与足量锌反应生成H 体积为VL。下列说法错误的是( )
n 2 2
A.H X和HY生成氢气的物质的量之比一定为
m n
资料收集整理【淘宝店铺:向阳百分百】B.H X和HY消耗铝和锌的物质的量之比一定为
m n
C.
D.由题给条件无法确定m和n的具体数值
28.某100 mL溶液中仅含有以下三种溶质:
向该溶液中加入过量的铁粉,标准状况下产生的气体体积最多为( )
A.8.96 L B.6.72 L C.4.48 L D.2.24 L
29.表是某人在医院血液生化检查时,化验单的部分内容:
项目名称 数据 参考值
尿素氮 3.95 2.00-6.10mmol·L-1
葡萄糖 4.50 3.89-6.11mmol·L-1
总胆固醇 3.80 <5.20mmol·L-1
甘油三酯 1.85↑ <1.70mmol·L-1
已知:1摩尔(mol)等于1000毫摩尔(mmol),血液中葡萄糖简称血糖,分子式为C H O,请根据以上
6 12 6
信息回答下列问题:
(1)这个人的血糖含量属___________(填“正常”、“偏高”或“偏低”)
(2)上表中的血液化验单各项指标的物理量是___________(填字母)
A.质量分数B.溶解度C.摩尔质量D.物质的量浓度
(3)这个人的1mL血液中含葡萄糖___________g。(有解题过程,否则不得分)
30.(2023·安徽省合肥市联考)实验室用NaCO·10H O固体配制0.2mol·L-1的NaCO 溶液 。
2 3 2 2 3
(1)配制溶液时,如下图所示的仪器中,肯定不需要的仪器是_______(填名称),需要增加的玻璃仪器是
_______(填名称),该仪器使用前必须进行的一步操作是_______。
资料收集整理【淘宝店铺:向阳百分百】(2)配制该溶液需要称量_______ g Na CO·10H O固体,若称量的固体有部分失水,则所配溶液浓度
2 3 2
_______(填“偏大”“偏小”或“无影响”)。
(3)定容时的操作是当加水至离刻度线 ,_______,若加蒸馏水时不慎超过了刻度线,应如何处
理_______。
(4)取任意体积的该溶液,下列物理量中不随所取溶液体积的多少而变化的是_______(填字母);若取
溶液稀释至 ,稀释过程中基本保持不变的是_______(填字母)。
a.溶液中 的物质的量 b.溶液的浓度 c.溶液中CO2-的数目 d.溶液的密度
3
(5)取所配溶液100mL与80mL未知浓度的BaCl 溶液充分混合,恰好完全反应,则 溶液的物质
2
的量浓度为_______。
31.“84消毒液”能有效杀灭新冠病毒,某同学购买了一瓶84消毒液,该消毒液通常稀释到100倍
(体积比)使用。查阅相关资料和消毒液包装说明得到如图信息:
84消毒液
(有效成分)NaClO
(规格)1000mL
(质量分数)25%
(密度)1.19g/cm3
(1)该84消毒液NaClO物质的量浓度约为_________mol/L(保留1位小数)。
(2)工业上84消毒液可通过电解饱和食盐水制备,同时生成氢气,请写出该反应的化学方程式
___________________________。
(3)取10mL该84消毒液稀释至1000mL。下列有关该实验的说法不正确的是
_____________________(填字母)。
A.如图所示的仪器中,需用的仪器有①②③④⑥
B.使用前要检查容量瓶是否漏液
C.容量瓶上标有容积、温度和浓度
D.容量瓶用蒸馏水洗净后,须烘干后再使用
E.容量瓶使用完毕后,应洗净、晾干,对于玻璃磨口瓶塞,应在瓶塞与瓶口处垫一张纸条,以免瓶
资料收集整理【淘宝店铺:向阳百分百】