文档内容
考点 11 氮及其化合物
(好题冲关)
【基础过关】
1.(2022·重庆市育才中学模拟预测)氯化汞与氨水发生反应2NH +HgCl=Hg(NH )Cl↓+NH Cl,相关物质
3 2 2 4
的化学用语正确的是( )
A. 的结构示意图为 B. 的结构式为
C.NH 的电子式为 D.Hg(NH)Cl中N的化合价为
3 2
2.(2023·海南省海口市高三联考)下列关于氮及其化合物的探究,结论和解释正确的是( )
操作和现象 结论和解释
A 铜丝溶解于稀HNO,生成无色气体 金属能与强酸反应置换出氢气
3
B NH 能使热的氧化铜产生红色物质 NH 有还原性
3 3
C N 与H 混合加热不反应 N的非金属性弱
2 2
D NO 被 溶液吸收 NO 是酸性氧化物
2 2
3.下列制取NH HCO 的实验原理与装置能达到实验目的的是( )
4 3
A.用装置甲制取NH B.用装置乙制取CO
3 2
C.用装置丙制取NH HCO 溶液 D.用装置丁获得NH HCO 固体
4 3 4 3
4.(2023·广东省深圳市高三模拟)含氮化合物的反应具有多样性。下列有关反应方程式书写不正确的
是( )
A.将少量浓氨水滴入盛有CaO的烧瓶制备NH :NH ∙H O + CaO =Ca(OH) + NH ↑
3 3 2 2 3
B.将Cu丝伸入装有稀硝酸的试管:Cu + 2HNO = Cu(NO ) + H ↑
3 3 2 2
C.浓硝酸受热分解:4H++4NO- 4NO ↑+ O ↑+ 2H O
3 2 2 2
资料收集整理【淘宝店铺:向阳百分百】D.镁条在N 中燃烧:3Mg + N Mg N
2 2 3 2
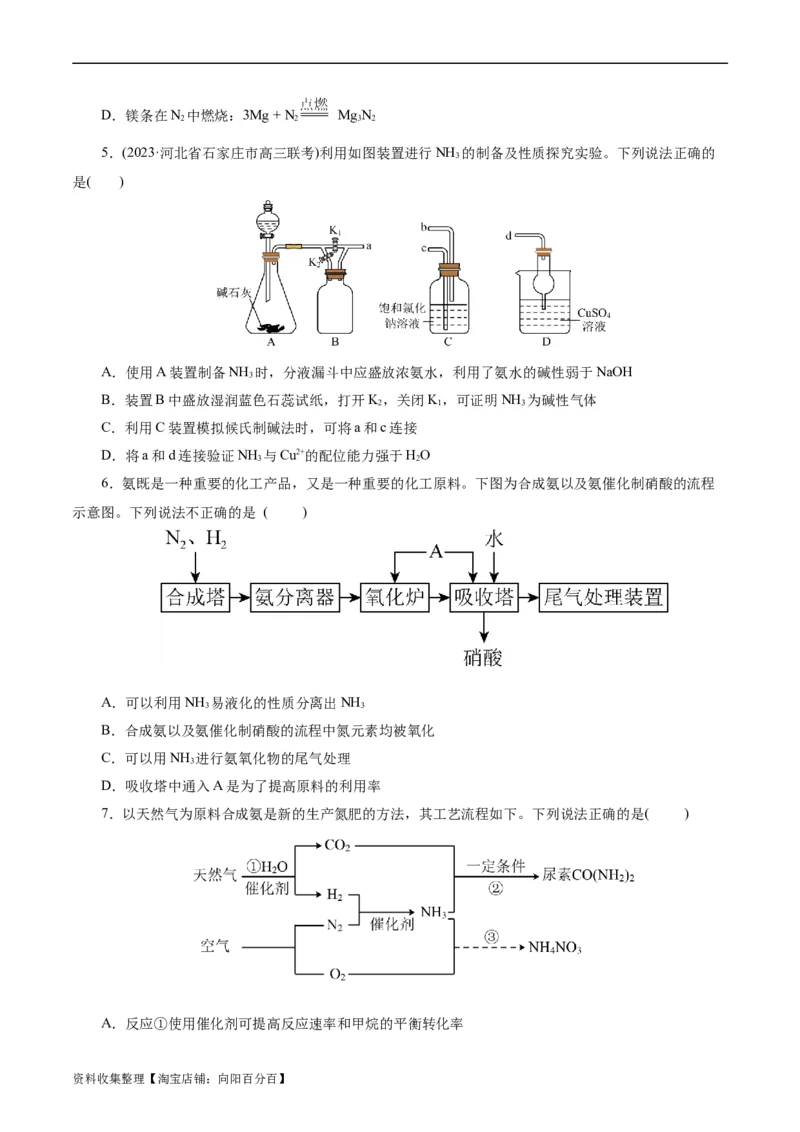
5.(2023·河北省石家庄市高三联考)利用如图装置进行NH 的制备及性质探究实验。下列说法正确的
3
是( )
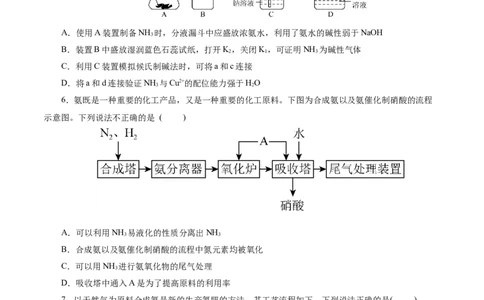
A.使用A装置制备NH 时,分液漏斗中应盛放浓氨水,利用了氨水的碱性弱于NaOH
3
B.装置B中盛放湿润蓝色石蕊试纸,打开K,关闭K,可证明NH 为碱性气体
2 1 3
C.利用C装置模拟候氏制碱法时,可将a和c连接
D.将a和d连接验证NH 与Cu2+的配位能力强于HO
3 2
6.氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨催化制硝酸的流程
示意图。下列说法不正确的是 ( )
A.可以利用NH 易液化的性质分离出NH
3 3
B.合成氨以及氨催化制硝酸的流程中氮元素均被氧化
C.可以用NH 进行氨氧化物的尾气处理
3
D.吸收塔中通入A是为了提高原料的利用率
7.以天然气为原料合成氨是新的生产氮肥的方法,其工艺流程如下。下列说法正确的是( )
A.反应①使用催化剂可提高反应速率和甲烷的平衡转化率
资料收集整理【淘宝店铺:向阳百分百】B.反应②的原子利用率为100%
C.生成1.0 mol NH NO 至少需要0.75 mol CH
4 3 4
D.反应③理论上当n( NH):n(O )= 4:3时,恰好完全反应
3 2
8.氮及其化合物在生产生活中具有广泛的应用。氨气可用于生产氮肥和处理NO 等气体,氨水可用
x
于吸收SO ,NO 可用于制取硝酸,硝酸可洗涤试管上的银镜。NO 能与悬浮在大气中海盐粒子相互作用,
2 x 2
反应为2NO +NaCl=NaNO +ClNO(ClNO中N为中心原子,各原子均达到8电子稳定结构)。NO能被FeSO
2 3 4
溶液吸收生成[Fe(NO)HO) ]SO 。在给定条件下,下列选项所示的物质间转化均能实现的是( )
2 5 4
A.NH ·H O(aq) NH HSO (aq) B.NH NO
3 2 4 3 3 2
C.NO HNO D.Ag H
3 2
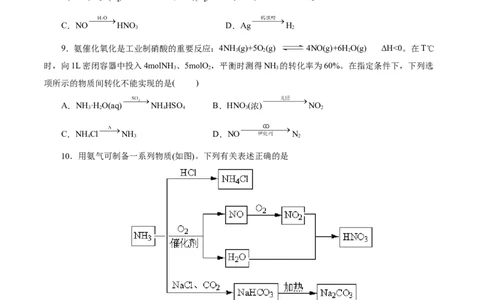
9.氨催化氧化是工业制硝酸的重要反应:4NH (g)+5O(g) 4NO(g)+6H O(g) ΔH<0。在T℃
3 2 2
时,向1L密闭容器中投入4molNH 、5molO ,平衡时测得NH 的转化率为60%。在指定条件下,下列选
3 2 3
项所示的物质间转化不能实现的是( )
A.NH ·H O(aq) NH HSO B.HNO(浓) NO
3 2 4 4 3 2
C.NH Cl NH D.NO N
4 3 2
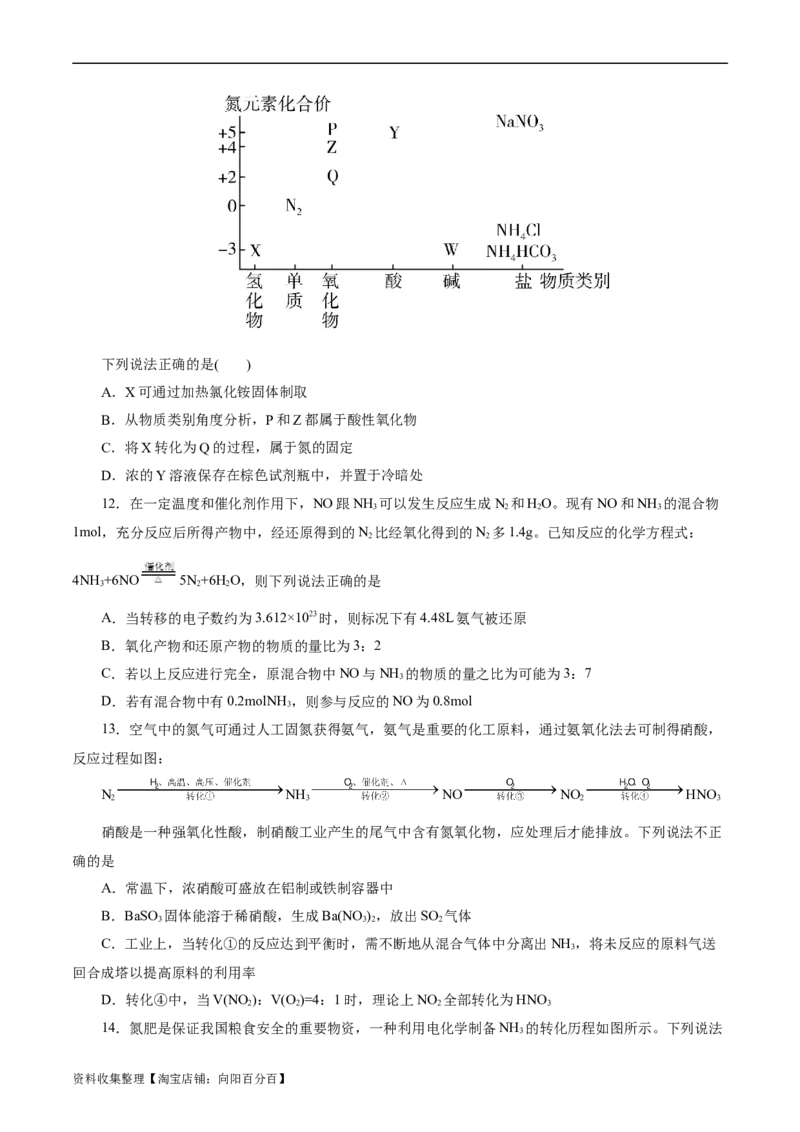
10.用氨气可制备一系列物质(如图)。下列有关表述正确的是
A.可加热分解NH Cl制NH
4 3
B.NH Cl和NaHCO 都是常见的化肥
4 3
C.NH 和NO 在一定条件下可发生反应
3 2
D.NH Cl、HNO 和NaCO 受热时都易分解
4 3 2 3
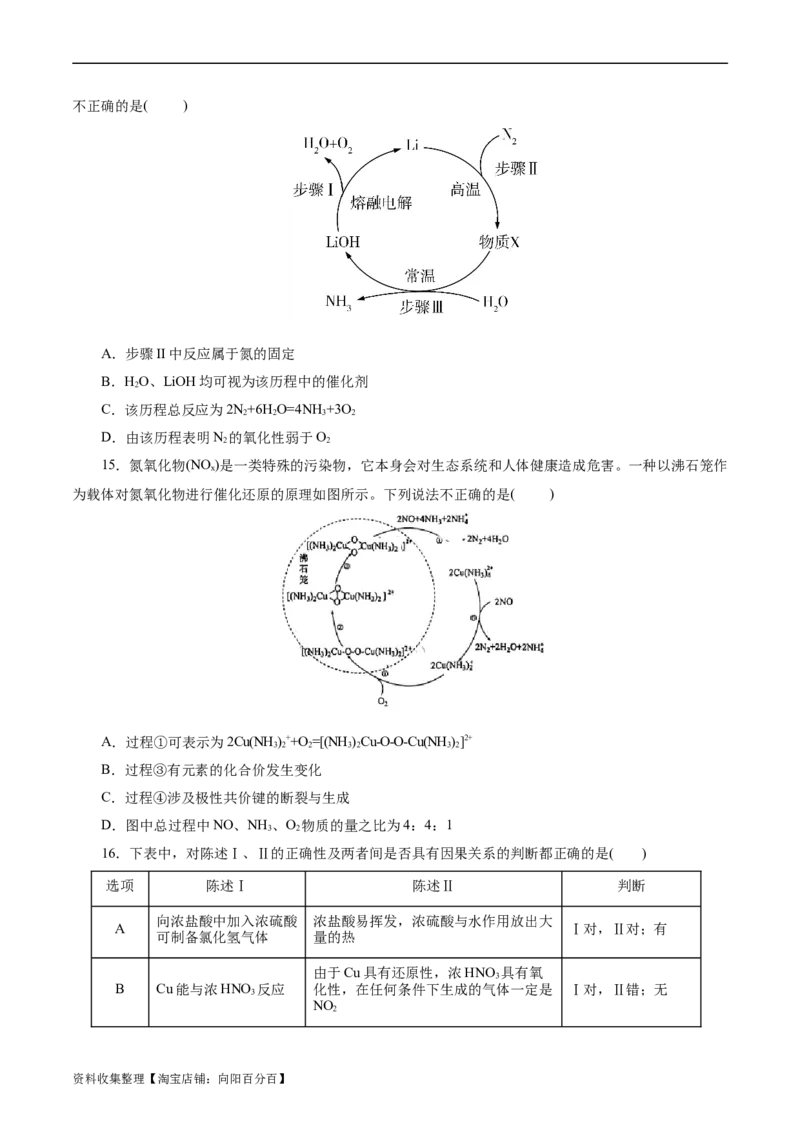
11.(2023·福建省德化一中、永安一中、漳平一中三校协作体高三联考)氮及其化合物的“价—类”二
维图如下所示。
资料收集整理【淘宝店铺:向阳百分百】下列说法正确的是( )
A.X可通过加热氯化铵固体制取
B.从物质类别角度分析,P和Z都属于酸性氧化物
C.将X转化为Q的过程,属于氮的固定
D.浓的Y溶液保存在棕色试剂瓶中,并置于冷暗处
12.在一定温度和催化剂作用下,NO跟NH 可以发生反应生成N 和HO。现有NO和NH 的混合物
3 2 2 3
1mol,充分反应后所得产物中,经还原得到的N 比经氧化得到的N 多1.4g。已知反应的化学方程式:
2 2
4NH +6NO 5N+6H O,则下列说法正确的是
3 2 2
A.当转移的电子数约为3.612×1023时,则标况下有4.48L氨气被还原
B.氧化产物和还原产物的物质的量比为3:2
C.若以上反应进行完全,原混合物中NO与NH 的物质的量之比为可能为3:7
3
D.若有混合物中有0.2molNH ,则参与反应的NO为0.8mol
3
13.空气中的氮气可通过人工固氮获得氨气,氨气是重要的化工原料,通过氨氧化法去可制得硝酸,
反应过程如图:
N NH NO NO HNO
2 3 2 3
硝酸是一种强氧化性酸,制硝酸工业产生的尾气中含有氮氧化物,应处理后才能排放。下列说法不正
确的是
A.常温下,浓硝酸可盛放在铝制或铁制容器中
B.BaSO 固体能溶于稀硝酸,生成Ba(NO ),放出SO 气体
3 3 2 2
C.工业上,当转化①的反应达到平衡时,需不断地从混合气体中分离出NH ,将未反应的原料气送
3
回合成塔以提高原料的利用率
D.转化④中,当V(NO):V(O )=4:1时,理论上NO 全部转化为HNO
2 2 2 3
14.氮肥是保证我国粮食安全的重要物资,一种利用电化学制备NH 的转化历程如图所示。下列说法
3
资料收集整理【淘宝店铺:向阳百分百】不正确的是( )
A.步骤II中反应属于氮的固定
B.HO、LiOH均可视为该历程中的催化剂
2
C.该历程总反应为2N+6H O=4NH +3O
2 2 3 2
D.由该历程表明N 的氧化性弱于O
2 2
15.氮氧化物(NO )是一类特殊的污染物,它本身会对生态系统和人体健康造成危害。一种以沸石笼作
x
为载体对氮氧化物进行催化还原的原理如图所示。下列说法不正确的是( )
A.过程①可表示为2Cu(NH )++O =[(NH )Cu-O-O-Cu(NH )]2+
3 2 2 3 2 3 2
B.过程③有元素的化合价发生变化
C.过程④涉及极性共价键的断裂与生成
D.图中总过程中NO、NH 、O 物质的量之比为4:4:1
3 2
16.下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选项 陈述Ⅰ 陈述Ⅱ 判断
向浓盐酸中加入浓硫酸 浓盐酸易挥发,浓硫酸与水作用放出大
A Ⅰ对,Ⅱ对;有
可制备氯化氢气体 量的热
由于Cu具有还原性,浓HNO 具有氧
3
B Cu能与浓HNO 反应 化性,在任何条件下生成的气体一定是 Ⅰ对,Ⅱ错;无
3
NO
2
资料收集整理【淘宝店铺:向阳百分百】硫单质在纯氧中燃烧有
C 部分二氧化硫被氧化为SO Ⅰ对,Ⅱ对;无
少量SO 生成 3
3
硝酸铵和碱石灰共热用
D 铵盐与碱能发生复分解反应 Ⅰ对,Ⅱ对;有
于实验室制备NH
3
17.研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价-物质类别关系图如图
回答下列问题:
(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是_______。
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:_______。
(3)实验室中,检验溶液中含有NH 的操作方法是_______。
4+
(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:_______,当反应消耗0.15 mol物质B
时,转移电子的物质的量为_______。
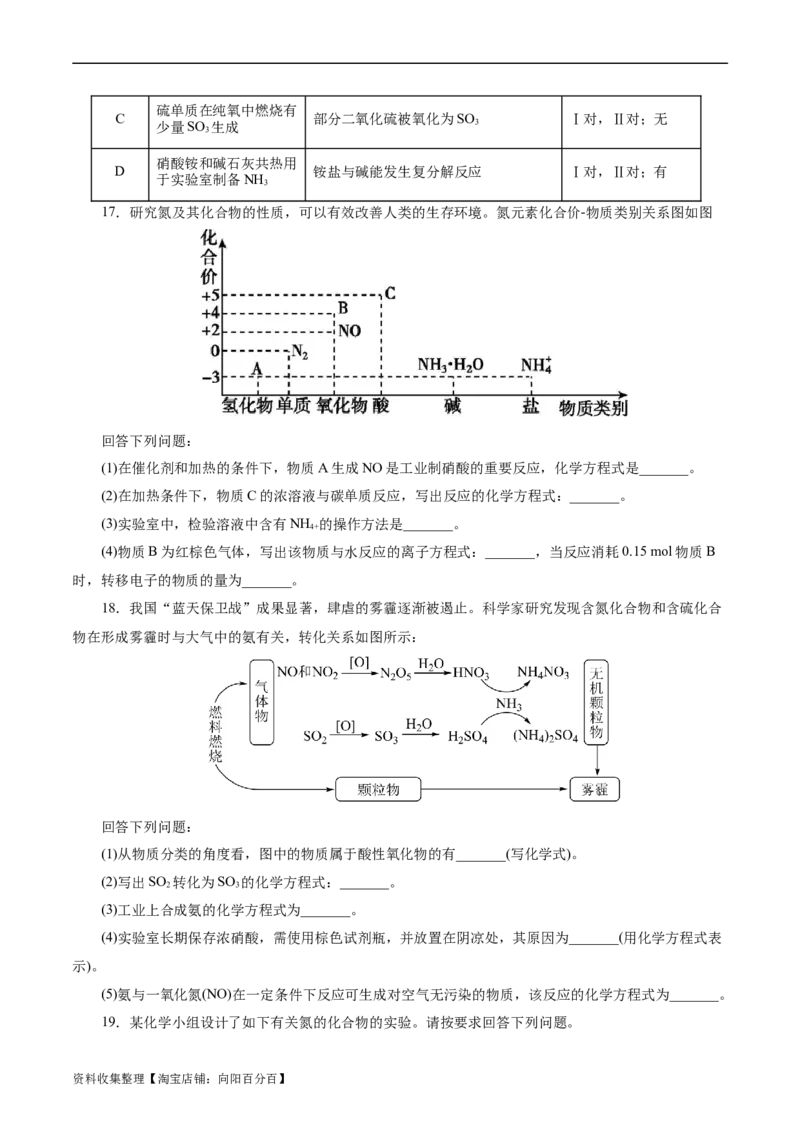
18.我国“蓝天保卫战”成果显著,肆虐的雾霾逐渐被遏止。科学家研究发现含氮化合物和含硫化合
物在形成雾霾时与大气中的氨有关,转化关系如图所示:
回答下列问题:
(1)从物质分类的角度看,图中的物质属于酸性氧化物的有_______(写化学式)。
(2)写出SO 转化为SO 的化学方程式:_______。
2 3
(3)工业上合成氨的化学方程式为_______。
(4)实验室长期保存浓硝酸,需使用棕色试剂瓶,并放置在阴凉处,其原因为_______(用化学方程式表
示)。
(5)氨与一氧化氮(NO)在一定条件下反应可生成对空气无污染的物质,该反应的化学方程式为_______。
19.某化学小组设计了如下有关氮的化合物的实验。请按要求回答下列问题。
资料收集整理【淘宝店铺:向阳百分百】(1)氨气的喷泉实验:如下图装置所示,干燥的圆底烧瓶里充满NH ,欲观察到烧瓶中产生喷泉,需进
3
行的操作是_______。
(2)硝酸的制备实验:如图所示a~f装置。
①装置a的最佳选择为(填“图3”或“图4”)_______。
②装置b中NaO 的作用是_______。
2 2
(3)硝酸的性质实验:
①常温下,同学甲在上图实验结束后,用pH计测装置e中溶液的pH=1.00。
ⅰ.这说明e中发生的反应可能为(写化学方程式)_______。
ⅱ.同学乙做同样实验,测得e中溶液的pH=6.00,可能原因是_______。
②用如图所示装置进行硝酸与铜的反应实验。
资料收集整理【淘宝店铺:向阳百分百】ⅰ.请在h方框中补全该实验所需装置图并标注所需试剂_______。
ⅱ.硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因:_______。
ⅲ.g中为稀硝酸时,反应开始后,g中溶液颜色变蓝。写出g中反应的离子方程式:_______。
ⅳ.g中为浓硝酸时,g中溶液颜色变绿。反应较ⅱ中剧烈许多的原因是_______。
ⅴ.对比ⅲ与ⅳ反应后g中溶液颜色,推测其原因是ⅳ反应后g溶液中溶有NO 且达饱和。为证明该
2
推测正确,向ⅳ反应后g溶液中加入_______,会观察到溶液颜色由绿色变为蓝色。
ⅵ.已知[Cu(H O) ]2+(aq)呈蓝色、[CuCl ]2-(aq)呈黄色。取ⅰ中少量蓝色溶液于试管中,向其中滴加饱
2 4 4
和NaCl溶液,观察到溶液颜色由蓝变为蓝绿色,再加热该混合溶液,溶液颜色逐渐变为黄绿色。结合离
子反应方程式解释其原因:_______。
20.含氮化合物的处理对环境保护意义重大。
(1)用H 或CO催化还原NO均能达到消除污染的目的,反应的氧化产物为_______。
2
(2)实验室常用NaOH溶液吸收NO (NO和NO 的混合气体),反应的化学方程式如下:(已知NO不能
x 2
与NaOH溶液反应,不考虑NO 与NO 的转化)
2 2 4
NO+NO +2NaOH=2NaNO +H O
2 2 2
2NO +2NaOH=NaNO +NaNO +H O
2 2 3 2
①若NO 能被NaOH溶液完全吸收,则x的取值范围为_______
x
②若nmolNaOH恰好完全反应,则被吸收的NO 的体积为_____L(标准状况)。
x
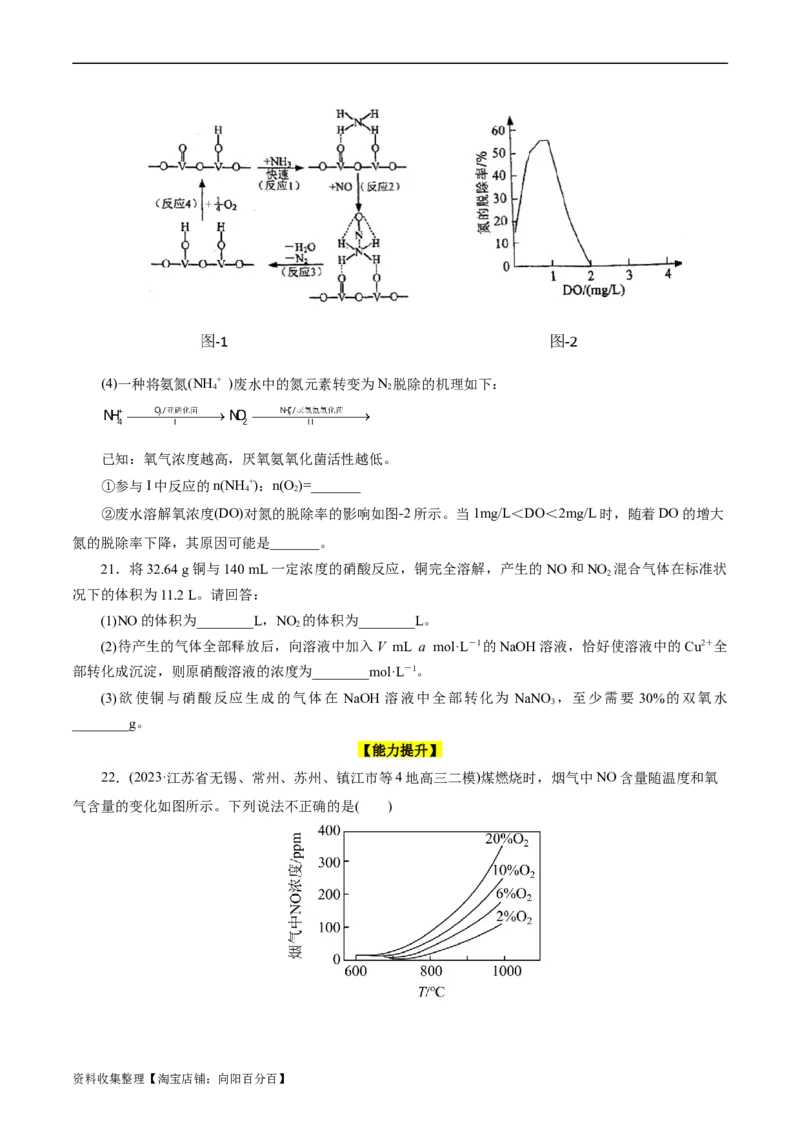
(3)用VO 作催化剂,NH 将NO还原成N 的一种反应历程如图-1所示,则总反应方程式为_____。
2 5 3 2
资料收集整理【淘宝店铺:向阳百分百】(4)一种将氨氮(NH + )废水中的氮元素转变为N 脱除的机理如下:
4 2
已知:氧气浓度越高,厌氧氨氧化菌活性越低。
①参与I中反应的n(NH +):n(O )=_______
4 2
②废水溶解氧浓度(DO)对氮的脱除率的影响如图-2所示。当1mg/L<DO<2mg/L时,随着DO的增大
氮的脱除率下降,其原因可能是_______。
21.将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO 混合气体在标准状
2
况下的体积为11.2 L。请回答:
(1)NO的体积为________L,NO 的体积为________L。
2
(2)待产生的气体全部释放后,向溶液中加入V mL a mol·L-1的NaOH溶液,恰好使溶液中的Cu2+全
部转化成沉淀,则原硝酸溶液的浓度为________mol·L-1。
(3)欲使铜与硝酸反应生成的气体在 NaOH 溶液中全部转化为 NaNO ,至少需要 30%的双氧水
3
________g。
【能力提升】
22.(2023·江苏省无锡、常州、苏州、镇江市等4地高三二模)煤燃烧时,烟气中NO含量随温度和氧
气含量的变化如图所示。下列说法不正确的是( )
资料收集整理【淘宝店铺:向阳百分百】A.燃煤过程中发生了氮的固定 B.燃煤温度越高NOx污染越重
C.含氧量越高越容易生成NO D.煤燃烧不影响自然界氮循环
23.(2023·江苏省扬州市高三联考)NH 是重要的化工原料,可用于某些配合物的制备,如NiSO 溶于
3 4
氨水形成[Ni(NH )]SO 。液氨可以微弱的电离产生NH -和NH +,NH 中的一个H原子若被-NH 取代可形成
3 6 4 2 4 3 2
NH(联氨),若被-OH取代可形成NH OH (羟胺)。NH 经过转化可形成N、NO、NO 、NO(无色)HNO 等。
2 4 2 3 2 2 2 4 3
NH 与NO 反应有气体生成,同时放出大量热。下列化学反应的表示不正确的是( )
2 4 2
A.向硫酸镍中通入过量氨气:Ni2++6 NH ·H O =Ni(NH )]2++6H O
3 2 3 6 2
B.氨气的燃烧热:4NH (g)+ 3O (g)=2N (g)+6HO(g)ΔH=-1526 kJ·mol-1
3 2 2 2
C.向稀硝酸中加入过量铁粉:3Fe+8HNO =3Fe(NO)+2NO↑+4H O
3 3 2 2
D.硫酸铵溶液和氢氧化钡溶液反应: 2NH +SO2-+ Ba2++2OH-=BaSO ↓+2 NH ·H O
4 4 4 3 2
24.(2023·重庆市拔尖强基联合高三定时检测)某实验小组探究NiO能否催化NO和CO反应生成无毒
物质。已知:①Ni、Fe的氢氧化物化学性质相似;②2NO(g)+ 2CO(g) N (g)+2CO(g) ΔH<0 。
2 2
现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是( )
A.从理论上推断,NO(g)与CO(g)生成N (g)和CO (g)的反应,高温有利于自发进行
2 2
B.在空气中加热Ni(OH) 可制备NiO
2
C.打开装置1中气球,通过观察气体是否变为红棕色判断是否生成N
2
D.若以上实验证明NiO能够成功催化该反应,且固体A是Ni O,则装置2中的反应方程式为:
2 3
Ni O+CO 2NiO+CO
2 3 2
25.化学小组探究铜与硝酸反应的快慢及产物。
实验 开始无明显现象,渐有小气泡生成,液面上方出现
Ⅰ 浅红棕色气体,溶液呈蓝色。
实验 最初反应较慢,随后加快,反应剧烈;产生红棕色
Ⅱ 气体;溶液呈绿色。
资料:铜与浓HNO 反应一旦发生就变快,生成的NO 可溶于水形成HNO(弱酸),反应就加快。
3 2 2
下列说法正确的是( )
资料收集整理【淘宝店铺:向阳百分百】