文档内容
考点 19 电解池
(核心考点精讲精练)
一、3年真题考点分布
考点内容 考题统计
2023浙江1月选考11题,3分;2023辽宁卷7题,3分;2022广东卷
电解原理 10题,2分;2022北京卷13题,3分;2021海南卷9题,4分;2021
天津卷11题,3分;
2023湖北卷10题,3分;2023全国甲卷13题,6分;2023浙江6月
选考13题,3分;2023北京卷5题,3分;2023广东卷13题,4分;
2023广东卷16题,4分;2022重庆卷12题,4分;2022海南卷9
电解原理综合应用 题,4分;2022湖北卷14题,3分;2022湖南卷8题,3分;2022浙
江1月选考21题,2分;2022浙江6月选考21题,2分;2021全国
甲卷13题,6分;2021广东卷16题,4分;2021湖北卷15题,3
分;2021辽宁卷13题,3分;
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,电解的原理和应用是历年高考热点,主要在选择题中电化学题、工艺流程题、
原理综合题中出现。主要包含金属的精炼、氯碱工业、活泼金属的制取、有关电解产物的判断和计算等内
容。必须熟悉微粒在各种电极上的放电次序,这样才能准确地判断出相关的电解产物,然后进行有关的计
算。有关电解的计算通常可根据电解方程式或电极反应式列比例求解或是利用各电极、线路中转移的电子
数目守恒列等式求解。
【备考策略】
备考时注重实物图分析、新型电解装置分析,从氧化还原反应的角度认识电化学,注重与元素化合物、
有机化学、电解质溶液、化学实验设计、新能源等知识的联系。关注氯碱工业、电镀和粗铜的电解精炼等,
通过新的电解装置的应用,能对与化学有关的热点问题作出正确的价值判断,能参与有关化学问题的社会
实践。
【命题预测】
预测2024年高考仍会考查电解原理在实际化工生产中的应用,结合物质制备、分离和提纯等知识综合
考查,涉及电极反应式的书写、物质的提纯操作以及电极反应产物的判断等。能多角度、动态地分析电解
池中发生的反应,掌握好放电顺序,总结好电解规律,对于设题方式多且灵活多变的实物图分析问题,应
加以关注。
资料收集整理【淘宝店铺:向阳百分百】考法 1 电解池的工作原理
1.电解和电解池
(1)电解:在电流作用下,电解质在两个电极上分别发生氧化反应和还原反应的过程。
(2)电解池:电能转化为化学能的装置。
(3)电解池的构成
①有与电源相连的两个电极。
②电解质溶液(或熔融电解质)。
③形成闭合回路。
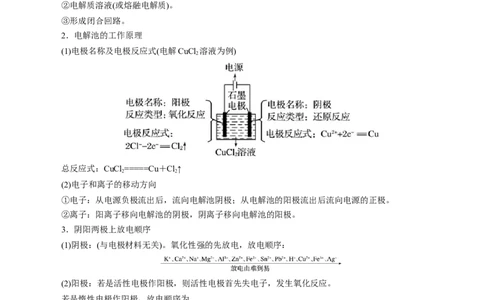
2.电解池的工作原理
(1)电极名称及电极反应式(电解CuCl 溶液为例)
2
总反应式:CuCl =====Cu+Cl↑
2 2
(2)电子和离子的移动方向
①电子:从电源负极流出后,流向电解池阴极;从电解池的阳极流出后流向电源的正极。
②离子:阳离子移向电解池的阴极,阴离子移向电解池的阳极。
3.阴阳两极上放电顺序
(1)阴极:(与电极材料无关)。氧化性强的先放电,放电顺序:
(2)阳极:若是活性电极作阳极,则活性电极首先失电子,发生氧化反应。
若是惰性电极作阳极,放电顺序为
注意:①阴极不管是什么材料,电极本身都不反应,一定是溶液(或熔融电解质)中的阳离子放电。②
最常用、最重要的放电顺序为阳极:Cl->OH-;阴极:Ag+>Cu2+>H+。③电解水溶液时,K+~Al3+不可
能在阴极放电,即不可能用电解水溶液的方法得到K、Ca、Na、Mg、Al等金属。
4.“五类”依据判断电解池电极
判断依据
电极材料 电极反应 电子流向 离子移向 电极现象
电极
阳极 与电源正极相连 氧化反应 流出 阴离子移向 电极溶解或
资料收集整理【淘宝店铺:向阳百分百】pH减小
电极增重或
阴极 与电源负极相连 还原反应 流入 阳离子移向
pH增大
5.电化学综合计算的三种常用方法
(1)根据总反应式计算
先写出电极反应式,再写出总反应式,最后根据总反应式列出比例式计算。
(2)根据电子守恒计算
①用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中转移的电
子数相等。
②用于混合溶液中电解的分阶段计算。
(3)根据关系式计算
根据得失电子守恒定律建立起已知量与未知量之间的桥梁,构建计算所需的关系式。
如以通过4 mol e-为桥梁可构建如下关系式:
(式中M为金属,n为其离子的化合价数值)
该关系式具有总揽电化学计算的作用和价值,熟记电极反应式,灵活运用关系式便能快速解答常见的
电化学计算问题。
1.惰性电极电解电解质溶液的产物判断(图示)
2.“串联”类装置的解题流程
资料收集整理【淘宝店铺:向阳百分百】请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)电解质溶液的导电过程就是电解质溶液被电解的过程( )
(2)某些不能自发进行的氧化还原反应,通过电解可以实现( )
(3)直流电源跟电解池连接后,电子从电源负极流向电解池阳极( )
(4)电解稀硫酸制H、O 时,可用不活泼的铜做阳极( )
2 2
(5)电解CuCl 溶液,阴极逸出的气体能够使湿润的淀粉碘化钾试纸变蓝色( )
2
(6)电解盐酸、硫酸等溶液,H+放电,溶液的pH均增大( )
(7)电解时,电子的移动方向为:电源负极→阴极→阳极→电源正极( )
(8)电解盐酸、硫酸等溶液,H+放电,溶液的pH逐渐增大( )
(9)用惰性电极电解CuSO 溶液一段时间后,加入Cu(OH) 可使电解质溶液恢复到电解前的情况( )
4 2
答案:(1)√ (2)√ (3)× (4)× (5)× (6)× (7)× (8)× (9)×
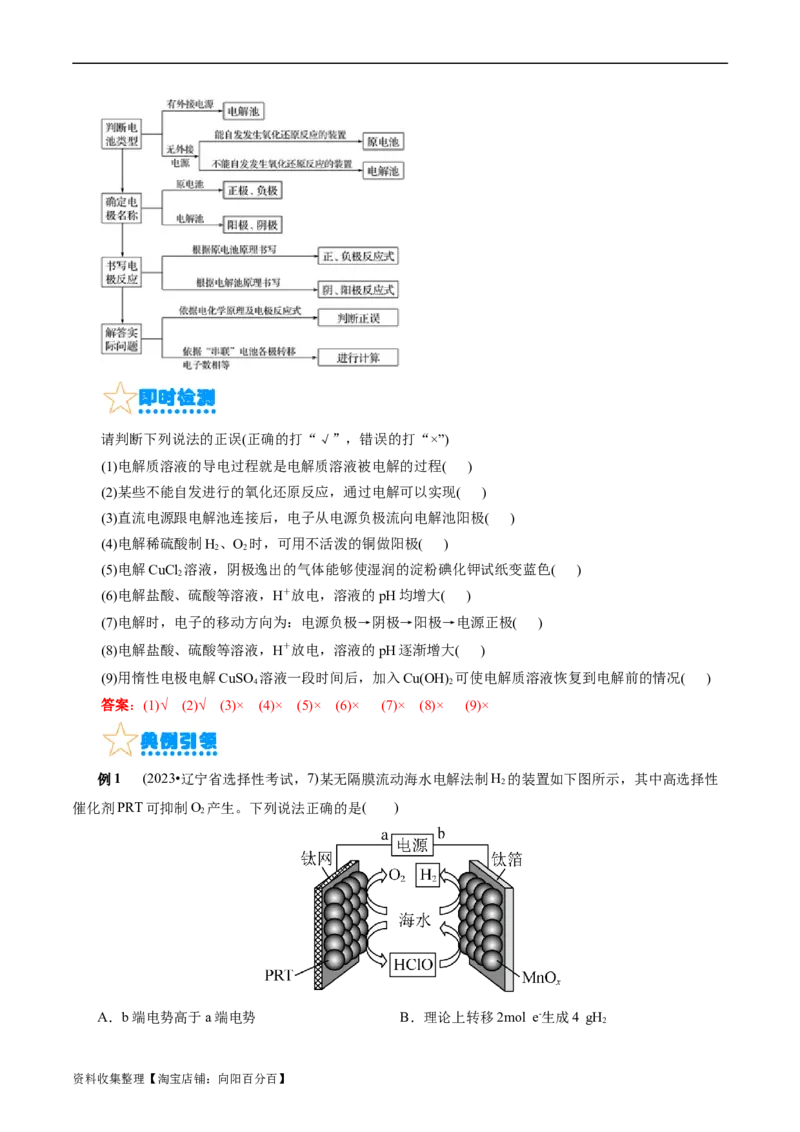
例1 (2023•辽宁省选择性考试,7)某无隔膜流动海水电解法制H 的装置如下图所示,其中高选择性
2
催化剂PRT可抑制O 产生。下列说法正确的是( )
2
A.b端电势高于a端电势 B.理论上转移2mol e-生成4 gH
2
资料收集整理【淘宝店铺:向阳百分百】C.电解后海水pH下降 D.阳极发生:Cl-+H O-2e-=HClO+H+
2
【答案】D
【解析】由图可知,左侧电极产生氧气,则左侧电极为阳极,电极a为正极,右侧电极为阴极,b电极
为负极,该装置的总反应产生氧气和氢气,相当于电解水。A项,由分析可知,a为正极,b电极为负极,
则a端电势高于b端电势,A错误;B项,右侧电极上产生氢气的电极方程式为:2H++2e-=H ↑,则理论上
2
转移2mol e-生成2 gH ,B错误;C项,由图可知,该装置的总反应为电解海水的装置,随着电解的进行,
2
海水的浓度增大,但是其pH基本不变,C错误;D项,由图可知,阳极上的电极反应为:Cl-+H O-2e-
2
=HClO+H+,D正确;故选D。
例2 (2022·浙江省6月选考)通过电解废旧锂电池中的LiMn O 可获得难溶性的LiCO 和MnO ,电
2 4 2 3 2
解示意图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不
计)。下列说法不正确的是( )
A.电极A为阴极,发生还原反应
B.电极B的电极发应:2HO+Mn2+-2e-=MnO+4H+
2 2
C.电解一段时间后溶液中Mn2+浓度保持不变
D.电解结束,可通过调节 除去Mn2+,再加入NaCO 溶液以获得LiCO
2 3 2 3
【答案】C
【解析】A项,由电解示意图可知,电极B上Mn2+转化为了MnO ,锰元素化合价升高,失电子,则
2
电极B为阳极,电极A为阴极,得电子,发生还原反应,A正确;B项,由电解示意图可知,电极B上
Mn2+失电子转化为了MnO ,电极反应式为:2HO+Mn2+-2e-=MnO+4H+,B正确;C项,电极A为阴极,
2 2 2
LiMn O 得电子,电极反应式为:2LiMn O+6e-+16H+=2Li++4Mn2++8H O,依据得失电子守恒,电解池总反
2 4 2 4 2
应为:2LiMn O+4H+=2Li++Mn2++3MnO+2H O,反应生成了Mn2+,Mn2+浓度增大,C错误;D项,电解池
2 4 2 2
总反应为:2LiMn O+4H+=2Li++Mn2++3MnO+2H O,电解结束后,可通过调节溶液pH将锰离子转化为沉
2 4 2 2
淀除去,然后再加入碳酸钠溶液,从而获得碳酸锂,D正确;故选C。
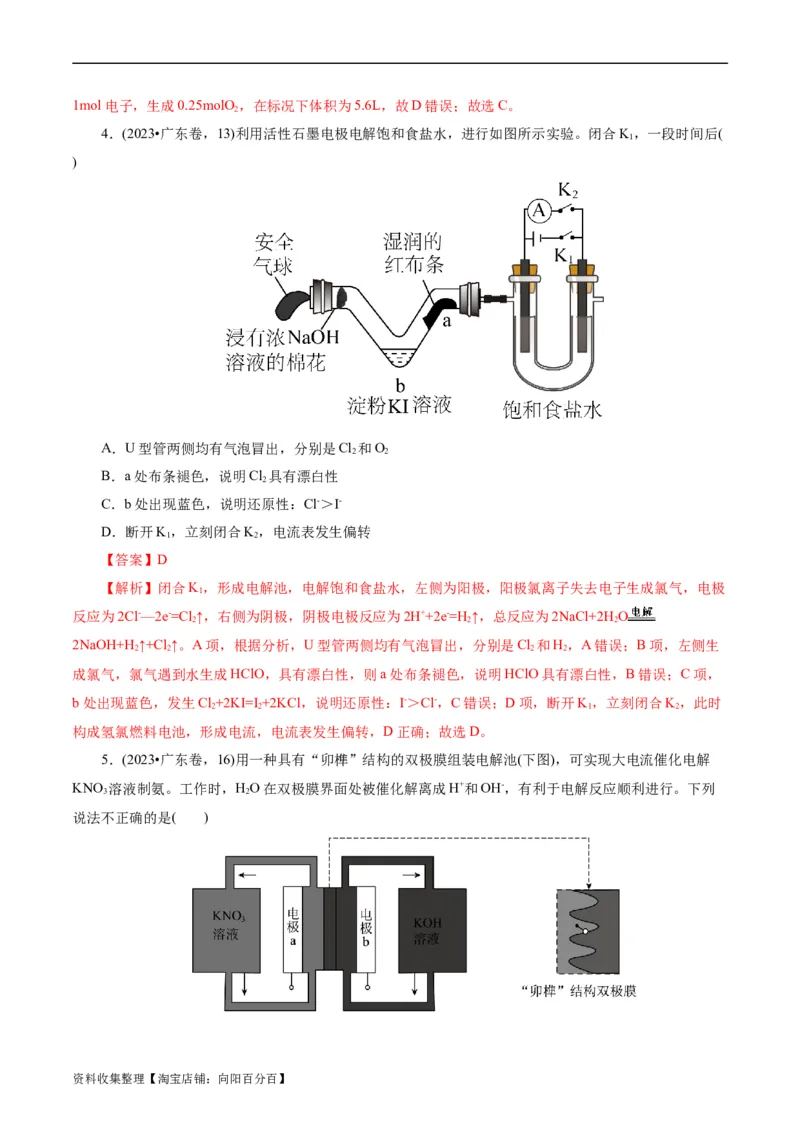
资料收集整理【淘宝店铺:向阳百分百】对点1 电解饱和食盐水,若生成4 mol的NaOH,(a为饱和食盐水),下列说法正确的是( )
A.在X极生成2 mol Cl B.在X极生成2 mol H
2 2
C.在Y极生成4 mol Cl D.NaOH在Y极生成
2
【答案】B
【解析】由装置图可知Y为电解池的阳极,电极反应:2Cl--2e-===Cl↑,X为阴极,电极反应为:
2
2H++2e-===H ↑。A 项,X 电极为阴极,生成的是氢气,错误;B 项,由总反应方程式 2NaCl+
2
2HO=====H↑+Cl↑+2NaOH知,生成4 mol的NaOH,同时生成2 mol H ,正确;C项,Y电极为电解
2 2 2 2
池阳极,由总反应方程式2NaCl+2HO=====H↑+Cl↑+2NaOH可知,生成4 mol 的NaOH,同时生成氯
2 2 2
气2 mol,错误;D项,阴极附近氢离子放电促进水电离,溶液中氢氧根离子浓度增大,NaOH在X极生成,
错误。
对点2 用石墨做电极,电解稀NaSO 溶液的装置如图所示,通电后在石墨电极A和B附近分别滴
2 4
加一滴石蕊溶液。下列有关叙述正确的是( )
A.逸出气体的体积:A电极<B电极
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.A电极附近呈红色,B电极附近呈蓝色
D.电解一段时间后,将全部电解液转移到同一烧杯中,充分搅拌后溶液呈中性
【答案】D
【解析】SO、OH-移向B电极,在B电极OH-放电,产生O,B电极附近c(H+)>c(OH-),石蕊溶液
2
变红,Na+、H+移向A电极,在A电极H+放电产生H ,A电极附近c(OH-)>c(H+),石蕊溶液变蓝,C项
2
错误、D项正确;A电极产生的气体体积大于B电极,A项错误;两种气体均为无色无味的气体,B项错
误。
考法 2 电解原理的运用
(1)电解饱和食盐水
①电极反应:阳极:2Cl--2e-===Cl↑(氧化反应)
2
阴极:2H++2e-===H ↑(还原反应)
2
资料收集整理【淘宝店铺:向阳百分百】②总反应方程式:
2NaCl+2HO=====2NaOH+H↑+Cl↑
2 2 2
离子方程式:2Cl-+2HO=====2OH-+H↑+Cl↑
2 2 2
③应用:氯碱工业制烧碱、氯气和氢气。
(2)电镀和电解精炼铜
电镀(Fe上镀Cu) 电解精炼铜
阳
电极材料 镀层金属铜 粗铜(含Zn、Fe、Ni、Ag、Au等杂质)
极
Cu-2e-===Cu2+,Zn-2e-===Zn2+,Fe-2e-
电极反应 Cu-2e-===Cu2+
===Fe2+,Ni-2e-===Ni2+
阴 电极材料 待镀金属Fe 纯铜
极 电极反应 Cu2++2e-===Cu
电解质溶液 含Cu2+的盐溶液
电解精炼铜时,粗铜中的Ag、Au等不反应,沉积在电解池底部形成阳极泥
(3)电冶金
利用电解熔融盐的方法来冶炼活泼金属Na、Ca、Mg、Al等。
总方程式 阳极、阴极反应式
冶炼钠 2NaCl(熔融)=====2Na+Cl↑ 2Cl--2e-===Cl↑,2Na++2e-===2Na
2 2
冶炼镁 MgCl (熔融)=====Mg+Cl↑ 2Cl--2e-===Cl↑,Mg2++2e-===Mg
2 2 2
6O2--12e-===3O ↑,4Al3++12e-
2
冶炼铝 2Al O(熔融)=====4Al+3O↑
2 3 2
===4Al
三”步完胜电极反应式的书写
请判断下列说法的正误(正确的打“√”,错误的打“×”)
资料收集整理【淘宝店铺:向阳百分百】(1)在镀件上电镀铜时,也可以用惰性材料做阳极,用硫酸铜溶液做电解液( )
(2)电解饱和食盐水时,两个电极均不能用金属材料( )
(3)电镀铜和电解精炼铜时,电解质溶液中c(Cu2+)均保持不变( )
(4)电解冶炼镁、铝通常电解MgCl 和Al O,也可以电解MgO和AlCl ( )
2 2 3 3
(5)电解精炼时,阳极泥可以作为提炼贵重金属的原料( )
(6)用Zn做阳极,Fe做阴极,ZnCl 做电解质溶液,由于放电顺序H+>Zn2+,不可能在铁上镀锌( )
2
(7)用铜做阴极,石墨做阳极,电解饱和食盐水时,阳极的电极反应式为2Cl--2e-===Cl↑( )
2
(8)粗铜精炼时,与电源正极相连的应是粗铜,该极发生的电极反应只有Cu-2e-===Cu2+( )
(9)电镀铜和电解精炼铜时,电解质溶液中c(Cu2+)均保持不变( )
(10)电解饱和食盐水时,两个电极均不能用金属材料( )
(11)电解冶炼镁、铝通常电解MgCl 和Al O,也可以电解MgO和AlCl ( )
2 2 3 3
(12)电解精炼时,阳极泥可以作为提炼贵重金属的原料( )
(13)用Zn作阳极,Fe作阴极,ZnCl 作电解质溶液,由于放电顺序H+>Zn2+,不可能在铁上镀锌( )
2
答案:(1)√ (2)× (3)× (4)× (5)√ (6)× (7)√ (8)× (9)× (10)× (11)× (12)√ (13)×
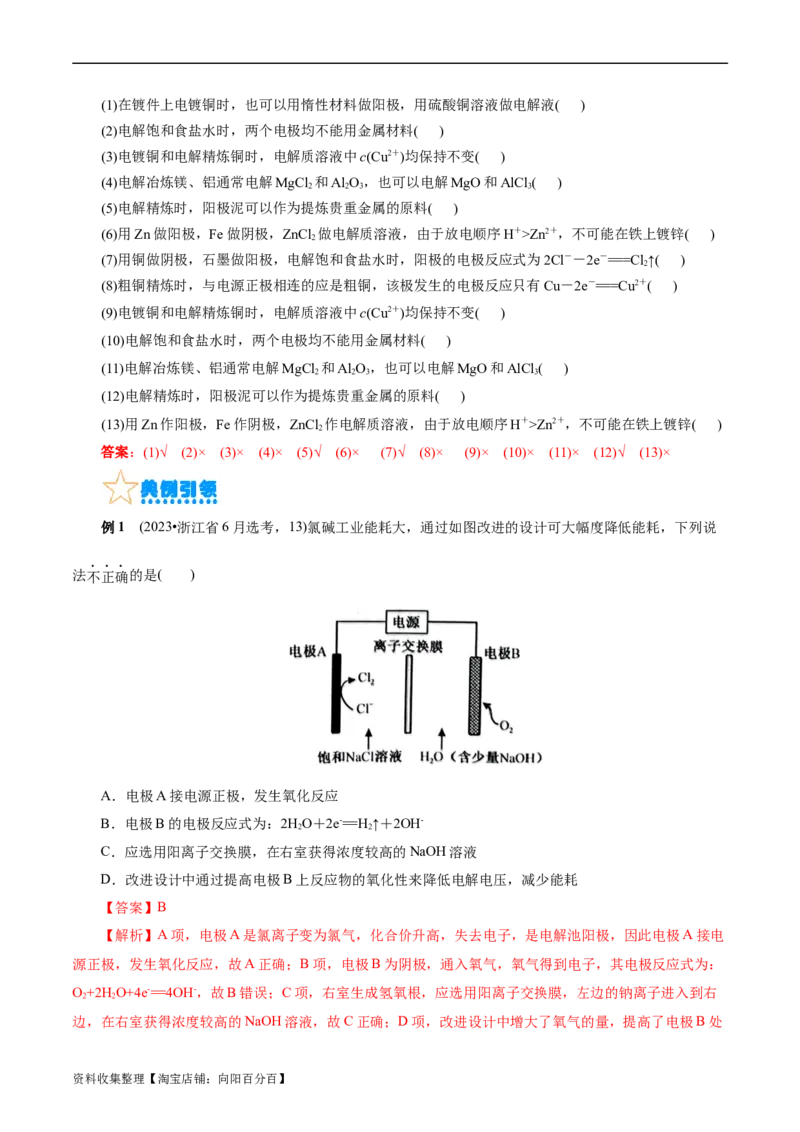
例1 (2023•浙江省6月选考,13)氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗,下列说
法不正确的是( )
A.电极A接电源正极,发生氧化反应
B.电极B的电极反应式为:2HO+2e-=H↑+2OH-
2 2
C.应选用阳离子交换膜,在右室获得浓度较高的NaOH溶液
D.改进设计中通过提高电极B上反应物的氧化性来降低电解电压,减少能耗
【答案】B
【解析】A项,电极A是氯离子变为氯气,化合价升高,失去电子,是电解池阳极,因此电极A接电
源正极,发生氧化反应,故A正确;B项,电极B为阴极,通入氧气,氧气得到电子,其电极反应式为:
O+2H O+4e-=4OH-,故B错误;C项,右室生成氢氧根,应选用阳离子交换膜,左边的钠离子进入到右
2 2
边,在右室获得浓度较高的NaOH溶液,故C正确;D项,改进设计中增大了氧气的量,提高了电极B处
资料收集整理【淘宝店铺:向阳百分百】的氧化性,通过反应物的氧化性来降低电解电压,减少能耗,故D正确。故选B。
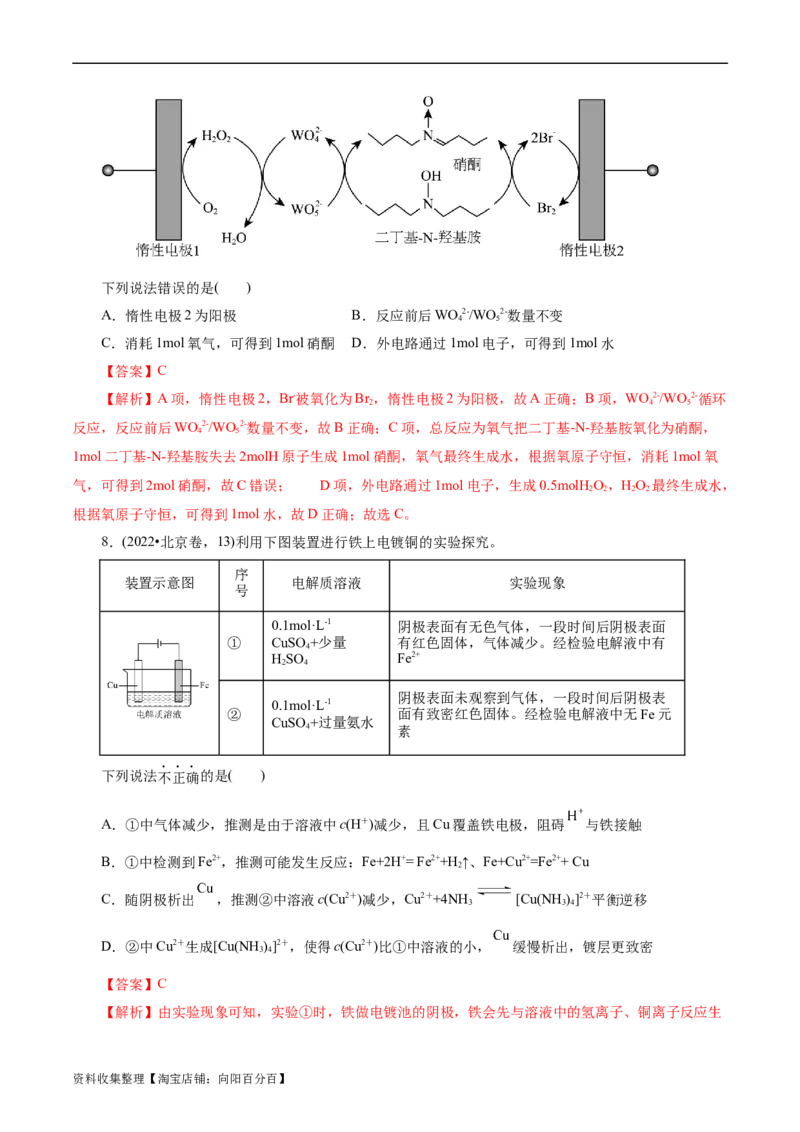
例2 (2023•北京卷,5)回收利用工业废气中的CO 和SO ,实验原理示意图如下。
2 2
下列说法不正确的是( )
A.废气中SO 排放到大气中会形成酸雨
2
B.装置a中溶液显碱性的原因是HCO -的水解程度大于HCO -的电离程度
3 3
C.装置a中溶液的作用是吸收废气中的CO 和SO
2 2
D.装置 中的总反应为SO 2-+CO +H O电 HCOOH+SO 2-
3 2 2 解 4
【答案】C
【解析】A项,SO 是酸性氧化物,废气中SO 排放到空气中会形成硫酸型酸雨,故A正确;B项,
2 2
装置a中溶液的溶质为NaHCO ,溶液显碱性,说明HCO -的水解程度大于电离程度,故B正确;C项,装
3 3
置a中NaHCO 溶液的作用是吸收SO 气体,CO 与NaHCO 溶液不反应,不能吸收CO,故C错误;D项,
3 2 2 3 2
由电解池阴极和阳极反应式可知,装置b中总反应为SO 2-+CO +H O电 HCOOH+SO 2-,故D正确;故选
3 2 2 解 4
C。
对点1 电化学原理在工业生产中发挥着巨大的作用。NaFeO 是制造高铁电池的重要原料,同时也是
2 4
一种新型的高效净水剂。在工业上通常利用如图装置生产NaFeO,下列说法正确的是( )
2 4
A.阳极的电极反应式为Fe+8OH--6e-=FeO 2-+4H O
4 2
B.右侧的离子交换膜为阳离子交换膜
资料收集整理【淘宝店铺:向阳百分百】C.阴极区a%>b%
D.阴极产生的气体是氧气
【答案】A
【解析】A项,由图所示,Fe为阳极,故发生氧化反应生成FeO2-,电极反应式为Fe+8OH--6e-=FeO 2-
4 4
+4H O,A正确;B项,阳极反应消耗阴离子氢氧根离子,向右侧阳极移动,故右侧交换膜为能使阴离子
2
通过的阴离子交换膜,B错误;C项,阴极区水被电解产生H 和OH-,故产出的NaOH浓度变大,
2
a%