文档内容
考点 41 原子结构与性质
(核心考点精讲精练)
一、3年真题考点分布
考点内容 考题统计
2023全国乙卷35(1)题,15分;2023浙江1月选考17(2)题,10分;2023北京卷
15(1)(2)题,10分;2022 海南卷5题,2分;2022全国乙卷35(1)题,15分;2022
核外电子排布 重庆卷18(1)(2)题,15分;2022北京卷15(1)(2)(3)题,10分;2022海南卷19(1)
(2)题,14分;2022广东卷20(1)题,14分;2021全国乙卷35(1)题,15分;2021
河北卷17(1)题,15分;2021湖南卷18(1)题,15分;
2021江苏卷3题,3分;2022全国甲卷35(1)(2)题,15分;2022河北卷17(1)(2)
题,15分;2022湖南卷18(1)(2)题,15分;2021湖北卷13题,3分;2021山东
元素周期律
卷16(1)(2)题,12分;2022广东卷20(2)(3)题,14分;2021 海南卷19(1)(2)(3)
题,14分;
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,本知识点在全国卷中为选考题考查内容,近年来已有较多省市已列入高考必
考题,分析近几年高考卷,对原子结构与性质的考查形式趋于稳定,一般以给定相关元素的情境,考查电
子排布式、元素的电离能及电负性等,从宏观和微观相结合的视角分析原子结构与元素性质的关系,对核
外电子排布、元素第一电离能的特殊性等,面对异常现象敢于提出自己的见解。
【备考策略】
1.了解原子核外电子的运动状态、能级分布和排布原理,能正确书写1~36号元素原子核外电子、价
电子的排布式和电子排布图。
2.了解电离能的含义,并能用以说明元素的某些性质。
3.了解电子在原子轨道之间的跃迁及其简单应用。
4.了解电负性的概念,并能用以说明元素的某些性质。
【命题预测】
预测2024年本考点将继续考查核外电子排布规律,特别是基态原子的核外电子排布式是考查重点,侧
重于电负性与电离能的考查,注意掌握常见元素电负性与电离能的比较方法及特殊情况,备考时加以关注。
考法 1 原子核外电子排布
1.电子层、能级与原子轨道
资料整理【淘宝店铺:向阳百分百】(1)电子层(n):在多电子原子中,核外电子的能量是不同的,按照电子的能量差异将其分成不同电子层。
通常用K、L、M、N……表示,能量依次升高。
(2)能级:同一电子层里电子的能量也可能不同,又将其分成不同的能级,通常用 s、p、d、f等表示,
同一电子层里,各能级的能量按s、p、d、f的顺序依次升高,即:E(s)<E(p)<E(d)<E(f)。
(3)原子轨道:电子云轮廓图给出了电子在核外经常出现的区域。这种电子云轮廓图称为原子轨道。
原子轨道 轨道形状 轨道个数
s 球形 1
p 哑铃形 3
温馨提示:第一电子层(K),只有s能级;第二电子层(L),有s、p两种能级,p能级上有三个原子轨
道p、p、p,它们具有相同的能量;第三电子层(M),有s、p、d三种能级。
x y z
2.原子核外电子的排布规律
①能量最低原 原子核外电子总是优先占据能量更低的原子轨道
理 1s→2s→2p→3s→3p→4s→3d→4p→5s→4d→5p→6s…
当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个
②洪特规则
轨道,且自旋状态相同
③泡利原理 每个原子轨道上最多只能容纳2个自旋方向相反的电子
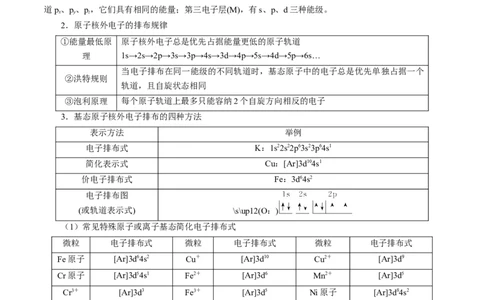
3.基态原子核外电子排布的四种方法
表示方法 举例
电子排布式 K:1s22s22p63s23p64s1
简化表示式 Cu:[Ar]3d104s1
价电子排布式 Fe:3d64s2
电子排布图
(或轨道表示式) \s\up12(O:)
(1)常见特殊原子或离子基态简化电子排布式
微粒 电子排布式 微粒 电子排布式 微粒 电子排布式
Fe原子 [Ar]3d64s2 Cu+ [Ar]3d10 Cu2+ [Ar]3d9
Cr原子 [Ar]3d54s1 Fe2+ [Ar]3d6 Mn2+ [Ar]3d5
Cr3+ [Ar]3d3 Fe3+ [Ar]3d5 Ni原子 [Ar]3d84s2
(2)基态原子电子排布图书写的常见错误
错误类型 错因剖析 改正
违背能量最低原理
违背泡利原理
违背洪特规则
违背洪特规则
资料整理【淘宝店铺:向阳百分百】1.基态原子核外电子排布的四方法
表示方法 举例
电子排布式 Cr:1s22s22p63s23p63d54s1
简化表示式 Cu:[Ar]3d104s1
价电子排布式 Fe:3d64s2
电子排布图(或轨道表
示式)
2.当出现d轨道时,虽然电子按ns、(n-1)d、np的顺序填充,但在书写电子排布式时,仍把(n-1)d
放在 ns 前,如 Fe:1s22s22p63s23p63d64s2,而失电子时,却先失 4s 轨道上的电子,如 Fe3+:
1s22s22p63s23p63d5。
3.注意比较原子核外电子排布式、简化电子排布式、价电子排布式的区别与联系。如 Cu的电子排布
式:1s22s22p63s23p63d104s1;简化电子排布式:[Ar]3d104s1;价电子排布式:3d104s1。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)基态钠原子的电子排布式为1s22s22p62d1( )
(2)基态磷原子的电子排布图为 ( )
(3)同一原子中,2p、3p、4p能级的轨道数依次增多( )
(4)Cr的电子排布式为1s22s22p63s23p63d44s2( )
(5)p能级的能量一定比s能级的能量高( )
(6)同一原子中,2p、3p、4p能级的轨道数依次增多( )
(7)2p和3p轨道形状均为哑铃形,能量也相等( )
(8)2p、2p、2p 的能量相等( )
x y z
(9)铁元素基态原子的电子排布式为1s22s22p63s23p64s23d6( )
(10)Cr的基态原子的简化电子排布式为[Ar]3d44s2( )
(11)基态原子电子能量的高低顺序为E(1s)<E(2s)<E(2p)<E(2p)<E(2p) ( )
x y z
(12)电子排布式( Ti)1s22s22p63s23p10违反了能量最低原则( )
22
(13)磷元素基态原子的轨道表示式为 ( )
答案:(1)× (2)× (3)× (4)× (5)× (6)× (7)× (8)√ (9)× (10)× (11)× (12)× (13)×
资料整理【淘宝店铺:向阳百分百】例1 (2023·陕西省宝鸡市期中)下列说法中正确的是( )
A.同一原子处于激发态时的能量一定大于其处于基态时的能量
B.基态碳原子的电子排布式为1s22s12p3
C.焰色反应是化学变化
D.某些金属元素的特殊焰色是金属原子的电子从基态跃迁到激发态时产生的
【答案】A
【解析】A项,基态原子吸收能量变为激发态原子,所以激发态原子能量大于基态原子能量的,故A
正确;B项,基态C原子核外有6个电子,根据构造原理知C元素基态原子核外电子排布式为1s22s22p2,
故B错误;C项,焰色反应为元素的性质,过程中没有新物质生成,属于物理变化,故C错误;D项,电
子由基态跃迁到激发态需要吸收光子,获得能量,从由激发态跃迁到能量较低的激发态乃至基态以光能形
式释放能量,产生焰色反应,故D错误;故选A。
例2 下列各组表述中,两个微粒一定不属于同种元素原子的是( )
A.3p能级有一个空轨道的基态原子和核外电子排布式为1s22s22p63s23p2的原子
B.M层全充满而N层为4s2的原子和核外电子排布式为1s22s22p63s23p63d64s2的原子
C.最外层电子数是核外电子总数的的原子和价电子排布式为4s24p5的原子
D.2p能级有一个未成对电子的基态原子和原子的价电子排布式为2s22p5的原子
【答案】B
【解析】A项,3p能级有一个空轨道,说明3p能级有2个电子,3s能级肯定已填满,价电子排布式
为3s23p2,因此A中两微粒相同,不符合题意。B项,M层全充满而N层为4s2,M层上有d轨道,即价电
子排布为3d104s2,应该是锌元素,3d64s2是铁元素的价电子排布式,符合题意。C项,价电子排布式为
4s24p5,则3d能级已排满10个电子,核外电子排布式为1s22s22p63s23p63d104s24p5,最外层电子数是核外电
子总数的的原子,可按下述方法讨论:若最外层电子数为1,核外电子总数为5,不可能;最外层电子数为
2,核外电子总数为10,不可能;同理,只有最外层电子数为7,核外电子总数为35时合理,其电子排布
式也是1s22s22p63s23p63d104s24p5,二者是同种元素的原子,不符合题意。D项,2p能级有一个未成对电子,
可以是2p1,也可以是2p5,因此二者不一定属于同种元素的原子,不符合题意。
对点1 下列关于价电子排布为3s23p4的原子描述正确的是( )
A.它的元素符号为O
B.它的核外电子排布式为1s22s22p63s23p4
C.可以与H 化合生成液态化合物
2
D.其轨道表示式为
【答案】B
【解析】价电子排布为3s23p4的粒子,其基态原子核外电子排布式为1s22s22p63s23p4,其核外电子数为
资料整理【淘宝店铺:向阳百分百】16,为S元素, A错误, B正确;一定条件下,它可与H 生成气态化合物HS,C错误;S原子核外电子
2 2
排布遵循能量最低原理、泡利不相容原理、洪特规则,其轨道表示式为 ,D
错误。
对点2 X、Y、Z、W、P五种元素,其核电荷数依次增大。X基态原子核外只有三个能级,且各能级
电子数相等;Z原子的核外电子有8种运动状态;Z与W元素位于同一族;P原子核外有4个能层,最外
层只有1个电子,其余各层均排满电子。下列说法正确的是( )
A.Z、Y、X元素的第一电离能依次减小
B.Y基态原子的轨道表示式:
C.P原子的价层电子排布为
D.P单质分别与Z、W单质反应,产物中P的化合价一定相同
【答案】B
【解析】X基态原子核外只有三个能级,且各能级电子数相等,为1s22s22p2,为C元素,Z原子的核
外电子有8种运动状态,Z为O原子,Y为N元素,Z与W元素位于同一族,W为S元素,P原子核外有
4个能层,最外层只有1个电子,其余各层均排满电子,为 ,为Cu元素。A项,Z为
O元素,Y为N元素,X为C元素,第一电离能的大小为:N>C>O,A错误;B项,Y为N元素,基态
原子的轨道表示式: ,B正确;C项,P为Cu元素,价层电子排布为: ,
C错误;D项,Cu和O 反应生成CuO,Cu元素的化合价为+2价,Cu和S反应生成Cu S,Cu元素的化合
2 2
价为+1价,D错误;故选B。
考法 2 元素周期表与元素周期律
1.原子结构与周期表的关系
(1)原子结构与周期表的关系(完成下列表格)
每周期第一个元素 每周期最后一个元素
电子
周期 原子 基态原子的简化电 原子序
层数 基态原子的电子排布式
序数 子排布式 数
2 2 3 [He]2s1 10 1s22s22p6
3 3 11 [Ne]3s1 18 1s22s22p63s23p6
4 4 19 [Ar]4s1 36 1s22s22p63s23p63d104s24p6
1s22s22p63s23p63d104s24p64d10
5 5 37 [Kr]5s1 54
5s25p6
资料整理【淘宝店铺:向阳百分百】1s22s22p63s23p63d104s24p64d10
6 6 55 [Xe]6s1 86
4f145s25p65d106s26p6
(2)每族元素的价层电子排布特点
①主族
主族 ⅠA ⅡA ⅢA ⅣA
排布特点 ns1 ns2 ns2np1 ns2np2
主族 ⅤA ⅥA ⅦA
排布特点 ns2np3 ns2np4 ns2np5
②0族:He:1s2;其他ns2np6。
③过渡元素(副族和第Ⅷ族):(n-1)d1~10ns1~2。
(3)元素周期表的分区与价层电子排布的关系
①周期表的分区
②各区价层电子排布特点
分区 价层电子排布
s区 ns1~2
p区 ns2np1~6(除氦外)
d区 (n-1)d1~9ns1~2(除钯外)
ds区 (n-1)d10ns1~2
f区 (n-2)f0~14(n-1)d0~2ns2
2.原子半径
(1)影响因素
(2)变化规律
元素周期表中的同周期主族元素从左到右,原子半径逐渐减小;同主族元素从上到下,原子半径逐渐
增大。
3.电离能
(1)第一电离能:气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,符号:
I,单位:kJ·mol-1。
1
(2)规律
①同周期:第一种元素的第一电离能最小,最后一种元素的第一电离能最大,总体呈现从左至右逐渐
资料整理【淘宝店铺:向阳百分百】增大的变化趋势。
②同族元素:从上至下第一电离能逐渐减小。
③同种原子:逐级电离能越来越大(即I<I<I…)。
1 2 3
4.电负性
(1)含义:元素的原子在化合物中吸引键合电子能力的标度。元素的电负性越大,表示其原子在化合物
中吸引键合电子的能力越强。
(2)标准:以最活泼的非金属氟的电负性为4.0作为相对标准,计算得出其他元素的电负性(稀有气体未
计)。
(3)变化规律
金属元素的电负性一般小于2,非金属元素的电负性一般大于2,而位于非金属三角区边界的“类金
属”(如锗、锑等)的电负性则在2左右。
在元素周期表中,同周期从左至右,元素的电负性逐渐增大,同主族从上至下,元素的电负性逐渐减
小。
5.对角线规则
在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,如 。
1.元素第一电离能的周期性变化规律
同一周期,随着原子序数的增加,元素的第一电离能呈现增大的趋势,稀有气体元素的
一般
第一电离能最大,碱金属元素的第一电离能最小;同一主族,随着电子层数的增加,元
规律
素的第一电离能逐渐减小
第一电离能的变化与元素原子的核外电子排布有关。通常情况下,当原子核外电子排布
特殊
在能量相等的轨道上形成全空(p0、d0、f0)、半满(p3、d5、f7)和全满(p6、d10、f14)结构时,
情况
原子的能量较低,该元素具有较大的第一电离能
2.电离能、电负性大小判断
规律 在周期表中,电离能、电负性从左到右逐渐增大,从上往下逐渐减小
同周期主族元素,第ⅡA族(ns2)全充满、第ⅤA族(np3)半充满,比较稳定,所以其第一
特性
电离能大于同周期相邻的第ⅢA族和第ⅥA族元素
常常应用化合价及物质类别判断电负性的大小,如 O与Cl的电负性比较:①HClO中Cl
方法 为+1价、O为-2价,可知O的电负性大于Cl;②Al O 是离子化合物、AlCl 是共价化
2 3 3
合物,可知O的电负性大于Cl
请判断下列说法的正误(正确的打“√”,错误的打“×”)
资料整理【淘宝店铺:向阳百分百】(1)价电子排布为5s25p1的元素位于第5周期ⅠA族,是s区元素( )
(2)主族元素的电负性越大,元素原子的第一电离能一定越大( )
(3)在元素周期表中,同周期主族元素电负性从左到右越来越大( )
(4)在形成化合物时,电负性越小的元素越容易显示正价( )
(5)正三价阳离子的电子排布式为1s22s22p63s23p63d5的元素在周期表中位于Ⅷ族( )
(6)钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能( )
(7)第2周期主族元素的原子半径随核电荷数的增大依次减小( )
(8)C、N、O、F四种元素第一电离能从大到小的顺序是N>O>F>C( )
(9)正三价阳离子的电子排布式为1s22s22p63s23p63d5的元素在周期表中位于Ⅷ族( )
(10)价电子排布式为4s24p3的元素位于第4周期ⅤA族,是p区元素( )
(11)元素的电负性越大,非金属性越强,第一电离能也越大( )
答案:(1)× (2)× (3)√ (4)√ (5)√ (6)× (7)√ (8)× (9)√ (10)√ (11)×
例1 (2023•浙江省6月选考,11)X、Y、Z、W四种短周期主族元素,原子序数依次增大。X、Y与
Z位于同一周期,且只有X、 Y元素相邻。X基态原子核外有2个未成对电子,W原子在同周期中原子半
径最大。下列说法不正确的是( )
A.第一电离能: Y>Z>X
B.电负性: Z>Y>X>W
C.Z、W原子形成稀有气体电子构型的简单离子的半径:W<Z
D.WX 与水反应生成产物之一是非极性分子
2 2
【答案】A
【元素推断】X、Y、Z、W四种短周期主族元素,原子序数依次增大。X、Y与Z位于同一周期,且
只有X、 Y元素相邻。X基态原子核外有2个未成对电子,则X为C,Y为N,Z为F,W原子在同周期
中原子半径最大,则W为Na。
【解析】A项,根据同周期从左到右第一电离能呈增大趋势,但第 IIA族大于第IIIA族,第VA族大
于第VIA族,则第一电离能: Z>Y>X,故A错误;B项,根据同周期从左到右电负性逐渐增大,同主
族从上到下电负性逐渐减小,则电负性:Z>Y>X>W,故B正确;C项,根据同电子层结构核多径小,
则Z、W原子形成稀有气体电子构型的简单离子的半径:W<Z,故C正确;D项,WX 与水反应生成产
2 2
物之一为乙炔,乙炔是非极性分子,故D正确。故选A。
例2 (2023•全国新课标卷,9)一种可吸附甲醇的材料,其化学式为[C(NH )][B(OCH )]Cl,部分晶
2 3 4 3 4
体结构如下图所示,其中[C(NH )]+为平面结构。
2 3
资料整理【淘宝店铺:向阳百分百】下列说法正确的是( )
A.该晶体中存在N-H…O氢键
B.基态原子的第一电离能:
C.基态原子未成对电子数:
D.晶体中B、N和O原子轨道的杂化类型相同
【答案】A
【解析】A项,由晶体结构图可知,[C(NH )]+中的-NH 的H与[B(OCH )]-中的O形成氢键,因此,
2 3 2 3 4
该晶体中存在N-H…O氢键,A正确;B项,同一周期元素原子的第一电离能呈递增趋势,但是第ⅡA、
ⅤA元素的原子结构比较稳定,其第一电离能高于同周期的相邻元素的原子,因此,基态原子的第一电离
能从小到大的顺序为C< O < N,B不正确;C项,B、C、O、N的未成对电子数分别为1、2、2、3,因此,
基态原子未成对电子数BC,而同周期自左向右,电负性增大,
E>B,故电负性E>C,故B错误;P、S、Cl三种元素形成的简单离子,电子层结构相同,原子序数越大,
离子半径越小,故C错误;元素的非金属性越强,对应的氢化物越稳定,则气态氢化物的稳定顺序:
D①>②
B.电子排布属于基态原子(或离子)的是:①②
C.电离一个电子所需最低能量:①>②>③
D.得电子能力:①>②
【答案】(2)AB
【解析】(2)电子排布式分别为:①[Ne]3s23p2、②[Ne]3s23p1、③[Ne]3s23p14s1,可推知分别为基态Si原
子、基态Al原子、激发态Si原子;A项,根据微粒电子层数及各层电子数多少可推知,微粒半径:
③>①>②,A正确;B项,根据上述分析可知,电子排布属于基态原子(或离子)的是:①②,B正确;C项,
Si为非金属失电子能力比Al弱,电离一个电子所需最低能量:①>③>②,C错误;D项,非金属Si的得
电子能力强于金属Al,得电子能力:②>①,D错误;故选AB。
6.(10分)(2023•北京卷,15节选)硫代硫酸盐是一类具有应用前景的浸金试剂。硫代硫酸根(S O2-)
2 3
可看作是SO 2-中的一个 原子被 原子取代的产物。
4
(1)基态 原子价层电子排布式是 。
(2)比较 原子和 原子的第一电离能大小,从原子结构的角度说明理由: 。
【答案】(1) 3s23p4
(2) I (O)>I (S),氧原子半径小,原子核对最外层电子的吸引力大,不易失去一个电子
1 1
【解析】(1)S是第三周期ⅥA族元素,基态S原子价层电子排布式为3s23p4;(2)S和O为同主族
元素,O原子核外有2个电子层,S原子核外有3个电子层,O原子半径小,原子核对最外层电子的吸引力
大,不易失去1个电子,即O的第一电离能大于S的第一电离能。
7.(15分) (2022•全国乙卷,35节选)卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回
答下列问题:
(1)氟原子激发态的电子排布式有_______,其中能量较高的是_______。(填标号)
a. 1s22s22p43s1 b. 1s22s22p43d2 c. 1s22s12p5 d. 1s22s22p33p2
【答案】(1) ad d
【解析】(1)F的原子序数为9,其基态原子电子排布式为1s22s22p5。a项,1s22s22p43s1,基态氟原子2p
能级上的1个电子跃迁到3s能级上,属于氟原子的激发态,a正确;b项,1s22s22p43d2,核外共10个电子,
不是氟原子,b错误;c项,1s22s12p5,核外共8个电子,不是氟原子,c错误;d项,1s22s22p33p2,基态氟
原子2p能级上的2个电子跃迁到3p能级上,属于氟原子的激发态,d正确;故选ad;而同一原子3p能级
的能量比3s能级的能量高,因此能量最高的是1s22s22p33p2,故选d。
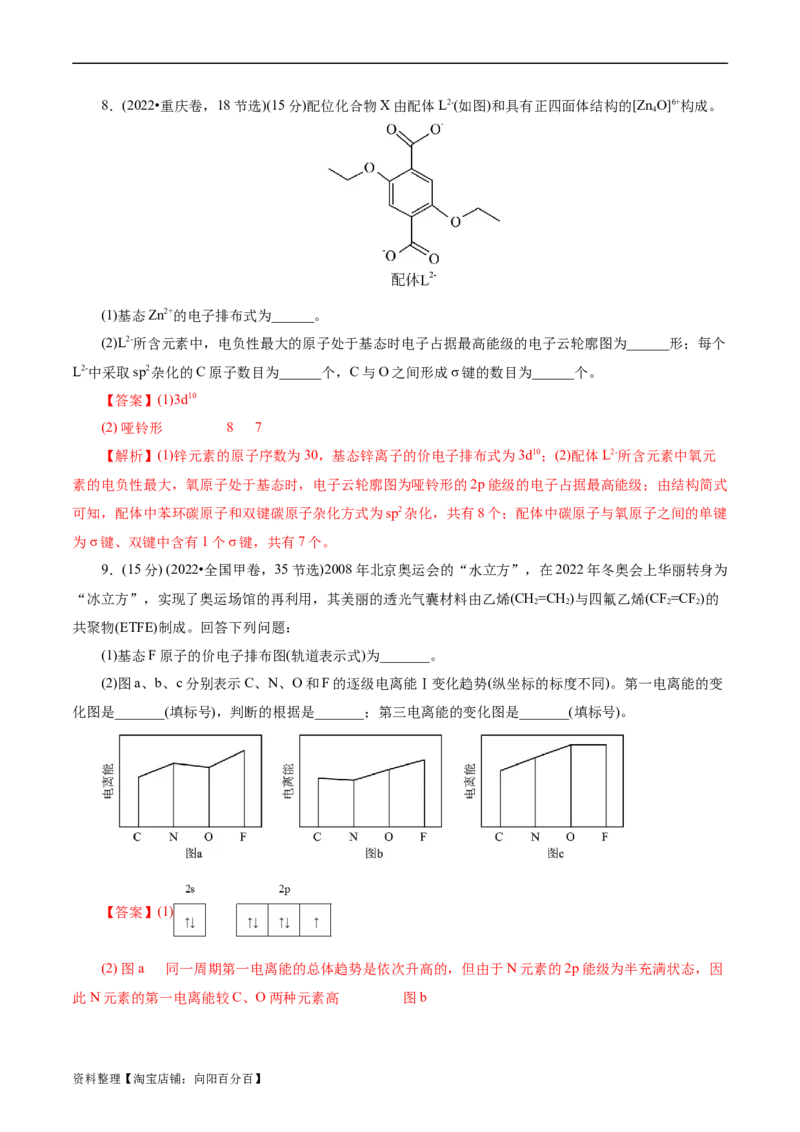
资料整理【淘宝店铺:向阳百分百】8.(2022•重庆卷,18节选)(15分)配位化合物X由配体L2-(如图)和具有正四面体结构的[Zn O]6+构成。
4
(1)基态Zn2+的电子排布式为______。
(2)L2-所含元素中,电负性最大的原子处于基态时电子占据最高能级的电子云轮廓图为______形;每个
L2-中采取sp2杂化的C原子数目为______个,C与O之间形成σ键的数目为______个。
【答案】(1)3d10
(2) 哑铃形 8 7
【解析】(1)锌元素的原子序数为30,基态锌离子的价电子排布式为3d10;(2)配体L2-所含元素中氧元
素的电负性最大,氧原子处于基态时,电子云轮廓图为哑铃形的2p能级的电子占据最高能级;由结构简式
可知,配体中苯环碳原子和双键碳原子杂化方式为sp2杂化,共有8个;配体中碳原子与氧原子之间的单键
为σ键、双键中含有1个σ键,共有7个。
9.(15分) (2022•全国甲卷,35节选)2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为
“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH=CH )与四氟乙烯(CF=CF )的
2 2 2 2
共聚物(ETFE)制成。回答下列问题:
(1)基态F原子的价电子排布图(轨道表示式)为_______。
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变
化图是_______(填标号),判断的根据是_______;第三电离能的变化图是_______(填标号)。
【答案】(1)
(2) 图a 同一周期第一电离能的总体趋势是依次升高的,但由于N元素的2p能级为半充满状态,因
此N元素的第一电离能较C、O两种元素高 图b
资料整理【淘宝店铺:向阳百分百】【解析】(1)F为第9号元素其电子排布为1s22s22p5,则其价电子排布图为 。
(2)C、N、O、F四种元素在同一周期,同一周期第一电离能的总体趋势是依次升高的,但由于N元素的2p
能级为半充满状态,因此N元素的第一电离能较C、O两种元素高,因此C、N、O、F四种元素的第一电
离能从小到大的顺序为C”“<”或“=”),原因是_______。
3 3
(2)富马酸亚铁(FeC HO)是一种补铁剂。富马酸分子的结构模型如图所示:
4 2 4
①富马酸分子中 键与 键的数目比为_______;
②富马酸亚铁中各元素的电负性由大到小的顺序为_______。
【答案】(1) [Ar] 3d104s24p4 6 > SeO 的空间构型为平面三角形,SeO2-的空间构型为三
3 3
资料整理【淘宝店铺:向阳百分百】角锥形
(2) 11:3 O>C>H>Fe
【解析】(1)①硒元素的原子序数为34,基态原子的电子排布式为[Ar] 3d104s24p4,故答案为:[Ar]
3d104s24p4;②由结构简式可知,乙烷硒啉的分子结构对称,分子中含有6种化学环境不同的碳原子;③三
氧化硒分子中硒原子的价层电子对数为3,孤对电子对数为0,分子的空间构型为平面三角形,键角为
120°,亚硒酸根离子中硒原子的价层电子对数为4,孤对电子对数为1,离子的空间构型为三角锥形,键角
小于120°;(2)①由球棍模型可知,富马酸的结构式为HOOCCH=CHCOOH,分子中的单键为σ键,双键中
含有1个σ键和1个π键,则分子中σ键和π键的数目比为11:3;②金属元素的电负性小于非金属元素,
则铁元素的电负性最小,非金属元素的非金属性越强,电负性越大,氢碳氧的非金属性依次增强,则电负
性依次增大,所以富马酸亚铁中四种元素的电负性由大到小的顺序为O>C>H>Fe。
14.(2022•广东选择性考试,20节选)硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域
具有重要应用。自我国科学家发现聚集诱导发光( )效应以来, 在发光材料、生物医学等领域引起
广泛关注。一种含 的新型 分子 的合成路线如下:
(1) Se与S同族,基态硒原子价电子排布式为_______。
【答案】(1)4s24p4
【解析】(1)基态硫原子价电子排布式为3s23p4,Se与S同族,Se为第四周期元素,因此基态硒原子价
电子排布式为4s24p4。
15.(2021•山东卷,16节选)非金属氟化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态F原子核外电子的运动状态有________种。
(2)O、F、Cl电负性由大到小的顺序为____________;OF 分子的空间构型为_______;OF 的熔、沸
2 2
点_______ (填“高于”或“低于”)Cl O,原因是______________________。
2
【答案】(1)9 (2)F>O>Cl 角(V)形 低于 OF 和ClO都是分子晶体,结构相似,ClO的
2 2 2
相对分子质量大,ClO的熔、沸点高
2
【解析】(1)基态F原子共有9个核外电子,则每个电子都有对应的轨道和自旋状态,所以核外电子的
运动状态有9种;(2)电负性一定程度上相当于得电子能力,半径越小,得电子能力越强,电负性越大,半
径由小到大的顺序为F、O、Cl,所以电负性大小顺序为F>O>Cl;根据VSEPR理论有 ,去
资料整理【淘宝店铺:向阳百分百】掉2对孤对电子,知OF 分子的空间构型是角形;OF 和ClO都是分子晶体,结构相似,ClO的相对分子
2 2 2 2
质量大,ClO的熔、沸点高。
2
16.(2021•全国乙卷,35节选)过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中
有着广泛应用。回答下列问题:
(1)对于基态Cr原子,下列叙述正确的是_______(填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为 [Ar]3d54s1
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
【答案】(1)AC
【解析】(1) A项,基态原子满足能量最低原理,Cr有24个核外电子,轨道处于半充满时体系总能量
低,核外电子排布应为[Ar]3d54s1,A正确;B项, Cr核外电子排布为[Ar]3d54s1,由于能级交错,3d轨道
能量高于4s轨道的能量,即3d电子能量较高,B错误;C项,电负性为原子对键合电子的吸引力,同周期
除零族原子序数越大电负性越强,钾与铬位于同周期,铬原子序数大于钾,故铬电负性比钾高,原子对键
合电子的吸引力比钾大,C正确; 故选AC。
17.(2021•湖南选择性考试,18节选)硅、锗(Ge)及其化合物广泛应用于光电材料领域。回答下列问题:
(1)基态硅原子最外层的电子排布图为 ,晶体硅和碳化硅熔点较高的是
(填化学式);
【答案】(1) ; SiC
【解析】(1)Si位于周期表中第3周期第ⅣA族,基态原子的价电子排布式为3s23p2,则基态Si原子的
价电子排布图为: ;晶体硅、碳化硅均属于原子晶体,原子半径:Si>C,键长:
C﹣Si<Si﹣Si,则键能:C﹣Si>Si﹣Si,所以熔点:碳化硅>晶体硅,晶体硅和碳化硅熔点较高的是
SiC。
18.(2021•河北选择性考试,17节选)KH PO 晶体具有优异的非线性光学性能。我国科学工作者制备
2 4
的超大KH PO 晶体已应用于大功率固体激光器,填补了国家战略空白。回答下列问题:
2 4
(1)在KH PO 的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是___________(填离
2 4
子符号)。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用- 表示,称
资料整理【淘宝店铺:向阳百分百】为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为____________。
【答案】(1)K+和P3- (2) 或
(3)在原子数目相同的条件下,N 比N 具有更低的能量,而P 比P 具有更低的能量,能量越低越稳定
2 4 4 2
【解析】(1)在KH PO 的四种组成元素各自所能形成的简单离子分别为H+ (或H-)、O2-、K+和P3-,其
2 4
中核外电子排布相同的是K+和P3-。(2)对于基态的磷原子,其价电子排布式为3s23p3,其中3s轨道的2个
电子自旋状态相反,自旋磁量子数的代数和为0;根据洪特规则可知,其3p轨道的3个电子的自旋状态相
同,因此,基态磷原子的价电子的自旋磁量子数的代数和为 或 。(3)根据表中的相关共价键的键能
可知,若6mol N形成类似白磷分子结构的N 分子,可以释放出的能量为193kJ6=1158kJ;若6mol N形成
4
N 分子,则可释放的能量为946kJ2=1892kJ,显然,形成N 分子放出的能量更多,故在N数目相同的条
2 2
件下,N 具有更低的能量,能量越低越稳定。同理,若6mol P形成P 分子,可以释放出的能量为
2 4
197kJ6=1182kJ;若6mol P形成P 分子,则可释放的能量为489kJ2=978kJ,显然,形成P 分子放出的能
2 4
量更多,故在P数目相同的条件下,P 具有更低的能量,能量越低越稳定。
4
19.(2021•广东选择性考试,19节选)很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例
如,解毒剂化合物I可与氧化汞生成化合物Ⅱ。
(1)基
态硫原子价电子排布式为__________。
(2)HS、CH、HO的沸点由高到低顺序为__________。
2 4 2
(3)汞的原子序数为80,位于元素周期表第______周期第ⅡB族。
【答案】(1)3s23p4 (2)HO>HS>CH (3)六
2 2 4
【解析】(1)基态硫原子核外电子排布式为1s22s22p63s23p4,因此基态硫原子价电子排布式为3s23p4;
(2)H S、CH、HO均为分子晶体,HO分子间存在氢键,沸点较高,HS、CH 的分子间范德华力随相对
2 4 2 2 2 4
分子质量增大而增加,因此沸点由高到低顺序为:HO>HS>CH;(3)第六周期0族元素的原子序数为86,
2 2 4
因此第80号元素Hg位于第六周期第ⅡB族。
20.(2021•海南选择性考试,19节选) (14分)金属羰基配位化合物在催化反应中有着重要应用。
HMn(CO) 是锰的一种简单羰基配位化合物,其结构示意图如下。
5
资料整理【淘宝店铺:向阳百分百】回答问题:
(1)基态锰原子的价层电子排布式为___________。
(2)配位化合物中的中心原子配位数是指和中心原子直接成键的原子的数目。HMn(CO) 中锰原子的配
5
位数为___________。
(3)第一电离能的大小:C___________O(填“大于”或“小于”)。
【答案】(1)3d54s2 (2)6 (3)小于
【解析】(1)Mn元素是第25号元素,其电子排布式为1s22s22p63s23p63d54s2,所以本问应填“3d54s2”;
(2)由题干图例所示,HMn(CO) 中Mn原子以配位键连接5个C原子,1个H原子,所以本问应填“6”;(3)
5
根据元素周期律,总体规律同一周期元素从左到右第一电离能依次增强,特殊规律同周期IIA族第一电离
能大于IIIA族,VA族第一电离能大于VIA族,C是IVA族,O是VIA族,不涉及特殊规律,所以本问应
填“小于”。
资料整理【淘宝店铺:向阳百分百】