文档内容
考点 47 无机工艺流程
【基础过关】
1.(2023·福建省宁德市高三联考)用含少量 的废铁屑为原料制备FeCO 的流程如图:
3
下列说法错误的是( )
A.“除油”中适当提高温度有利于去除油污
B.“浸出”中炭黑的作用是加快铁屑溶解
C.“浸出”产生的气体是HS
2
D.“沉铁”发生反应的离子方程式为:Fe2++2HCO-=FeCO ↓+CO ↑+H O
3 3 2 2
2.(2023·广东省惠州市一模)氨既是一种重要的化工产品,又是一种重要的化工原料。如图为合成氨
以及氨氧化制硝酸的流程示意图。下列说法不正确的是( )
A.合成塔内发生的反应中有非极性键的断裂和极性键的生成
B.氧化炉内发生的反应氧化剂与还原剂的物质的量之比为5∶4
C.使用 溶液吸收尾气中的氮氧化物, 和NO 是酸性氧化物
2
D.向吸收塔中通入O 的作用是氧化
2
3.(2023·河北省石家庄部分重点中学高三联考)化学工业为疫情防控提供了强有力的物质支撑。亚氯
酸钠(NaClO )具有强氧化性,受热易分解,可作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠
2
的工艺流程如下图所示。
已知:消毒能力即每克含氯消毒剂的氧化能力相当于多少克Cl 的氧化能力。
2下列说法错误的是( )
A.“母液”中溶质的主要成分是NaSO
2 4
B.相同质量ClO 的消毒能力是Cl 的2.5倍
2 2
C.“反应2”中氧化剂与还原剂的物质的量之比为2∶1
D.“减压蒸发”可以降低蒸发时的温度,提高产品产率
4.(2023·山东省济南市三模)生产软磁铁氧体的主要原料是α-FeOOH,以硫铁矿(主要成分是FeS ,含
2
少量Al O 、SiO 和Fe O)为原料制备α-FeOOH的工艺流程如下,相关数据见下表。下列说法错误的是 (
2 3 2 3 4
)
物质
开始沉淀pH(25℃) 1.9 7.6 4.0
沉淀完全pH(25℃) 3.2 9.7 5.2
A.“焙烧”的产物之一可用于工业制硫酸
B.“试剂a”可以为FeS,主要目的是除去过量硫酸
C.“试剂b”可以为氨水,调pH的范围为5.2~7.6
D.“沉淀”时,pH过高或者过低均不利于生成
5.(2023·河北省邢台市高三联考)钪(Sc)可用于制备铝钪合金、燃料电池、钪钠卤灯、示踪剂、激光晶
体等产品。以钛白酸性废水(主要含 、Fe2+、Sc3+)为原料制备氧化钪(ScO)的工艺流程如下。下列说法
2 3
正确的是( )
A.酸洗时加入HO 的目的是将Ti 4+还原为Ti2+
2 2
B.“操作Ⅰ”需要的玻璃仪器有分液漏斗
C.“滤渣Ⅰ”的主要成分是Ti (OH)、Fe(OH)
4 3
D.草酸钪焙烧时反应的化学方程式:2Sc(C O)+3O 2ScO+12CO
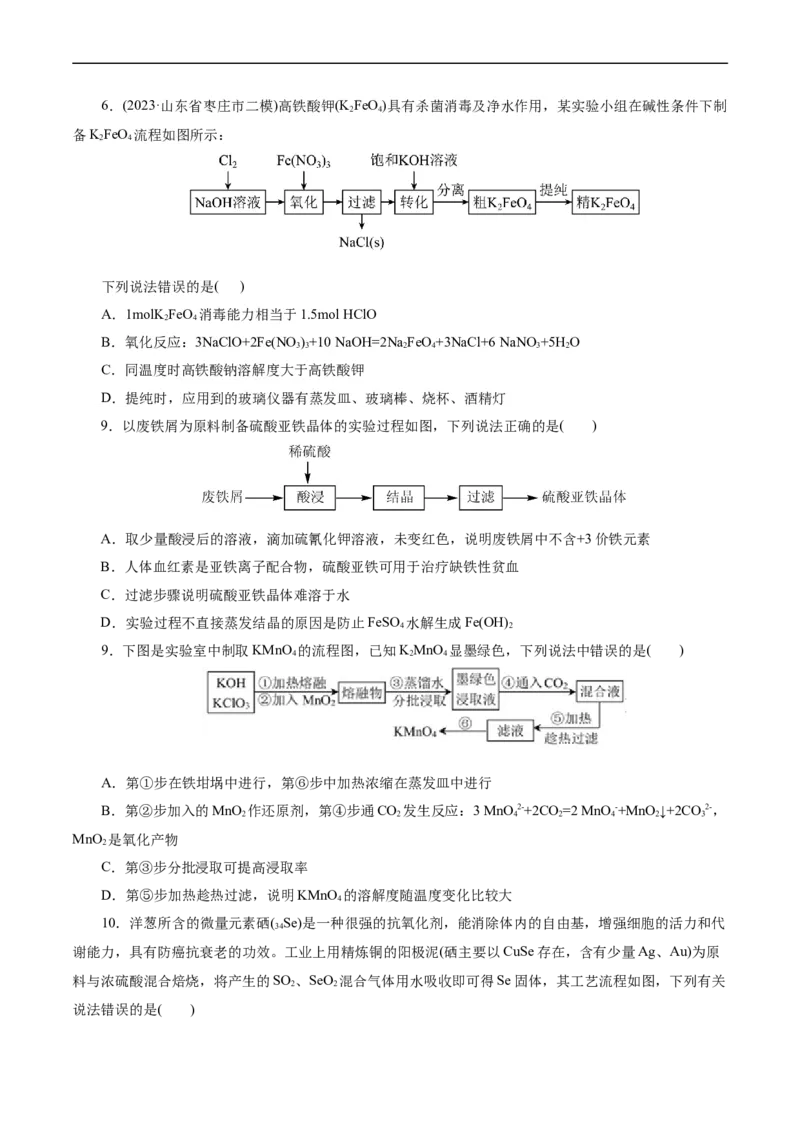
2 2 4 3 2 2 3 26.(2023·山东省枣庄市二模)高铁酸钾(K FeO)具有杀菌消毒及净水作用,某实验小组在碱性条件下制
2 4
备KFeO 流程如图所示:
2 4
下列说法错误的是( )
A.1molK FeO 消毒能力相当于1.5mol HClO
2 4
B.氧化反应:3NaClO+2Fe(NO )+10 NaOH=2Na FeO+3NaCl+6 NaNO +5H O
3 3 2 4 3 2
C.同温度时高铁酸钠溶解度大于高铁酸钾
D.提纯时,应用到的玻璃仪器有蒸发皿、玻璃棒、烧杯、酒精灯
9.以废铁屑为原料制备硫酸亚铁晶体的实验过程如图,下列说法正确的是( )
A.取少量酸浸后的溶液,滴加硫氰化钾溶液,未变红色,说明废铁屑中不含+3价铁元素
B.人体血红素是亚铁离子配合物,硫酸亚铁可用于治疗缺铁性贫血
C.过滤步骤说明硫酸亚铁晶体难溶于水
D.实验过程不直接蒸发结晶的原因是防止FeSO 水解生成Fe(OH)
4 2
9.下图是实验室中制取KMnO 的流程图,已知KMnO 显墨绿色,下列说法中错误的是( )
4 2 4
A.第①步在铁坩埚中进行,第⑥步中加热浓缩在蒸发皿中进行
B.第②步加入的MnO 作还原剂,第④步通CO 发生反应:3 MnO2-+2CO =2 MnO -+MnO↓+2CO 2-,
2 2 4 2 4 2 3
MnO 是氧化产物
2
C.第③步分批浸取可提高浸取率
D.第⑤步加热趁热过滤,说明KMnO 的溶解度随温度变化比较大
4
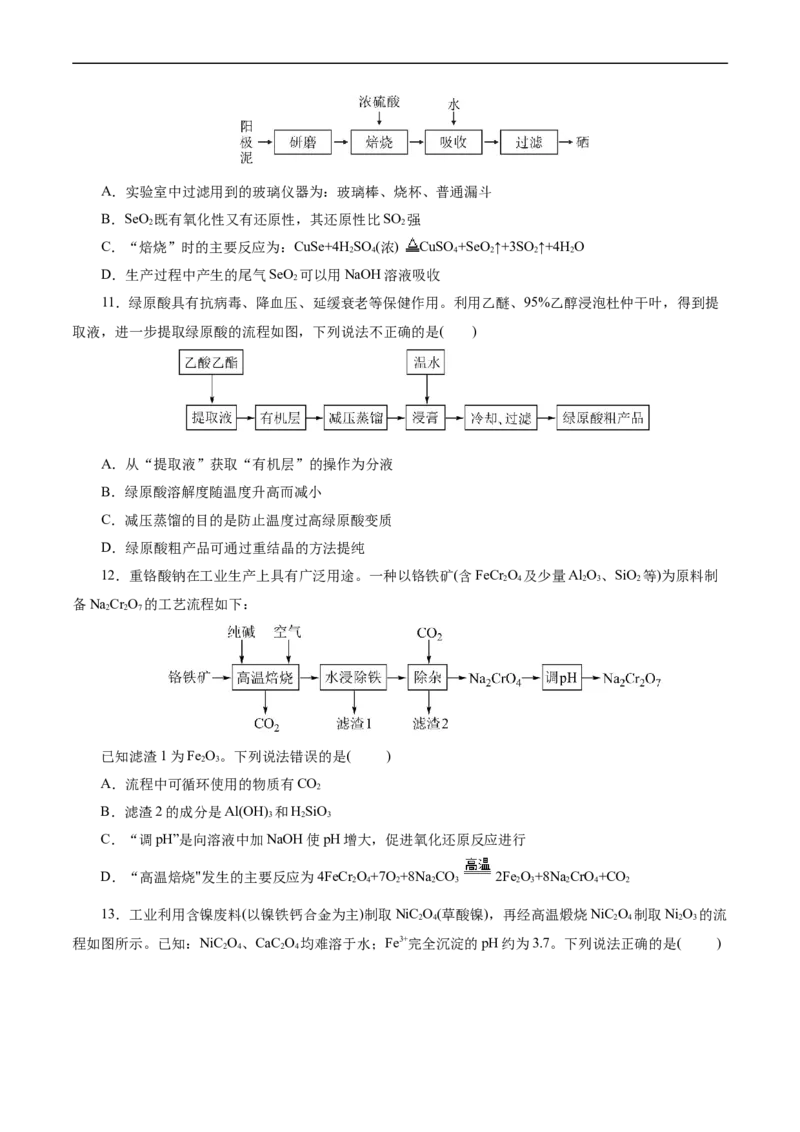
10.洋葱所含的微量元素硒( Se)是一种很强的抗氧化剂,能消除体内的自由基,增强细胞的活力和代
34
谢能力,具有防癌抗衰老的功效。工业上用精炼铜的阳极泥(硒主要以CuSe存在,含有少量Ag、Au)为原
料与浓硫酸混合焙烧,将产生的SO 、SeO 混合气体用水吸收即可得Se固体,其工艺流程如图,下列有关
2 2
说法错误的是( )A.实验室中过滤用到的玻璃仪器为:玻璃棒、烧杯、普通漏斗
B.SeO 既有氧化性又有还原性,其还原性比SO 强
2 2
C.“焙烧”时的主要反应为:CuSe+4H SO (浓) CuSO +SeO ↑+3SO↑+4H O
2 4 4 2 2 2
D.生产过程中产生的尾气SeO 可以用NaOH溶液吸收
2
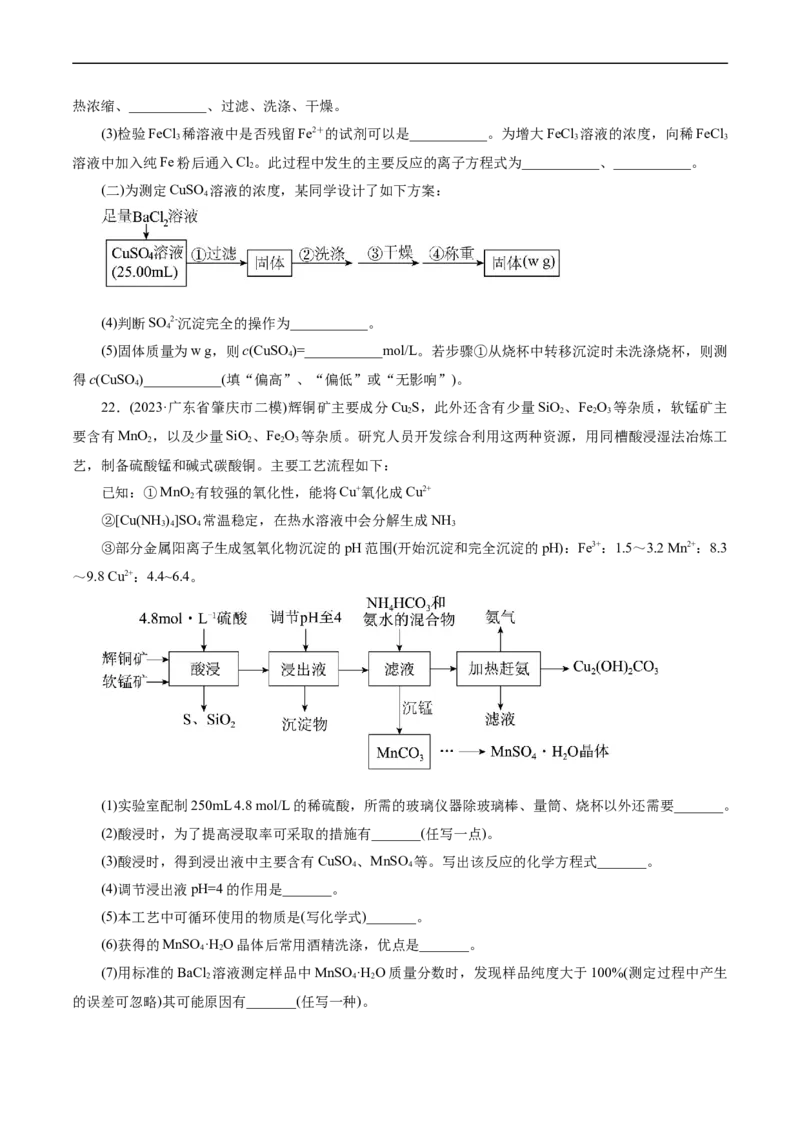
11.绿原酸具有抗病毒、降血压、延缓衰老等保健作用。利用乙醚、95%乙醇浸泡杜仲干叶,得到提
取液,进一步提取绿原酸的流程如图,下列说法不正确的是( )
A.从“提取液”获取“有机层”的操作为分液
B.绿原酸溶解度随温度升高而减小
C.减压蒸馏的目的是防止温度过高绿原酸变质
D.绿原酸粗产品可通过重结晶的方法提纯
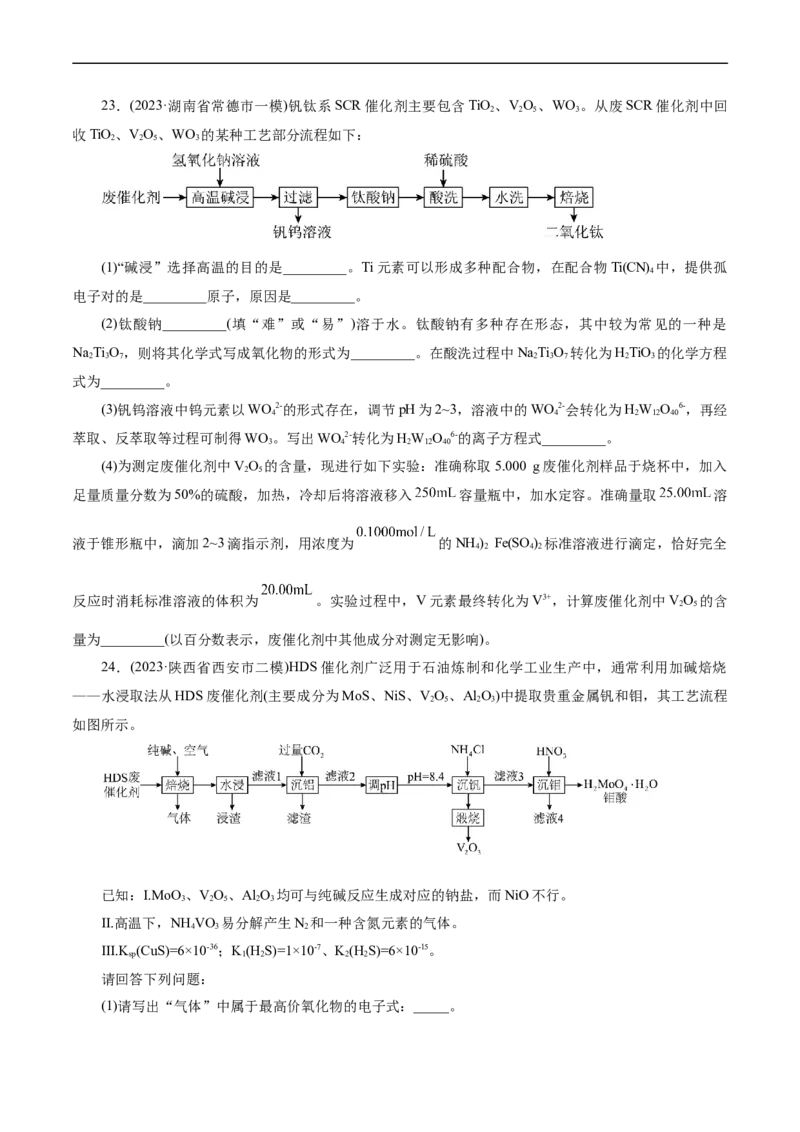
12.重铬酸钠在工业生产上具有广泛用途。一种以铬铁矿(含FeCr O 及少量Al O、SiO 等)为原料制
2 4 2 3 2
备NaCr O 的工艺流程如下:
2 2 7
已知滤渣1为Fe O。下列说法错误的是( )
2 3
A.流程中可循环使用的物质有CO
2
B.滤渣2的成分是Al(OH) 和HSiO
3 2 3
C.“调pH”是向溶液中加NaOH使pH增大,促进氧化还原反应进行
D.“高温焙烧"发生的主要反应为4FeCr O+7O +8Na CO 2Fe O+8Na CrO+CO
2 4 2 2 3 2 3 2 4 2
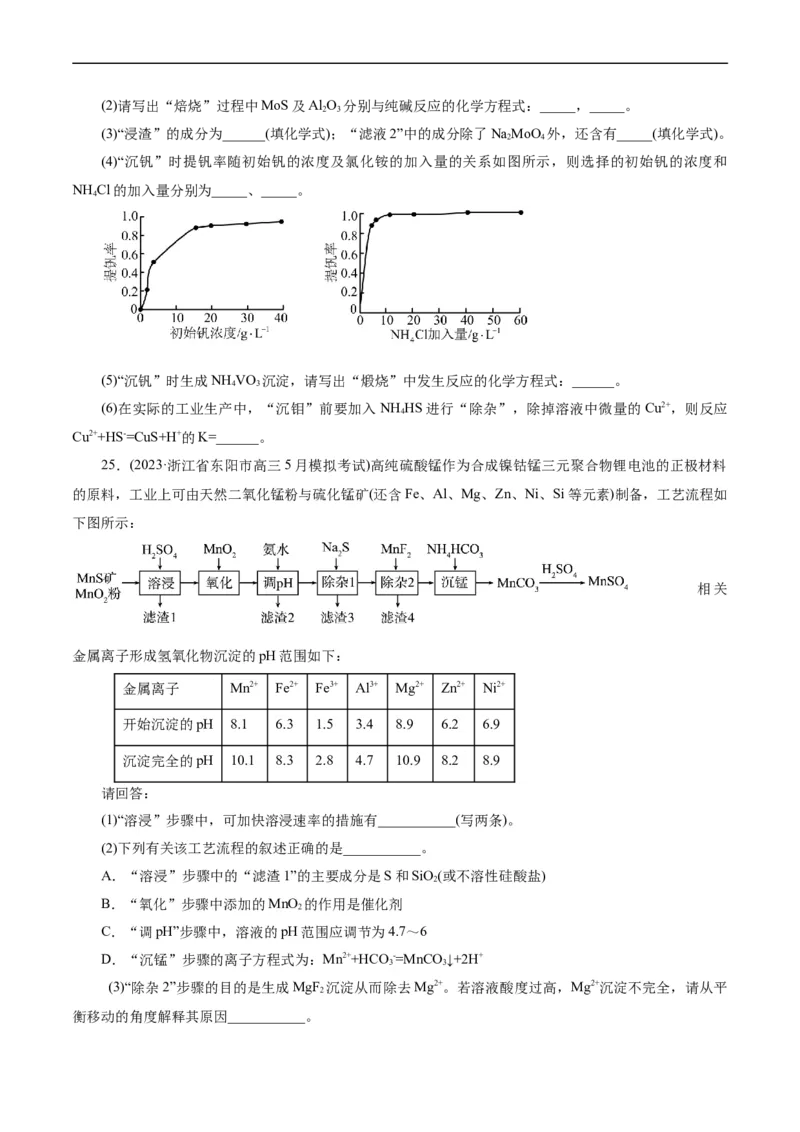
13.工业利用含镍废料(以镍铁钙合金为主)制取NiC O(草酸镍),再经高温煅烧NiC O 制取Ni O 的流
2 4 2 4 2 3
程如图所示。已知:NiC O、CaC O 均难溶于水;Fe3+完全沉淀的pH约为3.7。下列说法正确的是( )
2 4 2 4A.酸溶时,可加入大量硫酸来提高“酸溶”效率
B.调pH时,加入NaCO 溶液,目的是使Fe3+转化为Fe (CO) 沉淀
2 3 2 3 3
C.沉镍时,发生反应的离子方程式为:Ni2++C O2-=NiC O↓
2 4 2 4
14.四氧化三锰(Mn O)广泛应用于生产软磁材料、催化材料。一种以低品位锰矿(含MnCO 、
3 4 3
MnO、MnOOH及少量Fe O、Al O、SiO)为原料生产MnO 的工艺流程如图所示:
2 3 2 3 2 3 2 3 4
下列说法错误的是( )
A.“溶浸”过程MnO 发生反应的离子方程式是MnO+H O+4H+=2Mn2++O ↑+3H O
2 3 2 3 2 2 2 2
B.“滤渣2”的主要成分是Fe(OH) 、Al(OH)
3 3
C.由“母液”可获得(NH )SO
4 2 4
D.“氧化”反应后,溶液的pH增大
【能力提升】
15.(2023·浙江省浙南名校联盟高三第二次联考)某研究小组,利用Cl 氧化法高效制备KMnO 。制备
2 4
流程如下:
已知:3MnO +KClO +6KOH 3KMnO+ KCl+3H O (K MnO 呈墨绿色),
2 3 2 4 2 2 4
Cl+KMnO=2KMnO+2KCl
2 2 4 4
请回答下列问题:
(1) KClO 需过量的目的是___________
3
(2)下列说法不正确的是___________
A.过程1应在瓷坩埚中进行
B.MnO 应分批加入,以防止熔融物溢出
2C.可用酒精洗涤,得到较干燥的产品
D.该实验表明,在强碱性环境下Cl 的氧化性强于KMnO
2 4
(3)为检验过程1是否反应完全,应采取的实验操作是:___________。
(4)将纯化后的KMnO 配成溶液,并应用于废水中化学需氧量(COD)测定
4
化学需氧量(COD)是:在一定条件下,用强氧化剂氧化一定体积水中的还原剂及有机物时所消耗氧化
剂的量,折算成氧气的量。(单位为mg·L )来表示。
① 从 下 列 选 项 选 择 合 适 操 作 ( 操 作 不 能 重 复 使 用 ) 并 排 序 ___________ :
(___________)→(___________)→(___________)→(___________)→f
a.取废水样100mL加稀硝酸酸化
b.取废水样100mL加稀硫酸酸化
c.用0.01000mol·L 的KMnO 标准溶液滴定
4
d.加10.00mL0.01000mol·L 的KMnO 标准溶液,煮沸,冷却
4
e.加入0.01000mol·L 的NaC O 标准溶液至过量,消耗10.00mL
2 2 4
f.记录,滴定时,KMnO 标准溶液消耗量为8.20mL
4
②计算水样中COD为___________mg·L 。
16.(2023·贵州省三模)硫酸镁在印染等工业中应用广泛。一种以硼镁泥(主要成分为MgCO ,还含有
3
Ca、Fe、Al、 Mn、Si 的氧化物等成分)制取七水硫酸镁的流程如下:
已知:本题中涉及的部分难溶电解质的溶度积如下表:
难溶电解
Fe(OH) Fe(OH) Al(OH) Mg(OH)
质 3 2 3 2
K 4.0×10-38 8.0 ×10-16 4.6×10-33 1.8×10-11
sp
回答下列问题:
(1)“酸浸”中主要反应的化学方程式为__________ ,滤渣的成分为_________。
(2)“氧化” 的目的: (i)氧化Fe2+; (ii) 氧化Mn2+,其离子方程式为____________________。
(3)“调pH”时,最适宜使用的X试剂是_____ (填标号)。A.NH ·H O B.NaOH C.MgO
3 2
(4)当溶液中c(Al3+)= 4.6×10 -6mol·L-1时,则所调pH=________________。
(5)调pH后,要继续加热再过滤出沉淀,继续加热的目的是________________。
(6)已知 CaSO 与 MgSO 在水中的溶解度随温度变化的曲线如图所示,则“结晶 1”的操作为
4 4
______________、______________。
17.(2023·广东省高三调研)利用硫酸烧渣(主要含Fe O 、FeO,还含有SiO 和CuO等)来制取FeSO 溶
2 3 2 4
液。
(1)①将硫酸烧渣进行粉碎,其目的是_______。
②“酸浸”时,Fe O 发生反应的离子方程式是_______。
2 3
(2)“还原”时,铁粉将Fe3+、Cu2+还原为Fe2+和Cu。检验 是否已全部被还原,所选用试剂的化学式
是_______。
(3)将得到的FeSO 溶液进行下列操作,测定其物质的量浓度:
4
步骤一:取10.00mL FeSO 溶液,将其稀释成100.00mL溶液。
4
步骤二:取25.00mL稀释后的溶液,向其中加入 酸性KMnO 溶液。恰好反应时,记下消
4
耗KMnO 溶液的体积。
4
步骤三:重复上述实验3次,平均消耗KMnO 溶液20.00mL。
4
已知: (未配平)
①配平上述方程式_______。②“步骤一”中稀释时所用的水需先进行加热煮沸,其目的是_______。
③试通过计算,求原FeSO 溶液的物质的量浓度是多少?(写出计算过程)_______。
4
18.(2023·上海市高三质检)信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”
探究小组将一批废弃的线路板简单处理后,得到含70 %Cu、25%Al、4%Fe及少量Au、Pt等金属的混合
物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
一定
条件下,一些金属氢氧化物沉淀时的 如下表:
金属氢氧化物 Fe(OH) Fe(OH) Al(OH) Cu(OH)
3 2 3 2
开始沉淀的pH 2.3 6.8 3.5 4.4
完全沉淀的pH 3.2 8.3 4.6 6.4
完成下列填空:
(1)写出第①步中Cu与酸反应生成NO的离子方程式________________;第②步中使用HO 做氧化剂
2 2
的优点是__________,NaOH调节溶液pH的目的是使____________生成沉淀。
(2)第③步的操作为:滤液2加热蒸发、_______、_______、乙醇洗涤、干燥,得到胆矾。
(3)由滤渣2制取Al (SO )·18H O ,探究小组设计了三种方案:
2 4 3 2
上述三种方案中,____方案不可行,原因是________;从原子利用率角度考虑,_____方案更合理。
(4)探究小组用滴定法测定CuSO ·5H O含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干
4 2
扰离子后,用c mol ·L-1 EDTA(H Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL。滴定反应如下:
2
Cu2+ + H Y2-= CuY2- + 2H+
2
写出计算CuSO ·5H O质量分数的表达式ω= __________________________ 。
4 2
下列操作会导致CuSO ·5H O含量的测定结果偏高的是_________。
4 2
a.未干燥锥形瓶 b.滴定终点时滴定管尖嘴中产生气泡
c.未除净可与EDTA反应的干扰离子19.(2023·重庆市二模)仲钼酸铵(NH )MoO []是用作测定磷酸盐、镍、锗、二氧化硒、砷酸盐、生
4 6 7 24
物碱和铅等的试剂。用某含钼废料(主要含有MoS 、CoS和Al O)制备仲钼酸铵的工艺流程如下图所示:
2 2 3
请回答下列问题:
(1)基态Co原子的价层电子排布式为_______。
(2)焙烧的过程中采用如图所示的“多层逆流焙烧”,其优点是_______(任答两点即可)。
(3)焙烧时MoS 转化为MoO ,则MoS 焙烧时的化学方程式为_______。
2 3 2
(4)“操作”的名称是_______;实验室完成该“操作”用到的最主要的玻璃仪器是_______。
(5)“调pH为5.5”生成仲钼酸铵的化学方程式为_______。
(6)已知有如下转化关系,则8钼酸铵的化学式为_______。
(7钼酸根) (8钼酸根)
(7)若在某温度下,BaMoO 在水中的溶解平衡曲线如下图所示。向 100mL0.400mol/L Na MoO
4 2 4
溶液中滴加200mL Ba(OH) 溶液,恰好使MoO 2-完全沉淀[ ],则所加
2 4
入的Ba(OH) 溶液的浓度约为_______mol/L(混合后,溶液的体积变化忽略不计,计算结果保留到小数点后
2
3位)。
20.(2023·安徽省高三质量检测)以某混合氧化物(由MnO 、ZnO、CuO、Fe O 组成)为原料制备
2 2 3
KMnO 和FeSO ·7H O的工艺流程如下:
4 4 2已知:ZnO与Al O 的化学性质相似。
2 3
回答下列问题:
(1)基态Cu原子核外电子排布式为_______。
(2)写出“酸浸”时,CuO反应的化学方程式:_______。
(3)“去铜”时,除了生成CuCl外,还有SO 2- 、H+生成,该反应的离子方程式为_______。
4
(4)为检验“去铜”后是否含有Fe3+,选用的试剂是_______。
(5)“熔融”时MnO 转化为KMnO ,该反应中每转移1mol电子,消耗_______gMnO 。
2 2 4 2
(6)已知"“歧化”时反应为3KMnO +2CO =2KMnO +MnO↓+2K CO 。常温下,相关物质的溶解度数据
2 4 2 4 2 2 3
如下:
物质 KCO KHCO KSO KMnO CHCOOK
2 3 3 2 4 4 3
溶解度(g/100g水) 111 33.7 11.1 6.34 256
通入CO 至溶液pH达10~11时,应停止通CO ,不能继续通入CO 的原因是_______。可以替代CO
2 2 2 2
的试剂是_______(填“稀盐酸”“稀硫酸”或“稀醋酸”)。
(7)KMnO 的纯度测定:称取mgKMnO 粗品于烧杯中,加入蒸馏水和稀硫酸溶解,再用0.5mol·L-1的
4 4
NaC O 溶液滴定3次,平均消耗NaC O 溶液20.00mL。KMnO 样品的纯度为_______%(用含m的代数式
2 2 4 2 2 4 4
表示,杂质不参与反应)。已知酸性条件下KMnO 与NaC O 反应,生成Mn2+和CO。
4 2 2 4 2
21.(2023·上海市崇明区二模)铁、铜及其化合物是中学化学中常见化学物质,阅读材料回答问题:
(一)氯化铁是重要的化工原料,FeCl ·6H O的实验室制备流程图如下:
3 2
(1)废铁屑表面往往含有油污,去除废铁屑表面的油污的方法是___________。操作①要用到的玻璃仪
器有玻璃棒、烧杯和___________。
(2)加入含有少量铜的废铁屑比加入纯铁屑反应更快,原因为___________。操作②涉及的过程为:加热浓缩、___________、过滤、洗涤、干燥。
(3)检验FeCl 稀溶液中是否残留Fe2+的试剂可以是___________。为增大FeCl 溶液的浓度,向稀FeCl
3 3 3
溶液中加入纯Fe粉后通入Cl。此过程中发生的主要反应的离子方程式为___________、___________。
2
(二)为测定CuSO 溶液的浓度,某同学设计了如下方案:
4
(4)判断SO 2-沉淀完全的操作为___________。
4
(5)固体质量为w g,则c(CuSO )=___________mol/L。若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测
4
得c(CuSO )___________(填“偏高”、“偏低”或“无影响”)。
4
22.(2023·广东省肇庆市二模)辉铜矿主要成分Cu S,此外还含有少量SiO 、Fe O 等杂质,软锰矿主
2 2 2 3
要含有MnO ,以及少量SiO 、Fe O 等杂质。研究人员开发综合利用这两种资源,用同槽酸浸湿法冶炼工
2 2 2 3
艺,制备硫酸锰和碱式碳酸铜。主要工艺流程如下:
已知:①MnO 有较强的氧化性,能将Cu+氧化成Cu2+
2
②[Cu(NH )]SO 常温稳定,在热水溶液中会分解生成NH
3 4 4 3
③部分金属阳离子生成氢氧化物沉淀的pH范围(开始沉淀和完全沉淀的pH):Fe3+:1.5~3.2 Mn2+:8.3
~9.8 Cu2+:4.4~6.4。
(1)实验室配制250mL 4.8 mol/L的稀硫酸,所需的玻璃仪器除玻璃棒、量筒、烧杯以外还需要_______。
(2)酸浸时,为了提高浸取率可采取的措施有_______(任写一点)。
(3)酸浸时,得到浸出液中主要含有CuSO 、MnSO 等。写出该反应的化学方程式_______。
4 4
(4)调节浸出液pH=4的作用是_______。
(5)本工艺中可循环使用的物质是(写化学式)_______。
(6)获得的MnSO ·H O晶体后常用酒精洗涤,优点是_______。
4 2
(7)用标准的BaCl 溶液测定样品中MnSO ·H O质量分数时,发现样品纯度大于100%(测定过程中产生
2 4 2
的误差可忽略)其可能原因有_______(任写一种)。23.(2023·湖南省常德市一模)钒钛系SCR催化剂主要包含TiO 、VO 、WO 。从废SCR催化剂中回
2 2 5 3
收TiO 、VO、WO 的某种工艺部分流程如下:
2 2 5 3
(1)“碱浸”选择高温的目的是_________。Ti元素可以形成多种配合物,在配合物Ti(CN) 中,提供孤
4
电子对的是_________原子,原因是_________。
(2)钛酸钠_________(填“难”或“易”)溶于水。钛酸钠有多种存在形态,其中较为常见的一种是
NaTiO ,则将其化学式写成氧化物的形式为_________。在酸洗过程中NaTiO 转化为HTiO 的化学方程
2 3 7 2 3 7 2 3
式为_________。
(3)钒钨溶液中钨元素以WO2-的形式存在,调节pH为2~3,溶液中的WO2-会转化为HW O 6-,再经
4 4 2 12 40
萃取、反萃取等过程可制得WO。写出WO2-转化为HW O 6-的离子方程式_________。
3 4 2 12 40
(4)为测定废催化剂中VO 的含量,现进行如下实验:准确称取5.000 g废催化剂样品于烧杯中,加入
2 5
足量质量分数为50%的硫酸,加热,冷却后将溶液移入 容量瓶中,加水定容。准确量取 溶
液于锥形瓶中,滴加2~3滴指示剂,用浓度为 的NH ) Fe(SO ) 标准溶液进行滴定,恰好完全
4 2 4 2
反应时消耗标准溶液的体积为 。实验过程中,V元素最终转化为V3+,计算废催化剂中VO 的含
2 5
量为_________(以百分数表示,废催化剂中其他成分对测定无影响)。
24.(2023·陕西省西安市二模)HDS催化剂广泛用于石油炼制和化学工业生产中,通常利用加碱焙烧
——水浸取法从HDS废催化剂(主要成分为MoS、NiS、VO 、Al O)中提取贵重金属钒和钼,其工艺流程
2 5 2 3
如图所示。
已知:I.MoO、VO、Al O 均可与纯碱反应生成对应的钠盐,而NiO不行。
3 2 5 2 3
II.高温下,NH VO 易分解产生N 和一种含氮元素的气体。
4 3 2
III.K (CuS)=6×10-36;K(H S)=1×10-7、K(H S)=6×10-15。
sp 1 2 2 2
请回答下列问题:
(1)请写出“气体”中属于最高价氧化物的电子式:_____。(2)请写出“焙烧”过程中MoS及Al O 分别与纯碱反应的化学方程式:_____,_____。
2 3
(3)“浸渣”的成分为______(填化学式);“滤液2”中的成分除了NaMoO 外,还含有_____(填化学式)。
2 4
(4)“沉钒”时提钒率随初始钒的浓度及氯化铵的加入量的关系如图所示,则选择的初始钒的浓度和
NH Cl的加入量分别为_____、_____。
4
(5)“沉钒”时生成NH VO 沉淀,请写出“煅烧”中发生反应的化学方程式:______。
4 3
(6)在实际的工业生产中,“沉钼”前要加入NH HS进行“除杂”,除掉溶液中微量的Cu2+,则反应
4
Cu2++HS-=CuS+H+的K=______。
25.(2023·浙江省东阳市高三5月模拟考试)高纯硫酸锰作为合成镍钴锰三元聚合物锂电池的正极材料
的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺流程如
下图所示:
相关
金属离子形成氢氧化物沉淀的pH范围如下:
金属离子 Mn2+ Fe2+ Fe3+ Al3+ Mg2+ Zn2+ Ni2+
开始沉淀的pH 8.1 6.3 1.5 3.4 8.9 6.2 6.9
沉淀完全的pH 10.1 8.3 2.8 4.7 10.9 8.2 8.9
请回答:
(1)“溶浸”步骤中,可加快溶浸速率的措施有___________(写两条)。
(2)下列有关该工艺流程的叙述正确的是___________。
A.“溶浸”步骤中的“滤渣1”的主要成分是S和SiO(或不溶性硅酸盐)
2
B.“氧化”步骤中添加的MnO 的作用是催化剂
2
C.“调pH”步骤中,溶液的pH范围应调节为4.7~6
D.“沉锰”步骤的离子方程式为:Mn2++HCO-=MnCO↓+2H+
3 3
(3)“除杂2”步骤的目的是生成MgF 沉淀从而除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,请从平
2
衡移动的角度解释其原因___________。(4) MnCO 加入足量稀硫酸充分溶解后,经过一系列操作可得较纯的 MnSO 晶体。这一系列操作是
3 4
______→______→过滤→______→______→纯净的MnSO 晶体。______
4
(5) Mn2+含量可通过过硫酸铵—硫酸亚铁铵法进行测定。其原理是将试样溶于硫酸中,使溶液中的
Mn2+在硫磷混合酸的作用下,以硝酸银为催化剂,用过硫酸铵把Mn2+氧化为高锰酸,然后以标准硫酸亚铁
铵溶液滴定高锰酸,根据标准液消耗量计算Mn2+的含量。相关方程式如下:
2MnSO +5(NH)SO+8H O=2HMnO +5(NH)SO +7H SO
4 4 2 2 8 2 4 4 2 4 2 4
2HMnO +10(NH)Fe(SO )+7H SO =5Fe (SO )+10(NH)SO +2MnSO +8H O
4 4 2 4 2 2 4 2 4 3 4 2 4 4 2
①测定操作步骤如下,在横线内填写一件最关键仪器补全步骤:
用___________称量 MnSO 样品 0.250g→用 100mL 容量瓶将 MnSO 样品配成 100mL 溶液→用
4 4
___________取待测液25.00mL于锥形瓶中→加入适量硫磷混合酸和硝酸银,再加入足量过硫酸铵充分反
应→加热煮沸除去多余的过硫酸铵→用酸式滴定管盛装0.1000mol/L(NH )Fe(SO ) 标准溶液,滴定3次,
4 2 4 2
分别消耗20.04mL、19.30mL、19.96mL。
②根据以上数据计算样品中MnSO 的质量分数___________。
4
26.(2023·浙江省临海、新昌两地高三适应性考试5月模考)工业上以铬铁矿(FeCrO 质量分数为a%,
2 4
含Al O、SiO 等杂质)为主要原料制备红矾钠(Na Cr O•2H O)的工艺流程图如图,回答下列问题:
2 3 2 2 2 7 2
(1)焙烧的目的是将FeCr O 转化为NaCrO ,写出转化过程中生成可溶性含铝组分的化学方程式:
2 4 2 4
______。
(2)下列有关说法不正确的是______。
A.蒸发结晶时如果长时间蒸发,有利于提高NaCr O•2H O的产率
2 2 7 2
B.除了NaCr O 外,在上述工艺流程中可循环利用的物质还有HSO
2 2 7 2 4
C.含铁元素的化合物可在中和过程中被除去
D.焙烧时气流与矿料逆流而行,其目的是增大反应物接触面积,提高反应速率
(3)蒸发结晶,盛放样品的容器名称是_______。
(4)酸化的目的是(结合离子方程式说明)______。
(5)利用氧化还原滴定法测定NaCr O•2H O产品的纯度,从下列选项中选择合适的仪器和操作,补全
2 2 7 2
如下步骤[“_______”上填写一件最关键仪器,“(_______)”内填写一种操作,均用字母表示]。用______(称量产品2.50g)→在烧杯中__________→用容量瓶__________→用移液管(取25.00mL所配溶液于锥形瓶
中)→加入足量碘化钠溶液→加入 3 滴淀粉指示剂→用______(用 0.1200mol•L-1NaSO 标准溶液滴
2 2 3
定)→_________并且 内不恢复原来的颜色,消耗标准溶液40.00mL
仪器:a.碱式滴定管;b.酸式滴定管;c.电子天平;d.托盘天平;
操作:e.加硫酸溶解;f.加盐酸溶解;g.配制250mL溶液;h.观察到溶液蓝色褪去:i.观察到溶液变成
蓝色
(6)若以铬铁矿为原料制备mkg硼化铬(CrB),在工艺流程中Cr损失b%,则至少需要铬铁矿的质量为
______kg(用含字母的计算式表示)。
27.(2023·辽宁省鞍山市二模)钼酸钠(Na MoO)是一种金属缓蚀剂,金属钼是重要的合金材料,下图
2 4
是由辉钼矿(钼元素的主要存在形式为MoS)生产两种物质的流程:
2
请回答下列问题:
(1)Mo为第五周期元素,与Cr同族,其基态原子价层电子排布式为_______;
(2)辉钼矿在空气中焙烧时,加入氧化物X可减少空气污染物的排放,烧渣中 以CaMoO 的形态存
4
在,则X为_______(填化学式),焙烧方程式为_______;
(3)已知:25℃时,K (CaMoO)=1.6×10-5,则该温度下,CaMoO 饱和溶液中Ca2+的浓度为_______ ;
sp 4 4
(4) Na CO 溶液在对烧渣进行浸出时,温度对浸出率的影响如下图所示:
2 3
“操作1”需选择“高压浸出”的理由是_______;
(5)从上述流程中可分析出MoO 属于_______(填“酸性氧化物”或“碱性氧化物”);
3
(6)由MoO 获得 可以选择H 做还原剂,相关说法正确的是_______(填代号);
3 2a.其原理属于热还原法冶金
b. Mo的金属活动性可能位于Mg、Al之间
c.工业上可用 与钼酸盐溶液直接作用冶炼钼
(7)已知MoS 晶体有类似石墨的层状结构,预测其可能的用途是_______。
2
28.(2023·浙江省精诚联盟高三三模)实验室以废铜屑为原料制取碱式碳酸铜[[aCu(OH)·bCuCO]]的流
2 3
程如下:
已知:
①废铜屑的主要杂质有CuO、Al O、Fe O、FeO和SiO,“酸浸”使用的装置如图;
2 3 2 3 2
②相关数据见下表:
Cu(OH) Al(OH)
物质 Fe(OH) Fe(OH)
3 2
2 3
开始沉淀pH 1.9 6.5 4.2 3.4
沉淀完全pH 3.2 9.7 6.7 4.0
请回答:
(1)仪器Y的名称是 ,溶液Z的作用是 。
(2)流程中需要对滤液加热至70℃但又不宜过高,理由是 。
(3)下列有关说法正确的是 。
A.“酸浸”装置鼓入的N 也可用空气代替
2
B.物质X可能是CuO、NaOH溶液或浓氨水
C.滤渣的主要成分是SiO、Fe(OH) 、Fe(OH) 和Al(OH)
2 3 2 3
D.流程中两次对溶液调pH,其调节范围和操作目的均不相同
E.“系列操作”包括了充分搅拌、趁热过滤、蒸馏水洗和灼烧等步骤
(4)可采用滴定法、热重分析法分别对碱式碳酸铜[[aCu(OH)·bCuCO]]的组成进行分析。
2 3
①滴定法测定时需要用到酸式滴定管。其中,滴定步骤前可能需要的操作如下,请从中选出正确的操作并按序列出字母:
向滴定管加蒸馏水并观察是否漏液_____→_____→____→_____→_____→_____→在滴定管架上竖直
放置,静置后读数
a.用蒸馏水洗涤滴定管,再用标准溶液润洗
b.将活塞旋转180°后静置观察
c.使滴定管略倾斜,捏住橡皮管内玻璃球赶走管尖气泡
d.向滴定管中加入标准液并高于“0”刻度
e.竖直滴定管,调整标准液液面低于“0”刻度
f.一手握住并倾斜滴定管,一手开关活塞赶走管尖气泡
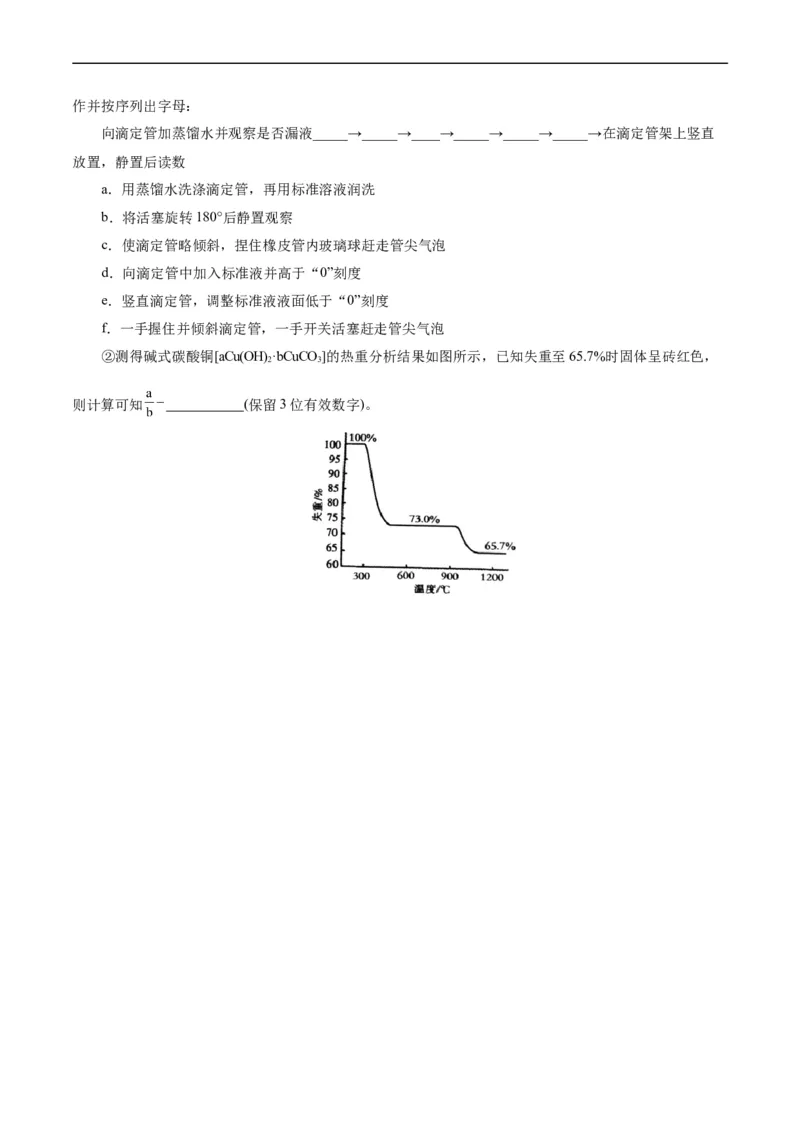
②测得碱式碳酸铜[aCu(OH)·bCuCO]的热重分析结果如图所示,已知失重至65.7%时固体呈砖红色,
2 3
则计算可知 (保留3位有效数字)。