文档内容
【基础知识】原电池 化学电源
考点一 原电池的工作原理及应用
【知识模型】
1、原电池的概念及构成条件
(1)定义:将 能 转化为 能 的装置。(太阳能电池:将 能 转化为 能 )
(2)原电池的形成条件
①能自发进行的 反应 。
②两个 不同 的电极(燃料电池的两个电极可以相同)。
③形成 回路 ,需满足三个条件:
a.存在电解质;b.两电极直接或间接接触;c.两电极插入电解质溶液或熔融电解质中。
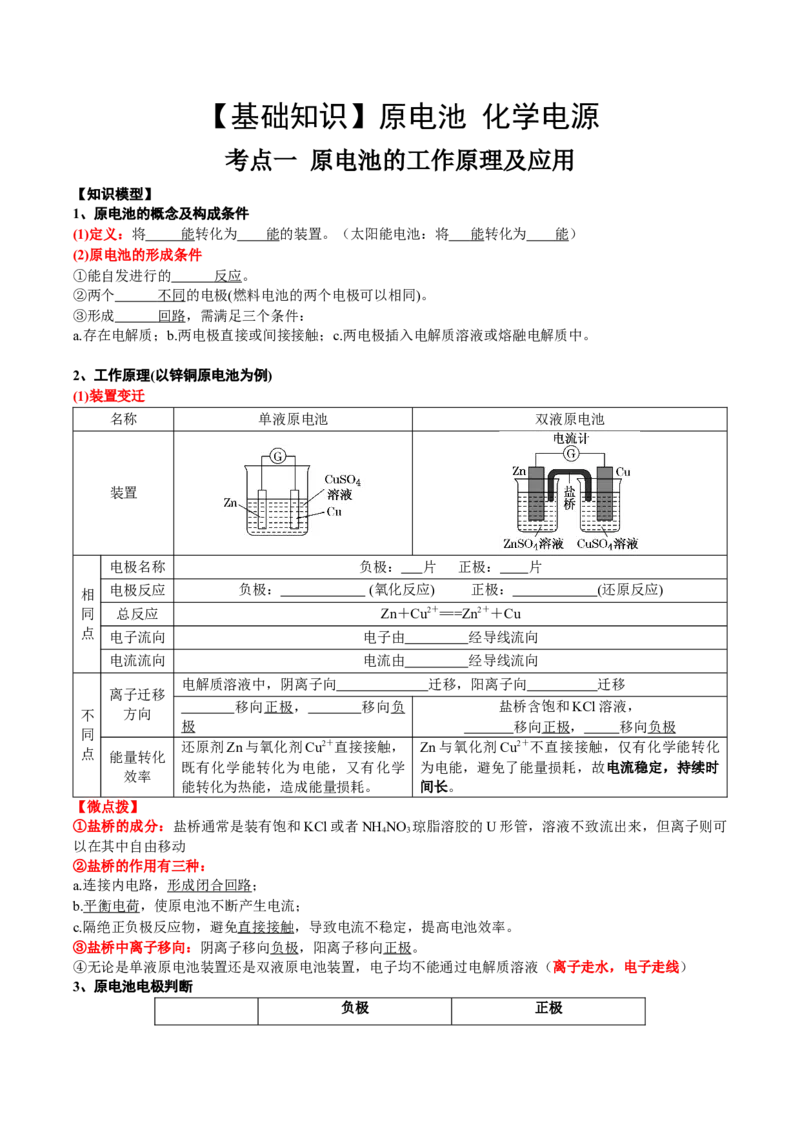
2、工作原理(以锌铜原电池为例)
(1)装置变迁
名称 单液原电池 双液原电池
装置
电极名称 负极: 片 正极: 片
相
电极反应 负极: (氧化反应) 正极: (还原反应)
同 总反应 Zn+Cu2+===Zn2++Cu
点
电子流向 电子由 经导线流向
电流流向 电流由 经导线流向
电解质溶液中,阴离子向 迁移,阳离子向 迁移
离子迁移
移向正极, 移向负 盐桥含饱和KCl溶液,
不 方向
极 移向正极, 移向负极
同
还原剂Zn与氧化剂Cu2+直接接触, Zn与氧化剂Cu2+不直接接触,仅有化学能转化
点 能量转化
既有化学能转化为电能,又有化学 为电能,避免了能量损耗,故电流稳定,持续时
效率
能转化为热能,造成能量损耗。 间长。
【微点拨】
①盐桥的成分:盐桥通常是装有饱和KCl或者NH NO 琼脂溶胶的U形管,溶液不致流出来,但离子则可
4 3
以在其中自由移动
②盐桥的作用有三种:
a.连接内电路,形成闭合回路;
b.平衡电荷,使原电池不断产生电流;
c.隔绝正负极反应物,避免直接接触,导致电流不稳定,提高电池效率。
③盐桥中离子移向:阴离子移向负极,阳离子移向正极。
④无论是单液原电池装置还是双液原电池装置,电子均不能通过电解质溶液(离子走水,电子走线)
3、原电池电极判断
负极 正极反应类型
得失电子
离子移向
电极材料
化合价变化
电势大小
4、原电池的应用
(1)加快氧化还原反应的速率:原电池中,氧化反应和还原反应分别在两极进行,使溶液中离子运动时相互
的干扰减小,使反应速率增大。
如:在Zn和稀硫酸反应时,滴加少量CuSO 溶液,则Zn置换出的铜和锌能构成原电池的正负极,从而加
4
快Zn与稀硫酸反应的速率
(2)比较金属活动性的强弱:原电池中,负极一般是活动性较强的金属,正极一般是活动性较弱的金属(或
非金属)
方法:电极质量减少作负极,较活泼;有气体生成、电极质量不断增加或不变作正极,较不活泼
(3)设计制作化学电源
①拆分反应:将氧化还原反应分成两个半反应
②选择电极材料:电极材料必须导电。根据氧化还原反应找出正、负极材料,一般选择活动性较强的金属
作为负极(或者在该氧化还原反应中,本身失去电子的材料);活动性较弱的金属或可导电的非金属(如石墨
等)作为正极
③构成闭合回路:将两个半反应分别在两个容器中进行(中间连接盐桥),则两个容器中的电解质溶液应选
择与电极材料相同的阳离子的溶液
【模型再构】
例1、常见原电池(写出以下总反应、正负极电极反应式)
①Fe | FeCl (aq) | Cu
3
总反应:
正极: 负极:
②Mg | NaOH(aq) | Al
总反应:
正极: 负极:
③Fe | 浓HNO(aq) | Cu
3
总反应:
正极: 负极:
④Zn | NaCl(aq) | Cu
总反应:
正极: 负极:
【微点拨】
自发发生的氧化还原反应并不一定是电极与电解质溶液反应,也可以是电极与溶解的O 等发生反应.
2
例2、设计原电池装置证明Fe3+的氧化性比Cu2+强。(1)写出能说明氧化性Fe3+大于Cu2+的离子方程式:_________________________________。
(2)若要将上述反应设计成原电池,电极反应式分别是:
①负极:________________________________________________________________________。
②正极:________________________________________________________________________。
(3)在方框中画出装置图,指出电极材料和电解质溶液:
①不含盐桥 ②含盐桥
【问题解决】
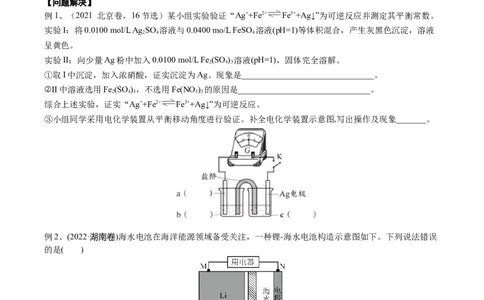
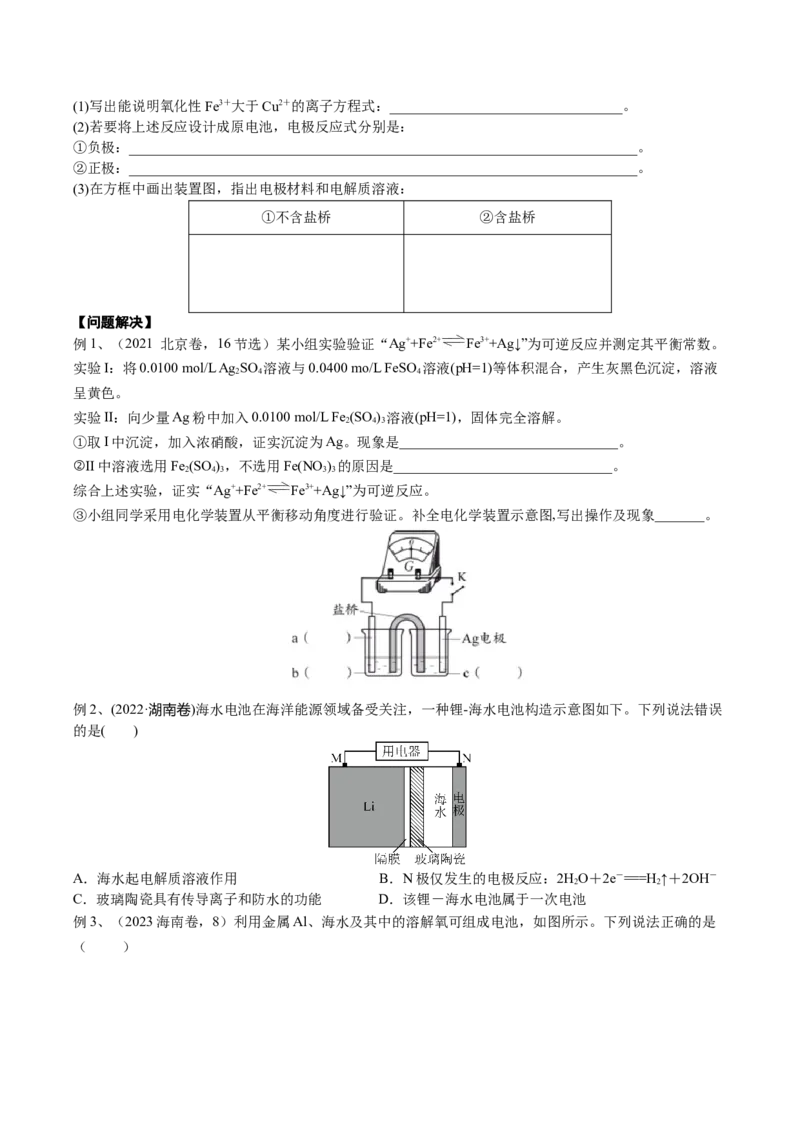
例1、(2021 北京卷,16节选)某小组实验验证“Ag++Fe2+ Fe3++Ag↓”为可逆反应并测定其平衡常数。
实验I:将0.0100 mol/L Ag SO 溶液与0.0400 mo/L FeSO 溶液(pH=1)等体积混合,产生灰黑色沉淀,溶液
2 4 4
呈黄色。
实验II:向少量Ag粉中加入0.0100 mol/L Fe (SO ) 溶液(pH=1),固体完全溶解。
2 4 3
①取I中沉淀,加入浓硝酸,证实沉淀为Ag。现象是_______________________________。
②II中溶液选用Fe (SO ),不选用Fe(NO ) 的原因是_______________________________。
2 4 3 3 3
综合上述实验,证实“Ag++Fe2+ Fe3++Ag↓”为可逆反应。
③小组同学采用电化学装置从平衡移动角度进行验证。补全电化学装置示意图,写出操作及现象_______。
例2、(2022·湖南卷)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错误
的是( )
A.海水起电解质溶液作用 B.N极仅发生的电极反应:2HO+2e-===H ↑+2OH-
2 2
C.玻璃陶瓷具有传导离子和防水的功能 D.该锂-海水电池属于一次电池
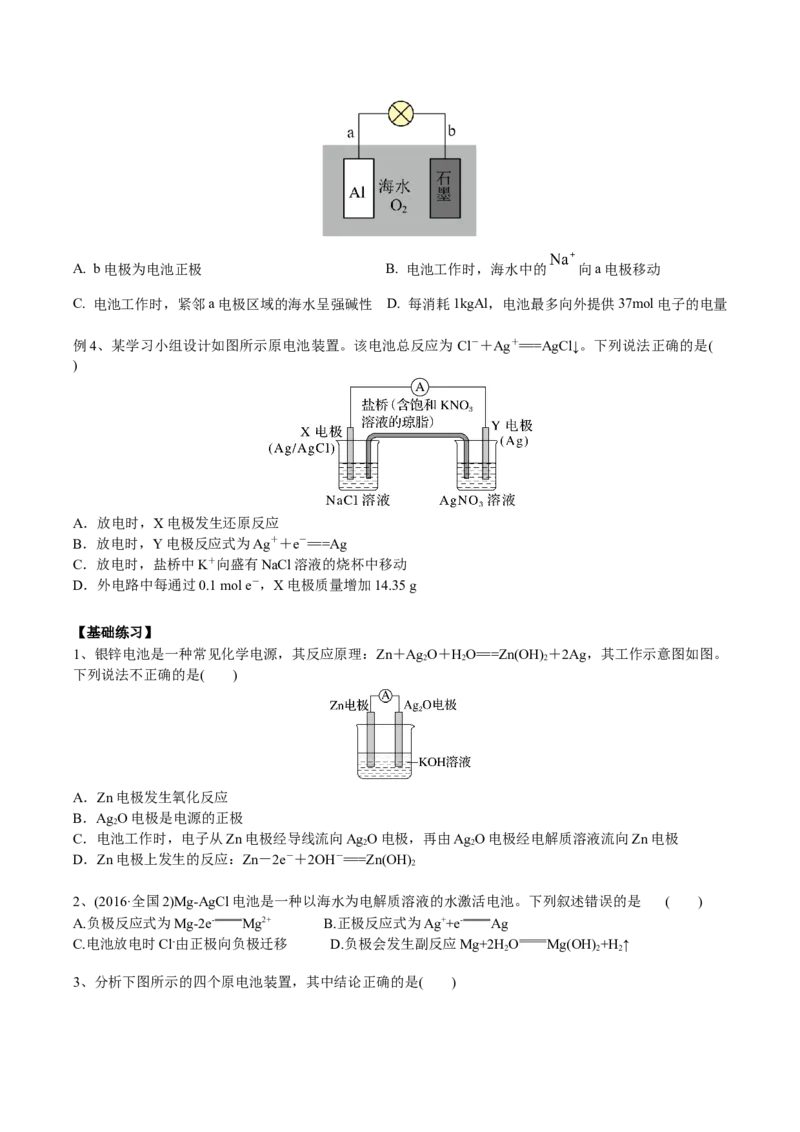
例3、(2023海南卷,8)利用金属Al、海水及其中的溶解氧可组成电池,如图所示。下列说法正确的是
( )A. b电极为电池正极 B. 电池工作时,海水中的 向a电极移动
C. 电池工作时,紧邻a电极区域的海水呈强碱性 D. 每消耗1kgAl,电池最多向外提供37mol电子的电量
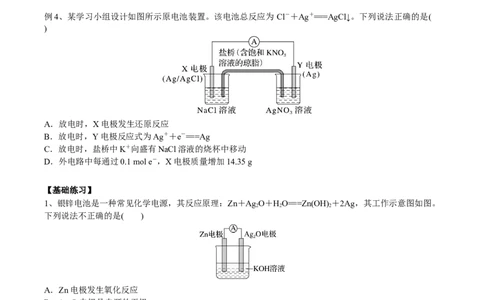
例4、某学习小组设计如图所示原电池装置。该电池总反应为 Cl-+Ag+===AgCl↓。下列说法正确的是(
)
A.放电时,X电极发生还原反应
B.放电时,Y电极反应式为Ag++e-===Ag
C.放电时,盐桥中K+向盛有NaCl溶液的烧杯中移动
D.外电路中每通过0.1 mol e-,X电极质量增加14.35 g
【基础练习】
1、银锌电池是一种常见化学电源,其反应原理:Zn+Ag O+HO===Zn(OH) +2Ag,其工作示意图如图。
2 2 2
下列说法不正确的是( )
A.Zn电极发生氧化反应
B.Ag O电极是电源的正极
2
C.电池工作时,电子从Zn电极经导线流向Ag O电极,再由Ag O电极经电解质溶液流向Zn电极
2 2
D.Zn电极上发生的反应:Zn-2e-+2OH-===Zn(OH)
2
2、(2016·全国2)Mg-AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是 ( )
A.负极反应式为Mg-2e- Mg2+ B.正极反应式为Ag++e- Ag
C.电池放电时Cl-由正极向负极迁移 D.负极会发生副反应Mg+2HO Mg(OH) +H ↑
2 2 2
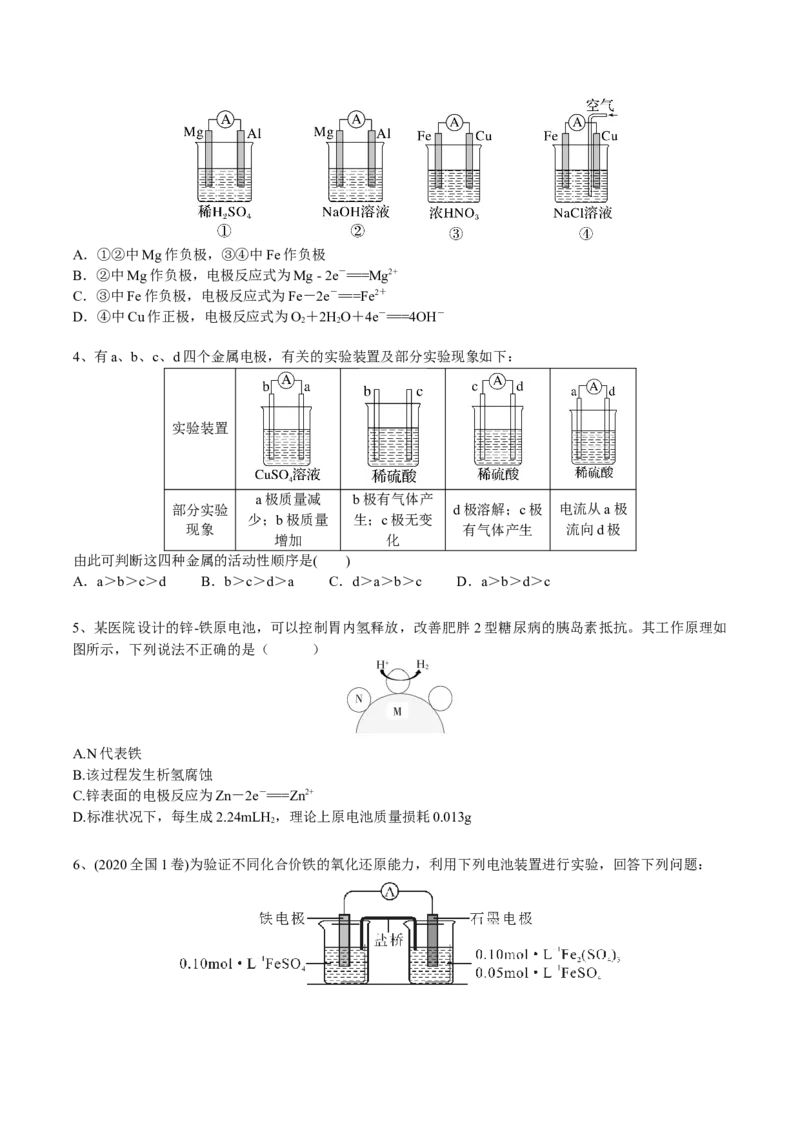
3、分析下图所示的四个原电池装置,其中结论正确的是( )A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作负极,电极反应式为Mg - 2e-===Mg2+
C.③中Fe作负极,电极反应式为Fe-2e-===Fe2+
D.④中Cu作正极,电极反应式为O+2HO+4e-===4OH-
2 2
4、有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验装置
a极质量减 b极有气体产
部分实验 d极溶解;c极 电流从a极
少;b极质量 生;c极无变
现象 有气体产生 流向d极
增加 化
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>d B.b>c>d>a C.d>a>b>c D.a>b>d>c
5、某医院设计的锌-铁原电池,可以控制胃内氢释放,改善肥胖2型糖尿病的胰岛素抵抗。其工作原理如
图所示,下列说法不正确的是( )
A.N代表铁
B.该过程发生析氢腐蚀
C.锌表面的电极反应为Zn-2e-===Zn2+
D.标准状况下,每生成2.24mLH,理论上原电池质量损耗0.013g
2
6、(2020全国1卷)为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验,回答下列问题:-1
(1)由 FeSO ·7H O 固体配制 0.10mol· L FeSO 溶液,需要的仪器有药匙、玻璃棒、
4 2 4
(从下列图中选择,写出名称。)
(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且
电迁移率( u )应尽可能地相近。根据下表数据,盐桥中应选择 作为电解质。
u 108 / m2 s1
阳离子 阴离子 u 108 / m2 s1 V1
V1
Li+ HCO -
4.07 3 4.61
Na+ NO -
5.19 3 7.40
Ca2+ Cl-
6.59 7.91
K+ SO 2-
7.62 4 8.27
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入 电极溶液中。
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+ )增加了0.02mol· L-1 。石墨电极上未见Fe 析出。可
知,石墨电极溶液中c(Fe2+ )= 。
(5)根据(3)(4)实验结果,可知石墨电极的电极反应式为 ,
铁电极的电极反应式为 。因此,验证
了Fe2+ 氧化性小于 ,还原小于 。
(6)实验前需要对铁电极表面活化。在FeSO 溶液中加入几滴Fe (SO ) 溶液,将铁电极浸泡一段时间,
4 2 4 3
铁电极表面被刻蚀活化。检验活化反应完成的方法是 。