文档内容
秘密★启用前
2014年初中毕业班十校联考质量检测
化学科试卷
说明:本试卷分为选择题和非选择题两部分,共8页,满分100分。考试时间80分钟。
注意事项:
1. 答卷前,考生务必在答题卡上用黑色字迹的钢笔或签字笔填写自己的考生号、姓名;再
用2B铅笔把对应考号的标号涂黑。
2. 选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号;不能答在试卷上。
3. 非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答卷上各题目指定区域内
的相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案,改动的答案也不能超出
指定的区域;不准使用铅笔、圆珠笔和涂改液。不按以上要求作答的答案无效。
4. 考生必须保持答题卡的整洁,考试结束时,将答题卡、答卷一并交回。
5. 全卷共三大题29小题,请考生检查题数。
可能用到的相对原子质量: H:1 C:12 O:16 S:32 Fe:56
第一部分 选择题 (共40分)
一.选择题(本题包括20小题,每小题只有一个选项符合题意.每小题2分,共40
分)
1、下列变化属于化学变化的是( )
A. 分离液态空气得到氧气 B. 铜片在酒精灯上加热变黑
C. 打开浓盐酸瓶盖时出现白雾 D. 水加热到沸腾,产生水蒸气
2、右图是元素X的原子结构示意图.下列说法正确的是( )
A. X属于非金属元素
B. 该原子的核外电子数为l3
C. X与Cl形成的化合物为XCl
D. 该原子最外电子层达到了稳定结构
3、化合物Ca (PO)(OH) 中,(PO)的化合价为( )
10 4 6 2 4
A.-1 B.+1 C. +3 D.-3
14、下列各图中“○”和“●”分别表示两种质子数不同的原子,下图所表示的四种物质中,
与另外三种不属于同一类别的物质是 ( )
5、下列图示实验操作正确的是( )
水 镊子
食盐水
pH试纸
浓硫酸
A.稀释浓硫酸 B.蒸发食盐水 C.测定溶液pH D.闻气体气味
6、炼铁高炉中发生了下列反应,其中属于化合反应的是( )
①焦炭充分燃烧 ②灼热的焦炭和二氧化碳反应
③高温煅烧石灰石 ④高温下一氧化碳将铁矿石还原为铁
A.①和② B.③和④ C.①和③ D.只有④
7、关于水电解实验的下列说法,正确的是( )
A. 水由氢气和氧气组成
B. 水由氢元素和氧元素组成
C. 电解水实验用的是交流电
D. 电解水实验中,正极析出的气体是氢气
8、将50g20%的氯酸钾溶液稀释到200g,稀释后所得溶液中的溶质质量分数是( )
A. 1% B. 5% C. 10% D. 20%
9、右图是物质间发生化学反应的颜色变化,其中X是( )
A. 稀硫酸 B. 氯化钠溶液 黄色溶液
C. 硫酸钠溶液 D. 澄清石灰水
Fe O
2 3
Fe CuO
浅绿色溶液 无色溶液X 蓝色溶液
石蕊试液
红色溶液
10、糖类是生命活动的重要供能物质,关于糖类中的淀粉化学式为(C H O),
6 10 5 n
下列说法正确的是( )
2A. (C H O) 属于无机化合物
6 10 5 n
B. (C H O) 的相对分子质量为162
6 10 5 n
C. 每个(C H O) 分子中,含有6n个碳原子
6 10 5 n
D. (C H O) 中碳、氢、氧三种元素的质量比为6:10:5
6 10 5 n
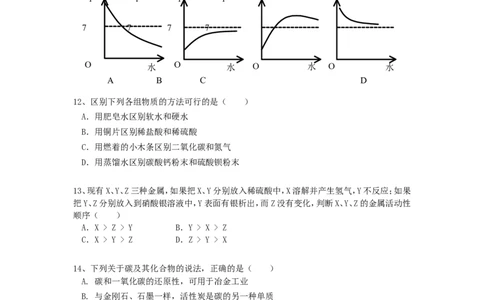
11、已知胃酸的主要成分是盐酸,胃液的正常pH范围是0.9-1.5,如果不断加水把胃液稀释,
则胃液的pH值与加水量关系图正确的是( )
pH pH pH pH
7 7 7 7
O 水 O 水 O 水 O 水
A B C D
12、区别下列各组物质的方法可行的是( )
A.用肥皂水区别软水和硬水
B.用铜片区别稀盐酸和稀硫酸
C.用燃着的小木条区别二氧化碳和氮气
D.用蒸馏水区别碳酸钙粉末和硫酸钡粉末
13、现有X、Y、Z三种金属,如果把X、Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应;如果
把Y、Z分别放入到硝酸银溶液中,Y表面有银析出,而Z没有变化,判断X、Y、Z的金属活动性
顺序( )
A.X > Z > Y B.Y > X > Z
C.X > Y > Z D.Z > Y > X
14、下列关于碳及其化合物的说法,正确的是( )
A. 碳和一氧化碳的还原性,可用于冶金工业
B. 与金刚石、石墨一样,活性炭是碳的另一种单质
C. 二氧化碳和一氧化碳都可以使动物死亡,所以都有毒性
D. CO 中混有少量的CO,可通过点燃混合气体的方法把CO转化为CO
2 2
15、中国第12届全国人民代表大会第2次会议于2013年3月5日开幕。今年冬季继续恶化
的细颗粒物“PM2.5”所产生的大气污染是会议的焦点之一。2012年2月,国务院发布了新
的《环境空气质量标准》,以下不属于“空气污染指数”需要监测污染物的是( )
A.二氧化碳 B.二氧化硫 C.一氧化碳 D.可吸入颗粒物
316、化学实验后我们要有清洗仪器的好习惯,以下清洗方法中,原理与另三种不同的是( )
A.用汽油除去衣服上的油污
B.内壁有碘的试管用酒精清洗
C.用水清洗蒸发皿中的少量食盐
D.内壁有植物油的试管用洗洁精清洗
17、羊城素有花城美誉,绿化向来是广州的标志之一,合理施肥和养护管理是城市绿化建设
的重要方面。以下不能作为氮肥施用的是( )。
A. Ca(PO) B.CO(NH) C.KNO D.NHHCO
3 4 2 2 2 3 4 3
18、根据《广州市城市生活垃圾分类管理暂行规定》第十一条,可回收垃圾主要包括废纸、塑
料、玻璃、金属和布料五大类,以下可回收垃圾中属于有机合成材料的是( )。
A.不锈钢 B.草稿纸 C.怡宝矿泉水瓶 D.羊毛衫
19、人们常用金属器皿来盛水,也常用铁、铝或铜制的水壶来烧水,说明这几种金属与热水是
不反应的,但金属钠却能与水发生以下反应:2Na + 2HO = 2R + H↑,而R是( )。
2 2
A. Na B. NaO C. NaO D. NaOH
2 2 2
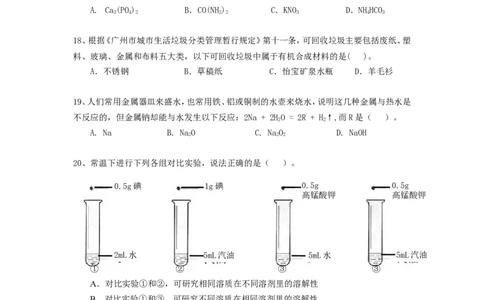
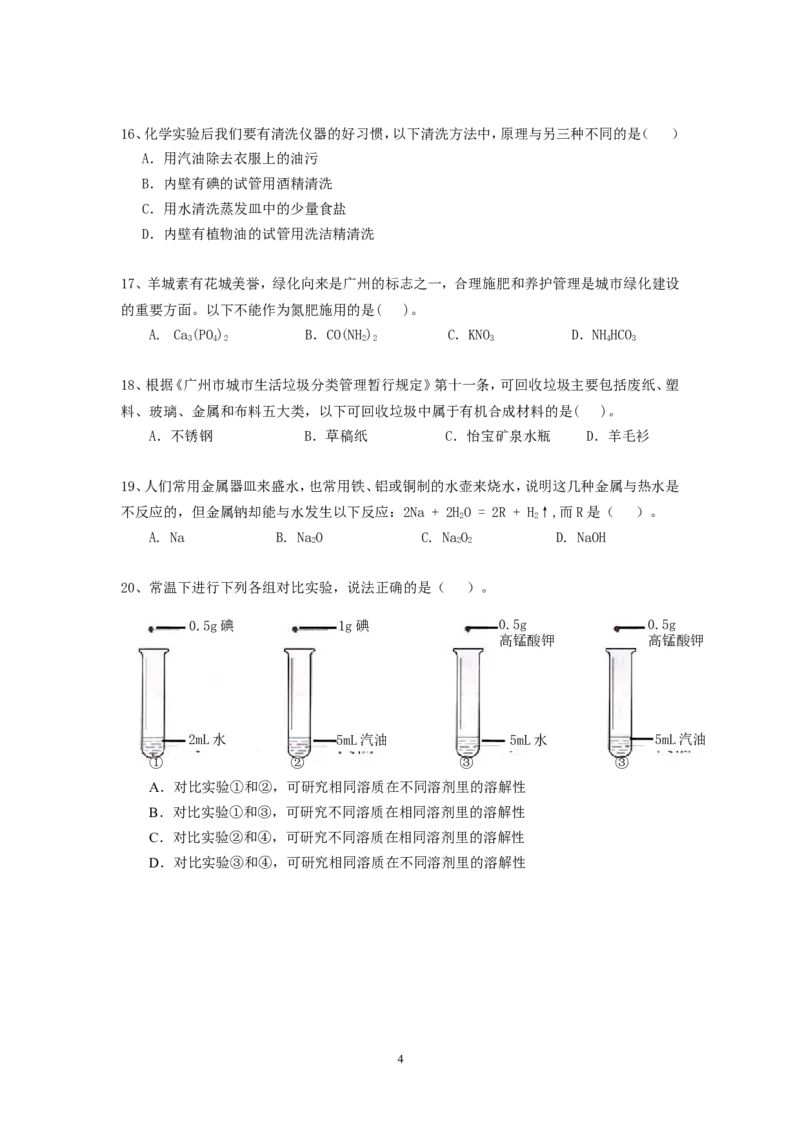
20、常温下进行下列各组对比实验,说法正确的是( )。
0.5g碘 1g碘 0.5g 0.5g
高锰酸钾 高锰酸钾
2mL水 5mL汽油 5mL水 5mL汽油
① ② ③ ③
A.对比实验①和②,可研究相同溶质在不同溶剂里的溶解性
B.对比实验①和③,可研究不同溶质在相同溶剂里的溶解性
C.对比实验②和④,可研究不同溶质在相同溶剂里的溶解性
D.对比实验③和④,可研究相同溶质在不同溶剂里的溶解性
4第二部分 非选择题 (共60分)
二.本题包括5小题,共29分
21、(3分)据澳大利亚媒体2013年8月13日报道,印度一名3个月大的男婴在出生后身体
已经4次自燃起火,印度一儿科称是罕见疾病“人体自燃症”,他皮肤毛孔中会分泌可燃气
体和液体,并建议其父母应尽量避免其在太阳下活动。
(1)结合燃烧的条件,分析要尽量避免其在太阳下活动的原因是:
。
(2)新近的一种解释是人体内可能存一种比原子还小的“燃粒子”,可以引起燃烧,
可见,这种“燃粒子”具有 性。
(3)结合所学知识,为保护好该婴儿,提出一条宝贵建议: 。
22、(10分)2014年3月8日在马来西亚吉隆坡国际机场起飞后失联的MH370是波音777。
飞机制造广泛采用新一代铝合金,同时在襟翼、扰流板、短舱和方向舵中采用碳复合材料。随
科技发展,飞机不再金属专制,碳复合材料占比已超金属。
飞机制造的部
(1)右图所示材料中不属于金属材料的是 分材料:
新型铝合金、
。
碳复合材料、
钛、钢和铝
(2)硬铝是铝、铜、镁、硅的合金,
常用于火箭、飞机、轮船等制造业,
则硬铝的强度和硬度比组成其纯金属的 (填“强”或“弱”)。
若把硬铝浸泡在稀盐酸中,观察到固体表面有气泡冒出,在所涉及的化学变化中,
用化学方程式表示出其中一个: 。
(3)不锈钢是生活中常用的合金,不锈钢的主要成分有铁、铬、镍。其中,铬常见化合价为
+3 、+6和+2,回答以下与金属铬(Cr)相关的问题。
①铬也可以形成化合价为+2价的氧化物,其化学式是 ,
其中+3价的氧化物化学式为Cr O,读作: 。
2 3
②CrO 是一种橙红色固体,将CrO 加热分解,发现固体逐渐变成绿色的Cr O,
3 3 2 3
同时产生一种能使带火星木条复燃的气体,其反应的化学方程式是 。
③CrCl 水溶液呈深绿色,它由深绿色难溶于水的氢氧化铬Cr(OH) 与盐酸作用制得。
3 3
写出上述制取CrCl 的化学方程式 ,
3
预测反应现象: 。
23、(8分)将下列各组中的两种溶液混合(溶液中的原有的水分子忽略不写):
5编号 反应物1 反应物2 混合后存在的粒子
A 稀盐酸(H+、Cl-) 氢氧化钾溶液(K+、OH-) K+、Cl-、HO
2
B Na+、SO 2-、Cu(OH)
4 2
C 氯化钠溶液(Na+、Cl-) 稀硫酸(H+、SO 2-) H+、SO 2- 、Na+、Cl-
4 4
(1)A组发生化学变化,化学方程式为 。
实质是反应物1中的 (填粒子符号,下同)与反应物2中的 结合形成 。
(2)B组发生化学变化,且B组反应物1是盐的水溶液,反应物2是碱的水溶液,
则B组中反应物1是 (填名称,下同),反应物2是 ;
(3)C组没有发生化学反应,原因是(微观角度解释): 。
24、(5分)煤、石油、天然气是化石燃料。
(1)石油属于 (填“纯净物”或“混合物”)
(2)天然气(主要成分CH)完全燃烧的方程式是 ;
4
(3) 煤是复杂的混合物,主要含有碳元素,还含有硫等元素,100t含硫4%的煤完全燃烧,会
向空气中排放 t二氧化硫。
25、(3分)地球上总储水量很大,但淡水很少,海水中溶解了很多物质,又苦又咸,除了含HO
2
外,还含有大量的Na+ 、Ca2+、Cl-、Mg2+、SO 2- 等。以海水为原料提取食盐的工艺流程如
4
下:
粗盐
海水 储水池 ① 结晶池
母液 多种化工产品
(1)图中①是 池(填“蒸发”或“冷却”)。
(2)根据海水晒盐的原理,下列说法中不正确的是 。
A. 得到的粗盐是纯净的氯化钠
B. 在①中,海水中水的质量逐渐减少
C. 在①中,海水中氯化钠的质量逐渐增加
D. 海水进入贮水池,海水的成分基本不变
(3)根据上述及工艺流程图,母液中所含的离子有 。
A. Ca2+、Mg2+、SO 2- 等 B. Na+ 、Ca2+、Cl-、Mg2+、SO 2-、HO等
4 4 2
C. Ca2+、Mg2+、SO 2- 、HO等 D. Na+ 、Ca2+、Cl-、Mg2+、SO 2-等
4 2 4
三.本题包括4小题,共31分
26、(7分) 下列是初中化学常见的实验或操作,回答下列问题:
6C+CuO
铁丝
澄清
石灰 火 氧
水 柴 气
A.量筒读数 B. 过滤 C.木炭还原氧化铜 D.铁丝在氧气中燃烧
(1)A实验中读出液体的体积是 mL。
(2) B实验中玻璃棒的作用是 。
(3)C实验中看到的实验现象: 。
(4)D实验中把铁丝盘成螺旋状的目的是 ,
铁丝燃烧的化学方程式 。
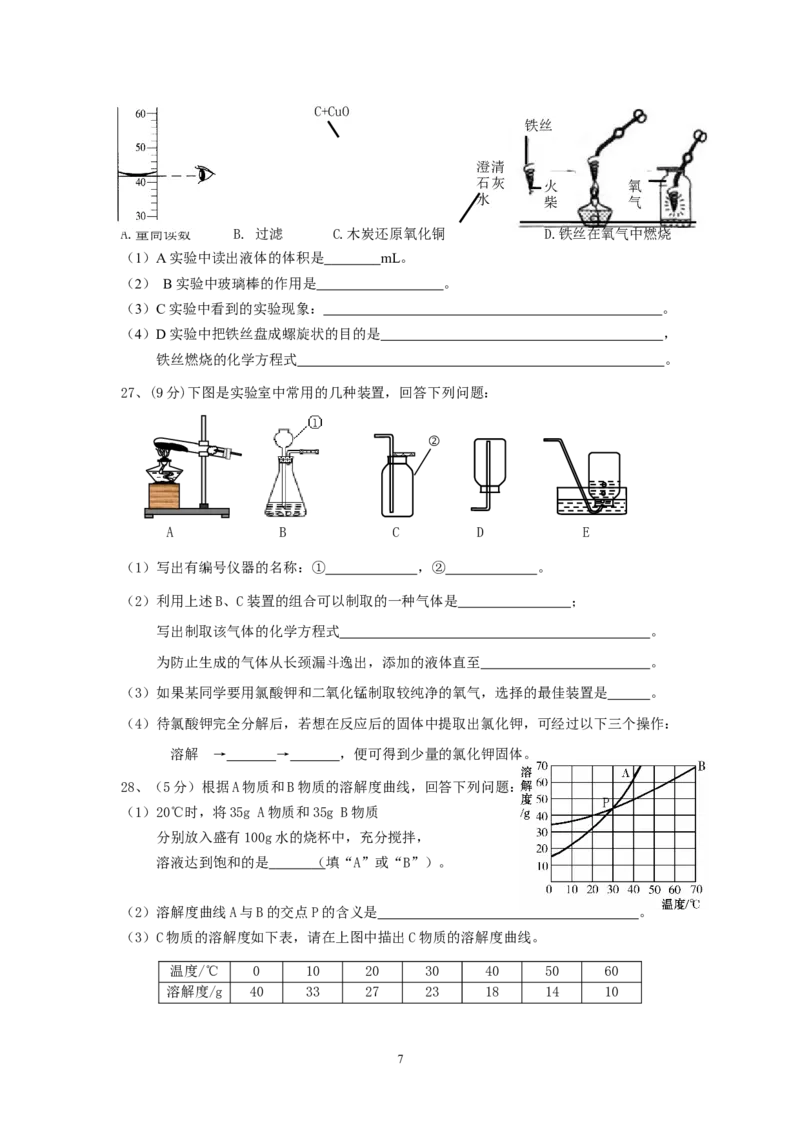
27、(9分)下图是实验室中常用的几种装置,回答下列问题:
②
A B C D E
(1)写出有编号仪器的名称:① ,② 。
(2)利用上述B、C装置的组合可以制取的一种气体是 ;
写出制取该气体的化学方程式 。
为防止生成的气体从长颈漏斗逸出,添加的液体直至 。
(3)如果某同学要用氯酸钾和二氧化锰制取较纯净的氧气,选择的最佳装置是 。
(4)待氯酸钾完全分解后,若想在反应后的固体中提取出氯化钾,可经过以下三个操作:
溶解 → → ,便可得到少量的氯化钾固体。
28、(5分)根据A物质和B物质的溶解度曲线,回答下列问题:
P
(1)20℃时,将35g A物质和35g B物质
分别放入盛有100g水的烧杯中,充分搅拌,
溶液达到饱和的是 ( 填“A”或“B”)。
(2)溶解度曲线A与B的交点P的含义是 。
(3)C物质的溶解度如下表,请在上图中描出C物质的溶解度曲线。
温度/℃ 0 10 20 30 40 50 60
溶解度/g 40 33 27 23 18 14 10
729、(10分)兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验:
(1)氢氧化钠固体要密封保存,原因有:
① ;② 。
【对固体猜想】
猜想一:全部是NaOH;猜想二:全部是NaCO;猜想三:是NaOH和NaCO 混合物
2 3 2 3
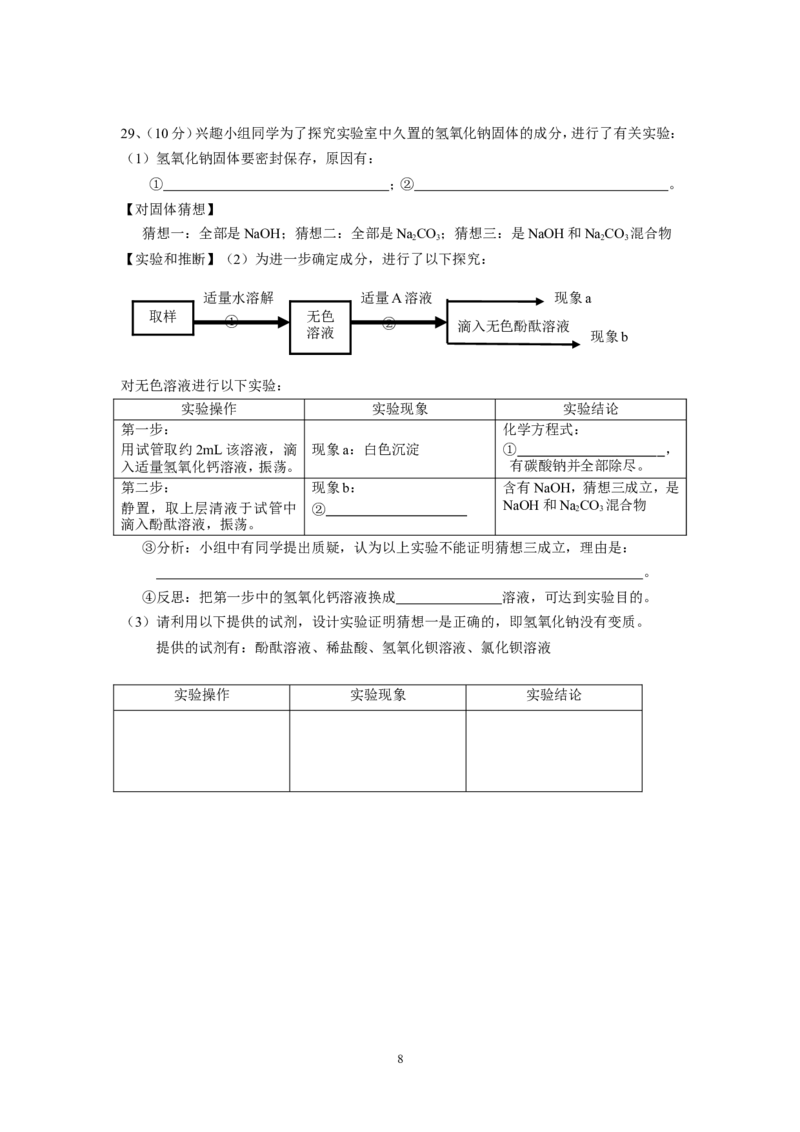
【实验和推断】(2)为进一步确定成分,进行了以下探究:
适量水溶解 适量A溶液 现象a
取样 无色
① ② 滴入无色酚酞溶液
溶液 现象b
对无色溶液进行以下实验:
实验操作 实验现象 实验结论
第一步: 化学方程式:
用试管取约2mL该溶液,滴 现象a:白色沉淀 ① ,
入适量氢氧化钙溶液,振荡。 有碳酸钠并全部除尽。
第二步: 现象b: 含有NaOH,猜想三成立,是
静置,取上层清液于试管中 ② NaOH和Na 2 CO 3 混合物
滴入酚酞溶液,振荡。
③分析:小组中有同学提出质疑,认为以上实验不能证明猜想三成立,理由是:
。
④反思:把第一步中的氢氧化钙溶液换成 溶液,可达到实验目的。
(3)请利用以下提供的试剂,设计实验证明猜想一是正确的,即氢氧化钠没有变质。
提供的试剂有:酚酞溶液、稀盐酸、氢氧化钡溶液、氯化钡溶液
实验操作 实验现象 实验结论
8秘密★启用前
2014年初中毕业班十校联考质量检测
化学科参考答案
一.选择题(每小题2分,共40分)
题号 1 2 3 4 5 6 7 8 9 10
答案 B B D A B A B B A C
题号 11 12 13 14 15 16 17 18 19 20
答案 B A C A A D A C D D
二.本题包括5小题,共29分
21、(3分)
(1)防止温度达到分泌物的着火点(1分)
(2)可燃(1分)
(3)远离火源(1分,答案不唯一,合理即可)
22、(12分)
(1)碳复合材料(1分)
(2)强(1分),
2Al+6HCl=AlCl+3H ↑或 Mg+2HCl=MgCl+H ↑或3Mg+2AlCl=3MgCl+2Al(2分)
3 2 2 2 3 2
(3)①CrO(1分),三氧化二铬(1分)。
△
② 4CrO = 2Cr O+3O↑(2分)。
3 2 3 2
③Cr(OH) + 3HCl = CrCl + 3HO(1分), 深绿色固体消失,液体呈深绿色(1分)。
3 3 2
23、(8分)
(1)HCl + KOH = KCl + HO(2分),H+ (1分),OH- (1分),HO(1分)。
2 2
(2)硫酸铜溶液(1分) ,氢氧化钠溶液(1分)。
(3)混合前后,溶液中的离子没有结合成新的分子(1分)
24、(5分)(1)混合物
点燃
(2) CH + 2O = 2HO + CO。 (2分) (3)8(2分)
4 2 2 2
25、(3分)
(1)蒸发(1分)。
(2)AC(1分)。 (3)D(1分)。
三.本题包括4小题,共31分
26、(7分)
(1)42 (1分) ,
9(2)引流(1分) 。
(3)黑色固体变红色,澄清石灰水中有气泡冒出,接着液体变浑浊(2分)。
(4)增大铁丝与氧气的接触面积(1分)
点燃
3Fe+2O =Fe O(2分)。
2 3 4
27、(9分)
(1)①长颈漏斗(1分),②集气瓶(1分)。
MnO
2
(2)CO(或O) (1分);CaCO+2HCl=CaCl+CO↑+HO或2HO=2HO+ O↑(2分)。
2 2 3 2 2 2 2 2 2 2
浸没长颈漏斗下端管口(1分)。
(3)AE (1分)。
(4)过滤 (1分), 蒸发 (1分) ,
28、(5分)
(1)A(1分)
(2)30℃时,AB两物质的溶解度相等(2分)
(3)图略(曲线1分,名称1分)
29、(10分)
(1)① 氢氧化钠固体易潮解 (1分) ;
② CO + 2NaOH = NaCO + HO或氢氧化钠与空气中二氧化碳反应变质(1分)。
2 2 3 2
(2)①NaCO+Ca(OH) = 2NaOH+ CaCO ↓(1分),
2 3 2 3
②液体变红(1分)
③第一步氢氧化钙溶液与碳酸钠溶液反应生成氢氧化钠,
干扰第二步氢氧化钠的检验(2分)
④氯化钙(或硝酸钙)(1分)
(3)(答案不唯一,合理即可)
实验操作 实验现象 实验结论
用试管取约 2mL 无色溶液 无明显现象(1分) 固体中没有碳酸钠,即猜想
(或取少量样品于试管中加 一正确(1分)
水溶解),滴入几滴氢氧化钡
溶液(或过量稀盐酸),振
荡。(1分)
10