文档内容
考点巩固卷 04 非金属及其化合物
考点一 碳、硅及无机非金属材料 分值:30分 建议用时:15分钟
一、选择题(每小题2分,共30分)
1.我国具有独立知识产权的电脑芯片“龙芯一号”的问世,填补了我国计算机制造史上的一项空白。下
列对硅及其化合物的有关叙述正确的是
A.二氧化硅既能与烧碱溶液反应又能与氢氟酸反应,所以二氧化硅是两性氧化物
B.晶体硅的化学性质不活泼,常温下不与任何物质发生反应
C.晶体硅是一种良好的半导体材料,但是它的提炼工艺复杂,价格极高
D.晶体硅和金刚石的硬度都很大
2.蕲春管窑镇被湖北省命名为“陶瓷之乡”,其管窑手工制陶技艺是湖北省第一批非物质文化遗产。下
列说法中错误的是
A.陶瓷的主要原料是黏土和石灰石
B.陶瓷烧制过程中发生了化学变化
C.新型超导陶瓷可应用于磁悬浮技术
D.高温结构陶瓷可应用于火箭发动机
3.硅的氧化物及硅酸盐构成了地壳中大部分的岩石、沙子和土壤。在无机非金属材料中,硅一直扮演着
主角。下面几种物质中含有硅单质的是
A B C D
玛瑙 光导纤维 太阳能电池板 水晶
A.A B.B C.C D.D
4.下列说法正确的是
A.因为HF与SiO 反应,故用氢氟酸在玻璃器皿上刻蚀标记
2B.下列转化在一定条件下能够实现:SiO SiCl Si
2 4
C.SiO 既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
2
D.Si和SiO 都用于制造光导纤维
2
5.有些科学家提出硅是“21世纪的能源”,下列说法正确的是
A.晶体硅具有半导体性质,可用于生产光导纤维
B.玻璃中含有的SiO 可与NaOH溶液反应,故常用NaOH溶液雕刻玻璃纹饰
2
C.碳化硅(SiC)俗称金刚砂,类似金刚石结构,是一种耐高温的半导体材料
D.陶瓷、水泥、石英玻璃都属于硅酸盐材料
6.光纤通信70年代后期发展起来的一种新型通信技术,目前长距离光纤通信系统已投入使用,光纤通信
的光学纤维是由下列哪种物质经特殊工艺制成的
A.碳 B.二氧化硅 C.锗 D.硅
7.以下对石墨烯的推测不正确的是
A.石墨烯性质稳定,不能在氧气中燃烧 B.石墨烯与石墨都具有导电性
C.石墨烯与金刚石互为同素异形体 D.石墨烯与石墨都具有较高的熔点
8.下列材料的特性及用途的说法中不正确的是
A.光导纤维传导光的能力很强,是非常好的通讯材料
B.氧化铝陶瓷具有两性,不可以用于制耐高温设备
C.氮化硅陶瓷耐高温且不易传热,可用来制造轴承
D.人造刚玉硬度高,可用来制造刚玉球磨机
9.制备硅单质时,主要化学反应如下:
①SiO (石英砂)+2C(焦炭) Si(粗硅)+2CO↑
2
②Si(粗硅)+2Cl SiCl
2 4
③SiCl +2H Si(纯硅)+4HCl
4 2
下列对上述三个反应的叙述中,不正确的是
A.①③为置换反应
B.①②③均为氧化还原反应C.②为化合反应
D.三个反应的反应物中硅元素均被还原
10.下列关于硅的说法不正确的是
A.硅是非金属元素,晶体硅是灰黑色有金属光泽的固体
B.硅的导电性能介于金属和绝缘体之间,是良好的半导体材料
C.硅的化学性质不活泼,常温下不与任何物质发生反应
D.加热到一定温度时,硅能与氯气、氧气等非金属单质反应
11.下列叙述正确的是
A.利用高纯硅可以制成光电池,将光能直接转化为电能
B.CO、CO 均易与血红蛋白结合而中毒
2
C.从SiO 制备高纯Si的过程反应中只涉及置换反应
2
D.SiO 和H O反应可直接制备H SiO
2 2 2 3
12.碳纳米管是由碳原子组成的六角形蜂巢状平面薄膜卷曲而成,具有许多异常的力学、电学和化学性
能。
下列关于碳纳米管的说法不正确的是
A.碳纳米管属于一种有机合成纤维
B.碳纳米管与金刚石互为同素异形体
C.常温下,碳纳米管具有较好的稳定性
D.碳纳米管比表面积大,可用作新型储氢材料
13.下列关于硅酸盐材料的说法错误的是
A.生活中常见的硅酸盐材料有玻璃、水泥、陶瓷
B.生产陶瓷的主要原料是黏土
C.普通玻璃的主要成分只有SiO
2
D.普通硅酸盐水泥的生产以石灰石和黏土为主要原料
14.下列关于 的叙述正确的是
① 能与水反应生成硅酸② 对应的水化物是可溶性弱酸
③硅原子和碳原子的最外层电子数相同, 和 的分子结构也相同
④ 既能与氢氧化钠溶液反应又能与氢氟酸反应,故 是两性氧化物
⑤ 中硅元素为 价,故 具有氧化性
⑥在 中,每个硅原子结合2个氧原子
A.①③⑤ B.①②④⑥ C.③ D.⑤
15.硅是组成无机非金属材料的一种主要元素,下列有关硅的化合物的叙述错误的是
A.氮化硅陶瓷是一种新型无机非金属材料,其化学式为
B.碳化硅( )的硬度大,熔点高,可用于制作高温结构陶瓷和轴承
C.光导纤维是一种新型无机非金属材料,其主要成分为
D.氮化硅( )、氧化铝( )、碳化硅( )和二氧化锆( )都可用作制高温结构陶瓷的材料
考点二 富集在海水中的元素——卤素 分值:40分 建议用时:20分钟
一、选择题(每小题2分,共28分)
1.下列关于HClO的性质叙述错误的是
A.HClO是一元弱酸 B.HClO不稳定,见光易分解
C.HClO具有强氧化性 D.HClO中氯元素的化合价为 价
2. 是一种重要的化工原料,下列叙述中正确的是
A.纯净的 在 中安静地燃烧,发出蓝色火焰
B. 通入冷的石灰乳中,制得漂白液
C. 能与水反应生成HClO和HCl,久置氯水的酸性变强
D.过量的Fe在 中燃烧,生成
3.漂白粉、“84”消毒液是生产生活中常用的消毒剂。下列说法中错误的是A.漂白粉是混合物,其有效成分是次氯酸钙
B.为了提高漂白粉的漂白效果,使用时可加少量盐酸
C.“84”消毒液和漂白粉的有效成分相同
D.漂白粉、“84”消毒液应置于阴凉处密封保存
4.下列关于卤素单质性质的说法错误的是
A.溴在常温下为液体,易挥发
B.碘在常温下为紫黑色固体,易挥发
C.溴可溶于水,更易溶于四氯化碳等有机溶剂中
D.碘蒸汽为紫色,碘水为棕黄色,碘的四氯化碳溶液呈紫红色
5.已知 性质与卤素相似,下列关于 的性质推测不合理的是
A. 属于化合物 B. 难溶于水
C. 具有强还原性 D.
6.实验室用如图装置制取、提纯、收集Cl 、尾气处理,不能达到实验目的的是
2
A.用装置甲制取Cl
2
B.用装置丙收集Cl
2
C.用装置丁吸收尾气中的Cl
2
D.用装置乙除去Cl 中的少量HCl
2
7.在新制氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质。下列实验现象和结论一致且正确的是
A.新制氯水呈浅黄绿色,且有刺激性气味,说明溶液中有 分子存在
B.用强光照射新制氯水一段时间后,溶液 增大,说明溶液中有 存在
C.将 加入新制氯水中,有无色气泡产生,说明溶液中有 存在
D. 溶液中滴加新制氯水,溶液变成棕黄色,说明新制氯水中有 存在
8.已知KMnO 与浓HCl在常温下反应能产生Cl 。若用如图所示的实验装置来制备纯净、干燥的氯气,并
4 2
试验它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是(不考虑①单元装置)
A.只有④处 B.只有②处 C.只有②和③处 D.②③④处
9.下列氯化物中,既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的是
A.CuCl B.FeCl C.FeCl D.AlCl
2 3 2 3
10.向盛有NaBr溶液的试管中加入少量氯水,振荡,再加入适量苯,振荡,静置。下列判断正确的是
选
A B C D
项
上 黄绿
橙红色 无色 无色
层 色
下
无色 无色 红棕色 黄绿色
层
A.A B.B C.C D.D
11.某化学小组探究卤族元素的性质,进行如图所示的实验( 均为浸有相应试液的棉花,夹持装置
略)。下列说法正确的是A.具支试管中发生反应的化学方程式为
B.若a处变为橙色,b处变为蓝色,说明非金属性
C.若c处褪色,说明 与 发生反应
D.若d处褪色,说明 具有漂白性
12.下列物质中,既含有氯分子,又含有氯离子的是
A.氯化钠溶液 B.新制氯水 C.漂白液 D.液氯
13.从淡化海水中提取溴的流程如下:
下列有关说法不正确的是
A.X试剂可用Na SO 饱和溶液
2 3
B.步骤Ⅲ的离子反应:
C.工业上每获得1molBr ,需要消耗Cl 22.4L
2 2
D.步骤Ⅳ包含萃取、分液和蒸馏
14.向 和 的混合溶液中通入氯气至恰好完全反应, 的物质的量的变化如下图所示。
下列说法正确的是A.还原性:
B.通入氯气的总量为5mol
C.若反应过程中滴入KSCN溶液,呈血红色,则
D.c点时加入过量NaOH溶液,反应后溶液中只含 四种离子
二、实验题(12分)
15.海洋蕴藏着中极为丰富的化学资源,如海水中就有80多种元素,所含的盐大部分是氯化钠。十九世纪
末工业上开始通过电解饱和食盐水的方法制备氯气、氨气和烧碱,并以它们为原料生产一系列含氯、含钠
产品(氯碱工业),请回答下列问题:
(1)天原化工厂是我国最早的氯碱企业,其创始人是______(单选)
A.侯德榜 B.吴蕴初 C.荣毅仁 D.戴安邦
(2)电解饱和食盐水时,与电源正极相连的电极叫阳极,阳极产物是氯气,可以用______检验,现象为
______,写出检验氯气的离子方程式_____________________
(3)工业上用氯气与消石灰制成漂白粉,漂白粉的有效成分为______(单选)
A. B. C. D.
(4)新制氧水呈浅黄绿色,是因为氯水中存在______(单选)
A. B. C. D.
(5)有两组学生根据不同的反应原理在实验室制取氯气。①请按要求填表。
实验
实验原理 发生装置(填编号)
组
第一
__________
组
第二
__________
组
②有同学建议第一组使用图所示装置作为氯气的发生装置,请谈谈你的看法______。
考点三 硫及其重要化合物 分值:40分 建议用时:20分钟
一、选择题(每小题2分,共24分)
1.下列污染现象主要与SO 有关的是
2
A.臭氧层空洞 B.光化学烟雾 C.酸雨 D.温室效应
2.下列反应中,硫酸既表现了氧化性又表现了酸性的是
A.2H SO (浓)+Cu CuSO +2H O+SO ↑ B.2H SO (浓)+C CO ↑+2H O+2SO ↑
2 4 4 2 2 2 4 2 2 2
C.H SO (浓)+NaNO NaHSO +HNO ↑ D.H SO +Na SO =Na SO +H O+SO ↑
2 4 3 4 3 2 4 2 3 2 4 2 2
3.探究铜和浓硫酸的反应,下列装置或操作错误的是A.上下移动装置甲中的铜丝体现绿色化学的思想
B.装置乙可用于收集 气体
C.将试管中的液体倒入装置丙中稀释,观察颜色可确定 的生成
D.利用装置丁将硫酸铜溶液加热浓缩、冷却结晶,可析出
4.下列物质能使品红溶液褪色,且褪色原理基本相同的是:①活性炭②新制氯水③二氧化硫④臭氧⑤过
氧化钠⑥过氧化氢溶液
A.①②④ B.②③⑤ C.②④⑤⑥ D.③④⑥
5.某无色溶液中加入氯化钡溶液有白色沉淀,再加稀盐酸沉淀不消失,则下列判断正确的是
A.一定有SO B.一定有CO C.一定有Ag+ D.一定有SO 或Ag+
6.查看葡萄酒标签上的成分信息时,常发现其成分中含有少量SO 。下列关于SO 说法正确的是
2 2
A.SO 具有还原性,不能用浓硫酸干燥
2
B.SO 不能作食品添加剂,不该添加到葡萄酒中
2
C.SO 具有还原性,少量的SO 可防止葡萄酒氧化变质
2 2
D.SO 可以使酸性 KMnO 溶液褪色,体现了它的漂白性
2 4
7.下列说法中正确的是
A.根据化合价可知,S在化学反应中只能作还原剂
B.试管内壁上的硫黄可用CS 清洗
2
C.S+O SO ,S被氧化,作氧化剂
2 2
D.硫只以化合态存在于自然界中
8.在硫酸的工业制法中,下列生产操作与说明生产操作的主要原因二者都正确的是
A.硫铁矿煅烧前要粉碎,因为大块硫铁矿不能燃烧B.从沸腾炉出来的气体只有SO
2
C.SO 氧化成SO ,SO 能全部转化为SO
2 3 2 3
D.SO 用98.3%的浓H SO 吸收,目的是防止形成酸雾,以便使SO 吸收更充分
3 2 4 3
9.下列制取SO 、验证其漂白性、收集并进行尾气处理的装置和原理能达到实验目的的是
2
甲 乙 丙 丁
A.用装置甲制取SO B.用装置乙验证SO 的漂白性
2 2
C.用装置丙收集SO D.用装置丁处理实验中的尾气
2
10.能正确表示下列反应的离子方程式的是
A.向澄清的石灰水中通入SO 气体: +SO =CaSO ↓
2 2 3
B.过量SO 气体通入氢氧化钠溶液中:SO +OH-=HSO
2 2
C.SO 气体通入溴水中:SO +Br +H O=2H++2Br-+SO
2 2 2 2
D.向氢硫酸(H S)中通入氯气:
2
11.下列说法正确的是
A.向HClO溶液中通入SO ,生成H SO ,证明H SO 的酸性比HClO强
2 2 4 2 4
B.SO 、H S为含硫化合物,都可用浓硫酸干燥
2 2
C.将SO 通入品红溶液,溶液褪色后加热恢复原色
2
D.蔗糖遇浓H SO 后变黑,膨胀,最后产生刺激性气味气体,说明浓H SO 具有脱水性、酸性和强氧化性
2 4 2 4
12.下列关于浓硫酸的叙述中,正确的是
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
C.把水加入浓硫酸中可稀释浓硫酸
D.浓硫酸在常温下能够使铁、铝等金属形成氧化膜而钝化
13.为了除去二氧化碳气体中的二氧化硫气体,下列仪器和药品组合合理的是仪器:①洗气瓶、②干燥管;
药品:③固态生石灰、④苏打溶液、⑤饱和小苏打溶液。
A.①⑤ B.②⑤ C.①③ D.①④
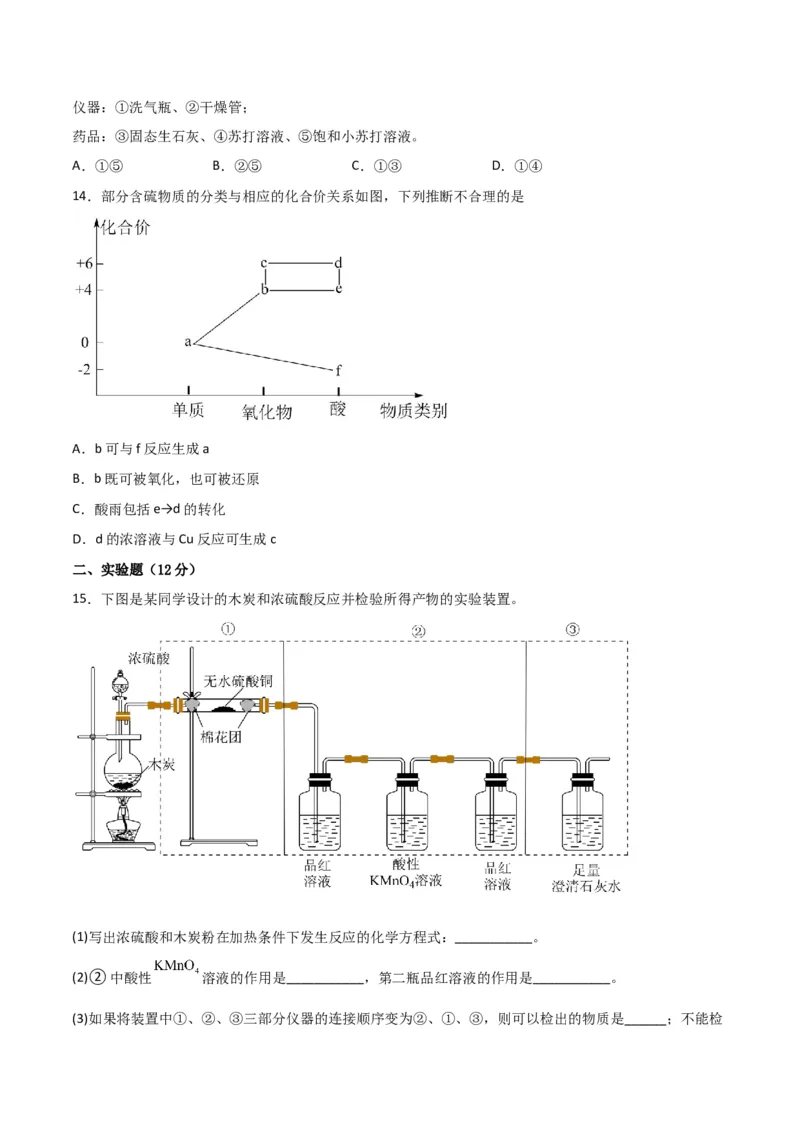
14.部分含硫物质的分类与相应的化合价关系如图,下列推断不合理的是
A.b可与f反应生成a
B.b既可被氧化,也可被还原
C.酸雨包括e→d的转化
D.d的浓溶液与Cu反应可生成c
二、实验题(12分)
15.下图是某同学设计的木炭和浓硫酸反应并检验所得产物的实验装置。
(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:___________。
(2)②中酸性 溶液的作用是___________,第二瓶品红溶液的作用是___________。
(3)如果将装置中①、②、③三部分仪器的连接顺序变为②、①、③,则可以检出的物质是______;不能检出的物质是________。
(4)如果将仪器的连接顺序变为①、③、②,则可以检出的物质是___________;不能检出的物质是
___________。
(5)有同学希望通过测量③中装置质量的增加来计算反应的木炭的质量,则在②③之间插入一个洗气瓶,其
中装___________(填写试剂名称)。
考点四 氮及其重要化合物 分值:40分 建议用时:20分钟
一、选择题(每小题2分,共24分)
1.下列反应属于氮的固定作用的是
A.NH 与氯化氢反应 B.硝酸工厂用NH 氧化制取NO
3 3
C.雷雨时空气中的N 转化为NO D.由NH 制碳酸氢铵和硫酸铵
2 3
2. 是重要的化工原料,工业上常采用氨氧化法制硝酸,其流程是将氨和空气混合后通入灼热的铂铑
合金网,反应生成 ,生成的一氧化氮与残余的氧气继续反应生成二氧化氮:
。随后将二氧化氨通入水中制取硝酸。在指定条件下,下列
选项所示的物质间转化能实现的是
A. B.稀
C. D.
3.下列关于氮的氧化物的叙述正确的是
A.氮的氧化物只有NO、NO
2
B.氮的氧化物均为红棕色气体
C.氮的氧化物均有毒
D.氮的氧化物在空气中能稳定存在
4.检验铵盐的方法是将待检物取出少量放入试管中,然后
A.加热,用湿润的红色石蕊试纸放在试管口检验
B.加水溶解,用红色石蕊试纸检验溶液的酸碱性
C.加入碱溶液,加热,再滴入酚酞试液
D.加入苛性钠溶液,加热,用湿润的红色石蕊试纸放在试管口检验
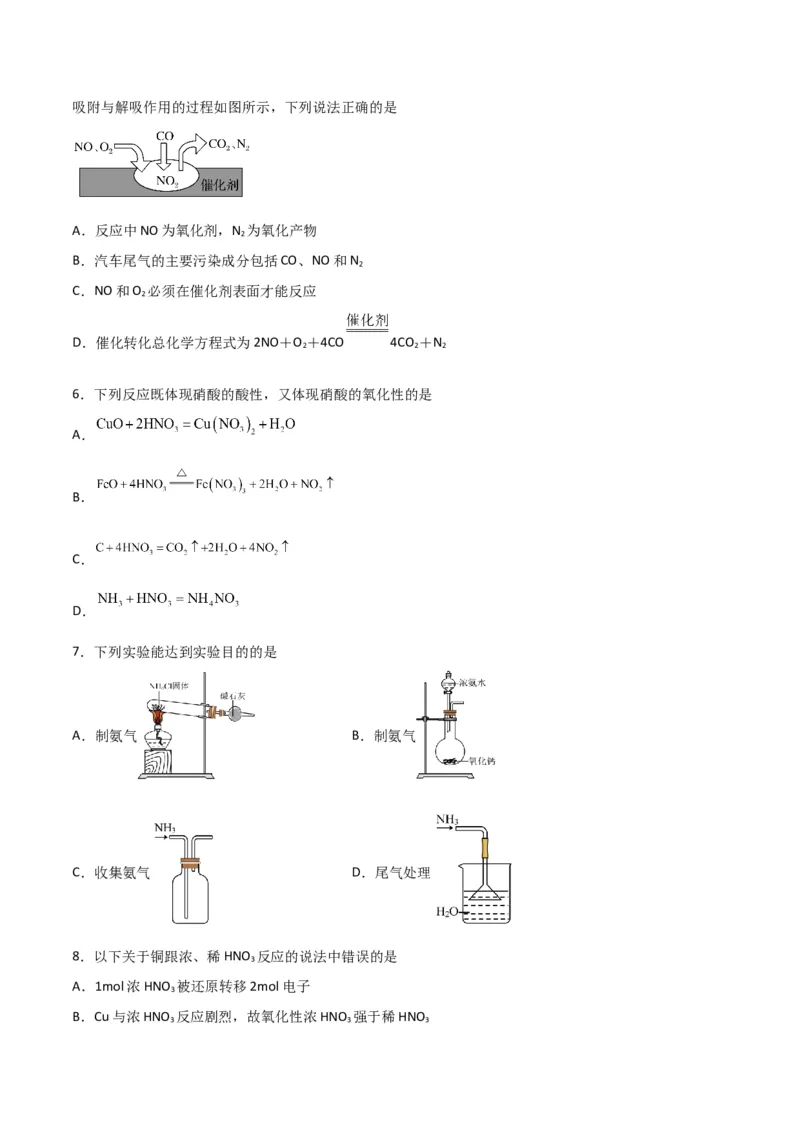
5.随着我国汽车年销量的大幅增加,空气环境受到了很大的污染。汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是
A.反应中NO为氧化剂,N 为氧化产物
2
B.汽车尾气的主要污染成分包括CO、NO和N
2
C.NO和O 必须在催化剂表面才能反应
2
D.催化转化总化学方程式为2NO+O +4CO 4CO +N
2 2 2
6.下列反应既体现硝酸的酸性,又体现硝酸的氧化性的是
A.
B.
C.
D.
7.下列实验能达到实验目的的是
A.制氨气 B.制氨气
C.收集氨气 D.尾气处理
8.以下关于铜跟浓、稀HNO 反应的说法中错误的是
3
A.1mol浓HNO 被还原转移2mol电子
3
B.Cu与浓HNO 反应剧烈,故氧化性浓HNO 强于稀HNO
3 3 3C.Cu与浓、稀HNO 反应都不需加热
3
D.生成等量的Cu(NO ) ,消耗浓HNO 的量多
3 2 3
9.在NO 被水吸收的反应中,发生还原反应和氧化反应的物质的量比为
2
A.3:1 B.1:3 C.1:2 D.2:1
10.硝酸与铜反应实验装置如图所示,下列有关叙述不正确的是
A.浓硝酸呈黄色是因溶有其分解产生的
B.用稀硝酸实验时试管上方气体略有红棕色
C.用浓硝酸实验时溶液呈绿色是因溶有
D.反应中浓硝酸较稀硝酸反应更剧烈、氧化性更强
11.下列事实不能说明浓硝酸氧化性比稀硝酸强的是
A.浓硝酸遇石蕊试液变红后褪色,稀硝酸遇石蕊试液只变红不褪色
B.浓硝酸能与NO反应生成NO ,而稀硝酸不能与NO反应
2
C.浓硝酸在加热条件下可与碳单质反应,而稀硝酸则不能
D.足量的铜还原1mol浓硝酸和1mol稀硝酸转移电子数分别为N 和3N
A A
12.如图装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液。挤压滴管的胶头,然后打开止
水夹。下列与实验事实不相符的是
A.Cl (饱和食盐水)无色喷泉 B.NH (H O含石蕊)蓝色喷泉
2 3 2C.HCl(H O含石蕊)红色喷泉 D.SO (NaOH溶液)无色喷泉
2 2
13.自然界的氮循环包括以下过程。下列说法中,不正确的是
A.硝化过程中,含氮物质被氧化
B.氨氧化过程中,亚硝态氮元素与铵态氮元素理论物质的量之比为3:4
C.N → 属于氮的固定,N 发生还原反应
2 2
D.土壤中Fe2+和Fe3+的存在有利于从与其接触的水体中除去氮元素
14.将2.56 g Cu和一定量的浓HNO 反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反
3
应完全时,共收集到气体1.12 L(已折算为标准状况),则反应中消耗HNO 的物质的量为
3
A.0.05 mol B.1 mol C.1.05 mol D.0.13 mol
二、实验题(12分)
15.氮的氧化物 是大气污染物之一,工业上在一定温度和催化剂条件下用 将 还原生成 。
在实验室利用如图装置探究 能否被 还原。
(1)A装置中盛放浓氨水的仪器名称是___________,D装置中盛放无水氯化钙的仪器名称是_______。
(2)试剂甲是 ___________,D中无水氯化钙的作用是___________。
(3)E装置中发生反应的离子方程式是___________。
(4)在一定温度和催化剂条件下,若 能够被 还原,发生的化学方程式 ___________,还可以在空气中使用具有碱性的 溶液来吸收 ,相关反应的化学方程式是___________。
(5)此实验装置存在一个明显的缺陷是___________。