文档内容
解密 02 化学常用计量
考点热度 ★★★★★
【考纲导向】
1.了解物质的量(n)及其单位摩尔(mol)、摩尔质量(M)、气体摩尔体积(V )、阿伏加德罗常数
m
(N )、物质的量浓度(c)的含义。
A
2.能根据微粒(原子、分子、离子)的物质的量、数目、气体体积(标准状况下)之间的相互关系进行有关计
算。
3.掌握配制一定溶质质量分数溶液和物质的量浓度的方法。
4.理解溶液中溶质的质量分数和物质的量浓度的概念,并能进行有关计算。
【命题分析】
1.阿伏加德罗常数(N )是高考的高频考点,主要以选择题的形式出现,着重考查物质的组成、结构、性质
A
等知识以及以物质的量为中心的相关计算,题目的落脚点往往以判断分子、原子、离子、电子等微粒数目
为主。
2.Ⅰ卷常与N 相结合进行简单计算的考查,Ⅱ卷主要以填空题形式考查物质含量与组成,有时对计算过
A
程有要求。命题时主要有混合物成分含量的确定,未知物化学式的确定,根据化学方程式的计算,多步连
续反应的计算等。2023年高考仍会围绕阿伏加德罗常数、气体摩尔体积设置知识陷阱,同时又隐含对物质
结构、氧化还原反应、电离、水解等知识的考查。核心考点一 有关N 的正误判断
A
一、与N 相关的命题主要围绕以下四个方面进行
A
解答此类题目应注重看清所求微粒的种类、分子的构成(是单原子分子还是双原子分子或多原子分子)以及
微粒中的质子数、中子数、电子数等。
如:常温常压下,14 g由N 和CO组成的混合气体中所含有的原子数目为N
2 A
提醒:由于二者的摩尔质量相等,所以二者无论以何种比例混合都不影响分子总数,故这一说法是正确的。
2.由体积求微粒的数目,主要应用N=·N 计算
A
解题时要注意:
(1)若题目给出物质的体积,一要看是否是标准状况,二要看物质在标准状况下是不是气体,若不是气体则
无法求其物质的量。标准状况下不是气体的物质:HF(液态)、SO (固态)、HO、乙醇、CCl 、苯、己烷、
3 2 4
CHCl (液态)。
3
(2)若题目给出气体的质量或物质的量,则微粒数目与外界条件无关。
(3)注意某些物质分子中的原子个数,例如:稀有气体为单原子分子、臭氧(O )为三原子分子、白磷(P )为四
3 4
原子分子。
3.由物质的量浓度求微粒的数目,主要应用N=c·V·N 计算
A
这类题目一般会和弱电解质的电离、盐类的水解等知识联系在一起,解题时要注意对“隐含条件”的挖掘。
如1 L 0.1 mol·L-1 NaHCO 溶液中含HCO的数目小于0.1 N 。
3 A
4.氧化还原反应中转移电子数目的计算
依据题目提供的反应,抓住氧化还原反应的实质,运用得失电子数规律,计算得失电子的数目。如 1 mol
Fe与足量稀HNO 反应,转移电子数目是3N 而不是2N 。
3 A A
二、常见三种组成类型溶液的配制方法
(1)体积比浓度溶液配制:
将浓溶液或纯液体溶质和水按体积比用量筒量取,然后在烧杯中混合即可,所需仪器:量筒、烧杯、玻璃
棒;
(2)质量百分比浓度溶液配制:
称取一定质量固体溶质或用量筒量取一定体积浓溶液或纯液体溶质,用量筒量取所需体积的水,在烧杯中
混合溶解即可。所需仪器:量筒、烧杯、玻璃棒、托盘天平(溶质为固体);
(3)一定物质的量浓度溶液的配制:
①配制步骤简要概括为:算—称—溶—移—洗—荡—定—摇。
②数据的处理及要求
数据 要求或解释
药品的 托盘天平称量固体药品,只能精确到0.1 g,记录数据时只能保留小数点后一位
质量 数字,如14.6 g,不能写为14.60 g
a.选择容量瓶时应该与所配溶液体积相等或稍大。如需配制 480 mL某溶液,应
容量瓶
选择500 mL容量瓶;
的规格
b.回答仪器容量瓶名称时同时应该注明其规格,如“500 mL容量瓶”,不能只回答“容量瓶”
考法1 有关N 的正误判断(题型预测:选择题)
A
1.(2022·全国卷) 为阿伏加德罗常数的值,下列说法正确的是
A.25℃, 下, 氢气中质子的数目为
B. 溶液中, 的数目为
C. 苯甲酸完全燃烧,生成 的数目为
D.电解熔融 ,阴极增重 ,外电路中通过电子的数目为
【答案】C
【解析】A.25℃、101kPa不是标准状况,不能用标况下的气体摩尔体积计算氢气的物质的量,故A错误;
B.Al3+在溶液中会发生水解生成Al(OH) ,因此2.0L 1.0 mol/L的AlCl 溶液中Al3+数目小于2.0N ,故B错
3 3 A
误;
C.苯甲酸燃烧的化学方程式为 ,1mol苯甲酸燃烧生成7molCO ,则
2
0.2mol苯甲酸完全燃烧生成1.4molCO,数目为1.4N ,故C正确;
2 A
D.电解熔融CuCl 时,阳极反应为 ,阴极反应为 ,阴极增加的重量为Cu的质
2
量,6.4gCu的物质的量为0.1mol,根据阴极反应可知,外电路中通过电子的物质的量为0.2mol,数目为
0.2N ,故D错误;
A
答案选C。
2.(2022·河北卷)N 是阿伏加德罗常数的值。下列说法正确的是
A
A.3.9gNa O 与足量水反应,转移电子个数为0.1N
2 2 A
B.1.2gMg在空气中燃烧生成MgO和MgN,转移电子个数为0.1N
3 2 A
C.2.7gAl与足量NaOH溶液反应,生成H 的个数为0.1N
2 A
D.6.0gSiO 与足量NaOH溶液反应,所得溶液中SiO 的个数为0.1N
2 A【答案】B
【解析】A.过氧化钠与水反应生成氢氧化钠和氧气,则3.9g过氧化钠与足量水反应,转移电子个数为
×1×N mol-1=0.05N ,故A错误;
A A
B.镁在空气中燃烧无论生成氧化镁,还是氮化镁,镁均转化为镁离子,则1.2gMg在空气中燃烧生成氧化
镁和氮化镁时,转移电子个数为 ×2×N mol-1=0.1N ,故B正确;
A A
C.铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,则2.7g铝与足量氢氧化钠溶液反应生成氢气的个数为
× ×N mol-1=0.15N ,故C错误;
A A
D.二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,硅酸钠在溶液中发生水解反应,则由原子个数守恒可
知,6.0g二氧化硅与足量氢氧化钠溶液反应所得溶液中硅酸根离子的个数小于 ×N mol-1=0.1N ,故
A A
D错误;
故选B。
考法2 物质的量浓度及误差分析(题型预测:选择题)
3.(2022·黑龙江哈尔滨·高三学业考试)下列实验误差分析不正确的是
A.配制一定物质的量浓度的溶液定容时俯视容量瓶刻度线,所配溶液浓度偏大
B.用湿润的pH试纸测某酸雨样品的pH,所测pH数值偏大
C.测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏低
D.滴定前滴定管尖嘴内有气泡,终点读数时气泡消失,所测体积偏小
【答案】D
【解析】A.配制一定物质的量浓度的溶液定容时俯视容量瓶刻度线,导致读数偏大,溶液体积偏小,所
配溶液浓度偏大,A正确;
B.用湿润的pH试纸测某酸雨样品的pH,雨水溶液变小,酸性变弱,所测pH数值偏大,B正确;
C.测定中和反应的反应热时,将碱缓慢倒入酸中,导致损失热量,所测温度值偏低,C正确;
D.滴定前滴定管尖嘴内有气泡,终点读数时气泡消失,导致滴定液用量偏大,所测体积偏大,D错误;
故选D。一、阿伏加德罗常数应用时的“六注意”
1.注意气体摩尔体积的适用条件及物质的状态
一要看是否为标准状况下;二要看物质在标准状况下是否为气态,如 CCl 、水、液溴、SO 、己烷、苯等
4 3
是非气体。
2.注意与计算无关的一些干扰条件
给出非标准状况下气体的物质的量或质量,干扰判断,实质上,此时物质所含的粒子数与温度、压强等外
界条件无关。
3.注意物质的组成与结构
(1)特殊物质中所含微粒(分子、原子、电子、质子、中子等)的数目,如Ne、DO、18O、O、P、H37Cl等。
2 2 3 4
(2)物质中所含化学键的数目,如SiO、CO、C H 等。
2 2 n 2n+2
(3)最简式相同的物质中的微粒数目,如NO 和NO、乙烯和丙烯、(O 和O)等
2 2 4 2 3
4.注意难电离、易水解的粒子数目
一看是否有弱电解质的电离;二看是否有弱离子的水解;三看是否指明了溶液的体积;弱电解质在水溶液
中部分电离,可水解盐溶液中离子发生微弱水解,都会导致粒子数目减少。
5.注意电子转移(得失)数目
一要注意是否发生歧化反应,二要注意变价元素,三要注意过量问题,
反应 参考物质 转移电子的物质的量或电子数目
NaO+CO 1 mol Na O 1 mol或N
2 2 2 2 2 A
(或HO) 1 mol O 2 mol或2N
2 2 A
Cl+NaOH 1 mol Cl 1 mol或N
2 2 A
1 mol Cl 2 mol或2N
2 A
Cl+Fe
2
1 mol Fe 3 mol或3N
A
6.注意一些特殊条件
一要注意一些特殊的反应,如NO和O 不需要条件即可反应,NO 和NO 之间存在相互转化,合成氨反应
2 2 2 4
等属于可逆反应;二要注意特殊的物质,如摩尔质量相同或成整数倍的关系的物质:N 和CO、C H ;
2 2 4
NaS和NaO;CaCO 与KHCO ;NaHCO 与MgCO ;Cu S和CuO;NO 与NO。
2 2 2 3 3 3 3 2 2 2 4
二、一定物质的量浓度溶液配制的常考点分析
1.配制一定物质的量浓度的溶液,填写缺少的仪器
一般从以下三种仪器中选择:容量瓶、胶头滴管、玻璃棒,填写时一定要注明容量瓶的规格。
2.误差分析的来源
(1)导致c 偏低的错误操作:垫滤纸称量NaOH固体;左码右物(用游码);称量时间过长(潮解);洗涤或转
B
移时溶液溅出;未洗涤烧杯及玻璃棒;超过刻度时用滴管吸出液体;定容时仰视;定容后发现液面低于刻
度线再加水。
(2)导致c 偏高的错误操作:砝码生锈;定容时俯视;未等溶液冷却至室温就定容。
B
(3)定容时俯视、仰视对结果的影响:务必确保按眼睛视线→刻度线→凹液面最低点的顺序,做到“三点一线”。
①仰视刻度线(图1),导致溶液体积偏大。
②俯视刻度线(图2),导致溶液体积偏小。
变式1 考查气体的摩尔体积
1.(2022·河北·邢台市第二中学高三阶段练习)下列说法正确的是
①标准状况下,6.02×1023个分子所占的体积约是22.4L
②0.5 mol H 所占体积为11.2 L
2
③标准状况下,1 mol HO的体积为22.4 L
2
④标准状况下,28 g CO与N 混合气体的体积约为22.4 L
2
⑤各种气体的气体摩尔体积都约为22.4 L/mol
⑥标准状况下,体积相同的气体的分子数相同
A.①②⑤ B.④⑥ C.③④⑥ D.①④⑥
【答案】B
【解析】①标准状况下,6.02×1023个分子为1mol,但该物质不一定是气体,故所占的体积不一定是
22.4L,错误;
②0.5 mol H 所处的状态不一定是标准状况,气体摩尔体积不一定是22.4L/mol,所占体积不一定是11.2
2
L,错误;
③标准状况下,HO不是气体,1 mol HO的体积不是22.4 L,错误;
2 2
④标准状况下,28 g CO与N 混合气体物质的量为1mol,体积约为22.4 L,正确;
2
⑤影响气体摩尔体积的因素有温度、压强、气体所处的状态不确定,各气体的气体摩尔体积不一定是
22.4L/mol,错误;
⑥标准状况下,体积相同的气体的分子数相同,正确;
故选B。
变式2 考查物质的组成与结构
2.(2022·贵州·模拟预测)N 表示阿伏加德罗常数的值,下列说法正确的是
A
A.22.4L的CO和CO 混合气体中含有的碳原子数为1N
2 A
B.0.5molAlCl 完全转化成氢氧化铝胶体,生成胶粒数目为0.5N
3 AC.常温常压下,13.6g金刚烷 中所含C-C键的数目为1.2N
A
D.7.8gNa O 中含有的阴离子数为0.2N
2 2 A
【答案】C
【解析】A.在未告诉标况时不能得知混合气体的物质的量,错误。
B.0.5molAlCl 完全转化成氢氧化铝胶体生成胶粒数目小于0.5N ,错误。
3 A
C.常温常压下,13.6g金刚烷为0.1mol,其中所含C-C键的数目为1.2N ,正确。
A
D.7.8gNa O 的物质的量为0.1mol,阴离子为O ,所以其中含有的阴离子数为0.1N ,错误。
2 2 A
故选C。
变式3 考查电解质溶液中粒子的数目
3.(2022·辽宁卷)设 为阿伏加德罗常数的值。下列说法正确的是
A. 中含有的中子数为
B. 分子中含有的 键数目为
C.标准状况下, 气体中 数目为
D. 的 溶液中 数目为
【答案】A
【解析】A.1个 原子中含有10个中子, 的物质的量为 ,故 中含有
中子的物质的量为 ,中子数为 ,故A正确;
B.乙烯分子的结构式为 ,1个乙烯分子中含有5个 键, 的物质的量为 ,
所以 分子中含有的 键数目为 ,B错误;
C. 是共价化合物, 分子中不存在 ,故C错误;D.没有给出 溶液的体积,无法计算 的 溶液中 的数目,故D错误;
选A。
变式4 考查氧化还原反应中电子转移的数目
16.(2022·天津·耀华中学模拟预测)若N 表示阿伏加德罗常数的数值,下列说法中正确的是
A
A.向FeI 溶液中通入氯气,当有2molFe2+被氧化时,转移电子的数目为2N
2 A
B.0.01L1mol/L饱和FeCl 溶液滴入沸水完全水解生成Fe(OH) 胶体粒子数为0.01N
3 3 A
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为N
A
D.12gNaHSO 中含有0.1N 个阳离子
4 A
【答案】D
【解析】A.由于还原性I->Fe2+,因此当Fe2+被氧化时,溶液中的I-已经氧化完全,因此无法计算转移的电
子数目,故A错误;
B.Fe3+胶体粒子是多个Fe3+微粒的聚集体,因此无法计算Fe(OH) 胶体粒子的数目,故B错误;
3
C.电解饱和食盐水时,阴阳两极产生的气体分别为氢气和氯气,因此若阴阳两极产生气体的总质量为
73g,则生成H、Cl,转移电子数为2N ,故C错误;
2 2 A
D.12gNaHSO 的物质的量为0.1mol,因此含有N 个阳离子(钠离子),故D正确;
4 A
故答案为D
变式5 考查可逆反应
13.(2022·四川雅安·模拟预测)N 表示阿伏加德罗常数,下列说法正确的是
A
A. 中含有的中子数为6N
A
B.标准状况下, 与 的混合气中电子数为N
A
C. 溶液中阴离子数少于0.1N
A
D. 和 充分反应后,分子总数为0.2N
A
【答案】B
【解析】A.核素的表示方法为:元素符号左下角为质子数,左上角为质量数,质量数等于质子数加中子
数; 的物质的量为1mol,含有的中子的物质的量为8mol,数目为8N ,A错误;
A
B.甲烷和氨气均为10电子分子,标准状况下, 与 的混合气的物质的量为0.1mol,则含有电子数为N ,B正确;
A
C.溶液体积未知,不能计算离子的物质的量,C错误;
D.二氧化硫和氧气反应可逆反应,反应进行不完全,反应后分子总数不是0.2 N ,D错误;
A
故选B。
变式6 考查化学反应的“特殊性”
18.(2022·河南·模拟预测)设 为阿伏加德罗常数的值。下列说法正确的是
A.5.5g ( )中含 键的数目为0.3
B.1L0.1 溶液中含 的数目为0.2
C.0.2 乙酸与0.1 乙醇在浓硫酸催化下充分反应,生成的乙酸乙酯分子数为0.1
D.22.4L 发生反应 ,转移的电子数为1.5
【答案】A
【解析】A.5.5g 的物质的量为 =0.025mol,每个分子中含有12个 键,则5.5g 中
含 键的数目为0.025 12 =0.3 ,故A正确;
B. 为弱酸根离子,发生水解,则1L0.1 溶液中含 的数目小于0.2 ,故B错
误;
C.酯化反应为可逆反应,反应不能进行到底,则0.2 乙酸与0.1 乙醇在浓硫酸催化下充分反应,生
成的乙酸乙酯分子数小于0.1 ,故C错误;
D.未指明状态,不能确定22.4L 的物质的量是1 ,无法计算转移的电子数,故D错误;
答案选A。
变式7 物质的量浓度配制及误差分析33.(2022·黑龙江哈尔滨·高三学业考试)下列实验误差分析不正确的是
A.配制一定物质的量浓度的溶液定容时俯视容量瓶刻度线,所配溶液浓度偏大
B.用湿润的pH试纸测某酸雨样品的pH,所测pH数值偏大
C.测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏低
D.滴定前滴定管尖嘴内有气泡,终点读数时气泡消失,所测体积偏小
【答案】D
【解析】A.配制一定物质的量浓度的溶液定容时俯视容量瓶刻度线,导致读数偏大,溶液体积偏小,所
配溶液浓度偏大,A正确;
B.用湿润的pH试纸测某酸雨样品的pH,雨水溶液变小,酸性变弱,所测pH数值偏大,B正确;
C.测定中和反应的反应热时,将碱缓慢倒入酸中,导致损失热量,所测温度值偏低,C正确;
D.滴定前滴定管尖嘴内有气泡,终点读数时气泡消失,导致滴定液用量偏大,所测体积偏大,D错误;
故选D。
1.(2022·四川绵阳·一模)N 为阿伏加德罗常数的值。下列说法正确的是
A
A.2.0 g 与 的混合物中所含中子数为0.8N
A
B.标准状况下,11.2 L丙烷具有的共价键数为5.0N
A
C.电解精炼铜时,若电路中转移电子0.2N ,阳极质量减少6.4 g
A
D.常温下,0.5 mol Al投入浓硫酸中,反应转移的电子数为1.5N
A
【答案】B
【解析】A. 和 相对分子质量都是20,其中含有10个中子;则2.0 g 和 的物质的量
是0.1 mol,其中所含中子数为N ,A错误;
A
B.标准状况下,11.2 L丙烷的物质的量是0.5 mol,由于在丙烷C H 分子中含有10个共价键,则在0.5
3 8
mol C H 中含有的共价键数为5.0N ,B正确;
3 8 A
C.阳极上发生氧化反应的元素除Cu外,还可能有Zn、Fe等活动性比Cu强的金属,而活动性比Cu弱的
金属,则形成阳极泥沉淀在阳极底部,故电解精炼铜时,若电路中转移电子0.2N ,阳极质量减少可能是
A
6.4 g,也可能不是6.4 g,C错误;
D.常温下,Al遇浓硫酸会发生钝化而不能进一步发生反应,因此不能计算出反应过程中电子转移数目,
D错误;
故合理选项是B。2.(2022·全国·模拟预测)N 为阿伏加德罗常数的值,下列说法错误的是
A
A.1.7g羟基(-OH)和1.7gOH-中含有的质子数均为0.9N
A
B.标况下,11.2LNO与11.2LO 混合后的分子数目为0.75N
2 A
C.相同条件下,23gNa与78gNaO 分别与足量水反应生成的气体体积相同
2 2
D.100g质量分数为46%的乙醇溶液中含有氢原子数为12N
A
【答案】B
【解析】A.羟基(-OH)和OH-的质子数均为9,1.7g羟基(-OH)和1.7gOH-中含有质子数均为0.9N ,选项A
A
正确;
B.标况下,11.2LNO与11.2LO 混合后发生的反应为2NO+O ═2NO ,生成0.5molNO 和剩余0.25molO,
2 2 2 2 2
气体总物质的量为0.75mol,但存在2NO NO,则反应后的气体的物质的量小于0.75mol,混合后所含
2 2 4
分子数目小于0.75N ,选项B错误;
A
C.根据反应2Na+2HO=2NaOH+H ↑可知,23gNa与足量水反应生成0.5molH, 根据反应
2 2 2
2NaO+2H O=4NaOH+O ↑可知,78g Na O 与足量水反应生成0.5molO,相同条件下,生成的气体体积相同,
2 2 2 2 2 2 2
选项C正确;
D.100g质量分数为46%的乙醇溶液中含有氢原子数为
=12N ,选项D正确;
A
答案选B。
3.(2021·四川广安·模拟预测)设N 为阿伏加德罗常数的值,下列说法中正确的是
A
A.标准状况下,22.4L H O含有电子数为10N
2 A
B.56g Fe与足量Cl 完全反应,转移的电子数为2 N
2 A
C.密闭容器中2molSO 与lmolO 充分反应后生成SO 分子数为2 N
2 2 3 A
D.1LpH=2的CHCOOH溶液中含有的H+数目为0.01 N
3 A
【答案】D
【解析】A标况下水为液体,不确定水的物质的量,A错误;
B.铁与氯气生成氯化铁,56g Fe为1mol,与足量Cl 完全反应,转移的电子数为3 N ,B错误;
2 A
C.二氧化硫与氧气反应为可逆反应,反应进行不彻底,生成SO 分子数小于2 N ,C错误;
3 A
D.pH=2的CHCOOH溶液中氢离子浓度为0.01mol/L,则1L pH=2的CHCOOH溶液中含有的H+数目为
3 3
0.01 N , D正确;
A
故选D。
4.(2021·浙江卷)设 为阿伏加德罗常数的值,下列说法不正确的是A.标准状况下, 中含有中子数为
B. (分子结构: )中的共价键数目为
C. 的 水溶液中含有氧原子数为
D. 三肽 (相对分子质量:189)中的肽键数目为
【答案】C
【解析】A.标准状况下, 的物质的量为:0.05mol,一个 中含有中子数为: 个,所以
中含有中子数为 ,A正确;
B. 的物质的量为:0.25mol,根据白磷的分子结构可知一个白磷分子里含有六条共价键,所以共价
键数目为: ,B正确;
C. 的 水溶液中含有溶质氢氧化钠和溶剂水,氧原子数目为二者氧原子数目的加和,
C错误;
D. 三肽 的物质的量为:0.1mol,三分子氨基酸脱水缩合形成三肽,三肽中含有两个肽键,
所以 三肽 中的肽键数目为 ,D正确;
答案为:C。
5.(2021·天津市实验中学滨海学校高三开学考试)下列误差分析正确的是
A.用容量瓶配制溶液,定容时仰视刻度线,所配溶液浓度偏小
B.用湿润的pH试纸测NaCO 溶液的pH值,测定值偏大
2 3
C.滴定前滴定管内有气泡,终点读数时无气泡,所测体积偏小
D.中和热测定实验中,用铜制环形搅拌器代替环形玻璃搅拌棒,所测中和热的数值偏大
【答案】A
【解析】A.用容量瓶配制溶液,定容时仰视刻度线,所配溶液的体积偏大,溶液浓度偏小,故A正确;
B.NaCO 溶液的pH>7,用湿润的pH试纸测NaCO 溶液的pH值,相当于对溶液稀释,测定值偏小,故
2 3 2 3B错误;
C.滴定前滴定管内有气泡,终点读数时无气泡,所测体积偏大,故C错误;
D.中和热测定实验中,用铜制环形搅拌器代替环形玻璃搅拌棒,热量损失较多,所测中和热的数值偏小,
故D错误;
选A。
核心考点二 以物质的量为中心的多角度计算
化学计算中的三种常用方法
1.守恒法
2.关系式法
(1)在进行多步反应的计算时,要找出起始物与目标物之间的定量关系,一般的解题步骤:
如工业上用黄铁矿(FeS )生产硫酸涉及的化学反应:
2
4FeS+11O=====2Fe O+8SO
2 2 2 3 2
2SO +O2SO
2 2 3
SO +HO===H SO
3 2 2 4
故FeS 与HSO 之间的关系式为
2 2 4
FeS~2SO ~2SO ~2HSO
2 2 3 2 4
(2)多步反应也可以利用原子守恒建立关系式
如工业上用氨气生产硝酸涉及的化学反应:
4NH +5O=====4NO+6HO
3 2 2
2NO+O===2NO
2 2
3NO +HO===2HNO +NO
2 2 3
可利用生产过程中氮原子守恒直接建立NH 和硝酸的关系式:
3NH ―――――→HNO
3 3
3.差量法
差量法是指根据化学反应前后有关物理量发生的变化,找出“理论差量”。这种差量可以是质量、物质的
量、气态物质的体积和压强、反应过程中的热量等。用差量法解题时先把化学方程式中的对应差量(理论差
量)跟实际差量列成比例,然后求解。
如 2C(s)+O(g)===2CO(g)
2
固体差量 24 g Δm=24 g
物质的量差量 2 mol 1 mol 2 mol Δn=1 mol
体积差量 1 L 2 L ΔV=1 L
考法 以物质的量为中心的多角度计算(题型预测:选择题)
1.(2022·天津南开·高三期中)设 为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下, 中含有分子数为
B.常温常压下, 中含有离子总数是
C. 和 混合气体中含有原子总数为
D.50mL18.4mol/L浓硫酸与足量铜微热反应,生成 分子数为
【答案】C
【解析】A. 标准状况下, 为固体,无法计算其物质的量,故A错误;
B. 常温常压下, 物质的量为0.1mol, 是由Na+和 构成的,则含有离子总数是 ,
故B错误;
C. 和 的最简式均为 ,则 和 混合气体中相当于含有1mol ,则原子总数为
,故C正确;
D. 随反应进行浓硫酸变稀,反应停止,无法计算 分子数,故D错误;故选C。
2.(2022·上海市崇明区横沙中学高二期末)pg某结晶水合物A·nH O受热失去全部结晶水,质量变为
2
qg,由此可以知道结晶水合物的式量为
A. B. C. D.
【答案】D
【解析】设结晶水合物的摩尔质量为M,根据质量守恒定律可知, ,解得M=
g/mol,故结晶水合物的式量为 ;
故选D
1.化学方程式中化学计量数与相关物理量的关系c
2.以物质的量为中心的各种计量关系
变式1 守恒法、关系式法、差量法的运用
1.(2022·浙江·高一期中)在NaCl、MgCl 、MgSO 形成的混合溶液中, ,
2 4, ,则 为
A. B. C. D.
【答案】A
【解析】溶液呈电中性,也就是阳离子所带的正电荷总数与阴离子所带的负电荷总数相等,所以c(Na+)
+2c(Mg2+)=c(Cl-)+2 c( ),从而得出c( )=[c(Na+)+2c(Mg2+)-c(Cl-)] 2=(0.20+0.30×2-0.30)
÷
molL-1 2=0.25 molL-1,故选A。
∙ ÷ ∙
2.(2022·全国)硫黄制硫酸时发生的反应有S+O SO 、2SO +O 2SO 、SO +HO=HSO
2 2 2 2 3 3 2 2 4。
(1)由硫黄制取硫酸的关系式是_______。
(2)假设64g硫黄完全反应,可制取硫酸的质量是_______。
【答案】(1)S~HSO
2 4
(2)196 g
【解析】(1)由S+O SO 、2SO +O 2SO 、SO +HO=HSO ,可知S~SO ~SO ~HSO ,
2 2 2 2 3 3 2 2 4 2 3 2 4
可得S~HSO ;
2 4
(2)64g硫黄物质的量为 = =2mol,由小问1可知S~HSO ,n(H SO )=n(S)=2mol,制取硫酸的
2 4 2 4
质量为m=nM=2mol×98g/mol=196g;
变式2 物质的量的计算在图像中的应用
3.(2022·河南·高三阶段练习)已知W、X、Y和Z为前20号元素,且原子序数依次增大,W的原子半
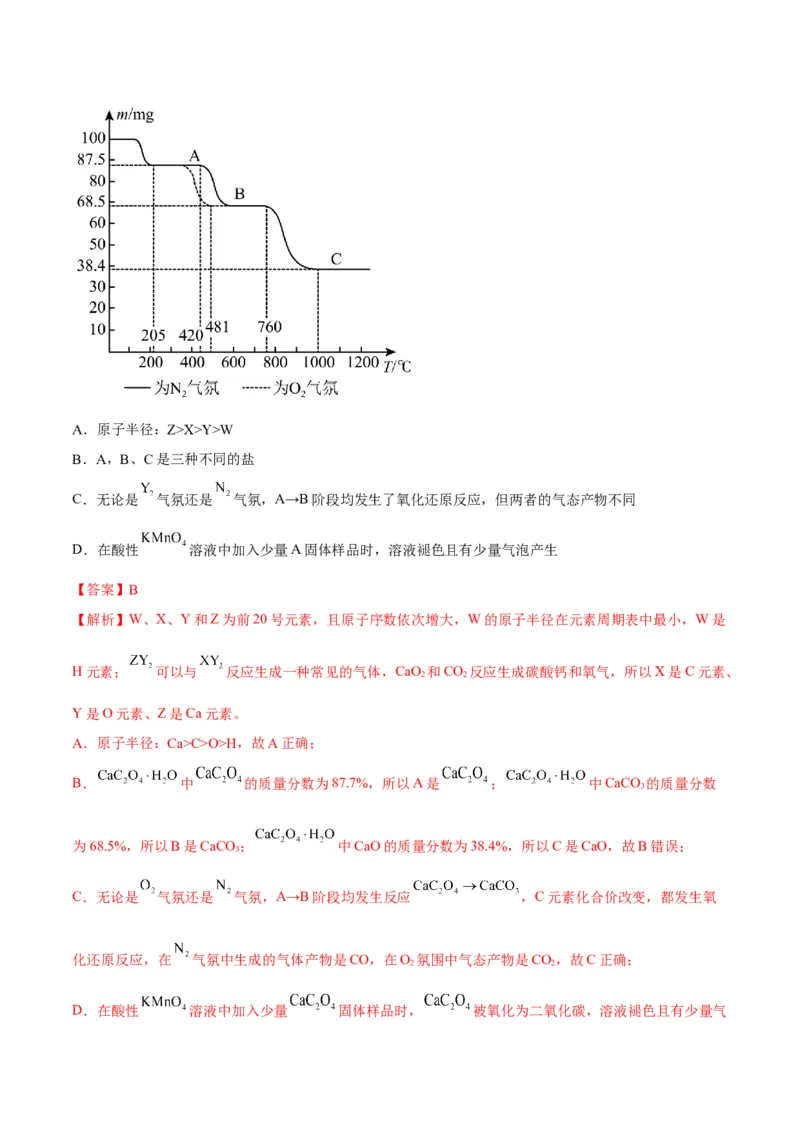
径在元素周期表中最小, 可以与 反应生成一种常见的气体。化合物( )在 和 气氛
中的热重曲线(样品质量随温度变化的曲线)如图所示。下列有关说法错误的是A.原子半径:Z>X>Y>W
B.A,B、C是三种不同的盐
C.无论是 气氛还是 气氛,A→B阶段均发生了氧化还原反应,但两者的气态产物不同
D.在酸性 溶液中加入少量A固体样品时,溶液褪色且有少量气泡产生
【答案】B
【解析】W、X、Y和Z为前20号元素,且原子序数依次增大,W的原子半径在元素周期表中最小,W是
H元素; 可以与 反应生成一种常见的气体,CaO 和CO 反应生成碳酸钙和氧气,所以X是C元素、
2 2
Y是O元素、Z是Ca元素。
A.原子半径:Ca>C>O>H,故A正确;
B. 中 的质量分数为87.7%,所以A是 ; 中CaCO 的质量分数
3
为68.5%,所以B是CaCO ; 中CaO的质量分数为38.4%,所以C是CaO,故B错误;
3
C.无论是 气氛还是 气氛,A→B阶段均发生反应 ,C元素化合价改变,都发生氧
化还原反应,在 气氛中生成的气体产物是CO,在O 氛围中气态产物是CO,故C正确;
2 2
D.在酸性 溶液中加入少量 固体样品时, 被氧化为二氧化碳,溶液褪色且有少量气泡产生,故D正确;
选B。
1.(2022·湖南·长沙一中高三阶段练习)设 为阿伏加德罗常数的值,下列叙述不正确的是
A.标准状况下, 中含有的中子数目为2
B.常温常压下, 与足量 溶液反应。转移电子的数目为0.1
C.常温下, 的 溶液中,水电离出的 的数目为 0-9N
A
D. 中含有的非极性键的数目为0.1
【答案】C
【解析】A.一个 分子中含有的中子数目为20,标准状况下, 为 ,所以含有的中子
物质的量为 ,数目为 ,正确;
B.一个 分子与足量 溶液完全反应转移 ,所以 转移电子的数目为 ,正确;
C.常温下, 的 溶液中,水电离出的 的数目为 ,错误;
D.一个 中含一个 非极性键,所以 中含有的非极性键的数目为 ,正确;
故选C。
2.(2022·广东广东·高三期中)设N 为阿伏加德罗常数的数值,下列说法正确的是
A
A.5.6g铁分别与足量氯气和稀硝酸反应,转移的电子数目均为0.3N
A
B.标准状况下,氧原子总数为0.2N 的CO 和NO 的混合气体,其体积为2.24L
A 2 2
C.100g 46%乙醇溶液中所含氧原子数目为N
A
D.常温下,pH=1的盐酸溶液中,由水电离出的H+个数为10-13N
A
【答案】A
【解析】A.铁分别与足量氯气和稀硝酸反应,都生成Fe3+,5.6g铁的物质的量为0.1mol,则转移的电子
数为0.3N ,故A正确;
AB.由于二氧化氮和二氧化碳中均含2个氧原子,故氧原子总数为0.2N 的CO 和NO 的混合气体中含有的
A 2 2
CO 和“NO ”物质的量共为0.1mol,而在NO 气体中存在平衡:2NO NO,导致分子个数减少,故
2 2 2 2 2 4
气体的物质的量会小于0.1mol,则体积小于2.24L,故B错误;
C.在乙醇溶液中,除了乙醇外,水也含氧原子,100g46%的乙醇溶液中,乙醇的质量为46g,物质的量为
1mol,则含1mol氧原子;水的质量为54g,物质的量为3mol,故含3mol氧原子,故此溶液共含4mol氧原
子即4N 个,故C错误;
A
D.溶液体积不明确,故溶液中水电离出的氢离子的个数无法计算,故D错误;
故选A。
2.(2022·浙江)在NaCl、MgCl 、MgSO 形成的混合溶液中, ,
2 4
, ,则 为
A. B. C. D.
【答案】A
【解析】溶液呈电中性,也就是阳离子所带的正电荷总数与阴离子所带的负电荷总数相等,所以c(Na+)
+2c(Mg2+)=c(Cl-)+2 c( ),从而得出c( )=[c(Na+)+2c(Mg2+)-c(Cl-)] 2=(0.20+0.30×2-0.30)
÷
molL-1 2=0.25 molL-1,故选A。
∙ ÷ ∙
4.(2022·江西赣州·高三期中)碱式碳酸铝镁 常用作塑料阻燃剂。为确定碱
式碳酸铝镁的组成,进行如下实验:
Ⅰ.准确称取3.390g样品与足量稀盐酸充分反应,生成 (已换算成标准状况下)。
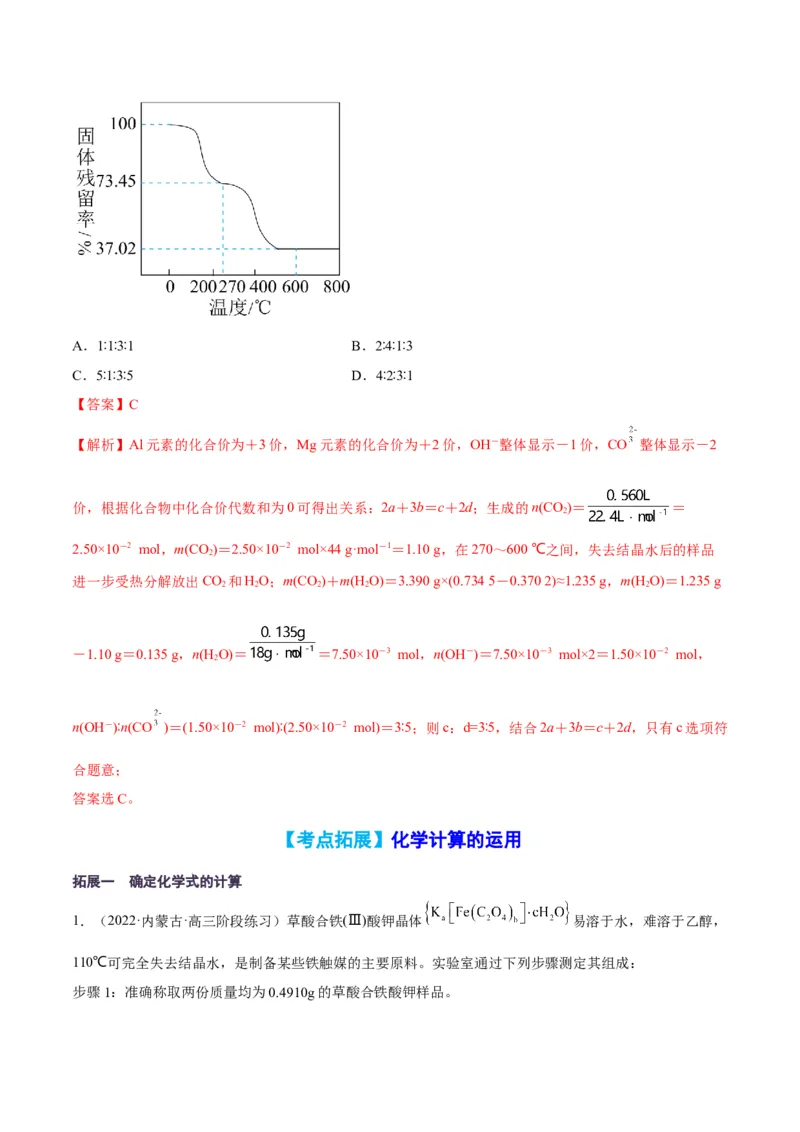
Ⅱ.另取一定量样品在空气中加热,样品的固体残留率( ×100%)随温度的变化如图所
示。(样品在270℃时已完全失去结晶水,600℃以上残留固体为金属氧化物的混合物)
则 为A.1∶1∶3∶1 B.2∶4∶1∶3
C.5∶1∶3∶5 D.4∶2∶3∶1
【答案】C
【解析】Al元素的化合价为+3价,Mg元素的化合价为+2价,OH-整体显示-1价,CO 整体显示-2
价,根据化合物中化合价代数和为0可得出关系:2a+3b=c+2d;生成的n(CO)= =
2
2.50×10-2 mol,m(CO)=2.50×10-2 mol×44 g·mol-1=1.10 g,在270~600 ℃之间,失去结晶水后的样品
2
进一步受热分解放出CO 和HO;m(CO)+m(H O)=3.390 g×(0.734 5-0.370 2)≈1.235 g,m(H O)=1.235 g
2 2 2 2 2
-1.10 g=0.135 g,n(H O)= =7.50×10-3 mol,n(OH-)=7.50×10-3 mol×2=1.50×10-2 mol,
2
n(OH-)∶n(CO )=(1.50×10-2 mol)∶(2.50×10-2 mol)=3∶5;则c:d=3∶5,结合2a+3b=c+2d,只有c选项符
合题意;
答案选C。
【考点拓展】化学计算的运用
拓展一 确定化学式的计算
1.(2022·内蒙古·高三阶段练习)草酸合铁(Ⅲ)酸钾晶体 易溶于水,难溶于乙醇,
110℃可完全失去结晶水,是制备某些铁触媒的主要原料。实验室通过下列步骤测定其组成:
步骤1:准确称取两份质量均为0.4910g的草酸合铁酸钾样品。步骤2:一份在 氛围下保持110℃加热至恒重,称得残留固体质量为0.4370g。
步骤3:另一份完全溶于水后,让其通过装有某阴离子交换树脂的交换柱
,用蒸馏水冲洗交换柱,收集交换出的 ,以 为指示剂,
用 的 溶液滴定至终点,消耗 溶液20.00mL。通过计算确定草酸合铁酸钾晶体
的化学式为
A. B.
C. D.
【答案】A
【解析】n(H O)= = ,n(Cl-)=n(Ag+)=0.1500mol/L 20.00 L= ;
2
根据离子交换柱中 ,可得样品中,n(K+)=n(Cl-)=
, ,110℃残留固体是晶体失去结晶水后的产物即K+和
的总质量,为 ;
中根据电荷守恒关系可得:a+3=2b,得a=3,b=3;n =
,n(K+): n : n(H O)=3:1:3,则样品的化学式为 ;答案选A。
2
拓展二 热重曲线的计算
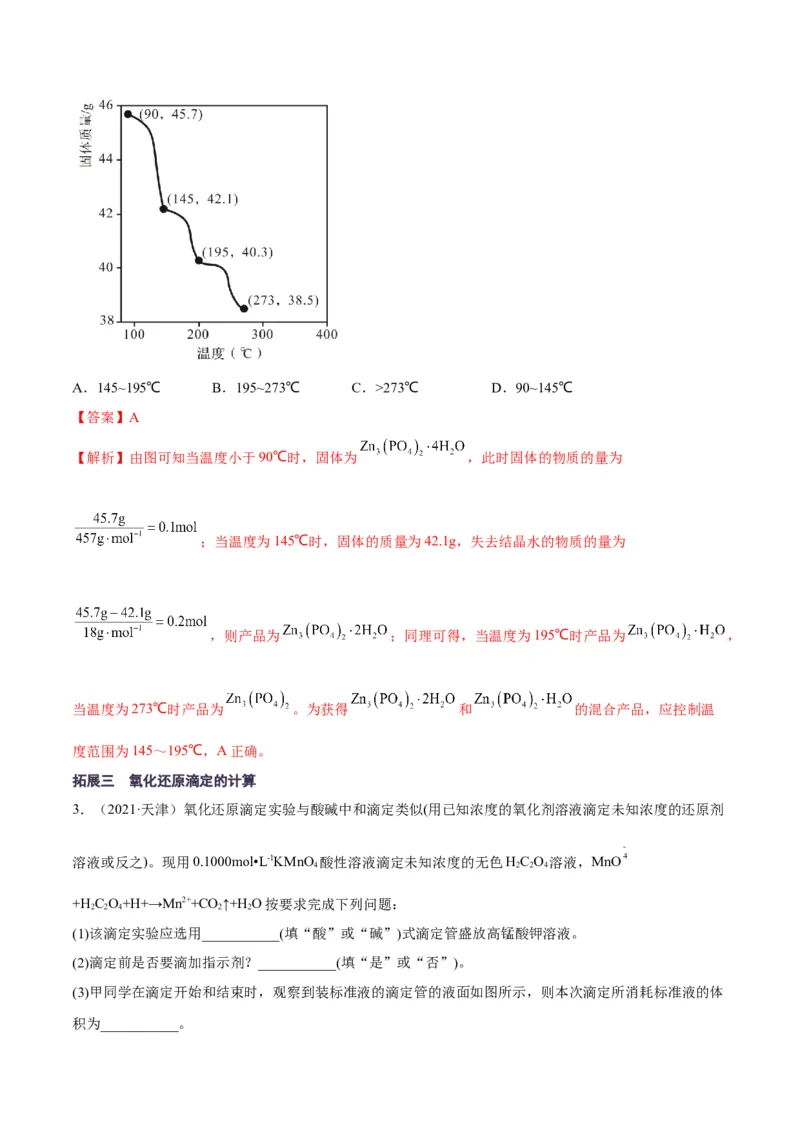
2.(2022·山西吕梁·高三阶段练习)称取 进行热重分析,固体质量随温度的变化关
系如图所示,为获得 和 的混合产品,烘干时的温度范围为A.145~195℃ B.195~273℃ C.>273℃ D.90~145℃
【答案】A
【解析】由图可知当温度小于90℃时,固体为 ,此时固体的物质的量为
;当温度为145℃时,固体的质量为42.1g,失去结晶水的物质的量为
,则产品为 ;同理可得,当温度为195℃时产品为 ,
当温度为273℃时产品为 。为获得 和 的混合产品,应控制温
度范围为145~195℃,A正确。
拓展三 氧化还原滴定的计算
3.(2021·天津)氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂
溶液或反之)。现用0.1000mol•L-1KMnO 酸性溶液滴定未知浓度的无色HC O 溶液,MnO
4 2 2 4
+H C O+H+→Mn2++CO ↑+H O按要求完成下列问题:
2 2 4 2 2
(1)该滴定实验应选用___________(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液。
(2)滴定前是否要滴加指示剂?___________(填“是”或“否”)。
(3)甲同学在滴定开始和结束时,观察到装标准液的滴定管的液面如图所示,则本次滴定所消耗标准液的体
积为___________。(4)乙学生按照滴定步骤进行了3次实验,分别记录有关数据如表:
0.1000mol•L-1KMnO 的体积/mL
4
滴定次数 待测HC O 溶液的体积/mL
2 2 4
滴定前刻度 滴定后刻度 溶液体积/mL
第一次 25.00 0.00 26.11 26.11
第二次 25.00 1.56 30.30 28.74
第三次 25.00 0.22 26.31 26.09
依据上表数据计算该HC O 溶液的物质的量浓度为___________mol/L(保留4位有效数字)。
2 2 4
【答案】(1)酸
(2)否
(3)26.10mL
(4)0.2610
【解析】(1)高锰酸钾具有强氧化性能腐蚀碱式滴定管中的橡胶管,所以不用碱式滴定管盛放高锰酸钾
溶液,应该用酸式滴定管;故答案为:酸;
(2)高锰酸钾溶液本身有颜色,为紫色,在开始滴入草酸中时被还原,颜色消失,当达到滴定终点时,
加入最后一滴高锰酸钾溶液颜色不褪去,溶液由无色变为浅紫色,且半分钟内不褪色。故答案为:否;
(3)酸式滴定管中的液面如图所示,起始读数为0.00mL,终点读数为26.10mL,则本次滴定所消耗标准
液的体积为26.10mL,故答案为:26.10mL;
(4)配平2MnO +5H C O+6H+=2Mn2++10CO ↑+8H O,根据数据的有效性,舍去第2组数据,然后求出
2 2 4 2 2
1、3组平均消耗 =26.10mL,由关系式:2MnO +5H C O,可得
2 2 4
5c(HC O)×0.025L= ×0.1000mol/L×0.02610L,解得:c(H C O)=0.2610mol/L,故答案为:0.2610;
2 2 4 2 2 4