文档内容
解密 02 化学常用计量
考点热度 ★★★★★
【考纲导向】
1.了解物质的量(n)及其单位摩尔(mol)、摩尔质量(M)、气体摩尔体积(V )、阿伏
m
加德罗常数(N )、物质的量浓度(c)的含义。
A
2.能根据微粒(原子、分子、离子)的物质的量、数目、气体体积(标准状况下)之间的相互
关系进行有关计算。
3.掌握配制一定溶质质量分数溶液和物质的量浓度的方法。
4.理解溶液中溶质的质量分数和物质的量浓度的概念,并能进行有关计算。
【命题分析】
1.阿伏加德罗常数(N )是高考的高频考点,主要以选择题的形式出现,着重考查物质的组
A
成、结构、性质等知识以及以物质的量为中心的相关计算,题目的落脚点往往以判断分子
原子、离子、电子等微粒数目为主。
2.Ⅰ卷常与N 相结合进行简单计算的考查,Ⅱ卷主要以填空题形式考查物质含量与组成,
A
有时对计算过程有要求。命题时主要有混合物成分含量的确定,未知物化学式的确定,根
据化学方程式的计算,多步连续反应的计算等。2023年高考仍会围绕阿伏加德罗常数、气
体摩尔体积设置知识陷阱,同时又隐含对物质结构、氧化还原反应、电离、水解等知识的考
查。
核心考点一 有关N 的正误判断
A
一、与N 相关的命题主要围绕以下四个方面进行
A
解答此类题目应注重看清所求微粒的种类、分子的构成(是单原子分子还是双原子分子或多
原子分子)以及微粒中的质子数、中子数、电子数等。如:常温常压下,14 g由N 和CO组成的混合气体中所含有的原子数目为N
2 A
提醒:由于二者的摩尔质量相等,所以二者无论以何种比例混合都不影响分子总数,故这
一说法是正确的。
2.由体积求微粒的数目,主要应用N=·N 计算
A
解题时要注意:
(1)若题目给出物质的体积,一要看是否是标准状况,二要看物质在标准状况下是不是气体,
若不是气体则无法求其物质的量。标准状况下不是气体的物质:HF(液态)、SO (固态)、
3
HO、乙醇、CCl 、苯、己烷、CHCl (液态)。
2 4 3
(2)若题目给出气体的质量或物质的量,则微粒数目与外界条件无关。
(3)注意某些物质分子中的原子个数,例如:稀有气体为单原子分子、臭氧(O )为三原子分
3
子、白磷(P )为四原子分子。
4
3.由物质的量浓度求微粒的数目,主要应用N=c·V·N 计算
A
这类题目一般会和弱电解质的电离、盐类的水解等知识联系在一起,解题时要注意对“隐
含条件”的挖掘。如1 L 0.1 mol·L-1 NaHCO 溶液中含HCO的数目小于0.1 N 。
3 A
4.氧化还原反应中转移电子数目的计算
依据题目提供的反应,抓住氧化还原反应的实质,运用得失电子数规律,计算得失电子的
数目。如1 mol Fe与足量稀HNO 反应,转移电子数目是3N 而不是2N 。
3 A A
二、常见三种组成类型溶液的配制方法
(1)体积比浓度溶液配制:
将浓溶液或纯液体溶质和水按体积比用量筒量取,然后在烧杯中混合即可,所需仪器:量
筒、烧杯、玻璃棒;
(2)质量百分比浓度溶液配制:
称取一定质量固体溶质或用量筒量取一定体积浓溶液或纯液体溶质,用量筒量取所需体积
的水,在烧杯中混合溶解即可。所需仪器:量筒、烧杯、玻璃棒、托盘天平(溶质为固体);
(3)一定物质的量浓度溶液的配制:
①配制步骤简要概括为:算—称—溶—移—洗—荡—定—摇。
②数据的处理及要求
数据 要求或解释
药品的 托盘天平称量固体药品,只能精确到0.1 g,记录数据时只能保留小数点后一位
质量 数字,如14.6 g,不能写为14.60 g
a.选择容量瓶时应该与所配溶液体积相等或稍大。如需配制 480 mL某溶液,应
容量瓶 选择500 mL容量瓶;
的规格 b.回答仪器容量瓶名称时同时应该注明其规格,如“500 mL容量瓶”,不能
只回答“容量瓶”考法1 有关N 的正误判断(题型预测:选择题)
A
1.(2022·全国卷) 为阿伏加德罗常数的值,下列说法正确的是
A.25℃, 下, 氢气中质子的数目为
B. 溶液中, 的数目为
C. 苯甲酸完全燃烧,生成 的数目为
D.电解熔融 ,阴极增重 ,外电路中通过电子的数目为
2.(2022·河北卷)N 是阿伏加德罗常数的值。下列说法正确的是
A
A.3.9gNa O 与足量水反应,转移电子个数为0.1N
2 2 A
B.1.2gMg在空气中燃烧生成MgO和MgN,转移电子个数为0.1N
3 2 A
C.2.7gAl与足量NaOH溶液反应,生成H 的个数为0.1N
2 A
D.6.0gSiO 与足量NaOH溶液反应,所得溶液中SiO 的个数为0.1N
2 A
考法2 物质的量浓度及误差分析(题型预测:选择题)
3.(2022·黑龙江哈尔滨·高三学业考试)下列实验误差分析不正确的是
A.配制一定物质的量浓度的溶液定容时俯视容量瓶刻度线,所配溶液浓度偏大
B.用湿润的pH试纸测某酸雨样品的pH,所测pH数值偏大
C.测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏低
D.滴定前滴定管尖嘴内有气泡,终点读数时气泡消失,所测体积偏小
一、阿伏加德罗常数应用时的“六注意”
1.注意气体摩尔体积的适用条件及物质的状态
一要看是否为标准状况下;二要看物质在标准状况下是否为气态,如 CCl 、水、液溴、
4
SO 、己烷、苯等是非气体。
3
2.注意与计算无关的一些干扰条件
给出非标准状况下气体的物质的量或质量,干扰判断,实质上,此时物质所含的粒子数与
温度、压强等外界条件无关。
3.注意物质的组成与结构
(1)特殊物质中所含微粒(分子、原子、电子、质子、中子等)的数目,如Ne、DO、18O 、
2 2
O、P、H37Cl等。
3 4
(2)物质中所含化学键的数目,如SiO、CO、C H 等。
2 2 n 2n+2
(3)最简式相同的物质中的微粒数目,如NO 和NO、乙烯和丙烯、(O 和O)等
2 2 4 2 3
4.注意难电离、易水解的粒子数目
一看是否有弱电解质的电离;二看是否有弱离子的水解;三看是否指明了溶液的体积;弱
电解质在水溶液中部分电离,可水解盐溶液中离子发生微弱水解,都会导致粒子数目减少。5.注意电子转移(得失)数目
一要注意是否发生歧化反应,二要注意变价元素,三要注意过量问题,
反应 参考物质 转移电子的物质的量或电子数目
NaO+CO 1 mol Na O 1 mol或N
2 2 2 2 2 A
(或HO) 1 mol O 2 mol或2N
2 2 A
Cl+NaOH 1 mol Cl 1 mol或N
2 2 A
1 mol Cl 2 mol或2N
2 A
Cl+Fe
2
1 mol Fe 3 mol或3N
A
6.注意一些特殊条件
一要注意一些特殊的反应,如NO和O 不需要条件即可反应,NO 和NO 之间存在相互转
2 2 2 4
化,合成氨反应等属于可逆反应;二要注意特殊的物质,如摩尔质量相同或成整数倍的关
系的物质:N 和CO、C H ;NaS和NaO ;CaCO 与KHCO ;NaHCO 与MgCO ;Cu S
2 2 4 2 2 2 3 3 3 3 2
和CuO;NO 与NO。
2 2 4
二、一定物质的量浓度溶液配制的常考点分析
1.配制一定物质的量浓度的溶液,填写缺少的仪器
一般从以下三种仪器中选择:容量瓶、胶头滴管、玻璃棒,填写时一定要注明容量瓶的规
格。
2.误差分析的来源
(1)导致c 偏低的错误操作:垫滤纸称量NaOH固体;左码右物(用游码);称量时间过长(潮
B
解);洗涤或转移时溶液溅出;未洗涤烧杯及玻璃棒;超过刻度时用滴管吸出液体;定容时
仰视;定容后发现液面低于刻度线再加水。
(2)导致c 偏高的错误操作:砝码生锈;定容时俯视;未等溶液冷却至室温就定容。
B
(3)定容时俯视、仰视对结果的影响:务必确保按眼睛视线→刻度线→凹液面最低点的顺序,
做到“三点一线”。
①仰视刻度线(图1),导致溶液体积偏大。
②俯视刻度线(图2),导致溶液体积偏小。
变式1 考查气体的摩尔体积
1.(2022·河北·邢台市第二中学高三阶段练习)下列说法正确的是
①标准状况下,6.02×1023个分子所占的体积约是22.4L
②0.5 mol H 所占体积为11.2 L
2
③标准状况下,1 mol HO的体积为22.4 L
2
④标准状况下,28 g CO与N 混合气体的体积约为22.4 L
2⑤各种气体的气体摩尔体积都约为22.4 L/mol
⑥标准状况下,体积相同的气体的分子数相同
A.①②⑤ B.④⑥ C.③④⑥ D.①④⑥
变式2 考查物质的组成与结构
2.(2022·贵州·模拟预测)N 表示阿伏加德罗常数的值,下列说法正确的是
A
A.22.4L的CO和CO 混合气体中含有的碳原子数为1N
2 A
B.0.5molAlCl 完全转化成氢氧化铝胶体,生成胶粒数目为0.5N
3 A
C.常温常压下,13.6g金刚烷 中所含C-C键的数目为1.2N
A
D.7.8gNa O 中含有的阴离子数为0.2N
2 2 A
变式3 考查电解质溶液中粒子的数目
3.(2022·辽宁卷)设 为阿伏加德罗常数的值。下列说法正确的是
A. 中含有的中子数为
B. 分子中含有的 键数目为
C.标准状况下, 气体中 数目为
D. 的 溶液中 数目为
变式4 考查氧化还原反应中电子转移的数目
16.(2022·天津·耀华中学模拟预测)若N 表示阿伏加德罗常数的数值,下列说法中正确
A
的是
A.向FeI 溶液中通入氯气,当有2molFe2+被氧化时,转移电子的数目为2N
2 A
B.0.01L1mol/L饱和FeCl 溶液滴入沸水完全水解生成Fe(OH) 胶体粒子数为0.01N
3 3 A
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为N
A
D.12gNaHSO 中含有0.1N 个阳离子
4 A
变式5 考查可逆反应
13.(2022·四川雅安·模拟预测)N 表示阿伏加德罗常数,下列说法正确的是
A
A. 中含有的中子数为6N
A
B.标准状况下, 与 的混合气中电子数为N
A
C. 溶液中阴离子数少于0.1N
A
D. 和 充分反应后,分子总数为0.2N
A
变式6 考查化学反应的“特殊性”
18.(2022·河南·模拟预测)设 为阿伏加德罗常数的值。下列说法正确的是A.5.5g ( )中含 键的数目为0.3
B.1L0.1 溶液中含 的数目为0.2
C.0.2 乙酸与0.1 乙醇在浓硫酸催化下充分反应,生成的乙酸乙酯分子数为0.1
D.22.4L 发生反应 ,转移的电子数为1.5
变式7 物质的量浓度配制及误差分析
33.(2022·黑龙江哈尔滨·高三学业考试)下列实验误差分析不正确的是
A.配制一定物质的量浓度的溶液定容时俯视容量瓶刻度线,所配溶液浓度偏大
B.用湿润的pH试纸测某酸雨样品的pH,所测pH数值偏大
C.测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏低
D.滴定前滴定管尖嘴内有气泡,终点读数时气泡消失,所测体积偏小
1.(2022·四川绵阳·一模)N 为阿伏加德罗常数的值。下列说法正确的是
A
A.2.0 g 与 的混合物中所含中子数为0.8N
A
B.标准状况下,11.2 L丙烷具有的共价键数为5.0N
A
C.电解精炼铜时,若电路中转移电子0.2N ,阳极质量减少6.4 g
A
D.常温下,0.5 mol Al投入浓硫酸中,反应转移的电子数为1.5N
A
2.(2022·全国·模拟预测)N 为阿伏加德罗常数的值,下列说法错误的是
A
A.1.7g羟基(-OH)和1.7gOH-中含有的质子数均为0.9N
A
B.标况下,11.2LNO与11.2LO 混合后的分子数目为0.75N
2 A
C.相同条件下,23gNa与78gNaO 分别与足量水反应生成的气体体积相同
2 2
D.100g质量分数为46%的乙醇溶液中含有氢原子数为12N
A
3.(2021·四川广安·模拟预测)设N 为阿伏加德罗常数的值,下列说法中正确的是
A
A.标准状况下,22.4L H O含有电子数为10N
2 A
B.56g Fe与足量Cl 完全反应,转移的电子数为2 N
2 A
C.密闭容器中2molSO 与lmolO 充分反应后生成SO 分子数为2 N
2 2 3 A
D.1LpH=2的CHCOOH溶液中含有的H+数目为0.01 N
3 A
4.(2021·浙江卷)设 为阿伏加德罗常数的值,下列说法不正确的是
A.标准状况下, 中含有中子数为B. (分子结构: )中的共价键数目为
C. 的 水溶液中含有氧原子数为
D. 三肽 (相对分子质量:189)中的肽键数目为
5.(2021·天津市实验中学滨海学校高三开学考试)下列误差分析正确的是
A.用容量瓶配制溶液,定容时仰视刻度线,所配溶液浓度偏小
B.用湿润的pH试纸测NaCO 溶液的pH值,测定值偏大
2 3
C.滴定前滴定管内有气泡,终点读数时无气泡,所测体积偏小
D.中和热测定实验中,用铜制环形搅拌器代替环形玻璃搅拌棒,所测中和热的数值偏大
核心考点二 以物质的量为中心的多角度计算
化学计算中的三种常用方法
1.守恒法
2.关系式法
(1)在进行多步反应的计算时,要找出起始物与目标物之间的定量关系,一般的解题步骤:
如工业上用黄铁矿(FeS )生产硫酸涉及的化学反应:
2
4FeS+11O=====2Fe O+8SO
2 2 2 3 2
2SO +O2SO
2 2 3
SO +HO===H SO
3 2 2 4
故FeS 与HSO 之间的关系式为
2 2 4
FeS~2SO ~2SO ~2HSO
2 2 3 2 4
(2)多步反应也可以利用原子守恒建立关系式
如工业上用氨气生产硝酸涉及的化学反应:4NH +5O=====4NO+6HO
3 2 2
2NO+O===2NO
2 2
3NO +HO===2HNO +NO
2 2 3
可利用生产过程中氮原子守恒直接建立NH 和硝酸的关系式:
3
NH ―――――→HNO
3 3
3.差量法
差量法是指根据化学反应前后有关物理量发生的变化,找出“理论差量”。这种差量可以
是质量、物质的量、气态物质的体积和压强、反应过程中的热量等。用差量法解题时先把
化学方程式中的对应差量(理论差量)跟实际差量列成比例,然后求解。
如 2C(s)+O(g)===2CO(g)
2
固体差量 24 g Δm=24 g
物质的量差量 2 mol 1 mol 2 mol Δn=1 mol
体积差量 1 L 2 L ΔV=1 L
考法 以物质的量为中心的多角度计算(题型预测:选择题)
1.(2022·天津南开·高三期中)设 为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下, 中含有分子数为
B.常温常压下, 中含有离子总数是
C. 和 混合气体中含有原子总数为
D.50mL18.4mol/L浓硫酸与足量铜微热反应,生成 分子数为
2.(2022·上海市崇明区横沙中学高二期末)pg某结晶水合物A·nH O受热失去全部结晶
2
水,质量变为qg,由此可以知道结晶水合物的式量为
A. B. C. D.
1.化学方程式中化学计量数与相关物理量的关系c2.以物质的量为中心的各种计量关系
变式1 守恒法、关系式法、差量法的运用
1.(2022·浙江·高一期中)在NaCl、MgCl 、MgSO 形成的混合溶液中,
2 4
, , ,则 为
A. B. C. D.
2.(2022·全国)硫黄制硫酸时发生的反应有S+O SO 、2SO +O 2SO 、SO
2 2 2 2 3 3
+HO=HSO
2 2 4。
(1)由硫黄制取硫酸的关系式是_______。
(2)假设64g硫黄完全反应,可制取硫酸的质量是_______。
变式2 物质的量的计算在图像中的应用
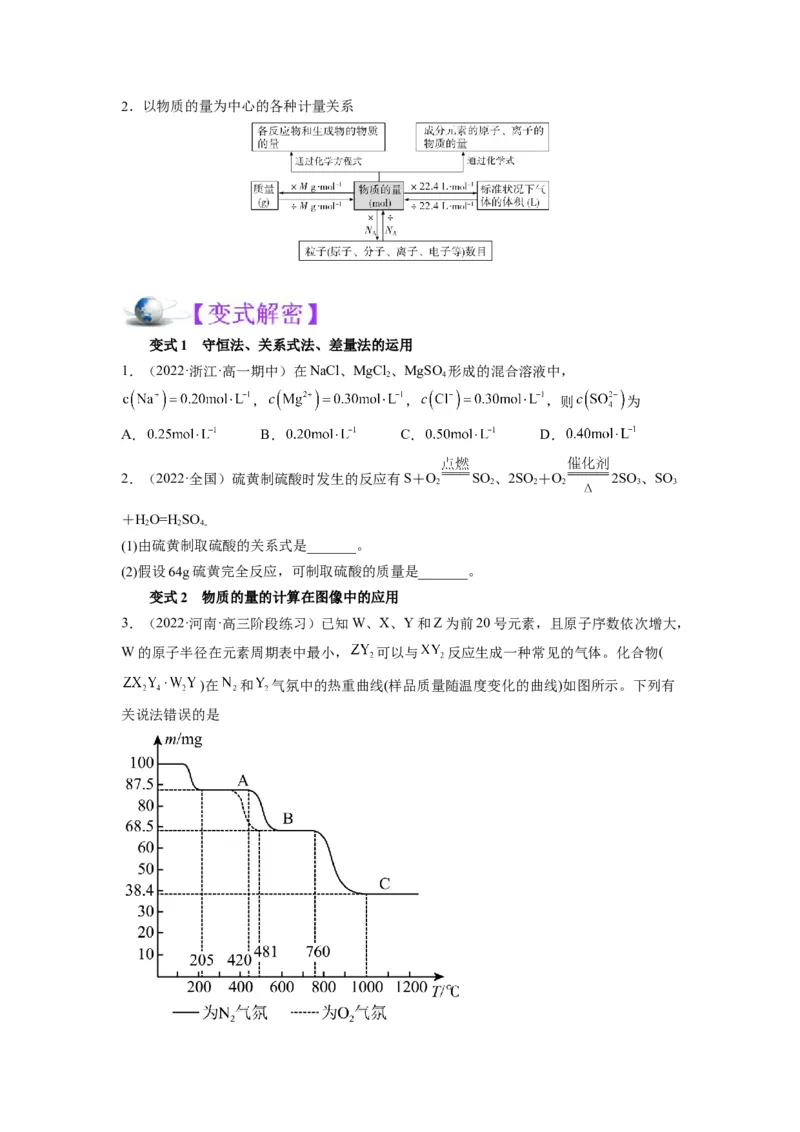
3.(2022·河南·高三阶段练习)已知W、X、Y和Z为前20号元素,且原子序数依次增大,
W的原子半径在元素周期表中最小, 可以与 反应生成一种常见的气体。化合物(
)在 和 气氛中的热重曲线(样品质量随温度变化的曲线)如图所示。下列有
关说法错误的是A.原子半径:Z>X>Y>W
B.A,B、C是三种不同的盐
C.无论是 气氛还是 气氛,A→B阶段均发生了氧化还原反应,但两者的气态产物不
同
D.在酸性 溶液中加入少量A固体样品时,溶液褪色且有少量气泡产生
1.(2022·湖南·长沙一中高三阶段练习)设 为阿伏加德罗常数的值,下列叙述不正确
的是
A.标准状况下, 中含有的中子数目为2
B.常温常压下, 与足量 溶液反应。转移电子的数目为0.1
C.常温下, 的 溶液中,水电离出的 的数目为 0-9N
A
D. 中含有的非极性键的数目为0.1
2.(2022·广东广东·高三期中)设N 为阿伏加德罗常数的数值,下列说法正确的是
A
A.5.6g铁分别与足量氯气和稀硝酸反应,转移的电子数目均为0.3N
A
B.标准状况下,氧原子总数为0.2N 的CO 和NO 的混合气体,其体积为2.24L
A 2 2
C.100g 46%乙醇溶液中所含氧原子数目为N
A
D.常温下,pH=1的盐酸溶液中,由水电离出的H+个数为10-13N
A
2.(2022·浙江)在NaCl、MgCl 、MgSO 形成的混合溶液中, ,
2 4
, ,则 为
A. B. C. D.
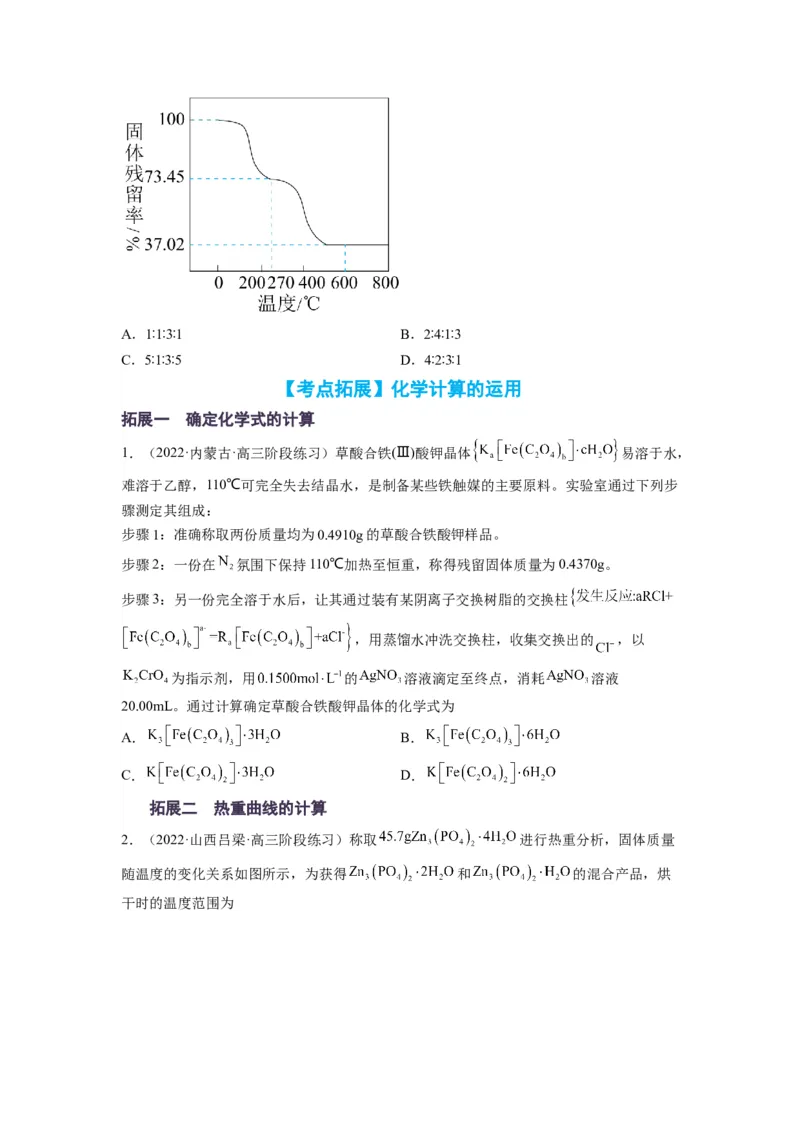
4.(2022·江西赣州·高三期中)碱式碳酸铝镁 常用作塑料阻
燃剂。为确定碱式碳酸铝镁的组成,进行如下实验:
Ⅰ.准确称取3.390g样品与足量稀盐酸充分反应,生成 (已换算成标准状况下)。
Ⅱ.另取一定量样品在空气中加热,样品的固体残留率( ×100%)随温
度的变化如图所示。(样品在270℃时已完全失去结晶水,600℃以上残留固体为金属氧化物
的混合物)
则 为A.1∶1∶3∶1 B.2∶4∶1∶3
C.5∶1∶3∶5 D.4∶2∶3∶1
【考点拓展】化学计算的运用
拓展一 确定化学式的计算
1.(2022·内蒙古·高三阶段练习)草酸合铁(Ⅲ)酸钾晶体 易溶于水,
难溶于乙醇,110℃可完全失去结晶水,是制备某些铁触媒的主要原料。实验室通过下列步
骤测定其组成:
步骤1:准确称取两份质量均为0.4910g的草酸合铁酸钾样品。
步骤2:一份在 氛围下保持110℃加热至恒重,称得残留固体质量为0.4370g。
步骤3:另一份完全溶于水后,让其通过装有某阴离子交换树脂的交换柱
,用蒸馏水冲洗交换柱,收集交换出的 ,以
为指示剂,用 的 溶液滴定至终点,消耗 溶液
20.00mL。通过计算确定草酸合铁酸钾晶体的化学式为
A. B.
C. D.
拓展二 热重曲线的计算
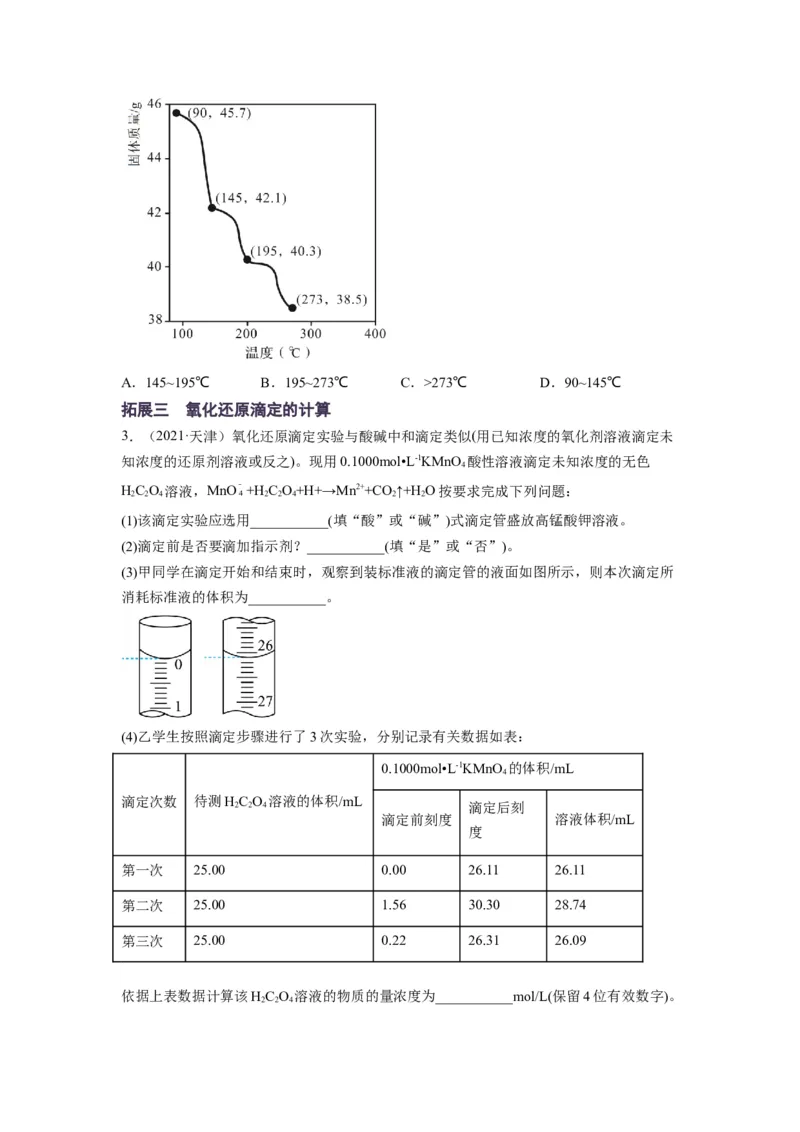
2.(2022·山西吕梁·高三阶段练习)称取 进行热重分析,固体质量
随温度的变化关系如图所示,为获得 和 的混合产品,烘
干时的温度范围为A.145~195℃ B.195~273℃ C.>273℃ D.90~145℃
拓展三 氧化还原滴定的计算
3.(2021·天津)氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未
知浓度的还原剂溶液或反之)。现用0.1000mol•L-1KMnO 酸性溶液滴定未知浓度的无色
4
HC O 溶液,MnO +H C O+H+→Mn2++CO ↑+H O按要求完成下列问题:
2 2 4 2 2 4 2 2
(1)该滴定实验应选用___________(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液。
(2)滴定前是否要滴加指示剂?___________(填“是”或“否”)。
(3)甲同学在滴定开始和结束时,观察到装标准液的滴定管的液面如图所示,则本次滴定所
消耗标准液的体积为___________。
(4)乙学生按照滴定步骤进行了3次实验,分别记录有关数据如表:
0.1000mol•L-1KMnO 的体积/mL
4
滴定次数 待测HC O 溶液的体积/mL
2 2 4 滴定后刻
滴定前刻度 溶液体积/mL
度
第一次 25.00 0.00 26.11 26.11
第二次 25.00 1.56 30.30 28.74
第三次 25.00 0.22 26.31 26.09
依据上表数据计算该HC O 溶液的物质的量浓度为___________mol/L(保留4位有效数字)。
2 2 4