文档内容
解密 02 化学常用计量
1.(2022·河北·石家庄精英中学高三阶段练习)下列叙述错误的是
①摩尔是国际单位制中七个基本物理量之一;
②1mol任何物质都含有约6.02×1023个原子;
③6.02×1023就是阿伏加德罗常数;
④氢原子的摩尔质量是1g;
⑤HCl的摩尔质量等于1molHCl分子的质量。
A.①②③ B.②③④ C.②③④⑤ D.全部
【答案】D
【解析】①摩尔是国际单位制中物质的量的单位,故错误;
②1mol任何物质都含有约6.02×1023个粒子,而物质不一定由单个原子构成,如氧气、二氧化碳等,故错误;
③阿伏加德罗常数的单位为mol-1,6.02×1023mol-1是阿伏加德罗常数的近似值,故错误;
④H的摩尔质量是1g·mol-1,故错误;
⑤HCl的摩尔质量以g·mol-1为单位时,数值上等于lmolHCl分子的质量(以克为单位),故错误;
故选D。
2.(2022·全国·高三专题练习)每年10月23日上午6:02到晚上6: 02被誉为“摩尔日”(MoleDay)。
下列说法正确的是
A.摩尔是物质的数量的单位
B.摩尔是联系宏观物质和微观粒子之间的物理量
C.二氧化碳的摩尔质量是44
D.0.5 mol HO中含有1 mol H
2
【答案】D
【解析】A.摩尔是物质的量的单位,不是物质的数量,A错误;
B.摩尔是物质的量的单位,不是物理量,B错误;
C.摩尔质量的单位为g/mol,二氧化碳的摩尔质量为44g/mol,C错误;
D.一个HO分钟含有2个H原子,则0.5 mol HO中含有1 mol H,D正确;
2 2
综上所述答案为D。
3.(2022·浙江温州·模拟预测)设[aX+bY]为a个X微粒和b个Y微粒组成的一个微粒集合体,N 为阿伏
A加德罗常数的值,下列说法正确的是
A.23gC HOH中C—H单键的数目为6N
2 5 A
B.20gND 溶于水形成的氨水溶液中质子数约为10N
3 A
C.常温下,pH=2的磷酸溶液中H+数目为0.01N
A
D.2SO
2
+O 2⇌2SO
3
,则每1mol[2SO
2
+O
2
]完全反应转移的电子数等于4N
A
【答案】D
【解析】A.23gC HOH的物质的量为 =0.5mol,一个C HOH分子含有5个C-H键,所以
2 5 2 5
23gC HOH中C—H单键的数目为2.5 N ,A错误;
2 5 A
B.20gND 的物质的量为 =1mol,但溶于水形成的氨水溶液中除了ND 中含有质子外,还有HO
3 3 2
中的质子,所以无法确定质子数,B错误;
C.溶液体积未知,无法确定溶液中的微粒数目,C错误;
D.每1mol[2SO +O ]完全反应,则有1molO 被还原,转移的电子数等于4N ,D正确;
2 2 2 A
综上所述答案为D。
4.(2022·福建·莆田一中高三期中)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.100g46%的乙醇水溶液中含有的氢原子数为6N
A
B.将22.4L(标准状况)Cl 通入足量水中,转移的电子数为N
2 A
C.12gNaHSO 固体中含阳离子数目为0.1N
4 A
D.64gSO 和32gO 混合,反应一段时间后总原子数为4N
2 2 A
【答案】C
【解析】A.100g46%的乙醇水溶液中含有乙醇分子 ,含有氢原子1mol×6×N /mol=
A
6N ,含有水的量为 ,含有氢原子3mol×2×N /mol=6N ,故溶液中共含有氢原子数
A A A
为12N ,故A错误;
A
B.氯气与水的反应为可逆反应,反应不能完全,将22.4L(标准状况)Cl 通入足量水中,转移的电子数
2
小于N ,故B错误;
A
C.12gNaHSO 固体中含阳离子数目为 ,故C正确;
4D.64gSO 和32gO 混合,含有子原总数为 ,故D错误;
2 2
故答案选C。
5.(2022·甘肃·高台县第一中学高三阶段练习)设 为阿伏加德罗常数的值。下列说法正确的是
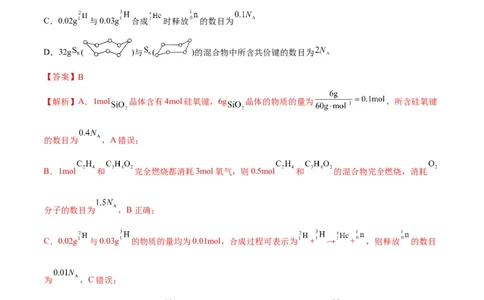
A.6g 晶体中所含硅氧键的数目约为
B.0.5mol 和 的混合物完全燃烧,消耗 分子的数目为
C.0.02g 与0.03g 合成 时释放 的数目为
D.32g ( )与 ( )的混合物中所含共价键的数目为
【答案】B
【解析】A.1mol 晶体含有4mol硅氧键,6g 晶体的物质的量为 ,所含硅氧键
的数目为 ,A错误;
B.1mol 和 完全燃烧都消耗3mol氧气,则0.5mol 和 的混合物完全燃烧,消耗
分子的数目为 ,B正确;
C.0.02g 与0.03g 的物质的量均为0.01mol,合成过程可表示为 + → + ,则释放 的数目
为 ,C错误;
D.32g 所含有共价键数目为 = ,32g 所含共价键数目为 = ,则32g
和 的混合物中所含共价键的数目为 ,D错误;故选B。
6.(2022·湖北·高三阶段练习)测定氯化钡晶体( )结晶水个数的步骤如下:准确称取
,配制 溶液,取 所配溶液,向其中滴加 溶液恰好使 沉淀完全。则 值为
A.2 B.4 C.6 D.8
【答案】C
【解析】 ;
,故 。
故选C。
7.(2021·全国·高三专题练习)某种元素原子的质量是ag,12C原子的质量是bg,N 是阿伏加德罗常数的
A
值,下列说法不正确的是
A.由已知信息可得N =
A
B.Wg该原子中含有 个该原子
C.Wg该原子的物质的量一定是 mol
D.该原子的摩尔质量是aN g
A
【答案】D
【解析】A.一个 原子的质量为bg,N 个 原子的质量为12g,可得N = ,故A正确;
A A
B.一个该原子的质量是ag,则Wg该原子的原子数目为 个,故B正确;
C.该原子的摩尔质量为aN g/mol,Wg该原子的物质的量为 mol,故C正确;
A
D.摩尔质量的单位是g/mol,该原子的摩尔质量是aN g/mol,故D错误;
A
综上所述,答案为D。
8.(2022·宁夏·银川市第六中学高三阶段练习) 和 的混合气体与 的NO比较,下列判断
错误的是
A.在同温同压下密度一定相等 B.在同温同体积下压强一定相等
C.在标准状况下体积一定相等 D.在任何状况下原子数一定相等
【答案】A
【解析】A.在同温同压下,物质的量相同所占的体积相同,但两组气体质量不一定相同,则密度不一定相等,故A错误;
B.根据理想气体状态方程式 可知在同温同体积下物质的量相同时压强一定相等,故B正确;
C.在标准状况下根据 可知,物质的量相同时体积一定相等,故C正确;
D.在任何状况下,物质的量相同则分子数相同,两组气体都是双原子分子,所以在任何状况下原子数一
定相等,故D正确;
故选A。
9.(2022·新疆石河子一中高三阶段练习)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.水溶液中,0.1molFeI 与0.2molCl 充分反应,转移的电子数为0.2N
2 2 A
B.已知核反应: U+ n→ Ba+ M+3 n,则1mol M中含中子数55N
A
C.1molAlCl 晶体中含有的Cl-数目为3N
3 A
D.1molZn与一定量浓硫酸反应后完全溶解,生成气体的体积(标准状况下)为22.4L
【答案】D
【解析】A.向溶质为0.1mol的FeI 溶液中通入0.2molCl ,反应为2FeI+3Cl=2FeCl +2I ,反应后氯气过
2 2 2 2 3 2
量,FeI 完全反应,FeI~3e-,则充分反应后转移的电子数为0.3N ,A错误;
2 2 A
B.已知核反应: ,则A=235+1-144-1 3=89,Z=92+0-56-0 3=36,中子数
N=A-Z=89-36=53,故 中含中子数= ,B错误;
C.AlCl 晶体为共价晶体,不含有Cl-,C错误;
3
D.根据反应Zn+2H SO (浓)=ZnSO +SO↑+2H O、Zn+H SO (稀)=ZnSO +H ↑,无论锌与浓硫酸还是稀硫酸
2 4 4 2 2 2 4 4 2
反应, 与一定量浓硫酸反应后完全溶解,生成气体的体积(标准状况下)为 ,D正确;
故选D。
10.(2022·四川省邻水县第二中学高三阶段练习)下列叙述正确的是
A.同温同压下,相同体积的任何气体,其原子数一定相等
B.同温同压下,相同质量的N 和NH 两种气体,其体积之比为17︰28
2 3
C.同温同压下,N 个NO与N 个N 和O 的混合气体的体积不相等
A A 2 2
D.温度和密度相同的CO、N 和H 三种气体,其压强(p)关系为p(CO)=p(N )>p(H )
2 2 2 2
【答案】B
【解析】A.依据阿伏加德罗定律,同温同压下,相同体积的任何气体,物质的量相同,但由于分子组成
不一定相同,所以其原子数不一定相等,A不正确;B.同温同压下,气体摩尔体积相同,相同质量的N 和NH 两种气体,物质的量之比为17︰28,则其体积
2 3
之比为17︰28,B正确;
C.同温同压下,气体摩尔体积相同,N 个NO与N 个N 和O 的混合气体物质的量相同,则它们的体积
A A 2 2
相等,C不正确;
D.温度和密度相同的CO、N 和H 三种气体,假设它们的体积相同,则质量相等,物质的量之比为
2 2
1:1:14,则其压强(p)关系之比为1:1:14,所以p(CO)=p(N )<p(H ),D不正确;
2 2
故选B。
11.(2022·内蒙古·高三阶段练习)标准状况下,在甲室中充入25.5gNH 与17gH 的混合气体,乙室中充
3 2
入HCl与N 的混合气体,静止时活塞位置如图。已知乙室中气体的质量比甲室中气体的质量多123g。将
2
活塞a去掉,当HCl与NH 完全反应后,活塞b将静止于刻度的位置是
3
A.11 B.12 C.13 D.14
【答案】B
【解析】n(NH )= =1.5mol,n(H )= =8.5mol,乙室中气体的质量比甲室中气体的质量多
3 2
123g,则乙室气体质量为123g+25.5g+17g=165.5g。n(NH )+ n(H )=1.5mol+8.5mol=10mol,占10格,而
3 2
HCl、N 占5格,则其物质的量为5mol。设HCl的物质的量为x,则N 的物质的量为5-x,36.5x+28(5-
2 2
x)=165.5,从而求出x=3mol,HCl为3mol,N 为2mol。
2
将活塞a去掉,当HCl与NH 完全反应后,NH 无剩余,剩余HCl1.5mol、H8.5mol、N2mol,混合气共计
3 3 2 2
12mol。因为活塞b与大气相通,室内压强与大气压强相同,且1格气体物质的量为1mol,则12mol混合
气占据12格,故选B。
12.(2022·辽宁沈阳·高三阶段练习)阿伏加德罗常数的值为N ,下列说法正确的是
A
A.物质的量浓度为0.5mol/L的 溶液中,含有 的数目为N
A
B.100gCaS与 的混合物中含有32g硫,则含有的氧原子数目为1.75N
A
C.将100ml 1mol/L 溶液水解制成胶体,所得胶体粒子数目为0.1N
AD. 与 溶液混合产生22.4L气体时,转移电子数目为2N
A
【答案】B
【解析】A.溶液体积不明确,故溶液中的氯离子的个数无法计算,A项错误;
B.100gCaS与CaSO 的混合物中钙元素、硫元素和氧元素质量总和为100g,其中硫元素32g,钙元素和硫元
4
素物质的量之比为1:1,计算得到钙元素质量为40g,得到氧元素质量 ,含有氧原
子数为: ,B项错误;
C.一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故所得的胶粒的个数小于0.1N 个 ,C项错误;
A
D.NaSO 与HSO 溶液混合产生二氧化硫气体,不是标况下,不能使用22.4L/mol计算生成二氧化硫的
2 2 3 2 4
物质的量,则无法计算转移电子的量,D项错误,
故选B。
13.(2022·海南·琼中中学高三阶段练习) 溶液中含有 ,取 该溶液用水稀释至
VmL,则稀释后 物质的量浓度为
A. B. C. D.
【答案】B
【解析】VmLAl (SO ) 溶液中含有Al3+mg,则 的物质的量为 mol,取 mL该溶液稀释至VmL,
2 4 3
则 的物质的量为 mol,则其物质的量浓度为 mol÷(V×10-3)L= ,故答案选B。
14.(2022·安徽省阜阳第一中学高三阶段练习) 为阿伏加德罗常数的值,下列说法错误的是
A.常温下,11.2L氯气所含的原子数小于
B.1mol Fe与足量氯气完全反应转移的电子数约为
C.标准状况下,3.36L HF含有氢氟键的数目为0.15D.标准状况下,11.2L NO与11.2L 混合后的分子数目可能为0.65
【答案】C
【解析】A.常温下11.2L氯气的物质的量小于0.5mol,原子数小于N ,A正确;
A
B.铁与氯气反应生成氯化铁,所以1molFe失去电子数约为 ,B正确;
C.标况下,氟化氢为液态,无法计算,C错误;
D.标况下,11.2LNO与11.2LO2混合后发生反应2NO+O =2NO,生成0.5molNO 并剩余0.25molO,气
2 2 2 2
体总的物质的量为0.75mol,但存在 ,则反应后的气体总的物质的量小于0.75mol大于
0.5mol,即所含分子数小于0.75N 大于0.5N ,D正确;
A A
故选C。
15.(2022·辽宁实验中学高三期中)下列叙述中正确的是
A.溶质质量分数为23%和10%的氨水等质量混合,混合液的溶质质量分数小于16.5%
B.同种溶质不同浓度的两种溶液混合,计算时可将体积直接加和
C.若溶质质量分数为 的乙醇溶液的物质的量浓度为 ,则将其加水稀释至溶质质量分数为 ,
所得稀溶液物质的量浓度大于
D.某溶液密度为 ,溶质摩尔质量为 ,若物质的量浓度为 ,则该溶液的溶质质量分
数为
【答案】C
【解析】A.溶质质量分数为23%和10%的氨水等质量混合,假设质量均为m,则混合液的溶质质量分数
,故A错误;
B.构成物质的微粒之间有间隔,且同种溶质不同浓度的两种溶液的密度不同,两者混合,计算时不可将
体积直接加和,故B错误;
C.由 可知,c=2y= ,铜离子稀释后c= , ,
1 2,乙醇密度小于水,则 ,故 ,故C正确;
D.由 可知,某溶液密度为 ,溶质摩尔质量为 ,若物质的量浓度为 ,则该
溶液的溶质质量分数为 ,故D错误;
故选C。
16.(2022·全国·高三专题练习)关于0.1 mol·L-1 HNO 溶液的叙述错误的是
3
A.1 L该溶液中含有HNO 的质量为6.3 g
3
B.0.5 L该溶液中氢离子的物质的量浓度为0.1 mol·L-1
C.从1 L该溶液中取出100 mL,则取出溶液中HNO 的物质的量浓度为0.01 mol·L-1
3
D.取该溶液10 mL,加水稀释至100 mL后HNO 的物质的量浓度为0.01 mol·L-1
3
【答案】C
【解析】A.1L该HNO 溶液中含有溶质的物质的量n=cV=0.1mol/L×1L=0.1mol,则其中含有溶质的质量
3
m=0.1mol×63g/mol=6.3g,A项正确;
B.硝酸为一元强酸,则0.5 L该溶液中氢离子的物质的量浓度为0.1 mol·L-1,B项正确;
C.溶液具有均一性,溶液的浓度与其取出的体积大小无关,所以从1L该溶液中取出100mL,则取出的溶
液中HNO 的物质的量浓度仍为0.1mol/L,C项错误;
3
D.溶液在稀释过程中溶质的物质的量不变,所以稀释后溶液的浓度c= =0.01mol/L,D
项正确;
答案选C。
1.(2022·全国·高三专题练习)下列说法中不正确的是
A.物质的量是一个物理量,物质的量的单位是摩尔
B. 水的摩尔质量是 水的摩尔质量的 倍
C.摩尔质量、气体摩尔体积的单位分别是 、
D.标准状况下, 二氧化碳和 一氧化碳所含有的原子数目相等
【答案】B【解析】A.物质的量是一个物理量,物质的量的单位是摩尔,故A正确;
B.水的摩尔质量是18g/mol,与物质的量的多少无关,故B错误;
C.摩尔质量的单位为 ,气体摩尔体积的单位为 ,故C正确;
D.标准状况下, 2L二氧化碳含有的原子的物质的量为 ×3= mol,和3L一氧化碳含有的原子
的物质的量为 ×2= mol,所含有的原子数目相等,故D正确;
故选B。
2.(2022·浙江·高考真题)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
【答案】A
【解析】A.1LpH为12的Ba(OH) 溶液中含有OH-的浓度为0.01mol/L,物质的量0.01mol/L
2
1L=0.01mol,OH-的数目为0.01N ,A正确;
A
B.1.8g重水(D O)的物质的量为:0.09mol,所含质子数为0.9N ,B错误;
2 A
C.足量的浓盐酸与8.7gMnO(0.1mol)反应,+4价Mn转化生成Mn2+,转移电子的数目为0.2N ,C错误;
2 A
D.甲醇的结构简式为:CHOH,32g (1mol)的分子中含有C—H键的数目为3N ,D错误;
3 A
答案选A。
3.(2022·广东佛山·模拟预测)下图是试剂标签上的部分内容。据此,下列说法错误的是
硫酸 化学纯 CP500
mL品名:硫酸
化学式:
相对分子质量:98
密度:
质量分数:98%
A.该硫酸物质的量浓度为
B.100mL该硫酸中,氧原子的数目大于7.36N
AC.取100mL该硫酸与足量铜反应,产生 的分子数小于0.92N
A
D.将该硫酸稀释至 ,溶液中 的数目为0.1 N
A
【答案】D
【解析】A.该硫酸物质的量浓度为 mol∙L-1= ,A正确;
B.100mL该硫酸溶液中,硫酸中含有的氧原子的数目为1.84mol/L×0.1N =7.36N ,该硫酸溶液中还含有水,
A A
水中含有氧原子,则氧原子的数目大于7.36N ,B正确;
A
C.取100mL该硫酸与足量铜反应,2HSO (浓)——SO ,因为稀硫酸不能与铜反应,所以产生 的分子
2 4 2
数小于 =0.92N ,C正确;
A
D.该硫酸溶液的体积未知,由 ,可求出c(H+),但无法求出溶液中 的数目,D不正确;
故选D。
4.(2022·全国·模拟预测)硫在不同温度下的状态和分子结构不同,单质硫S 环状分子的结构如图。
8
717.6K时硫变为蒸气,蒸气中存在:3S 4S 6S 12S。下列说法错误的是
8 6 4 2
A.S、S、S、S 互为同素异形体,其相互转化为化学变化
8 6 4 2
B.720K时,32gS 中含有的硫原子数为1mol
8
C.可用酒精洗涤试管中残留的硫单质
D.硫单质与少量的铁粉加热时,生成的产物为FeS
【答案】B
【解析】A.同素异形体是由同种元素形成的不同单质,S、S、S、S 互为同素异形体,同素异形体属于
8 6 4 2
不同物质,之间的转化为化学变化,A正确;
B.720K时,不管S以何种形式存在,S原子的总物质的量不变,32gS 中含有的硫的物质的量为
8
×8=1mol,个数为1N ,B错误;
A
C.硫是难溶于水,微溶于酒精,因此可用酒精洗涤试管中残留的硫单质,C正确;D.Fe与S反应生成FeS,S+Fe FeS,D正确;
故选B。
5.(2022·上海)元素X与Y组成A、B两种化合物,A中X的质量占 ,B中X的质量占 ,则化合物
A和B的分子式分别是 ( )
A.XY和XY B.XY和XY C.XY 和XY D.XY 和XY
2 2 2 3 2 2 3 2 4
【答案】D
【解析】A中X的质量占 ,B中X的质量占 ,B中X的质量分数大于A中X的质量分数,由选项确
定化合物的化学式。
A.由XY和XY 可知,A、B中X、Y的原子个数之比分别为1:1、1:2,则B中X的质量分数小,A错
2
误;
B.由XY和XY 可知,A、B中X、Y的原子个数之比分别为2:1、2:3,则B中X的质量分数小, B
2 2 3
错误;
C.由XY 和XY可知,A、B中X、Y的原子个数之比分别为1:2、2:1,则B中X的质量分数大,但
2 2
A中X与Y 的质量比为14:3,则B中X与Y的质量比应为56:3,不符合题意, C错误;
2
D.由XY 和XY 可知,A、B中X、Y的原子个数之比分别为1:3、1:2,则B中X的质量分数大,且
3 2 4
A中X与Y 的质量比为14:3,XY 中X与Y的原子个数比为1:3,则A中X原子与Y原子的质量比为
3 3
14:1,B中X 与Y 的质量比应为7:1,符合题意,D正确。
2 4
答案为D。
6.(2022·全国)下列选项中的物质所含指定原子数目一定相等的是( )
A.温度和压强不同,相同质量的一氧化二氮和二氧化碳两种气体的总原子数
B.等温等压下,相同体积的乙烯和乙炔、乙烷的混合气体的总原子数
C.等温等压下,相同体积的氧气和臭氧两种气体中的氧原子数
D.相同物质的量、不同体积的氨气和甲烷两种气体中的氢原子数
【答案】A
【解析】A项:NO和CO 摩尔质量都是44g/mol,相同质量时两种气体的分子总数、原子总数都相等,A
2 2
项正确;
B项:据阿伏加德罗定律,等温等压下,相同体积的乙烯和乙炔、乙烷的混合气体的分子总数相同,其原
子总数不一定相等;C项:据阿伏加德罗定律,等温等压相同体积的氧气和臭氧分子总数相同,氧原子数之比为2:3;
D项:相同物质的量的氨气和甲烷两种气体中,分子数相等,氢原子数之比为3:4;
本题选A。
7.(2022·四川巴中·模拟预测)N 为阿伏伽德罗常数的值,下 列说法正确的是
A
A.1mol DO比1mol HO多N 个质子
2 2 A
B.密闭容器中,2mol SO 和 1mol O 发生催化反应后分子总数小于2N
2 2 A
C.32g 异戊烷和40g新戊烷的混合物中共价键的数目为16N
A
D.C H 和C HO混合气体2.24L,完全燃烧,消耗O 的体积一定为6.72L
2 4 2 6 2
【答案】C
【解析】A. D与H相比,质子数相同,中子数多1,1 mol D O比1 mol H O多2N 个中子,故A错误;
2 2 A
B. 密闭容器中,2 mol SO 和1 mol O 催化反应为可逆反应,反应物不能完全转化为生成物,反应后气体
2 2
总分子数大于2N ,故B错误;
A
C. 32g异戊烷和40g新戊烷,共计72g,异戊烷与新戊烷相对分子质量相同为72,故混合物为1mol,混
合物中共价键的数目为16N ,故C正确;
A
D. 没有标明是标准状况,无法计算,故D错误;
故选C。
8.(2022·山东·模拟预测)三种气体X、Y、Z的相对分子质量关系为 ,下列说法
正确的是
A.原子数目相等的三种气体,质量最大的是Z
B.相同条件下,同质量的三种气体,气体密度最小的是X
C.若一定条件下,三种气体体积均为 ,则它们的物质的量一定均为
D.同温下,体积相同的两容器分别充 气体和 气体,则其压强比为2∶1
【答案】B
【解析】A.根据m=nM= M,分子数目相等的三种气体,NA质量最大的是相对分子质量最大的Z,原
子数目相等的三种气体,质量最大的无法判断,A错误;
B.根据密度p= ,气体处在相同的条件下,则密度和相对分子质量成正比,三种气体密度最小的是X,
B正确;C.气体的物质的量n= 和气体的状态有 关,三种气体体积均为2.24L,V 不一定等于22.4L/mol,所以
m
它们的物质的量不一定均为0.1mol,C错误;
D.同温下,体积相同的两容器分别充2gY气体和1gZ气体,Mr(Y)=0.5Mr(Z),则二者的物质的量之比是
4:1,同温同体积的气体物质的量之比等于压强之比,Y、Z气体所承受的压强比为4:1,D错误;
答案选B。
9.(2022·江苏南京·模拟预测)下列条件下,两瓶气体所含原子数一定相等的是
A.同质量、不同密度的N 和CO B.同温度、同体积的H 和N
2 2 2
C.同体积、不同密度的C H 和C H D.同压强、同体积的NO和CO
2 4 3 6 2 2
【答案】A
【解析】A、二者同质量,摩尔质量也相同,根据n= 知,二者分子物质的量相同,也就是分子数相同,
这两种分子还都含有2个原子,所以原子数相同,故A正确;
B、同温度、同体积,气体分子数目与压强呈正比,压强不定,无法判断气体分子数关系,故B错误;
C、同体积、不同密度的C H 和C H,质量不相等。C H 和C H 的最简式相同,质量相等的两种气体含有
2 4 3 6 2 4 3 6
相同的原子数,但质量不相等,则所含原子数不一定相同,故C错误;
D、同压强、同体积,气体分子数目与温度呈反比,温度不定,无法判断气体分子数关系,故D错误;
故选:A。
10.(2022·上海·模拟预测) 溶液中含有 ,取 该溶液用水稀释至VmL,则稀
释后 物质的量浓度为
A. B. C. D.
【答案】B
【解析】VmLAl (SO ) 溶液中含有Al3+mg,则 的物质的量为 mol,取 mL该溶液稀释至VmL,
2 4 3
则 的物质的量为 mol,则其物质的量浓度为 mol÷(V×10-3)L= ,故答案选B。
11.(2022·江西)某实验需要100 mL、1 mol/L的NaCO 溶液,现通过如下操作配制:
2 3
①把称量好的固体NaCO 放入小烧杯中,加适量蒸馏水溶解。为加快溶解可以用玻璃棒搅拌;
2 3
②把①所得溶液冷却到室温后,小心转入到容量瓶中③继续加蒸馏水至液面至刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面最低点与刻度线
相切;
④用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都小心转入容量瓶,并轻轻摇匀;
⑤将容量瓶塞紧,充分摇匀。
(1)操作步骤正确的顺序是(填序号)。①②_______⑤
(2)若没有操作④,则所配溶液的浓度会__________(填“偏高”或“偏低”)。
(3)若所配溶液的密度为1.06 g/mL,则该溶液的质量分数为_________ 。
(4)在配制100 mL、1 mol/L的NaCO 溶液时,下列操作中的_______ 会导致结果偏低(请用序号填
2 3
写)
①用托盘天平称量时砝码放在左盘
②将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
③定容时俯视刻度线
④定容时仰视刻度线
【答案】 (1) ④③ (2) 偏低 (3) 10% (4) ①②④
【解析】试题分析:没有80mL的容量瓶,所以应选择100mL容量瓶.即所配溶液体积为100mL,所以需
NaCO 的质量为m=0.1L×1mol•L-1×106g/mol=10.6g。
2 3
(1)操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,正确的操作顺序是
①②④③⑤,故答案为①②④③⑤;
(2)若没有操作④,则所配溶液中溶质的物质的量偏小,浓度偏低,故答案为偏低;
(3)根据c= 可知,碳酸钠溶液的质量分数ω= = =10%,故答案为10%;
(4)①称量碳酸钠固体时,砝码和物质的位置对调,如未使用游码,对碳酸钠的质量无影响,对所配溶
液浓度无影响;若使用游码,碳酸钠的实际质量减小,所配溶液的浓度偏低.本题碳酸钠质量为10.6
g,使用游码,所配溶液浓度偏低;②向容量瓶中转移溶液时,有溶液洒落在容量瓶外,转移到容量瓶中
碳酸钠的质量减小,所配溶液浓度偏低;③定容时,俯视容量瓶刻度线,使溶液的体积偏低,所以溶液浓
度偏高;④定容时,仰视容量瓶刻度线,使溶液的体积偏大,所以溶液浓度偏低;故选①②④。
12.(2022·浙江杭州·二模)以下方法常用于对废水中的苯酚进行定量测定:取 含苯酚废水,加
过量溴水使苯酚完全反应,煮沸,再加入过量 溶液生成三溴苯酚,再用 标准溶液滴定至终点,消耗 溶液 .已知
(三溴苯酚)
. 和 溶液颜色均为无色.
(1)消耗 的物质的量为________.
(2)废水中苯酚的物质的量浓度为_______(写出简要计算过程).
【答案】(1)
(2)
【解析】(1)滴定至终点时消耗 溶液 , 的浓度为 ,则消耗
的物质的量为 ;
(2)根据反应的方程式可知: ,则 ,即苯酚的物质的量为
,其体积为 ,则其浓度为 。