文档内容
解密 03 氧化还原反应
一、选择题
1.(2021·广东湛江市期末)根据反应2KClO+I =2KIO+Cl↑判断,下列结论不正确的是( )
3 2 3 2
A.I 具有还原性 B.当生成22.4LCl 时,转移10mol电子
2 2
C.KIO 是氧化产物 D.该反应属于置换反应
3
2.(2021·江苏盐城市期末)工业上曾经通过反应“3Fe+4NaOH Fe O+2H ↑+4Na↑”生产金属钠。下
3 4 2
列有关说法正确的是( )
A. 失去电子,作氧化剂
B. 得到电子,发生氧化反应
C.将生成的气体在空气中冷却可获得钠
D.每生成1molNa,转移的电子数为2×6.02×1023
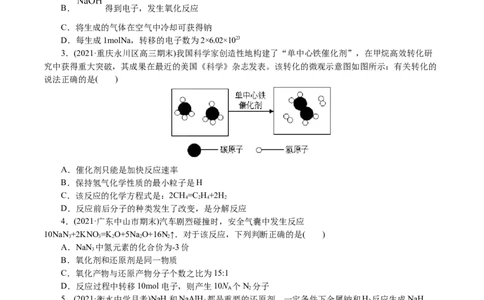
3.(2021·重庆永川区高三期末)我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研
究中获得重大突破,其成果在最近的美国《科学》杂志发表。该转化的微观示意图如图所示:有关转化的
说法正确的是( )
A.催化剂只能是加快反应速率
B.保持氢气化学性质的最小粒子是H
C.该反应的化学方程式是:2CH=C H+2H
4 2 4 2
D.反应前后分子的种类发生了改变,是分解反应
4.(2021·广东中山市期末)汽车剧烈碰撞时,安全气囊中发生反应
10NaN +2KNO =K O+5Na O+16N↑.对于该反应,下列判断正确的是( )
3 3 2 2 2
A.NaN 中氮元素的化合价为-3价
3
B.氧化剂和还原剂是同一物质
C.氧化产物与还原产物分子个数之比为15:1
D.反应过程中转移10mol电子,则产生10N 个N 分子
A 2
5.(2021·衡水中学月考)NaH和NaAlH 都是重要的还原剂,一定条件下金属钠和H 反应生成NaH。
4 2
NaH与水反应可生成H,NaH与AlCl 反应可得到NaAlH 。下列说法错误的是( )
2 3 4
A.NaAlH 中阴离子空间构型为正四面体
4
B.NaH与AlCl 得到NaAlH 的反应属于氧化还原反应
3 4
C.NaH在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe O)
2 3
D.金属钠和H 反应生成NaH的反应体系需要控制无氧、无水和无酸等条件
2
6.(2021·湖北恩施土家族苗族自治州高三月考)已知NH CuSO 与足量的10 mol/L硫酸混合微热,产生
4 3
下列现象:①有红色金属生成;②产生刺激性气味的气体;③溶液呈现蓝色。据此判断下列说法正确的是(
)
A.反应中硫酸作氧化剂 B.NH CuSO 中氮元素被氧化
4 3
C.刺激性气味的气体是SO D.1 mol NH CuSO 完全反应转移1 mol电子
2 4 37.(2021·吉林油田第十一中学高三月考)Na FeO 是一种高效的水处理剂,下列用于解释事实的离子方
2 4
程式中不正确的是
A.NaFeO 在酸性溶液中不稳定,与水反应生成Fe3+和O,离子方程式为:4FeO2-+10HO+4Fe3+
2 4 2 4 2
===20OH-+3O↑
2
B.工业上可用FeCl 、NaOH、NaClO三种物质反应制得NaFeO 离子方程式为:2Fe3++10OH-+
3 2 4
3ClO-===2FeO2-+3Cl-+5HO
4 2
C.NaFeO 消毒杀菌时得到的Fe3+可以净水,Fe3+能产生净水物质的原因是:Fe3++
2 4
3HO===Fe(OH) (胶体)+3H+
2 3
D.工业上可用铁做阳极,电解浓NaOH溶液的方法制NaFeO,阳极的电极反应为:Fe-6e-+8OH-
2 4
===FeO2-+4HO
4 2
8.(2021·任丘市第一中学高三月考)已知:KClO+C+S KCl+CO ↑+SO↑,下列判断不正确的是(
3 2 2
)
A.若反应中C和S的质量比为3:4,则n(KClO):n(CO)为1:1
3 2
B.若反应中C和S的质量比为3:16,则n(KClO):n(CO)为2:1
3 2
C.SO 通入NaHCO 溶液产生CO,可证明非金属性S强于C
2 3 2
D.KClO 与SO 在强酸性溶液中反应制得ClO ,可证明SO 的还原性强于ClO
3 2 2 2 2
9.(2021·甘肃武威市武威十八中高三期末)从矿物学资料查得,一定条件下自然界存在如下反应:
14CuSO +5FeS +12H O═7Cu S+5FeSO +12H SO ,下列说法正确的是( )
4 2 2 2 4 2 4
A.Cu S既是氧化产物又是还原产物
2
B.5mol FeS 发生反应,有10mol电子转移
2
C.产物中的SO 2-离子有一部分是氧化产物
4
D.FeS 只作还原剂
2
10.(2021·天津期末)用0.2mol/L Na SO 溶液32mL,还原含4×10-3molXO 2-的溶液,过量的NaSO 用
2 3 4 2 3
0.2mol/L KMnO 酸性溶液氧化(其中KMnO 被还原成Mn2+),共消耗KMnO 溶液0.8mL,则元素X在还原
4 4 4
产物中的化合价是( )
A.+1 B.+2 C.+3 D.+4
11.(2021·涡阳县育萃高级中学月考)在水溶液中,CrO2-呈黄色,Cr O2-呈橙色,重铬酸钾(K Cr O)在
4 2 7 2 2 7
水溶液中存在以下平衡:Cr O2-+H O 2CrO2-+2H+,下列说法正确的是( )
2 7 2 4
A.向该溶液中滴加适量的NaHSO 固体,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度比
4
原溶液大
B.该反应是氧化还原反应
C.向该溶液中加入过量浓NaOH溶液后,溶液呈橙色
D.向体系中加入少量水,平衡逆向移动
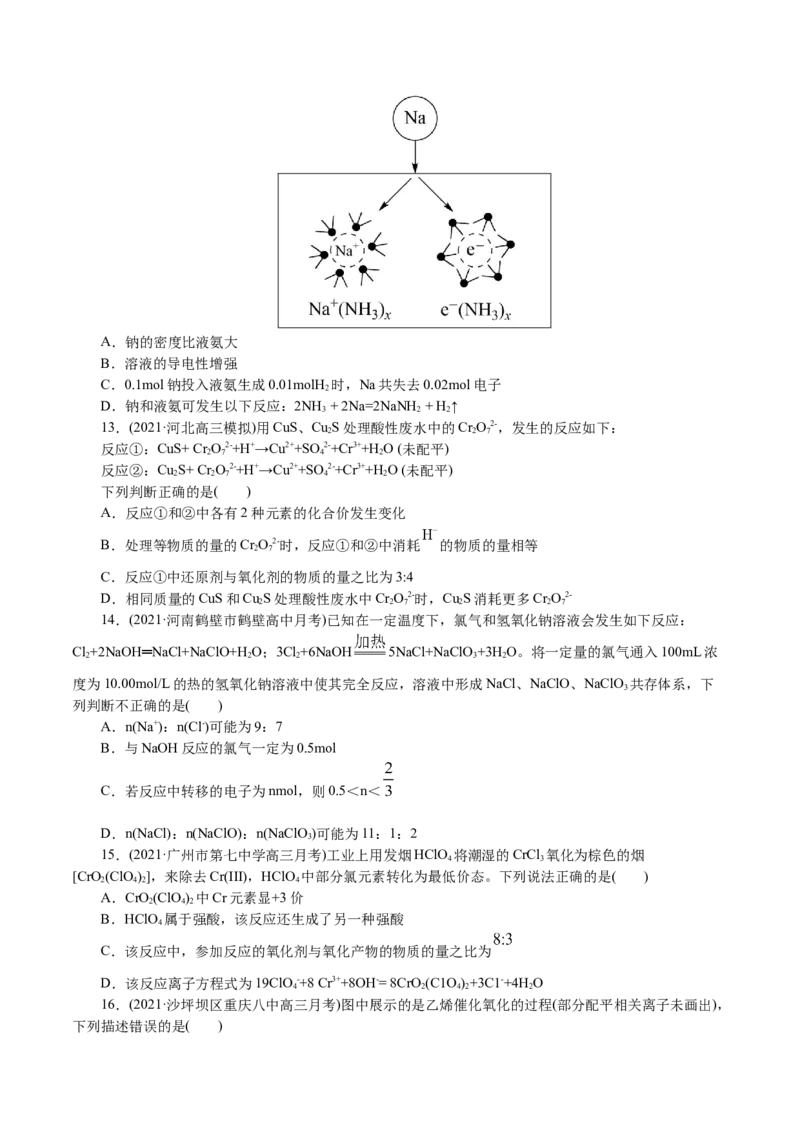
12.(2021·福建高三零模)钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,下图为钠投入液氨中
的溶剂化图。钠沉入液氨中,快速得到深蓝色溶液,并慢慢产生气泡。下列说法错误的是( )A.钠的密度比液氨大
B.溶液的导电性增强
C.0.1mol钠投入液氨生成0.01molH 时,Na共失去0.02mol电子
2
D.钠和液氨可发生以下反应:2NH + 2Na=2NaNH + H ↑
3 2 2
13.(2021·河北高三模拟)用CuS、Cu S处理酸性废水中的Cr O2-,发生的反应如下:
2 2 7
反应①:CuS+ Cr O2-+H+→Cu2++SO2-+Cr3++H O (未配平)
2 7 4 2
反应②:Cu S+ Cr O2-+H+→Cu2++SO2-+Cr3++H O (未配平)
2 2 7 4 2
下列判断正确的是( )
A.反应①和②中各有2种元素的化合价发生变化
B.处理等物质的量的Cr O2-时,反应①和②中消耗 的物质的量相等
2 7
C.反应①中还原剂与氧化剂的物质的量之比为3:4
D.相同质量的CuS和Cu S处理酸性废水中Cr O2-时,Cu S消耗更多Cr O2-
2 2 7 2 2 7
14.(2021·河南鹤壁市鹤壁高中月考)已知在一定温度下,氯气和氢氧化钠溶液会发生如下反应:
Cl+2NaOH═NaCl+NaClO+H O;3Cl+6NaOH 5NaCl+NaClO +3H O。将一定量的氯气通入100mL浓
2 2 2 3 2
度为10.00mol/L的热的氢氧化钠溶液中使其完全反应,溶液中形成NaCl、NaClO、NaClO 共存体系,下
3
列判断不正确的是( )
A.n(Na+):n(Cl-)可能为9:7
B.与NaOH反应的氯气一定为0.5mol
C.若反应中转移的电子为nmol,则0.5<n<
D.n(NaCl):n(NaClO):n(NaClO)可能为11:1:2
3
15.(2021·广州市第七中学高三月考)工业上用发烟HClO 将潮湿的CrCl 氧化为棕色的烟
4 3
[CrO (ClO )],来除去Cr(III),HClO 中部分氯元素转化为最低价态。下列说法正确的是( )
2 4 2 4
A.CrO (ClO ) 中Cr元素显+3价
2 4 2
B.HClO 属于强酸,该反应还生成了另一种强酸
4
C.该反应中,参加反应的氧化剂与氧化产物的物质的量之比为
D.该反应离子方程式为19ClO -+8 Cr3++8OH-= 8CrO (C1O)+3C1-+4H O
4 2 4 2 2
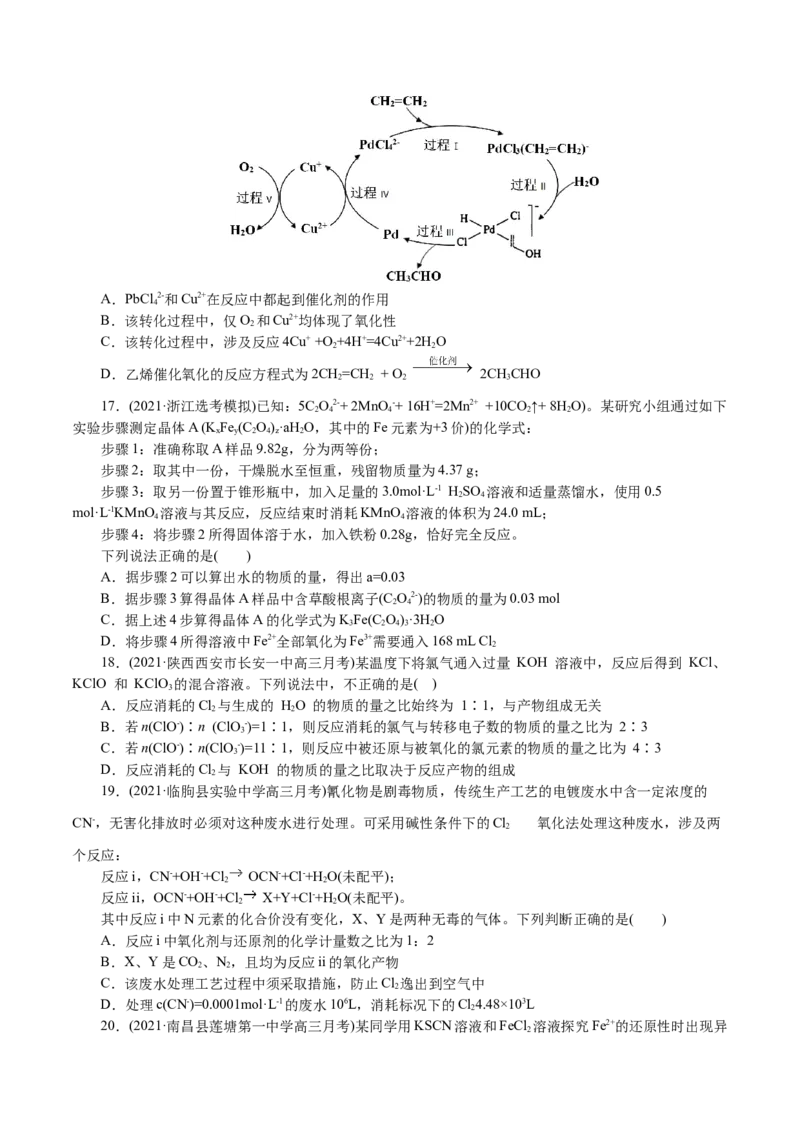
16.(2021·沙坪坝区重庆八中高三月考)图中展示的是乙烯催化氧化的过程(部分配平相关离子未画出),
下列描述错误的是( )A.PbCl 2-和Cu2+在反应中都起到催化剂的作用
4
B.该转化过程中,仅O 和Cu2+均体现了氧化性
2
C.该转化过程中,涉及反应4Cu+ +O +4H+=4Cu2++2H O
2 2
D.乙烯催化氧化的反应方程式为2CH=CH + O 2CHCHO
2 2 2 3
17.(2021·浙江选考模拟)已知:5C O2-+ 2MnO -+ 16H+=2Mn2+ +10CO ↑+ 8H O)。某研究小组通过如下
2 4 4 2 2
实验步骤测定晶体A (K Fe (C O)·aHO,其中的Fe元素为+3价)的化学式:
x y 2 4 z 2
步骤1:准确称取A样品9.82g,分为两等份;
步骤2:取其中一份,干燥脱水至恒重,残留物质量为4.37 g;
步骤3:取另一份置于锥形瓶中,加入足量的3.0mol·L-1 HSO 溶液和适量蒸馏水,使用0.5
2 4
mol·L-1KMnO 溶液与其反应,反应结束时消耗KMnO 溶液的体积为24.0 mL;
4 4
步骤4:将步骤2所得固体溶于水,加入铁粉0.28g,恰好完全反应。
下列说法正确的是( )
A.据步骤2可以算出水的物质的量,得出a=0.03
B.据步骤3算得晶体A样品中含草酸根离子(C O2-)的物质的量为0.03 mol
2 4
C.据上述4步算得晶体A的化学式为KFe(C O)·3H O
3 2 4 3 2
D.将步骤4所得溶液中Fe2+全部氧化为Fe3+需要通入168 mL Cl
2
18.(2021·陕西西安市长安一中高三月考)某温度下将氯气通入过量 KOH 溶液中,反应后得到 KCl、
KClO 和 KClO 的混合溶液。下列说法中,不正确的是( )
3
A.反应消耗的Cl 与生成的 HO 的物质的量之比始终为 1∶1,与产物组成无关
2 2
B.若n(ClO-)∶n (ClO -)=1∶1,则反应消耗的氯气与转移电子数的物质的量之比为 2∶3
3
C.若n(ClO-)∶n(ClO -)=11∶1,则反应中被还原与被氧化的氯元素的物质的量之比为 4∶3
3
D.反应消耗的Cl 与 KOH 的物质的量之比取决于反应产物的组成
2
19.(2021·临朐县实验中学高三月考)氰化物是剧毒物质,传统生产工艺的电镀废水中含一定浓度的
CN-,无害化排放时必须对这种废水进行处理。可采用碱性条件下的Cl 氧化法处理这种废水,涉及两
2
个反应:
反应i,CN-+OH-+Cl OCN-+Cl-+H O(未配平);
2 2
反应ii,OCN-+OH-+Cl X+Y+Cl-+H O(未配平)。
2 2
其中反应i中N元素的化合价没有变化,X、Y是两种无毒的气体。下列判断正确的是( )
A.反应i中氧化剂与还原剂的化学计量数之比为1:2
B.X、Y是CO、N,且均为反应ii的氧化产物
2 2
C.该废水处理工艺过程中须采取措施,防止Cl 逸出到空气中
2
D.处理c(CN-)=0.0001mol·L-1的废水106L,消耗标况下的Cl4.48×103L
2
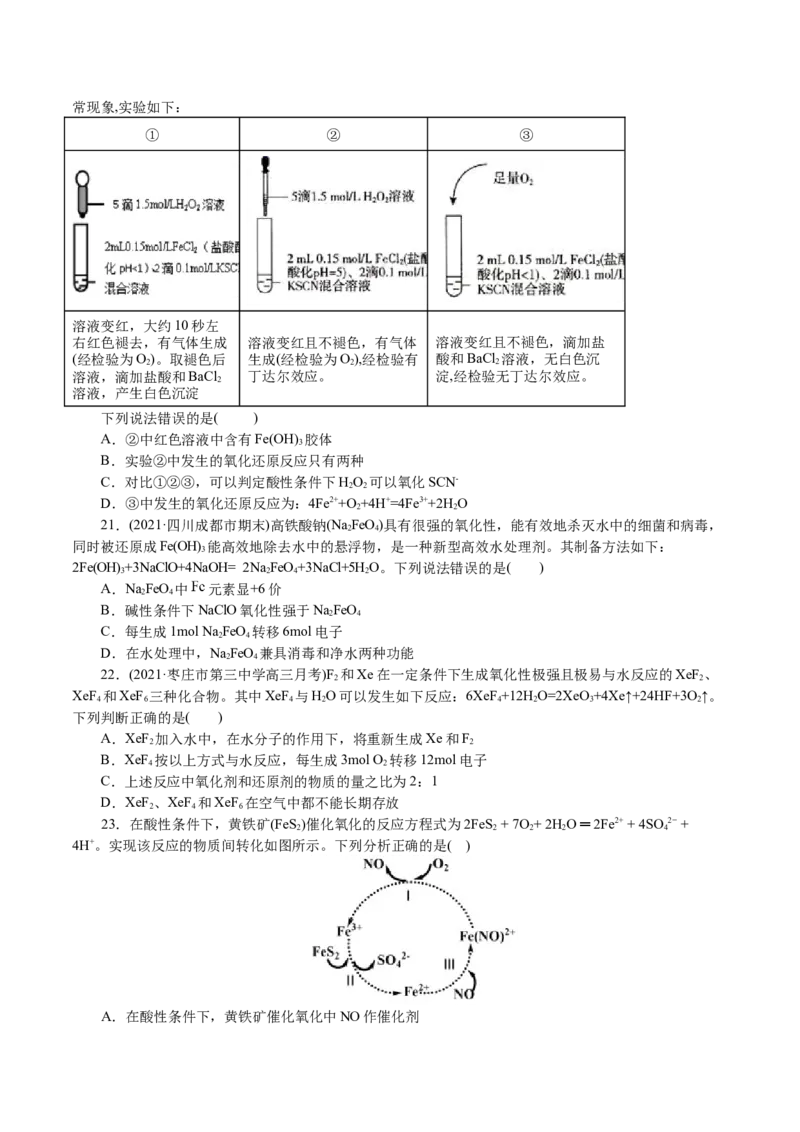
20.(2021·南昌县莲塘第一中学高三月考)某同学用KSCN溶液和FeCl 溶液探究Fe2+的还原性时出现异
2常现象,实验如下:
① ② ③
溶液变红,大约10秒左
右红色褪去,有气体生成 溶液变红且不褪色,有气体 溶液变红且不褪色,滴加盐
(经检验为O)。取褪色后 生成(经检验为O),经检验有 酸和BaCl 溶液,无白色沉
2 2 2
溶液,滴加盐酸和BaCl 丁达尔效应。 淀,经检验无丁达尔效应。
2
溶液,产生白色沉淀
下列说法错误的是( )
A.②中红色溶液中含有Fe(OH) 胶体
3
B.实验②中发生的氧化还原反应只有两种
C.对比①②③,可以判定酸性条件下HO 可以氧化SCN-
2 2
D.③中发生的氧化还原反应为:4Fe2++O +4H+=4Fe3++2H O
2 2
21.(2021·四川成都市期末)高铁酸钠(Na FeO)具有很强的氧化性,能有效地杀灭水中的细菌和病毒,
2 4
同时被还原成Fe(OH) 能高效地除去水中的悬浮物,是一种新型高效水处理剂。其制备方法如下:
3
2Fe(OH) +3NaClO+4NaOH= 2Na FeO+3NaCl+5H O。下列说法错误的是( )
3 2 4 2
A.NaFeO 中 元素显+6价
2 4
B.碱性条件下NaClO氧化性强于NaFeO
2 4
C.每生成1mol Na FeO 转移6mol电子
2 4
D.在水处理中,NaFeO 兼具消毒和净水两种功能
2 4
22.(2021·枣庄市第三中学高三月考)F 和Xe在一定条件下生成氧化性极强且极易与水反应的XeF 、
2 2
XeF 和XeF 三种化合物。其中XeF 与HO可以发生如下反应:6XeF +12H O=2XeO +4Xe↑+24HF+3O ↑。
4 6 4 2 4 2 3 2
下列判断正确的是( )
A.XeF 加入水中,在水分子的作用下,将重新生成Xe和F
2 2
B.XeF 按以上方式与水反应,每生成3mol O 转移12mol电子
4 2
C.上述反应中氧化剂和还原剂的物质的量之比为2:1
D.XeF 、XeF 和XeF 在空气中都不能长期存放
2 4 6
23.在酸性条件下,黄铁矿(FeS )催化氧化的反应方程式为2FeS + 7O + 2H O ═ 2Fe2+ + 4SO 2− +
2 2 2 2 4
4H+。实现该反应的物质间转化如图所示。下列分析正确的是( )
A.在酸性条件下,黄铁矿催化氧化中NO作催化剂B.反应Ⅱ中Fe3+作氧化剂,FeS 被还原
2
C.反应Ⅰ的离子方程式为4Fe(NO)2++ O + 4H+ ═ 4Fe3+ +4NO + 2H O,Fe(NO)2+作氧化剂
2 2
D.反应Ⅲ的离子方程式为Fe2+ + NO ═Fe(NO)2+,该反应是氧化还原反应
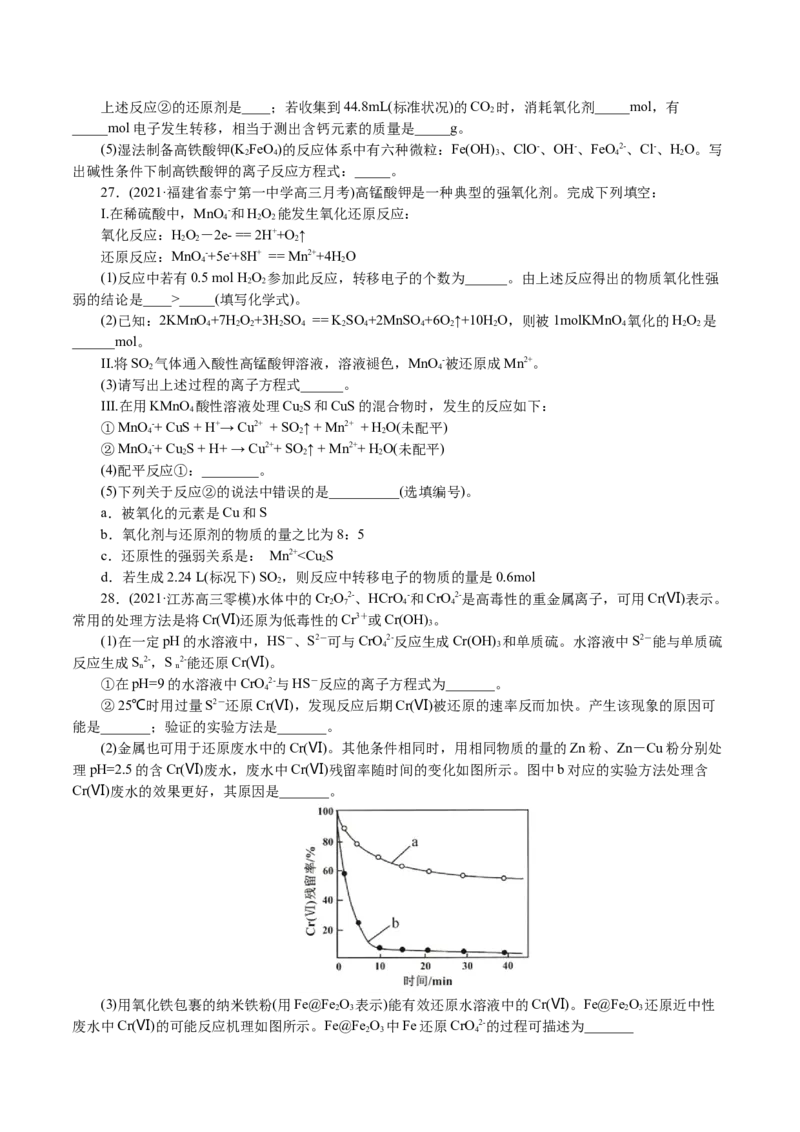
24.(2021·山东潍坊市·高三期末)制备铁红工业流程中,用FeS 还原铁盐溶液得到Fe2+和SO 2-,反应
2 4
机理如下图。下列说法不正确的是( )
A.过程I中每有60gFeS 参与反应,理论上可还原6molFe3+
2
B.过程Ⅱ中若SO2-过量会有气体生成
2 3
C.由过程Ⅱ可知还原性:SO2-_____(填写化学式)。
(2)已知:2KMnO +7H O+3H SO == K SO +2MnSO +6O ↑+10H O,则被1molKMnO 氧化的HO 是
4 2 2 2 4 2 4 4 2 2 4 2 2
______mol。
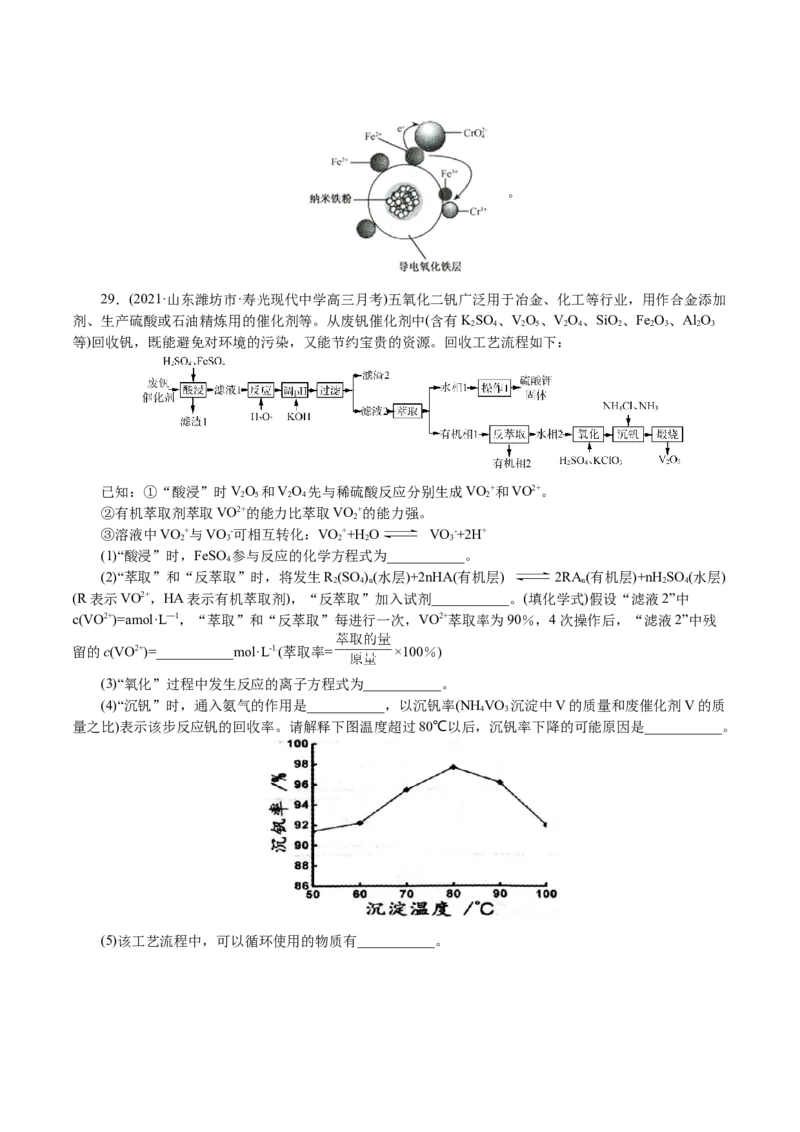
II.将SO 气体通入酸性高锰酸钾溶液,溶液褪色,MnO -被还原成Mn2+。
2 4
(3)请写出上述过程的离子方程式______。
III.在用KMnO 酸性溶液处理Cu S和CuS的混合物时,发生的反应如下:
4 2
①MnO -+ CuS + H+→ Cu2+ + SO ↑ + Mn2+ + H O(未配平)
4 2 2
②MnO -+ Cu S + H+ → Cu2++ SO ↑ + Mn2++ H O(未配平)
4 2 2 2
(4)配平反应①:________。
(5)下列关于反应②的说法中错误的是__________(选填编号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8:5
c.还原性的强弱关系是: Mn2+