文档内容
解密 08 化学反应与能量
一、选择题
1.(2021·浙江省“山水联盟”选考模拟)下列说法不正确的是( )
A.使固态生物质与水蒸气高温反应生成热值较高可燃气体,属于生物质能的热化学转化
B.石油的裂化和裂解、煤的干馏、玉米制醇都是化学变化
C.将固态化石燃料转化为气体,可有效提高燃烧效率,减少环境污染
D.水煤气、焦炉煤气均可来自于煤的气化
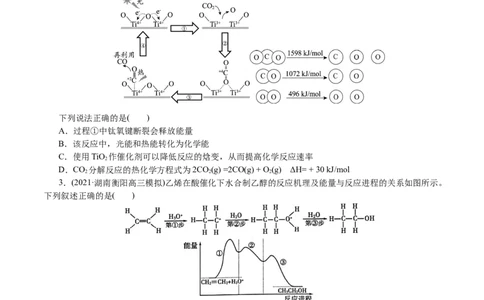
2.(2021·山东省青岛第五十八中学高三质检)以TiO 为催化剂的光热化学循环分解CO 反应为温室气体
2 2
减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如下图所示。
下列说法正确的是( )
A.过程①中钛氧键断裂会释放能量
B.该反应中,光能和热能转化为化学能
C.使用TiO 作催化剂可以降低反应的焓变,从而提高化学反应速率
2
D.CO 分解反应的热化学方程式为2CO(g) =2CO(g) + O (g) ΔH= + 30 kJ/mol
2 2 2
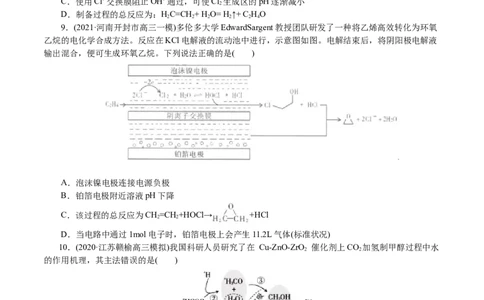
3.(2021·湖南衡阳高三模拟)乙烯在酸催化下水合制乙醇的反应机理及能量与反应进程的关系如图所示。
下列叙述正确的是( )
A.①、②、③三步均属于加成反应 B.总反应速率由第①步反应决定
C.第①步反应的中间体比第②步反应的中间体稳定 D.总反应不需要加热就能发生
4.(2021·江苏高三零模)在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式为
反应Ⅰ:CO(g)+4H(g)=CH (g)+2HO(g) ΔH= -164.7 kJ/mol
2 2 4 2
反应Ⅱ:CO(g)+H(g)=CO(g)+HO(g) ΔH= 41.2 kJ/mol
2 2 2
反应Ⅲ:2CO(g)+2H(g)=CO (g)+CH (g) ΔH= -247.1 kJ/mol
2 2 4
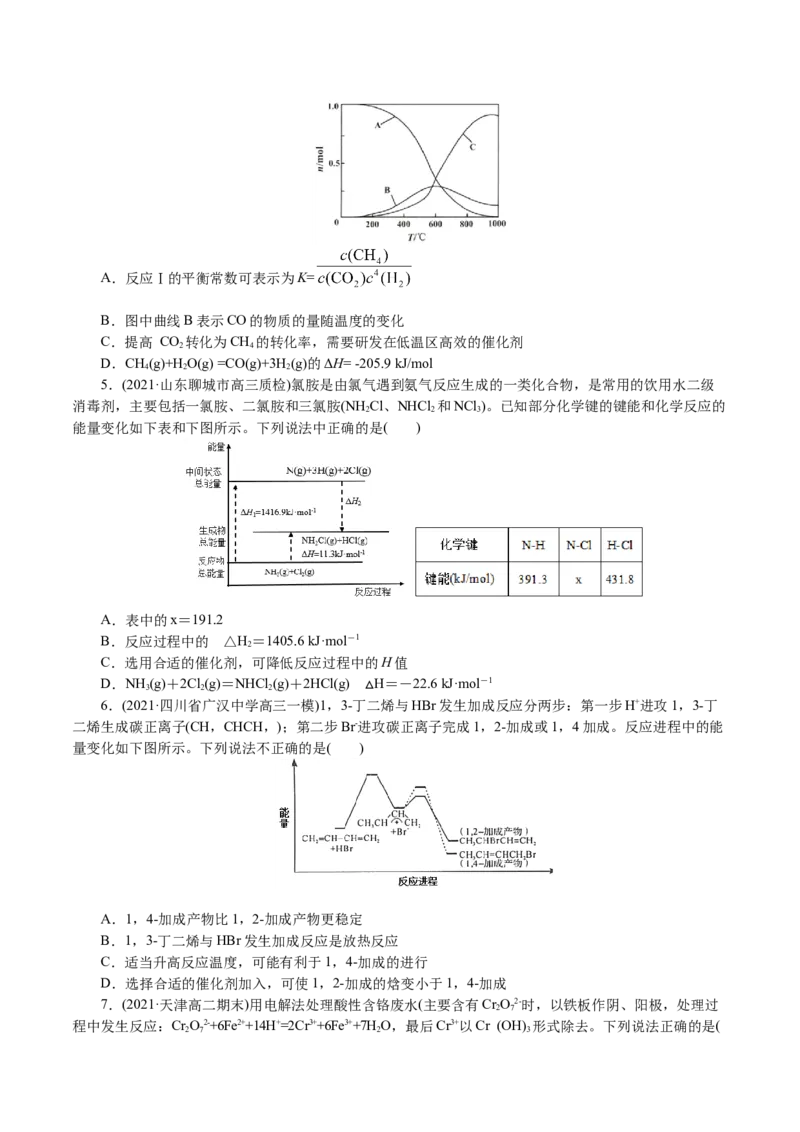
向恒压、密闭容器中通入1 mol CO 和4 mol H ,平衡时CH、CO、CO 的物质的量随温度的变化如图
2 2 4 2
所示。下列说法正确的是( )A.反应Ⅰ的平衡常数可表示为K=
B.图中曲线B表示CO的物质的量随温度的变化
C.提高 CO 转化为CH 的转化率,需要研发在低温区高效的催化剂
2 4
D.CH(g)+HO(g) =CO(g)+3H (g)的ΔH= -205.9 kJ/mol
4 2 2
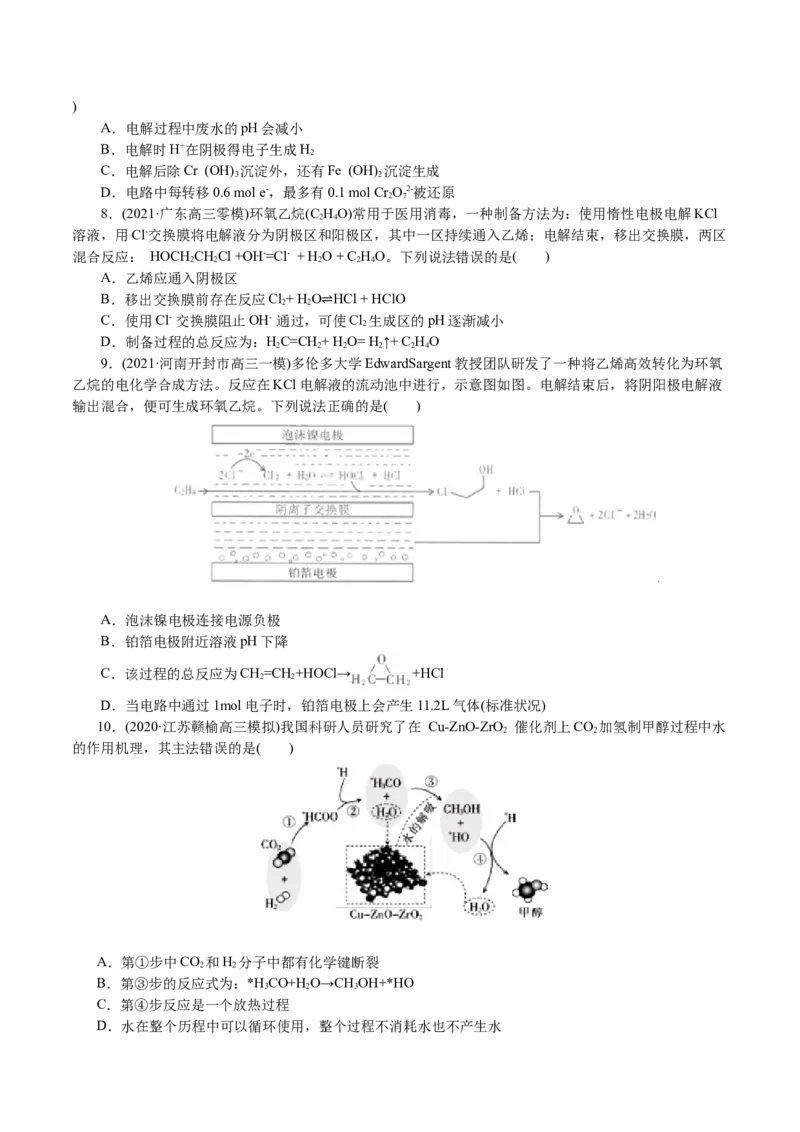
5.(2021·山东聊城市高三质检)氯胺是由氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级
消毒剂,主要包括一氯胺、二氯胺和三氯胺(NH Cl、NHCl 和NCl )。已知部分化学键的键能和化学反应的
2 2 3
能量变化如下表和下图所示。下列说法中正确的是( )
A.表中的x=191.2
B.反应过程中的 △H=1405.6 kJ·mol-1
2
C.选用合适的催化剂,可降低反应过程中的H值
D.NH (g)+2Cl(g)=NHCl (g)+2HCl(g) H=-22.6 kJ·mol-1
3 2 2
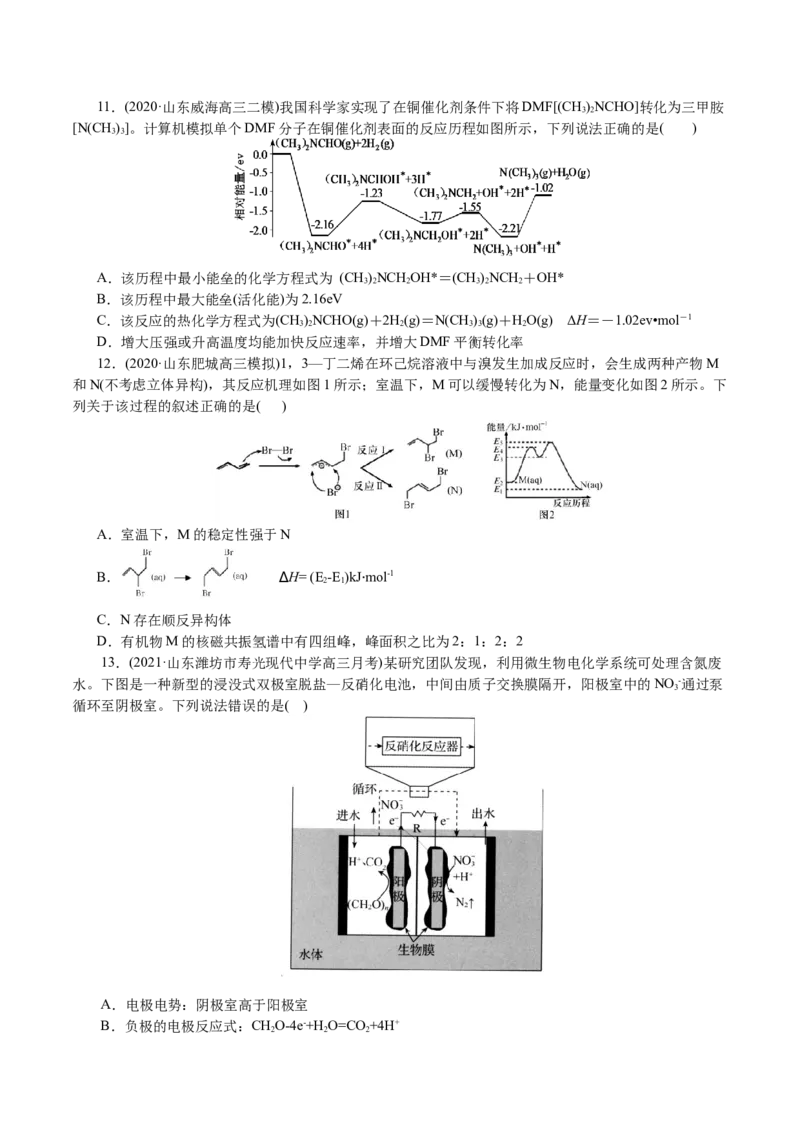
6.(2021·四川省广汉中学高三一模)1,3-丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3-丁
△
二烯生成碳正离子(CH,CHCH,);第二步Br-进攻碳正离子完成1,2-加成或1,4加成。反应进程中的能
量变化如下图所示。下列说法不正确的是( )
A.1,4-加成产物比1,2-加成产物更稳定
B.1,3-丁二烯与HBr发生加成反应是放热反应
C.适当升高反应温度,可能有利于1,4-加成的进行
D.选择合适的催化剂加入,可使1,2-加成的焓变小于1,4-加成
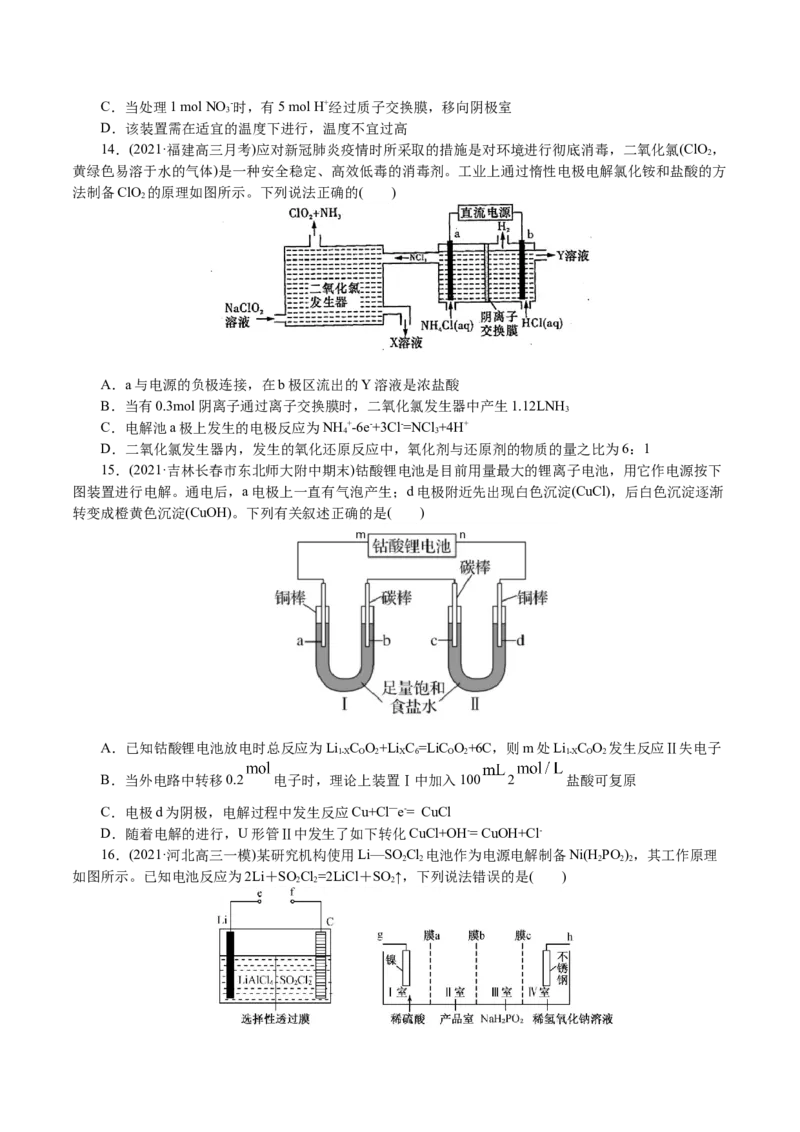
7.(2021·天津高二期末)用电解法处理酸性含铬废水(主要含有CrO2-时,以铁板作阴、阳极,处理过
2 7
程中发生反应:CrO2-+6Fe2++14H+=2Cr3++6Fe3++7H O,最后Cr3+以Cr (OH) 形式除去。下列说法正确的是(
2 7 2 3)
A.电解过程中废水的pH会减小
B.电解时H+在阴极得电子生成H
2
C.电解后除Cr (OH) 沉淀外,还有Fe (OH) 沉淀生成
3 2
D.电路中每转移0.6 mol e-,最多有0.1 mol CrO2-被还原
2 7
8.(2021·广东高三零模)环氧乙烷(C HO)常用于医用消毒,一种制备方法为:使用惰性电极电解KCl
2 4
溶液,用Cl-交换膜将电解液分为阴极区和阳极区,其中一区持续通入乙烯;电解结束,移出交换膜,两区
混合反应: HOCH CHCl +OH-=Cl- + H O + C HO。下列说法错误的是( )
2 2 2 2 4
A.乙烯应通入阴极区
B.移出交换膜前存在反应Cl+ H O HCl + HClO
2 2
C.使用Cl- 交换膜阻止OH- 通过,可使Cl 生成区的pH逐渐减小
2
⇌
D.制备过程的总反应为:HC=CH + H O= H ↑+ C HO
2 2 2 2 2 4
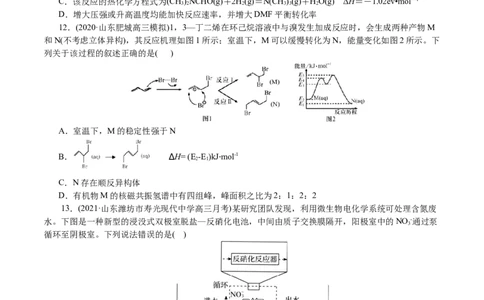
9.(2021·河南开封市高三一模)多伦多大学EdwardSargent教授团队研发了一种将乙烯高效转化为环氧
乙烷的电化学合成方法。反应在KCl电解液的流动池中进行,示意图如图。电解结束后,将阴阳极电解液
输出混合,便可生成环氧乙烷。下列说法正确的是( )
A.泡沫镍电极连接电源负极
B.铂箔电极附近溶液pH下降
C.该过程的总反应为CH=CH +HOCl→ +HCl
2 2
D.当电路中通过1mol电子时,铂箔电极上会产生11.2L气体(标准状况)
10.(2020·江苏赣榆高三模拟)我国科研人员研究了在 Cu-ZnO-ZrO 催化剂上CO 加氢制甲醇过程中水
2 2
的作用机理,其主法错误的是( )
A.第①步中CO 和H 分子中都有化学键断裂
2 2
B.第③步的反应式为:*HCO+HO→CH OH+*HO
3 2 3
C.第④步反应是一个放热过程
D.水在整个历程中可以循环使用,整个过程不消耗水也不产生水11.(2020·山东威海高三二模)我国科学家实现了在铜催化剂条件下将DMF[(CH )NCHO]转化为三甲胺
3 2
[N(CH )]。计算机模拟单个DMF分子在铜催化剂表面的反应历程如图所示,下列说法正确的是( )
3 3
A.该历程中最小能垒的化学方程式为 (CH)NCH OH*=(CH)NCH +OH*
3 2 2 3 2 2
B.该历程中最大能垒(活化能)为2.16eV
C.该反应的热化学方程式为(CH)NCHO(g)+2H(g)=N(CH )(g)+HO(g) ΔH=-1.02ev•mol-1
3 2 2 3 3 2
D.增大压强或升高温度均能加快反应速率,并增大DMF平衡转化率
12.(2020·山东肥城高三模拟)1,3—丁二烯在环己烷溶液中与溴发生加成反应时,会生成两种产物M
和N(不考虑立体异构),其反应机理如图1所示;室温下,M可以缓慢转化为N,能量变化如图2所示。下
列关于该过程的叙述正确的是( )
A.室温下,M的稳定性强于N
B. ∆H= (E -E )kJ‧mol-1
2 1
C.N存在顺反异构体
D.有机物M的核磁共振氢谱中有四组峰,峰面积之比为2:1:2:2
13.(2021·山东潍坊市寿光现代中学高三月考)某研究团队发现,利用微生物电化学系统可处理含氮废
水。下图是一种新型的浸没式双极室脱盐—反硝化电池,中间由质子交换膜隔开,阳极室中的NO -通过泵
3
循环至阴极室。下列说法错误的是( )
A.电极电势:阴极室高于阳极室
B.负极的电极反应式:CHO-4e-+H O=CO+4H+
2 2 2C.当处理1 mol NO -时,有5 mol H+经过质子交换膜,移向阴极室
3
D.该装置需在适宜的温度下进行,温度不宜过高
14.(2021·福建高三月考)应对新冠肺炎疫情时所采取的措施是对环境进行彻底消毒,二氧化氯(ClO ,
2
黄绿色易溶于水的气体)是一种安全稳定、高效低毒的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方
法制备ClO 的原理如图所示。下列说法正确的( )
2
A.a与电源的负极连接,在b极区流出的Y溶液是浓盐酸
B.当有0.3mol阴离子通过离子交换膜时,二氧化氯发生器中产生1.12LNH
3
C.电解池a极上发生的电极反应为NH +-6e-+3Cl-=NCl +4H+
4 3
D.二氧化氯发生器内,发生的氧化还原反应中,氧化剂与还原剂的物质的量之比为6:1
15.(2021·吉林长春市东北师大附中期末)钴酸锂电池是目前用量最大的锂离子电池,用它作电源按下
图装置进行电解。通电后,a电极上一直有气泡产生;d电极附近先出现白色沉淀(CuCl),后白色沉淀逐渐
转变成橙黄色沉淀(CuOH)。下列有关叙述正确的是( )
A.已知钴酸锂电池放电时总反应为Li C O+Li C =LiC O+6C,则m处Li C O 发生反应Ⅱ失电子
1-X O 2 X 6 O 2 1-X O 2
B.当外电路中转移0.2 电子时,理论上装置Ⅰ中加入100 2 盐酸可复原
C.电极d为阴极,电解过程中发生反应Cu+Cl—e-= CuCl
D.随着电解的进行,U形管Ⅱ中发生了如下转化CuCl+OH-= CuOH+Cl-
16.(2021·河北高三一模)某研究机构使用Li—SO Cl 电池作为电源电解制备Ni(H PO ),其工作原理
2 2 2 2 2
如图所示。已知电池反应为2Li+SO Cl=2LiCl+SO ↑,下列说法错误的是( )
2 2 2A.电池中C电极的电极反应式为SO Cl+2e-=2Cl-+SO ↑
2 2 2
B.电池的e极连接电解池的g极
C.膜a、c是阳离子交换膜,膜b是阴离子交换膜
D.电解池中不锈钢电极附近溶液的pH增大
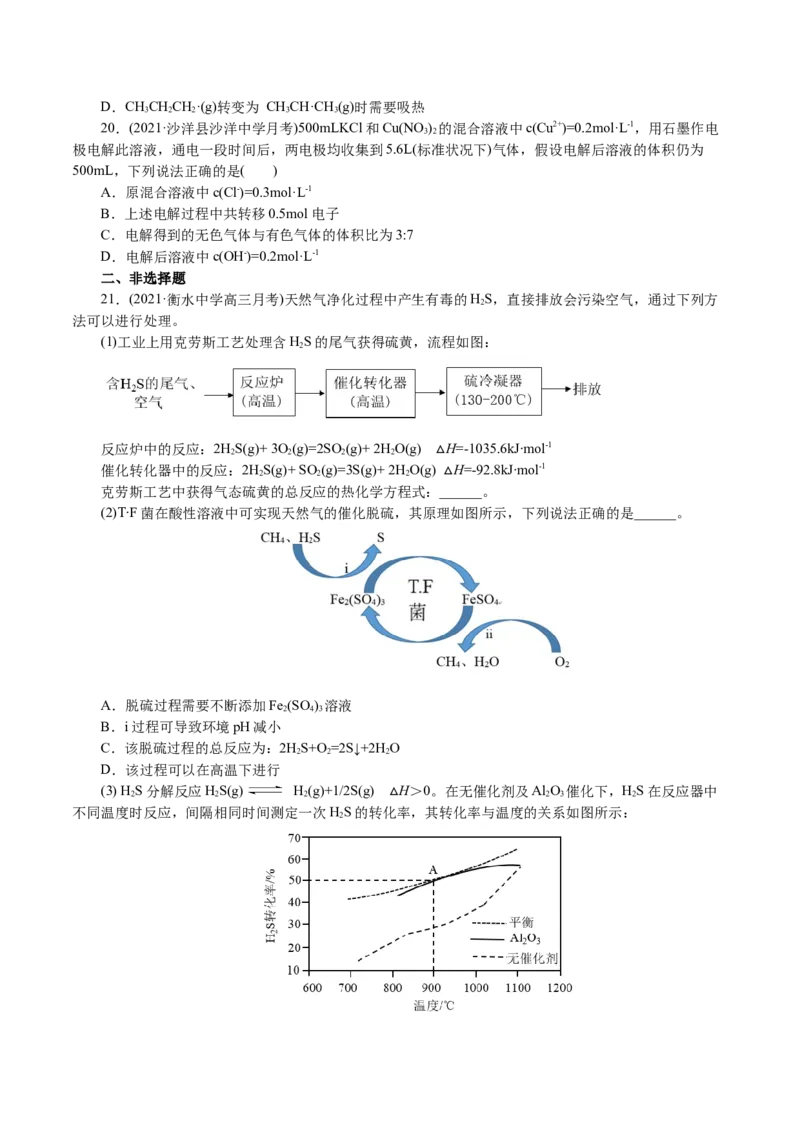
17.(2021·湖北武汉市·华中师大一附中高三月考)银-Ferrozine法检测甲醛(HCHO)的原理如下(在原电
池中完成氧化银与甲醛的反应)。下列说法正确的是(吸光度A=a·b·c,其中a为吸光系数,b为液层厚度,
c为溶液浓度) ( )
A.其他条件相同,溶液的吸光度越小,说明甲醛浓度越大
B.电池反应①中,H+向Ag O 极板迁移
2
C.整个过程看,最终化合价发生变化的元素有Ag、Fe和C
D.理论上,消耗HCHO和消耗Fe3+的物质的量之比为1∶2
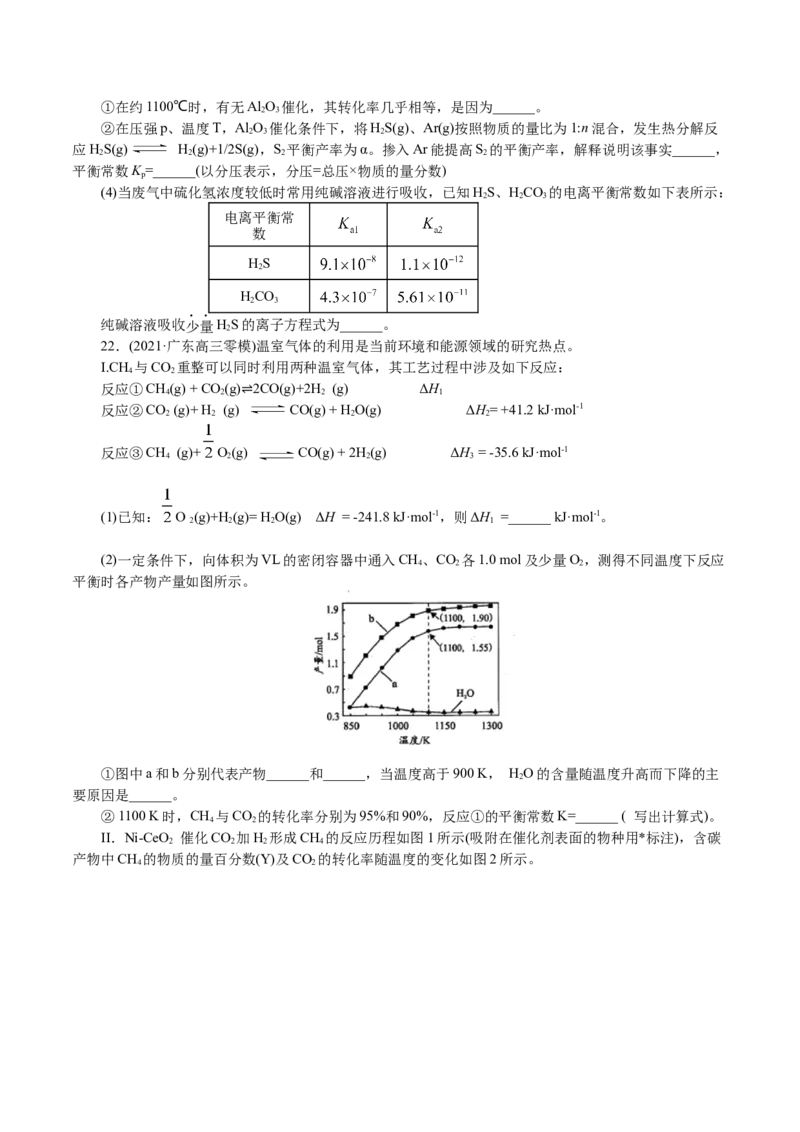
18.(2021·湖南常德市一中高三月考)相同金属在其不同浓度盐溶液中可形成浓差电池。如图所示装置
是利用浓差电池电解NaSO 溶液(a、b电极均为石墨电极),可以制得O、H、HSO 和NaOH。下列说法
2 4 2 2 2 4
不正确的是( )
A.a电极的电极反应为4HO+4e-=2H ↑+4OH-
2 2
B.c、d离子交换膜依次为阳子交换膜和阴离子交换膜
C.电池放电过程中,Cu(1)电极上的电极反应为Cu2++2e-=Cu
D.电池从开始工作到停止放电,电解池理论上可制得320g NaOH
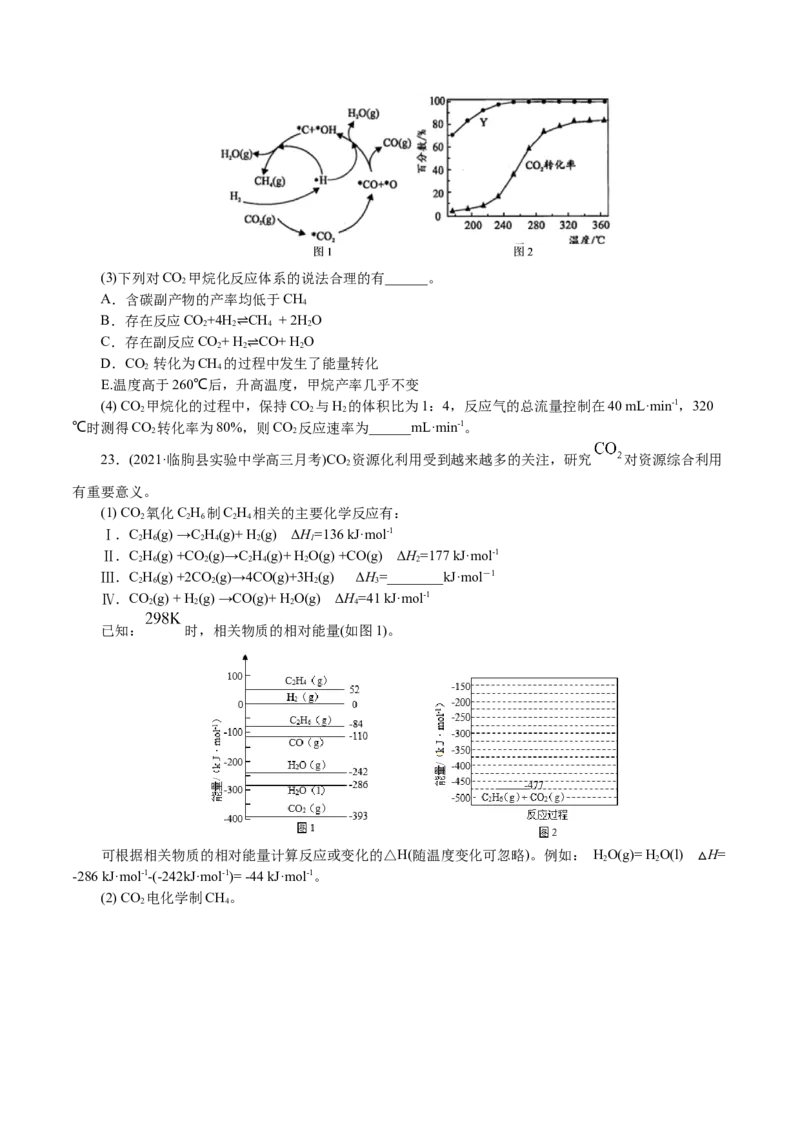
19.(2021·上海闵行区·高三一模)丙烷与溴原子能发生以下两种反应:
① CHCHCH(g) + Br·(g) → CH CHCH·(g) + HBr(g)
3 2 3 3 2 2
② CHCHCH(g) + Br·(g) → CH CH·CH (g) + HBr(g)
3 2 3 3 3
反应过程的能量变化如图所示。下列说法正确的是( )
A.反应①是放热反应
B.反应②使用了催化剂
C.产物中 CHCHCH·(g)含量比 CHCH·CH (g)低
3 2 2 3 3D.CHCHCH·(g)转变为 CHCH·CH (g)时需要吸热
3 2 2 3 3
20.(2021·沙洋县沙洋中学月考)500mLKCl和Cu(NO ) 的混合溶液中c(Cu2+)=0.2mol·L-1,用石墨作电
3 2
极电解此溶液,通电一段时间后,两电极均收集到5.6L(标准状况下)气体,假设电解后溶液的体积仍为
500mL,下列说法正确的是( )
A.原混合溶液中c(Cl-)=0.3mol·L-1
B.上述电解过程中共转移0.5mol电子
C.电解得到的无色气体与有色气体的体积比为3:7
D.电解后溶液中c(OH-)=0.2mol·L-1
二、非选择题
21.(2021·衡水中学高三月考)天然气净化过程中产生有毒的HS,直接排放会污染空气,通过下列方
2
法可以进行处理。
(1)工业上用克劳斯工艺处理含HS的尾气获得硫黄,流程如图:
2
反应炉中的反应:2HS(g)+ 3O (g)=2SO(g)+ 2H O(g) H=-1035.6kJ∙mol-1
2 2 2 2
催化转化器中的反应:2HS(g)+ SO (g)=3S(g)+ 2H O(g) H=-92.8kJ∙mol-1
2 2 2
△
克劳斯工艺中获得气态硫黄的总反应的热化学方程式:______。
△
(2)T∙F菌在酸性溶液中可实现天然气的催化脱硫,其原理如图所示,下列说法正确的是______。
A.脱硫过程需要不断添加Fe (SO ) 溶液
2 4 3
B.i过程可导致环境pH减小
C.该脱硫过程的总反应为:2HS+O=2S↓+2H O
2 2 2
D.该过程可以在高温下进行
(3) H S分解反应HS(g) H(g)+1/2S(g) H>0。在无催化剂及AlO 催化下,HS在反应器中
2 2 2 2 3 2
不同温度时反应,间隔相同时间测定一次HS的转化率,其转化率与温度的关系如图所示:
2
△①在约1100℃时,有无AlO 催化,其转化率几乎相等,是因为______。
2 3
②在压强p、温度T,AlO 催化条件下,将HS(g)、Ar(g)按照物质的量比为1:n混合,发生热分解反
2 3 2
应HS(g) H(g)+1/2S(g),S 平衡产率为α。掺入Ar能提高S 的平衡产率,解释说明该事实______,
2 2 2 2
平衡常数K =______(以分压表示,分压=总压×物质的量分数)
p
(4)当废气中硫化氢浓度较低时常用纯碱溶液进行吸收,已知HS、HCO 的电离平衡常数如下表所示:
2 2 3
电离平衡常
数
HS
2
HCO
2 3
纯碱溶液吸收少量HS的离子方程式为______。
2
22.(2021·广东高三零模)温室气体的利用是当前环境和能源领域的研究热点。
I.CH 与CO 重整可以同时利用两种温室气体,其工艺过程中涉及如下反应:
4 2
反应①CH(g) + CO (g) 2CO(g)+2H (g) ΔH
4 2 2 1
反应②CO (g)+ H (g) CO(g) + H O(g) ΔH= +41.2 kJ·mol-1
2 2 2 2
⇌
反应③CH (g)+ O(g) CO(g) + 2H (g) ΔH = -35.6 kJ·mol-1
4 2 2 3
(1)已知: O (g)+H(g)= H O(g) ΔH = -241.8 kJ·mol-1,则ΔH =______ kJ·mol-1。
2 2 2 1
(2)一定条件下,向体积为VL的密闭容器中通入CH、CO 各1.0 mol及少量O,测得不同温度下反应
4 2 2
平衡时各产物产量如图所示。
①图中a和b分别代表产物______和______,当温度高于900 K, HO的含量随温度升高而下降的主
2
要原因是______。
②1100 K时,CH 与CO 的转化率分别为95%和90%,反应①的平衡常数K=______ ( 写出计算式)。
4 2
II.Ni-CeO 催化CO 加H 形成CH 的反应历程如图1所示(吸附在催化剂表面的物种用*标注),含碳
2 2 2 4
产物中CH 的物质的量百分数(Y)及CO 的转化率随温度的变化如图2所示。
4 2(3)下列对CO 甲烷化反应体系的说法合理的有______。
2
A.含碳副产物的产率均低于CH
4
B.存在反应CO+4H CH + 2H O
2 2 4 2
C.存在副反应CO+ H CO+ H O
2 2 2
⇌
D.CO 转化为CH 的过程中发生了能量转化
2 4
⇌
E.温度高于260℃后,升高温度,甲烷产率几乎不变
(4) CO 甲烷化的过程中,保持CO 与H 的体积比为1:4,反应气的总流量控制在40 mL·min-1,320
2 2 2
℃时测得CO 转化率为80%,则CO 反应速率为______mL·min-1。
2 2
23.(2021·临朐县实验中学高三月考)CO 资源化利用受到越来越多的关注,研究 对资源综合利用
2
有重要意义。
(1) CO 氧化C H 制C H 相关的主要化学反应有:
2 2 6 2 4
Ⅰ.C H(g) →C H(g)+ H (g) ΔH=136 kJ·mol-1
2 6 2 4 2 1
Ⅱ.C H(g) +CO (g)→C H(g)+ H O(g) +CO(g) ΔH=177 kJ·mol-1
2 6 2 2 4 2 2
Ⅲ.C H(g) +2CO (g)→4CO(g)+3H (g) ΔH=________kJ·mol-1
2 6 2 2 3
Ⅳ.CO(g) + H(g) →CO(g)+ H O(g) ΔH=41 kJ·mol-1
2 2 2 4
已知: 时,相关物质的相对能量(如图1)。
可根据相关物质的相对能量计算反应或变化的△H(随温度变化可忽略)。例如: HO(g)= H O(l) H=
2 2
-286 kJ·mol-1-(-242kJ·mol-1)= -44 kJ·mol-1。
△
(2) CO 电化学制CH。
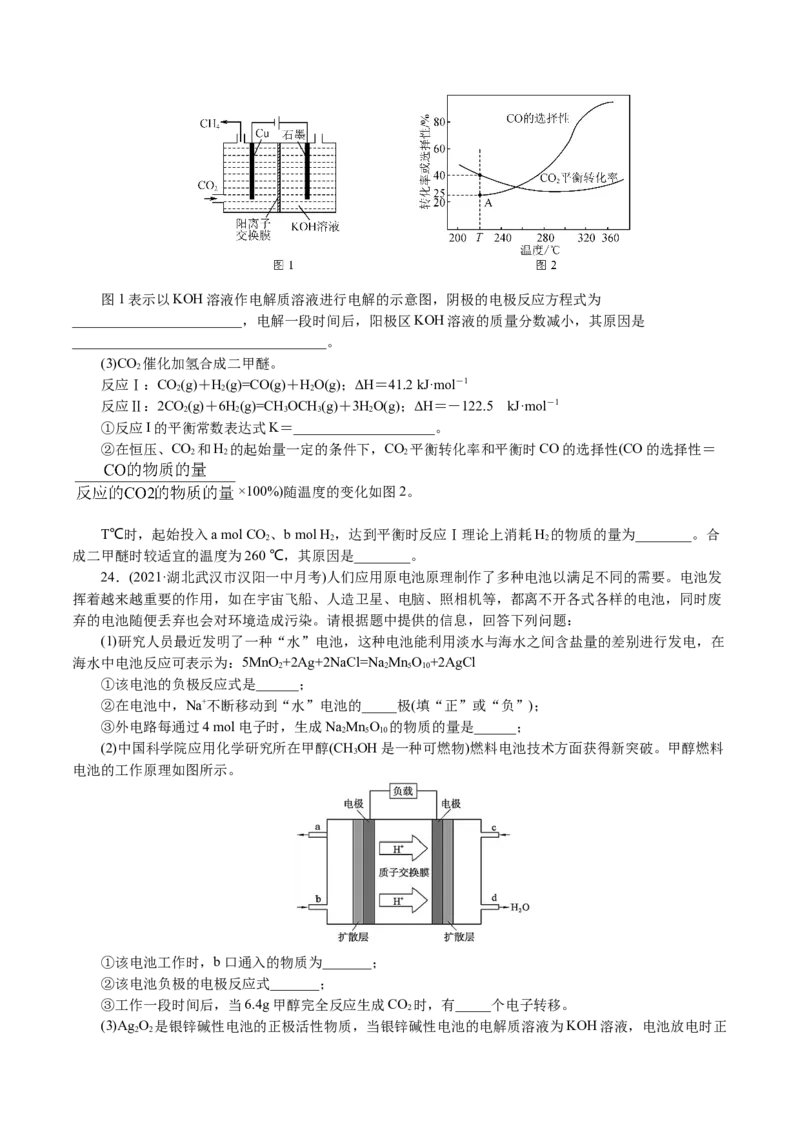
2 4图1表示以KOH溶液作电解质溶液进行电解的示意图,阴极的电极反应方程式为
________________________,电解一段时间后,阳极区KOH溶液的质量分数减小,其原因是
____________________________________。
(3)CO 催化加氢合成二甲醚。
2
反应Ⅰ:CO(g)+H(g)=CO(g)+HO(g);ΔH=41.2 kJ·mol-1
2 2 2
反应Ⅱ:2CO(g)+6H(g)=CH OCH (g)+3HO(g);ΔH=-122.5 kJ·mol-1
2 2 3 3 2
①反应I的平衡常数表达式K=____________________。
②在恒压、CO 和H 的起始量一定的条件下,CO 平衡转化率和平衡时CO的选择性(CO的选择性=
2 2 2
×100%)随温度的变化如图2。
T℃时,起始投入a mol CO 、b mol H ,达到平衡时反应Ⅰ理论上消耗H 的物质的量为________。合
2 2 2
成二甲醚时较适宜的温度为260 ℃,其原因是________。
24.(2021·湖北武汉市汉阳一中月考)人们应用原电池原理制作了多种电池以满足不同的需要。电池发
挥着越来越重要的作用,如在宇宙飞船、人造卫星、电脑、照相机等,都离不开各式各样的电池,同时废
弃的电池随便丢弃也会对环境造成污染。请根据题中提供的信息,回答下列问题:
(1)研究人员最近发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电,在
海水中电池反应可表示为:5MnO +2Ag+2NaCl=Na MnO +2AgCl
2 2 5 10
①该电池的负极反应式是______;
②在电池中,Na+不断移动到“水”电池的_____极(填“正”或“负”);
③外电路每通过4 mol电子时,生成NaMnO 的物质的量是______;
2 5 10
(2)中国科学院应用化学研究所在甲醇(CHOH是一种可燃物)燃料电池技术方面获得新突破。甲醇燃料
3
电池的工作原理如图所示。
①该电池工作时,b口通入的物质为_______;
②该电池负极的电极反应式_______;
③工作一段时间后,当6.4g甲醇完全反应生成CO 时,有_____个电子转移。
2
(3)Ag O 是银锌碱性电池的正极活性物质,当银锌碱性电池的电解质溶液为KOH溶液,电池放电时正
2 2极的Ag O 转化为Ag,负极的Zn转化为KZn(OH) ,写出该电池反应方程式_______;
2 2 2 4
(4)某微生物电池的工作原理如图所示
写出其正极的电极反应式______;负极的电极反应式_______
25.(2021·辽宁丹东市高三月考)64g 铜被一定浓度的硝酸完全溶解,产生的气体的体积为VL ,若将
1
所 得气体中混合V LO ,则恰好能被水完全转化为硝酸;若将所得气体完全被氢氧化钠溶液吸收,会生
2 2
成硝酸钠与亚硝酸钠(气体体积均在标准状况下测定),请回答:
①V = ______L。
2
②亚硝酸钠的物质的量为______mol 。
(2)在 25℃、101 kPa 下,已知 SiH 气体在氧气中完全燃烧后恢复至原状态,平均每转 移 1 mol 电
4
子放出热量 190.0 kJ,该反应的热化学方程式为_________。
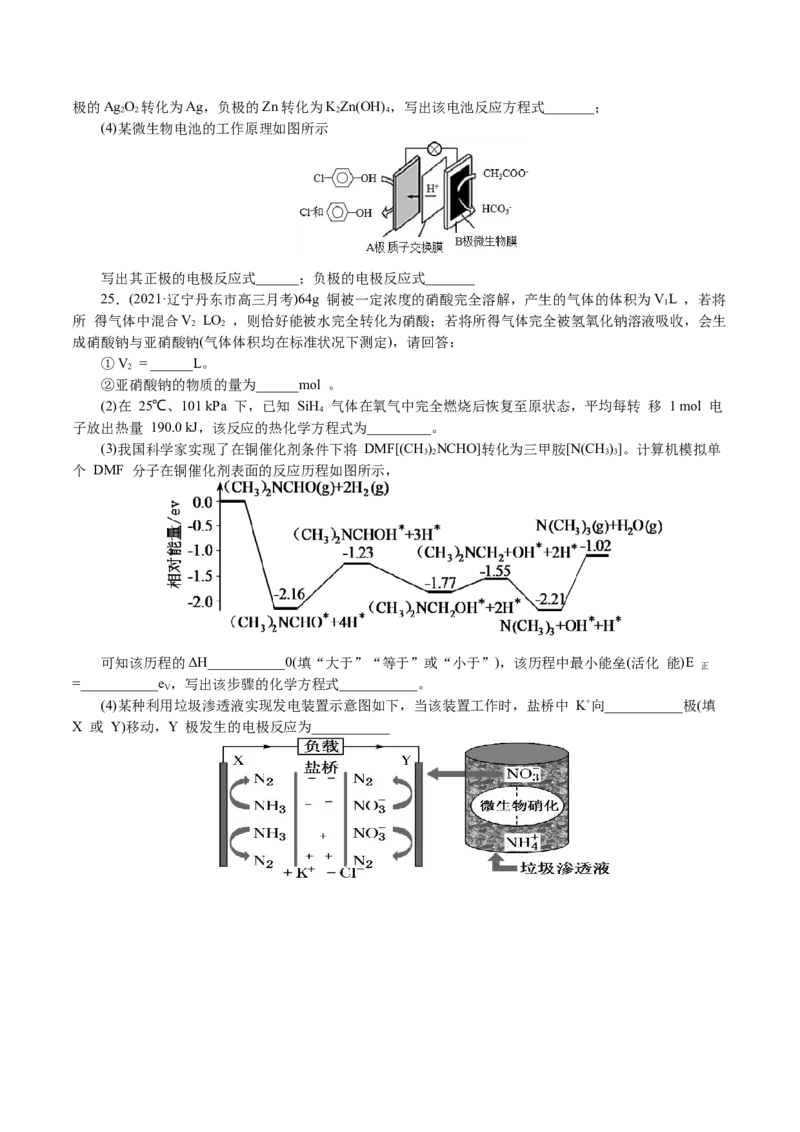
(3)我国科学家实现了在铜催化剂条件下将 DMF[(CH )NCHO]转化为三甲胺[N(CH )]。计算机模拟单
3 2 3 3
个 DMF 分子在铜催化剂表面的反应历程如图所示,
可知该历程的ΔH___________0(填“大于”“等于”或“小于”),该历程中最小能垒(活化 能)E
正
=___________e ,写出该步骤的化学方程式___________。
V
(4)某种利用垃圾渗透液实现发电装置示意图如下,当该装置工作时,盐桥中 K+向___________极(填
X 或 Y)移动,Y 极发生的电极反应为___________