文档内容
解密 18 物质结构与性质
一、单选题
1.(2023秋·北京朝阳·高三统考期末)下列化学用语或图示表达正确的是
A. 共价键电子云轮廓图:
B.基态 原子的价层电子排布式:
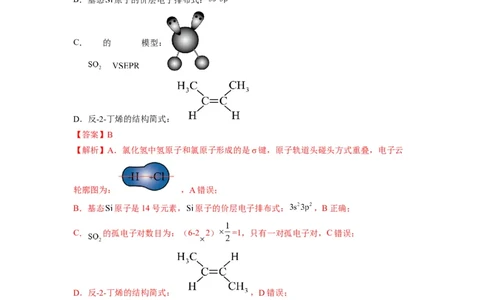
C. 的 模型:
D.反-2-丁烯的结构简式:
【答案】B
【解析】A.氯化氢中氢原子和氯原子形成的是σ键,原子轨道头碰头方式重叠,电子云
轮廓图为: ,A错误;
B.基态 原子是14号元素, 原子的价层电子排布式: ,B正确;
C. 的孤电子对数目为:(6-2 2) =1,只有一对孤电子对,C错误;
D.反-2-丁烯的结构简式: ,D错误;
故本题选B。
2.(2022秋·河北保定·高三校考阶段练习)绿矾 可用作净水剂,在空气中
极易被氧化。下列有关说法正确的是
A.H、O、S均位于元素周期表p区
B. 的价层电子轨道表示式为
C.基态S原子的未成对电子数为6
D.基态O原子核外电子占据的最高能级的电子云轮廓图是球形的【答案】B
【解析】A.H的价电子排布式为 ,位于元素周期表s区,A项错误;
B. 是铁原子生成4s2上的2个电子得到的,其价层电子轨道表示式为
,B项正确;
C.基态S原子的价电子排布式为 ,其未成对电子数为2,C项错误;
D.O原子核外电子排布式为 ,占据的最高能级为 ,故电子云轮廓图呈哑铃
形,D项错误。
答案选B。
3.(2023秋·天津西青·高三统考期末)下列物质性质的说法正确的是
A.离子晶体中存在阴阳离子,故离子晶体可以导电
B. 图中电子排布违反了能量最低原理
C.金属发生延展时,金属原子层间发生相对滑动,不改变原来的排列方式
D.由于 分子间可以存在氢键,水的热稳定性很强
【答案】C
【解析】A.导电需要自由移动的离子,故离子晶体中存在阴阳离子,但离子不可自由移
动也不可以导电,故A错误;
B.能量最低原理:原子核外的电子应优先排布在能量最低的能级里,然后由里到外,依
次排布在能量逐渐升高的能级里;洪特规则是指在相同能量的轨道上,电子总是尽可能分
占不同的轨道且自旋方向相同;图中电子排布违反了洪特规则,故B错误;
C.金属晶体中存在金属键,发生延展时,金属原子层间发生相对滑动,不改变原来的排
列方式,故C正确;
D.水的热稳定性很强是因为氢氧键键能很大,故D错误;
故选C。
4.(2023春·湖南湘潭·高三湘潭一中校考开学考试)X、Y、W、N是原子序数依次增大
的短周期主族元素,X原子的核外电子只有一种运动状态,Y的最外层电子数为其 轨道
电子数的3倍,W与Y位于同一主族。下列叙述正确的是
A.简单离子半径:
B.W、N的最高价氧化物对应水化物的酸性:
C.最简单氢化物的沸点:
D. 分子中只含极性共价键
【答案】C
【解析】X原子的核外电子只有一种运动状态,则X是H元素,Y的最外层电子数为其轨道电子数的3倍,其最外层电子排布式为2s22p4,则Y是O元素;W与Y位于同一主族,
则W是S元素,根据X、Y、W、N是原子序数依次增大的短周期主族元素,则N是Cl元
素。
A.简单离子半径: ,即 ,故A错误;
B.W、N的最高价氧化物对应水化物的酸性: ,则 ,故B错误;
C. 可以形成分子间氢键,沸点更高,所以 ,故C正确;
D. 分子即 ,其中不只含极性共价键,还有氧原子之间形成的非极性共价键,
故D错误;
故选C。
5.(2023春·湖北武汉·高三统考阶段练习)我国超高压输变电技术世界领先。 属于新
一代超高压绝缘介质材料,其制备反应原理为 。下列说
法正确的是
A.第一电离能: B. 是一种直线形分子
C. 分子的键角完全相同 D. 的沸点比 的高
【答案】A
【解析】A.同一主族随原子序数变大,原子半径变大,第一电离能变小;同一周期随着
原子序数变大,第一电离能呈变大趋势,第一电离能: ,A正确;
B. 分子中中心O原子价层电子对数为2+ =4,O原子采用sp3杂化,O原子上
含有2对孤电子对,所以分子不是直线形分子,B错误;
C. 分子构型为正八面体,键角不完全相同,C错误;
D. 能形成氢键,导致 的沸点比 的低,D错误;
故选A。
6.(2021春·湖北·高三校联考阶段练习)“ ”表示相关元素的原子中除去最外层电子
的剩余部分,“。”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表
示共价键。关于下述几种分子的说法正确的是
A.分子中,中心原子采用sp3杂化的只有①③
B.①分子为正四面体结构,④分子为平面形
C.②分子中σ键:π键=2:1D.四种分子的键角大小顺序为②>③>①>④
【答案】D
【解析】A.④的中心原子的价层电子对数为4,采取的也是sp3杂化,故A说法错误;
B.①和④的中心原子采取的都是sp3杂化,根据价层电子对互斥理论,①分子中含有孤对
电子,导致①分子不是正四面体结构、是三角锥形,④分子虽然也有2对孤电子对,但形
成的两个共价键共面,所以④分子为平面形,故B说法错误;
C.②分子中含有三键,中心原子采取的是sp杂化,但中心原子有2个,故分子中的σ键
是3,π键是2,则σ键:π键=3:2,故C说法错误;
D.根据价层电子对互斥理论,四种分子的键角大小顺序为②>③>①>④,故D说法正确;
本题答案D。
7.(2022秋·辽宁营口·高三统考期末)下列符号表征或说法正确的是
A. 电离: B.Fe位于元素周期表d区
C. 空间结构:三角锥形 D.羟基的电子式:
【答案】B
【解析】A. 是二元弱酸,电离分步进行,其一级电离方程式为
,A错误;
B.基态Fe原子的价电子排布式是 ,位于元素周期表d区,B正确;
C. 中心碳原子的价层电子对数为 ,故其空间结构为平面三角形,
C错误;
D.羟基含有1个未成对电子,电子式: ,D错误;
故选B。
8.(2023春·安徽·高三统考专题练习)在碱性溶液中, 可以与缩二脲形成紫色配离
子,其结构如图所示。下列说法错误的是
A.该配离子中非金属元素的电负性大小顺序为O>N>C>H
B.该配离子中能与水分子形成氢键的原子有N、O和H
C.1mol该配离子中含有的配位键数目为6 (设 为阿伏加德罗常数的值)D.已知缩二脲的分子式为 ,则由尿素 生成缩二脲的反应类型为取
代反应
【答案】C
【解析】A.同一周期从左到右主族元素的电负性逐渐变大,故电负性:O>N>C,且三者
电负性均大于氢,A正确;
B.由题图可知,N、O能与水分子中的氢原子形成氢键,H能与水分子中的氧原子形成氢
键,B正确;
C.由题图可知,该配离子中,两个铜离子与其他原子共形成4个配位键,故1mol该配离
子中含有的配位键数目为 ,C错误;
D.已知缩二脲的分子式为 ,根据题图可判断出缩二脲的结构简式为
,结合尿素的结构简式 判断,由尿素生成缩二
脲的反应类型为取代反应,D正确;
综上所述故选C。
9.(2023春·北京通州·高三统考开学考试)钛酸钙是典型的钙钛矿型化合物,该类化合物
具有特殊的理化性质,比如吸光性、电催化性等,其晶体结构如图所示。下列说法不正确
的是
A.钛酸钙的化学式为
B.钛与钙是同一周期元素
C.基态钛原子价电子排布式是
D.晶胞中与每个 距离最近且相等的 有6个
【答案】D
【解析】A.根据晶胞结构分析得到Ca、Ti、O的个数分别为 、1、 ,则钛
酸钙的化学式为 ,故A正确;
B.钛为22号元素,与钙是都是第四周期元素,故B正确;
C.钛为22号元素,基态钛原子电子排布式为[Ar] ,价电子排布式是 ,故C正确;
D. 所在的横截面有3个,每个横截面与Ca2+距离最近且相等的 有4个,因此晶胞
中与每个 距离最近且相等的 有12个,故D错误;
综上所述,答案为D。
10.(2023秋·河北沧州·高三统考期末)钴的某种氧化物广泛应用于硬质合金、超耐热合
金、绝缘材料和磁性材料的生产,其晶胞结构如图所示。下列有关说法正确的是
A.该氧化物的化学式为
B.晶胞中 的配位数为12
C.根据晶体类型推测,该物质熔点低于硫
D.若该氧化物的密度为 ,阿伏加德罗常数为 ,则晶胞中两个 间的最短
距离是
【答案】D
【解析】A.据“均摊法”,晶胞中含 个 、 个 ,该氧化
物的化学式为 ,A错误;
B.以体心钴离子为例,晶胞中 的配位数为6,B错误;
C.分子晶体沸点低于离子晶体,根据晶体类型推测, (分子晶体)熔点低于 (离子晶
体),C错误;
D.设晶胞棱长为acm,1个晶胞中含有4个 ,则晶体密度为
,晶胞棱长 ,两个 间的最短距离为 =
,D正确;
故选D。
二、填空题11.(2022·福建·高三统考专题练习)锂—磷酸氧铜电池正极的活性物质是 ,
可通过下列反应制备:
。
(1)写出基态 的电子排布式:_______________。
(2)P、S元素第一电离能大小关系为_______________,原因是_______________。
(3)氨基乙酸铜分子结构如图所示,碳原子的杂化方式为_______________,基态碳原子核
外电子有_______________种运动状态。
(4)在硫酸铜溶液中加入过量 ,生成配合物 ,则 该配合物含有 键的
数目为_______________( 表示阿伏加德罗常数的值)。
(5)晶体铜的晶胞结构如图甲所示,原子之间相对位置关系的平面图如图乙所示,铜原子的
配位数为_______________,铜的原子半径为 , 表示阿伏加德罗常数的值,晶
体铜的密度为_______________ (列出计算式即可)。
【答案】(1) (或 )
(2) P原子 轨道上的电子处于半充满状态,较稳定,比S难失去电子
(3) 和 6
(4)
(5) 12
【解析】(1)Cu2+核外有27个电子,根据核外电子排布规律,基态Cu2+的电子排布式是
(或 );
(2)P原子3p轨道半充满,结构较稳定,不易失电子,所以P、S元素第一电离能大小关
系为P>S;
(3)单键碳杂化方式为sp3、双键碳杂化方式为sp2, 中既有单键碳又有双键碳,所以碳原子的杂化方式为sp3、sp2;基态碳原子核外有6个电子,所
以基态碳原子核外电子有6种运动状态;
(4) 存在碳氨三键,1个碳氨三键中有2个 键,所以 该配合物含有 键,
数目为 ;
(5)离铜原子距离最近且相等的原子为铜原子的配位原子,根据图甲可知铜原子配位数是
12;根据图乙可知,晶胞的面对角线长为 ,则晶胞棱长为 ,
每个品跑合有铜原子数为 ,1个晶胞的体积为 ,质
量为 ,所以晶体铜的密度为 。
12.(2022秋·河南驻马店·高三统考期末)半导体材料对现代信息技术的发展至关重要。
硅(Si)、砷化铝(AlAs)均为半导体材料。
(1)基态砷原子的核外电子排布式为_______。第一电离能:As_______(填“>”或“<”)Se。
(2)高纯硅可用于制造芯片,其制备过程中会产生SiHCl、SiHCl、SiHCl 、SiCl 等物质。
3 2 2 3 4
熔沸点:SiH_______(填“>”或“<”)SiCl ,原因是_______。
4 4
(3)SiCl 可发生水解反应,水解机理如图1。SiCl 和SiCl (OH)中Si采取的杂化类型分别为:
4 4 3
_______、_______;Si、 、Cl的电负性由大到小的顺序为_______(填元素符号)。
(4)一种新型半导体材料砷化硼的晶胞结构示意图如图2。砷化硼的化学式为_______,该晶
胞中As的配位数为_______,该晶胞中As原子处于B原子形成的_______(填“正四面体”
或“正八面体”)空隙中,设该晶胞的边长均为apm,阿伏加德罗常数的值为N ,则该晶
A
体的密度为_______(列出计算式)g·cm-3。
【答案】(1) >(2) < 两种物质均是分子晶体,相对分子质量越大熔沸点越高
(3) 、 、
(4) 4 正四面体
【解析】(1)基态砷原子的核外电子排布式为 ,砷原子最外层的 能级处
于半满状态较稳定,硒原子最外层的 能级有4个电子,不稳定,所以第一电离能砷大于
硒,答案: ,>;
(2)两种物质均是分子晶体,分子晶体的相对分子质量越大分子间作用力越强,熔沸点越
高,答案:<,两种物质均是分子晶体,相对分子质量越大熔沸点越高;
(3)SiCl 和SiCl (OH)中Si的价层电子对都是4 ,中心原子采取的杂化类型都是 ,电
4 3
负性的变化规律同周期自左向右电负性依次增大,同主族自上而下依次减小,氧的电负性
大于氯,氯的电负性大于硅,答案:, , , 、 、 ,
(4)由晶胞结构可知硼原子位于晶胞的顶点和面心,所以一个晶胞均摊硼原子的个数
,砷原子处于晶胞的内部有4个,所以化学式 ,晶胞中距离As最近的
硼原子有4个,围城一个正四面体的结构,所以晶胞中As的配位数为4,该晶胞中As原
子处于B原子形成的正四面体空隙中,根据 ,答案: ,
4,正四面体, 。
一、单选题
1.(2023秋·吉林长春·高三长春市第二中学校考期末)下图为“点击化学”的一种反应,
下列关于Ⅰ~Ⅲ三种物质的说法正确的是
A.Ⅰ中C、N、O元素的第一电离能最大的是O
B.基态 的价层电子排布式为C.基态N原子 轨道的电子云轮廓图:
D.Ⅲ中基态氧原子最外层电子的轨道表示式:
【答案】C
【解析】A.同一周期随着原子序数变大,第一电离能变大,N的2p轨道为半充满稳定状
态,第一电离能大于同周期相邻元素,故I中N元素的第一电离能最大,A错误;
B.铜为29号元素,失去一个电子形成 ,故基态 的价层电子排布式为 ,B错
误;
C.基态N原子 轨道的电子云轮廓图: ,C正确;
D.O是第8号元素,基态氧原子最外层电子的轨道表示式: ,D错误;
故选C。
2.(2023春·广东广州·高三广州市第二中学校联考开学考试)FeSO ·7H O在工业生产中
4 2
有重要用途,其结构示意图如下,下列说法错误的是
A.电负性:O>S>H
B.基态Fe2+的价层电子排布式:3d6
C.上述结构中含化学键:离子键、共价键、氢键、配位键
D.HO中的O和 中的S均为sp3杂化,HO的键角小于 的键角
2 2
【答案】C
【解析】A.非金属性O>S>H,非金属性越强,电负性越大,则电负性:O>S>H,A
正确;B.基态Fe的价电子排布式为3d64s2,则基态Fe2+的价层电子排布式为3d6,B 正确;
C.FeSO ·7H O的晶体结构中,Fe2+与 间形成离子键,S-O、O-H间形成共价键,6个
4 2
HO与Fe2+间形成配位键,氢键不属于化学键,则含化学键:离子键、共价键、配位键,C
2
错误;
D.HO中的O和 中的S价层电子对数都为4,均发生sp3杂化,HO分子中O原子最
2 2
外层有2个孤电子对,对成键电子有排斥作用,而S原子最外层不存在孤电子对,所以
HO的键角小于 的键角,D正确;
2
故选C。
3.(2023春·重庆渝中·高三重庆巴蜀中学校考阶段练习)某固体电解质的化学式为
,其中R、X、Y、W为原子序数依次增大的短周期主族元素,R为金属元素,且
最外层电子数是次外层的一半,X、Y、W为第三周期的相邻非金属元素,Y与W形成的
分子中所有原子均满足8电子稳定结构。下列说法错误的是
A.R与W形成的化合物水溶液显酸性
B.X是四种元素中简单离子半径最大的
C.W的电负性大于Y
D.1molX与W形成的化合物一定含66mol电子
【答案】D
【解析】R、X、Y、W为原子序数依次增大的短周期主族元素,R为金属,且最外层电子
数是次外层的一半,R是Li元素;X、Y、W为第三周期的非金属元素,根据LiXY Z元
6 5
素化合价代数和等于0,可知X是P元素、Y是S元素、W是Cl元素。
A.R是Li,W是Cl,形成的化合物为LiCl,强酸弱碱盐,水溶液显酸性,A正确;
B.Li+电子层数少,半径小;电子层数相同,质子数越多半径越小,简单离子半径:Cl-
H O
4 2
B.元素的第一电离能: BF-
D.该锂盐的阴离子中含有配位键
【答案】A
【解析】A.HO中存在氢键,CH 中不存在氢键,则HO的沸点高于CH,A错误;
2 4 2 4
B.同周期元素从左到右,元素的第一电离能呈增大的趋势,第一电离能BF-,C正确;
D.B原子形成3条共价键之后没有多余的电子,其与其中一个F形成的共价键为配位键,
D正确;
故答案选A。
6.(2023·全国·高三专题练习)我国科研人员发现一种可用于“点击化学”的化合物,结
构如图所示。W、X、Y、Z为短周期主族元素且原子序数依次增大,X、Z同主族,Y原
子的最外层电子数与W原子的核外电子总数相等。下列说法正确的是
A.原子半径:B.四种元素中,最高价含氧酸酸性最强的为Y
C.第一电离能:
D.最简单氢化物的沸点:
【答案】D
【解析】由题干信息可知,W、X、Y、Z为短周期主族元素且原子序数依次增大,X形成
2个共价键,Z形成6个共价键,X、Z同主族,则X为O、Z为S;Y形成1个共价键,且
原子序数在O、S之间,则Y为F;W原子的核外电子总数与F的最外层电子数相等,则
W为N。
A.由分析可知,X为O,Y为F,Z为S,同周期主族元素从左到右,原子半径逐渐减小;
同主族元素从上到下,原子半径逐渐增大,则原子半径S>O>F即Z>X>Y,A错误;
B.由分析可知,Y为F,F无正价,不存在最高价含氧酸,B错误;
C.由分析可知,X为O,W为N,同周期主族元素从左到右,第一电离能总体上呈增大
趋势,但N的2p轨道处于半充满状态,第一电离能大于O的(同周期第ⅤA族元素的第
一电离能大于第ⅥA族元素的),C错误;
D.由分析可知,X为O,Z为S,HO能形成分子间氢键,而HS不能,故HO的沸点更
2 2 2
高,D正确;
故答案为:D。
7.(2023春·安徽·高三统考专题练习)水溶液锌电池(图1)的电极材料是研究热点之一、
一种在晶体 中嵌入 的电极材料充放电过程的原理如图2所示。下列叙述中正确的
是
A.①为 活化过程,其中 的价态不变
B.该材料在锌电池中作为负极材料
C.②代表电池放电过程
D.③中 晶体转移的电子数为
【答案】C
【解析】A.①过程中MnO晶胞中体心的Mn2+失去,产生空位,该过程为MnO活化过程,
根据化合物化合价为0可知Mn元素化合价一定发生变化,故A项错误;
B.锌电池中Zn失去电子生成Zn2+,Zn电极为负极材料,故B项错误;
C.②过程中电池的MnO电极上嵌入Zn2+,说明体系中有额外的Zn2+生成,因此表示放电过程,故C项正确;
D.MnO晶胞中棱边上所含Mn的个数为 ,同理 和 晶
胞中棱边上所含Mn的个数为3, 晶胞中Zn2+个数为 ,因此Mn与
Zn2+个数比为3:1,由此可知 晶胞中Zn2+个数为 ,③过程中1mol
晶体转移电子的物质的量为 ,故D项错误;
综上所述,叙述正确的是C项。
8.(2023·广东清远·清新一中校考模拟预测)几种工业上常见的晶体晶胞或结构(氟化钙,
氯化铵,氯化铝)如图所示,下列说法正确的是
A.图1中正负离子的配位数分别为4和8
B.熔点:图2所示物质>图1所示物质
C.图3中与体心原子等距离且最近的顶点原子有8个
D.图3中只存在离子键
【答案】C
【解析】A.由图1可知,晶胞中黑球个数为 ,白球个数为8,个数比为
4:8=1:2,根据化学式CaF 可知,黑球代表Ca2+,白球代表F-,白球位于相邻的4个黑球所
2
形成的正四面体的体心,因此,所示CaF 晶体中F-配位数为4,则Ca2+配位数为8,故A
2
错误;
B.氯化铝是共价化合物,图2代表AlCl ,图1代表CaF ,是离子晶体,一般离子晶体的
3 2
熔点高于共价晶体,故CaF 的熔点高于AlCl ,故B错误;
2 3
C.图3中与体心原子小黑球等距离且最近的顶点原子大黑球有8个,故C正确;
D.图3晶胞中大黑球个数为 ,白球个数为4,小黑球个数为1,根据氯化铵的化学
式NH Cl可知图3代表该物质,NH Cl中铵根和氯离子间存在离子键,铵根内N和H原子
4 4
间存在共价键,故D错误;
故选:C。
二、填空题
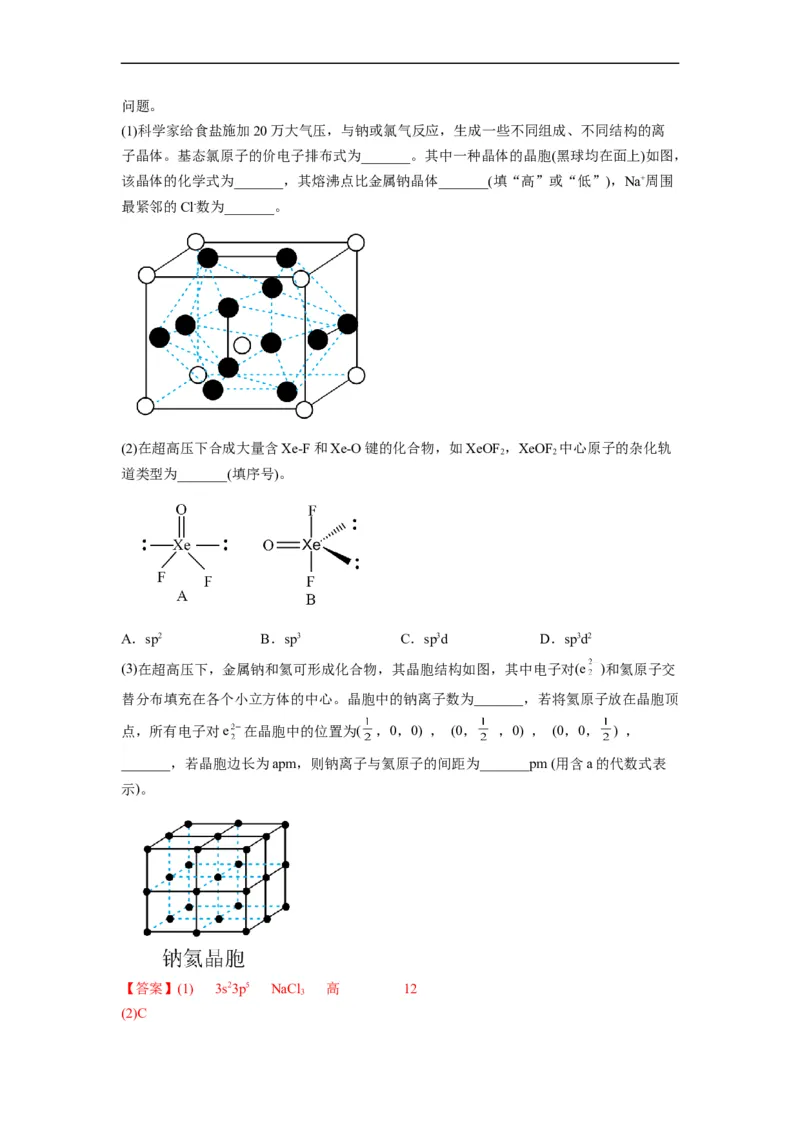
9.(2022秋·山东威海·高三统考期末)高压技术在物质研究中发挥着重要作用,回答下列问题。
(1)科学家给食盐施加20万大气压,与钠或氯气反应,生成一些不同组成、不同结构的离
子晶体。基态氯原子的价电子排布式为_______。其中一种晶体的晶胞(黑球均在面上)如图,
该晶体的化学式为_______,其熔沸点比金属钠晶体_______(填“高”或“低”),Na+周围
最紧邻的Cl-数为_______。
(2)在超高压下合成大量含Xe-F和Xe-O键的化合物,如XeOF ,XeOF 中心原子的杂化轨
2 2
道类型为_______(填序号)。
A.sp2 B.sp3 C.sp3d D.sp3d2
(3)在超高压下,金属钠和氦可形成化合物,其晶胞结构如图,其中电子对(e )和氦原子交
替分布填充在各个小立方体的中心。晶胞中的钠离子数为_______,若将氦原子放在晶胞顶
点,所有电子对e 在晶胞中的位置为( ,0,0) , (0, ,0) , (0,0, ) ,
_______,若晶胞边长为apm,则钠离子与氦原子的间距为_______pm (用含a的代数式表
示)。
【答案】(1) 3s23p5 NaCl 高 12
3
(2)C(3) 8 ( , , )
【解析】(1)氯为17号元素,基态氯原子的价电子排布式为3s23p5。氯原子半径大于钠,
则根据“均摊法”,晶胞中含 个Na、 个Cl,该晶体的化学式为
NaCl ,其为离子晶体熔沸点较高、钠单质熔沸点较低,故其熔沸点比金属钠晶体高;以体
3
心钠离子为例,最紧邻的Cl-为12个,故填12;
(2)中心原子形成3个σ键且存在2对公用电子对,则说明一个d轨道参与可杂化,故为
sp3d杂化,选C;
(3)根据“均摊法”,晶胞中含 个钠离子;电子对(e )和氦原子
交替分布填充在各个小立方体的中心,若将氦原子放在晶胞顶点,则两者相对位置如图,
,若所有电子对e 在晶胞中的位置为( ,0,0) , (0, ,0) , (0,
0, ) ,则另一个位置为( , , );若晶胞边长为apm,则钠离子与氦原子的间距为
体对角线的四分之一,故为 pm。
10.(2022·福建·高三统考专题练习)铜及其化合物在日常生产、生活中有着广泛的应用。
回答下列问题:
(1)基态Cu原子价电子排布式为_______。
(2)K与Cu同周期,最外层电子数相同,但Cu的熔点远高于K,因为_______。
(3)含铜废液可以利用铜萃取剂M,通过如下反应实现铜离子的富集,进行回收。
①M所含元素的电负性由大到小顺序是_______(用元素符号表示)。
②X化合物中中心原子铜的配位数是_______,上述反应中断裂和生成的化学键有
_______(填字母序号)。a.离子键 b.共价键 c.金属键 d.氢键 e.配位键
(4)高温下, 比CuO稳定的原因是_______。
(5)离子型配合物 中,阴离子的空间构型为_______,配体中碳原子的杂
化方式是_______。
(6)由Cu,Sb,Se组成的热电材料,其晶胞结构如图所示, , ,
该晶体的密度是_______ (列式即可)
【答案】(1)3d104s1
(2)Cu的半径比K的半径小,电荷数比K的多,金属键比K强,所以Cu的熔点远高于K
(3) O>N>C>H 4 be
(4)Cu的价电子为3d104s1,失去最外层1个电子即可达到全满稳定结构
(5) 正四面体 sp3、sp
(6)
【解析】(1)Cu元素为29号元素,原子核外有29个电子,所以核外电子排布式
为:1s2s22p63s23p63d104s1,基态铜原子价层电子排布式为3d104s1;
(2)Cu的半径比K的半径小,电荷数比K的多,金属键比K强,所以Cu的熔点远高于
K;
(3)①M中的元素由C、N、O、H,根据同周期元素,从左到右电负性依次增强,可得
M所含元素的电负性由大到小顺序为O>N>C>H;
②X化合物中有2个氮原子和2个氧原子提供孤对电子,所以中心原子铜的配位数是4;中
心原子提供空轨道,配体提供孤电子对形成配位键;氢键存在于与N、O、F等电负性很大
的原子形成共价键的H与另外的N、O、F等电负性很大的原子之间,配位键用“→”表示,
氢键用“…”表示,在该反应中,酚羟基中的O-H共价键断裂生成H+,所以上述反应中
断裂和生成的化学键有配位键、共价键,选be;
(4)Cu O中Cu+的外围电子排布式为3d10,CuO中Cu2+的外围电子排布式为3d9,前者达
2到全充满稳定结构;
(5)配合物 的阴离子为 ,中心原子B的价层电子对数为
=4,空间构型为正四面体形;配体CHCN 中,甲基上的碳是sp3杂化,
3
−CN中含有三键,碳原子是sp杂化;
(6)由Cu,Sb,Se组成的热电材料,其晶胞结构如图所示,根据均摊法可知Cu有10
+4 =6个,Sb有 2个,Se有8个, , ,该晶体的密度
是 = 。
11.(2023秋·天津河西·高三统考期末)羧酸在自然界中广泛存在,与人类生活关系密切。
已知:
ⅰ.烷基(R-)是推电子基团
ⅱ.25℃时,
( )
请按要求回答下列问题。
(1)甲酸、乙醛沸点分别为101℃、21℃,分析推测乙酸的沸点比丙醛的_______(填“高很
多”或“低很多”或“等于”),你推测的依据是_______。
(2)甲酸的结构式为_______;其分子中,碳原子的杂化轨道类型为_______;其分子中,电
负性最大的原子是_______。
(3)推测酸性强弱:乙酸_______十八酸即硬脂酸(填“>”或“<”)。
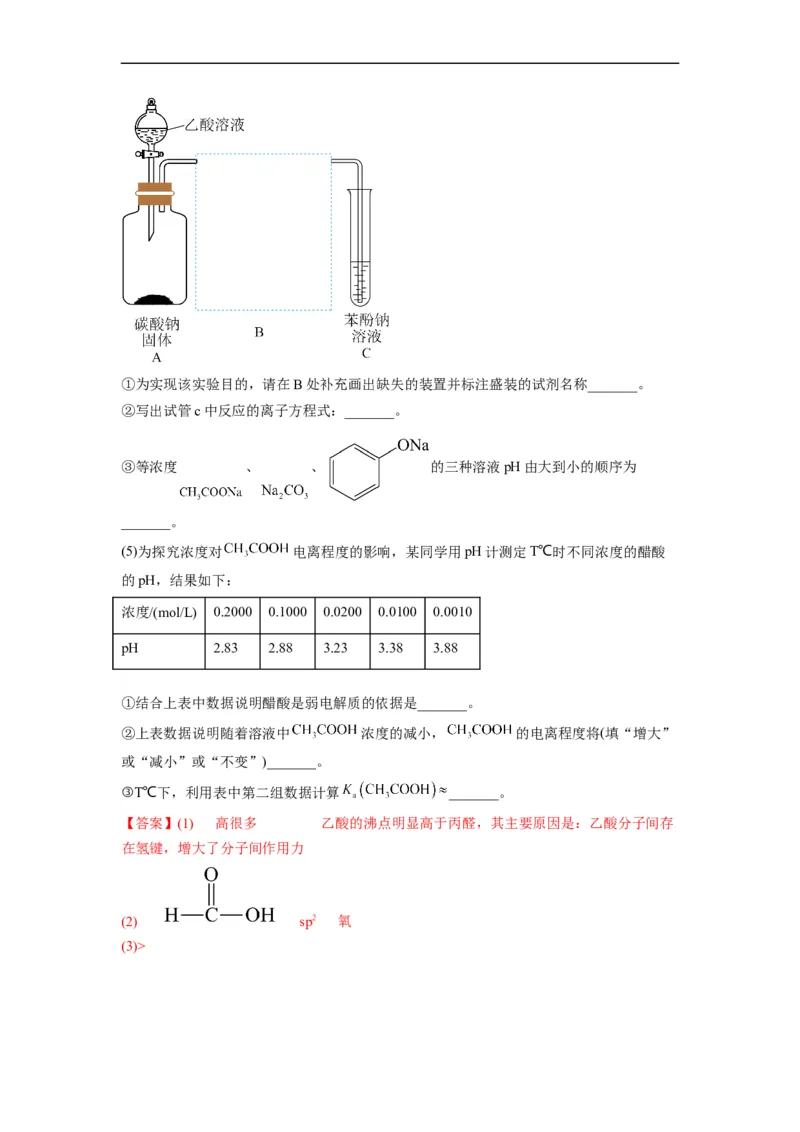
(4)某同学设计图所示装置探究乙酸、碳酸、乙酸溶液苯酚的酸性强弱。①为实现该实验目的,请在B处补充画出缺失的装置并标注盛装的试剂名称_______。
②写出试管c中反应的离子方程式:_______。
③等浓度 、 、 的三种溶液pH由大到小的顺序为
_______。
(5)为探究浓度对 电离程度的影响,某同学用pH计测定T℃时不同浓度的醋酸
的pH,结果如下:
浓度/(mol/L) 0.2000 0.1000 0.0200 0.0100 0.0010
pH 2.83 2.88 3.23 3.38 3.88
①结合上表中数据说明醋酸是弱电解质的依据是_______。
②上表数据说明随着溶液中 浓度的减小, 的电离程度将(填“增大”
或“减小”或“不变”)_______。
③T℃下,利用表中第二组数据计算 _______。
【答案】(1) 高很多 乙酸的沸点明显高于丙醛,其主要原因是:乙酸分子间存
在氢键,增大了分子间作用力
(2) sp2 氧
(3)>(4) CO+H O+ HCO +
2 2
> >
(5) 当醋酸溶液的浓度为10-3 mol/L时,pH = 3.88,c(H+) =10-3.88 mol/L <10-3 mol/L 增
大 10-4.76
【解析】(1)乙酸的沸点明显高于丙醛,其主要原因是:乙酸分子间存在氢键,增大了分
子间作用力,推测乙酸的沸点比丙醛的高很多;
(2)甲酸的结构式为 ;其分子中,碳原子的杂化轨道类型为sp2;其分子
中,电负性最大的原子是氧;
(3)已知:ⅰ.烷基(R-)是推电子基团,随着碳原子数的增加,推电子作用减弱,氧氢键极
性增强,使H更容易脱离氧即同元时烃基越短酸性越强,故乙酸>十八酸即硬脂酸;
(4)①二氧化碳中混有挥发的醋酸,需用装有饱和碳酸氢钠的洗气瓶洗气;②
> > >HCO ,复分解反应中较强酸可以制较弱酸:CO+H O+
2 2
HCO + ;
③ 、 、 都是强碱弱酸盐,水解显碱性。酸性强弱顺序为> > >HCO ,根据越弱越水解的规律,等浓度的三种溶液
pH由大到小的顺序为 > > ;
(5)①当醋酸溶液的浓度为10-3 mol/L时,pH = 3.88,c(H+) =10-3.88 mol/L <10-3 mol/L,
说明醋酸在溶液中不能完全电离,可证明醋酸时弱电解质;
②当醋酸溶液的浓度为10-3 mol/L时,pH =3.88,c(H+) =10-3.88 mol/L,当醋酸溶液浓度为
10-2mol·L-1时,pH=3.38,c(H+) =10-3.38 mol/L,综合以上数据,溶液浓度减小为原来的 ,
c(H+)大于原来的 ,由此可知,随醋酸浓度的减小,醋酸的电离程度增大;
③ 。
12.(2023春·安徽·高三统考专题练习)镍电池的电极活性材料为多组分合金(主要成分为
镍、钴,还含有铝、铁等),可重新回收利用。利用废镍电池资源化生产醋酸钴晶体
的工艺流程如下。
已知:①浸取母液中除铝元素外,其他金属元素的化合价均为 价。
②部分金属阳离子沉淀的 如下表。
沉淀物
开始沉淀
2.2 7.4 7.6 0.1 4.0 7.6
完全沉淀
3.2 8.9 9.2 1.1 5.2 9.2
请回答下列问题:
(1)“浸取”时可以提高浸取率的操作有_______(任写1条)。
(2)“调 ”时溶液的 范围是_______,所得滤渣1的主要成分为_______(填化学式)。(3)“氧化分离”操作控制溶液 ,加入 发生反应的离子方程式为_______。
(4)“溶解1”操作中加入 的作用为_______,“沉钴”操作过程中发生反应的离子方程
式为_______。
(5)“溶解2”操作后得到醋酸钴晶体,要使该醋酸钴晶体的纯度更高,所采取的实验操作名
称应为_______。
(6)碱金属可以插入石墨层中,钾 的石墨插层化合物具有超导性,其中K层平行于石墨
层。图1为其晶胞图,垂直于石墨层方向的原子投影如图2所示。
C—C键的键长为 ,则K层中m与n两个K原子之间的距离为_______ ,设 为
阿伏加德罗常数的值,若晶胞参数分别为 、 、 ,则该石墨插层化合物的晶胞
密度为_______ (用含x、y、z、 的代数式表示)。
【答案】(1)增大硫酸浓度,升高温度,延长浸取时间等
(2) 、
(3)
(4) 还原 生成
(5)重结晶
(6)
【解析】由题中流程可知,镍电池废料(主要成分为镍、钻,还含有铝、铁等),用硫酸浸
取后,金属元素转化为对应的离子进入溶液中,加入 的目的是将母液中的 氧化为
,调节溶液 ,使 和 完全转化为 沉淀和 沉淀,过滤,滤渣
1为 和 ,向滤液中加入 将 氧化变成 并水解生成
沉淀,然后向沉淀中加入 和 ,溶解得到 溶液,向溶液中加入
得到 沉淀,过滤后的沉淀溶解在冰醋酸中得到醋酸钴溶液,将醋酸钴溶液蒸发浓缩、
冷却结晶、过滤、洗涤、干燥得到醋酸钴晶体,据此解答。(1)为提高浸取速率,除适当升高温度外,还可采取的措施有延长浸取时间、适当增加硫
酸浓度等。故答案为:增大硫酸浓度,升高温度,延长浸取时间等;
(2)由后续流程可知,第一次调节 时,已经将铁、铝化合物全部除去,则滤渣1的成
分除了 外,还有 ,结合表中数据可知,为了使 完全沉淀而 不沉
淀,应当调节溶液 的范围是 ,故答案为: ;
(3)“母液”中含有的 能够和 发生氧化还原反应,根据得失电子守恒和原子
守恒,可知反应的离子方程式为 ,故答案为:
;
(4)向 中加入 、 混合液,结合后续流程,最后得到产物中, 以
二价离子化合物形式存在,所以此时加入的 为还原剂,离子方程式为:
,故答案为:还原 生成 ,
;
(5)为提高醋酸钴晶体纯度,需要重新溶解、浓缩、结晶析出纯度更高的晶体,即重结晶
操作,故答案为:重结晶;
(6)根据晶胞结构,K原子在晶胞的8个顶点、6个面心和4个在体内,1个晶胞中含K
原子的个数为 ;由晶胞结构知m与n的距离如图 中的
之间距离,C—C键的键长为 ,则 ;晶胞中每层石墨烯部分结
构中有4条边(8个C原子)处于晶胞面上,其他C原子处于晶胞内部,晶胞中C原子数目
,则晶胞的质量 ,晶胞的体积
,所以该晶胞的密度
,故答案为: , 。