文档内容
选择题标准练(七)
1.航天员翟志刚、王亚平、叶光富首次完成“天和”核心舱在轨6个月的任务后,于2022
年4月16日乘坐神舟十三号载人飞船返回地球,标志着我国载人航天工程处于世界前列。
下列有关说法正确的是( )
A.核心舱采用的氮化硼陶瓷属于新型无机非金属材料
B.核心舱采用的柔性太阳能电池翼可将光能转化为化学能
C.核心舱采用的镁合金具有在高温潮湿环境下耐腐蚀的化学特性
D.核心舱采用无水氢氧化锂净化二氧化碳的反应属于化合反应
答案 A
解析 柔性太阳能电池翼直接将光能转化为电能,B错误;镁是活泼金属元素,其在高温潮
湿环境中易被腐蚀,即镁合金不具有在高温潮湿环境下耐腐蚀的化学特性,C错误;核心舱
采用无水氢氧化锂净化二氧化碳的反应为2LiOH+CO===LiCO+HO,该反应不属于化合
2 2 3 2
反应,D错误。
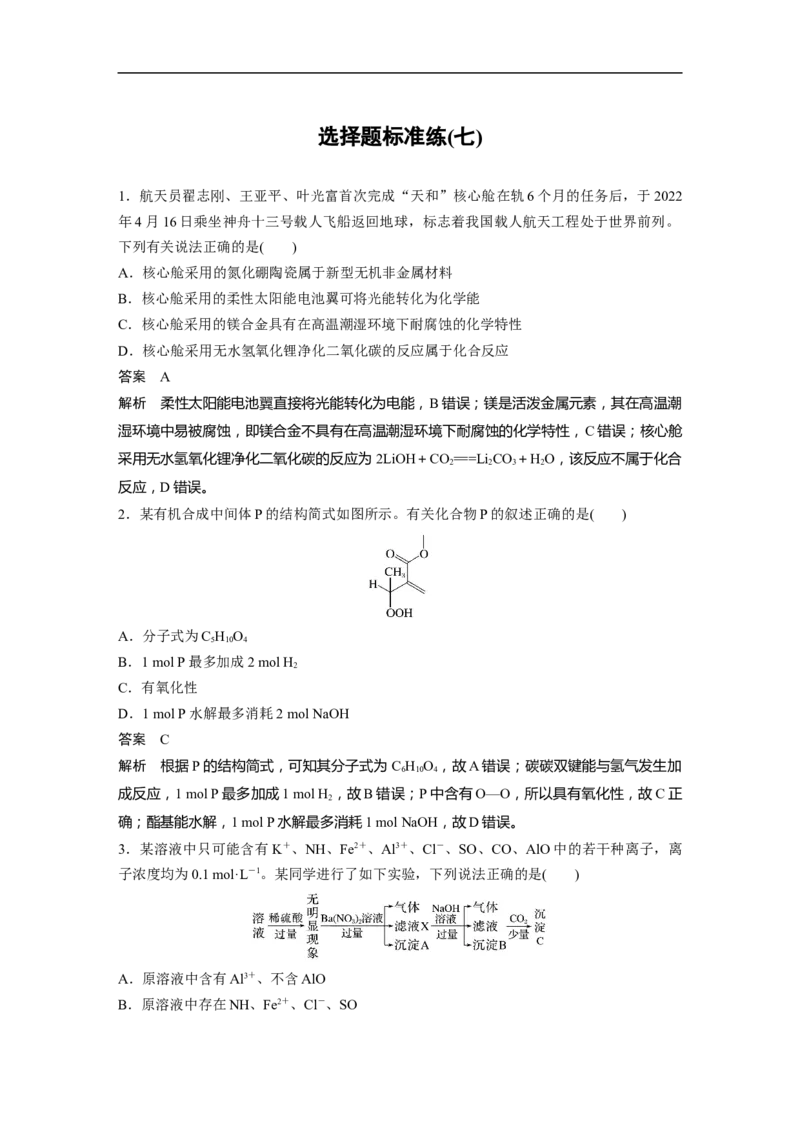
2.某有机合成中间体P的结构简式如图所示。有关化合物P的叙述正确的是( )
A.分子式为C H O
5 10 4
B.1 mol P最多加成2 mol H
2
C.有氧化性
D.1 mol P水解最多消耗2 mol NaOH
答案 C
解析 根据P的结构简式,可知其分子式为C H O ,故A错误;碳碳双键能与氢气发生加
6 10 4
成反应,1 mol P最多加成1 mol H ,故B错误;P中含有O—O,所以具有氧化性,故C正
2
确;酯基能水解,1 mol P水解最多消耗1 mol NaOH,故D错误。
3.某溶液中只可能含有K+、NH、Fe2+、Al3+、Cl-、SO、CO、AlO中的若干种离子,离
子浓度均为0.1 mol·L-1。某同学进行了如下实验,下列说法正确的是( )
A.原溶液中含有Al3+、不含AlO
B.原溶液中存在NH、Fe2+、Cl-、SOC.沉淀C中含有BaCO 、Al(OH)
3 3
D.滤液X中大量存在的阳离子有NH、Fe2+和Ba2+
答案 B
解析 溶液中加入稀硫酸无明显现象,说明无CO;加入硝酸钡溶液,有气体生成,说明发
生了氧化还原反应,则含有Fe2+,不含AlO;生成沉淀A,说明沉淀A为硫酸钡沉淀,但
不能说明含有SO,因为前面加入了硫酸;滤液X中加入过量NaOH溶液生成气体,则气体
为氨气,原溶液中含有NH;沉淀B含有氢氧化铁沉淀;滤液中通入少量二氧化碳有沉淀C
生成,沉淀C一定含有碳酸钡,由于溶液中离子浓度均为0.1 mol·L-1,结合电荷守恒可判
断不可能含有Al3+,只有含有NH、Fe2+、Cl-、SO才能保证电荷守恒,溶液中也不存在K
+,故A错误、B正确;根据上述分析可知,溶液中不含Al3+,则沉淀C为碳酸钡,不含
Al(OH) ,故C错误;滤液X中大量存在的阳离子有NH、Fe3+、H+和Ba2+,故D错误。
3
4.下列实验的现象与结论均正确的是( )
选项 操作 现象 结论
将铜片加入盛有稀硝酸的 Cu把稀HNO 中氮元素还
3
A 试管口有红棕色气体产生
试管中 原为NO
2
B 灼热的铁丝插入氯气瓶中 铁丝剧烈燃烧 Fe与Cl 反应生成FeCl
2 3
C 将洁净铁丝放入浓硫酸中 无明显现象 没有发生化学反应
只有极易溶于水的气体才
D 用HCl气体做喷泉实验 可以形成喷泉
能用来做喷泉实验
答案 B
解析 将铜片加入盛有稀硝酸的试管中,Cu把稀HNO 中氮元素还原为NO,NO在试管口
3
与O 反应生成红棕色的气体NO ,A不符合题意;灼热的铁丝插入氯气瓶中,铁丝能剧烈
2 2
燃烧,Fe与Cl 反应生成FeCl :2Fe+3Cl=====2FeCl ,B符合题意;将洁净铁丝放入浓硫
2 3 2 3
酸中,无明显现象是由于常温下铁遇到浓硫酸发生钝化,钝化属于化学变化,C不符合题意;
HCl极易溶于水,用HCl气体做喷泉实验,可以形成喷泉,但并不是只有极易溶于水的气体
才能用来做喷泉实验,如NaOH和CO 反应使得气体的压强快速下降也能形成喷泉,D不符
2
合题意。
5.如图是短周期主族元素的单质及其化合物(或其溶液)的转化关系。已知X、Y、Z原子序
数依次增大,A~F均为化合物,F为不含金属元素的含氧酸盐。下列说法正确的是( )
A.原子半径:X<Y<Z
B.物质的稳定性:A>C
C.E和F中存在的化学键类型完全相同D.常温下,可以用铁制容器盛装E的浓溶液
答案 D
解析 由已知信息推知,F为含氧酸铵盐,故X为H元素、Y为N元素、Z为O元素,X、
2
Y 、Z 分别为H 、N 、O ,结合转化关系可推知,A为NH 、B为NO、C为HO、D为
2 2 2 2 2 3 2
NO 、E为HNO 、F为NH NO 。同一周期元素从左向右原子半径逐渐减小,一般情况下电
2 3 4 3
子层数越多原子半径越大,则原子半径:HN,稳定性:NH