文档内容
选择题标准练(一)
(选择题1~10题,每小题3分,11~15题,每小题4分,共50分)
1.中华文化源远流长,下列有关说法错误的是( )
A.“斜月沉沉藏海雾,碣石潇湘无限路”,诗中的“海雾”可发生丁达尔效应
B.“大邑烧瓷轻且坚,扣如哀玉锦城传”,诗中的“瓷”属于传统无机非金属材料
C.“以曾青涂铁,铁赤色如铜”,句中的“曾青”为氢氧化铜
D.“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也。”句中的“法”
指蒸馏
答案 C
解析 “海雾”属于胶体,可发生丁达尔效应,A正确;“瓷”的主要成分为硅酸盐,属于传统无机非金
属材料,B正确;“曾青”为硫酸铜溶液,由于金属活动性:Fe>Cu,所以CuSO 与铁可以在溶液中发生
4
置换反应生成铜单质,C错误;“蒸令气上”可知该分离混合物的方法为蒸馏操作,D正确。
2.下列化学用语表达正确的是( )
A.基态Fe2+的价层电子轨道表示式为
B.N,N⁃ 二甲基苯甲酰胺的结构简式:
C.O 分子的球棍模型:
3
D.CaO 的电子式:
2
答案 B
解析 基态Fe2+的价层电子排布式为3d6,轨道表示式为 ,A错误; 为臭氧
分子的VSEPR模型,C错误;CaO 是由钙离子和过氧根离子构成,D错误。
2
3.类推的思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才
能判断其正确与否。下列类推结论正确的是( )
A.根据反应2H S+O ===2S+2H O可以证明氧气的氧化性大于硫的氧化性;由反应SiO +2C Si+2CO↑也
2 2 2 2
可以证明碳的氧化性大于硅的氧化性
B.分子式为C H Br的芳香族化合物的同分异构体有4种,则分子式为C H O的芳香族化合物的同分异构体
7 7 7 8
也是4种
C.CO 可以使滴有酚酞的NaOH溶液颜色变浅,则SO 也可以使滴有酚酞的NaOH溶液颜色变浅
2 2
D.乙醇与足量的酸性高锰酸钾溶液反应生成乙酸,则乙二醇与足量的酸性高锰酸钾溶液反应生成乙二酸答案 C
解析 根据反应SiO +2C Si+2CO↑只能证明碳的还原性大于硅的还原性,A错误;分子式为C H O的
2 7 8
芳香族化合物的同分异构体有5种: (—OH有1,2,3三种位置)、 、 ,B错误;
CO 、SO 的水溶液均呈酸性,可以使滴有酚酞的NaOH溶液颜色变浅,C正确;乙二醇与足量的酸性高锰
2 2
酸钾溶液反应生成乙二酸,乙二酸还可以与酸性高锰酸钾溶液反应生成二氧化碳,D错误。
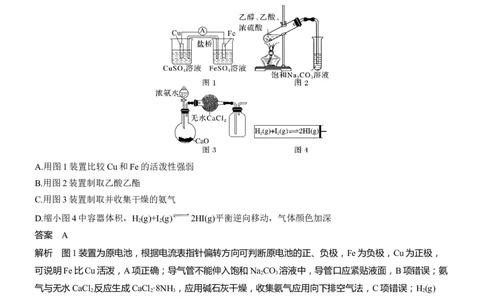
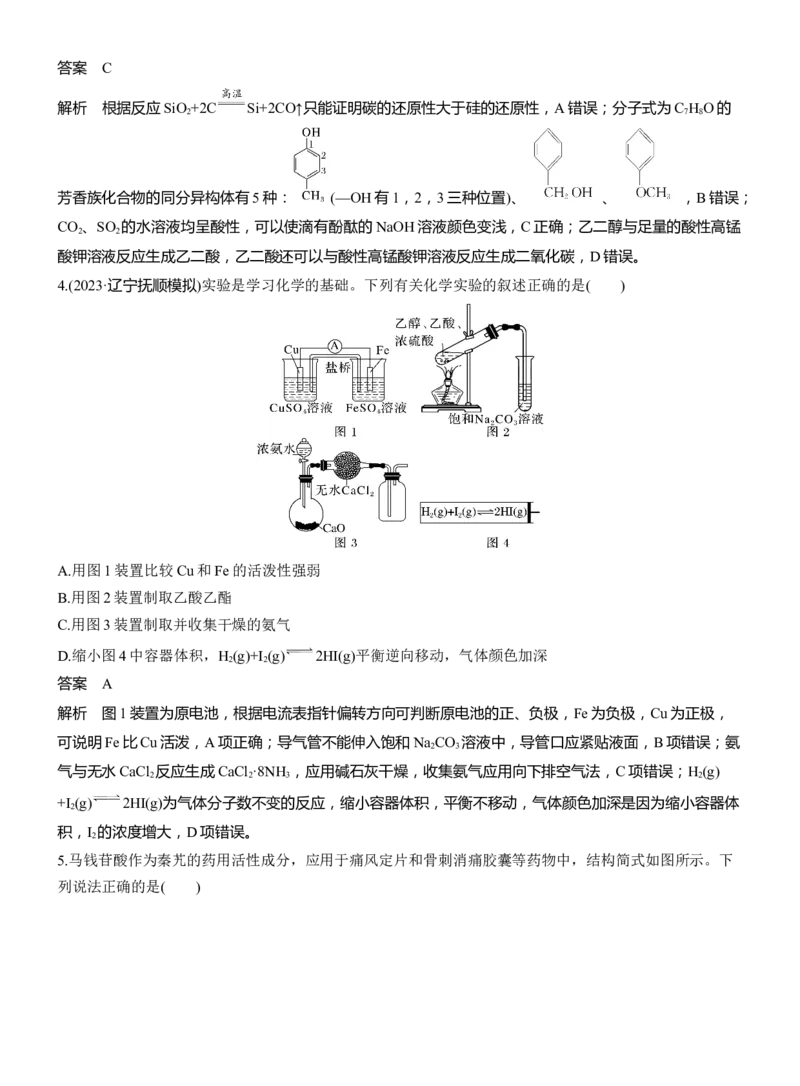
4.(2023·辽宁抚顺模拟)实验是学习化学的基础。下列有关化学实验的叙述正确的是( )
A.用图1装置比较Cu和Fe的活泼性强弱
B.用图2装置制取乙酸乙酯
C.用图3装置制取并收集干燥的氨气
D.缩小图4中容器体积,H (g)+I (g) 2HI(g)平衡逆向移动,气体颜色加深
2 2
答案 A
解析 图1装置为原电池,根据电流表指针偏转方向可判断原电池的正、负极,Fe为负极,Cu为正极,
可说明Fe比Cu活泼,A项正确;导气管不能伸入饱和Na CO 溶液中,导管口应紧贴液面,B项错误;氨
2 3
气与无水CaCl 反应生成CaCl ·8NH ,应用碱石灰干燥,收集氨气应用向下排空气法,C项错误;H (g)
2 2 3 2
+I (g) 2HI(g)为气体分子数不变的反应,缩小容器体积,平衡不移动,气体颜色加深是因为缩小容器体
2
积,I 的浓度增大,D项错误。
2
5.马钱苷酸作为秦艽的药用活性成分,应用于痛风定片和骨刺消痛胶囊等药物中,结构简式如图所示。下
列说法正确的是( )A.马钱苷酸分子中一定含有平面环状结构
B.马钱苷酸最多消耗Na、NaOH的物质的量之比为3∶2
C.马钱苷酸能使酸性KMnO 溶液和溴水褪色且原理相同
4
D.马钱苷酸能发生消去、酯化、加成等反应
答案 D
解析 马钱苷酸分子中环上含有多个sp3杂化的碳原子,不可能含有平面环状结构,A错误;马钱苷酸中
羟基和羧基能够和Na反应,羧基可以和NaOH反应,1 mol马钱苷酸消耗Na、NaOH的物质的量分别为6
mol、1 mol,B错误;马钱苷酸使酸性KMnO 溶液褪色是发生了氧化反应,而使溴水褪色是发生了加成反
4
应,C错误。
6.“6HCl+2Na [Ag(S O ) ]===6NaCl+Ag S↓+3S↓+3SO ↑+H SO +2H O”为定影液回收Ag S的原理。N 是阿
3 2 3 2 2 2 2 4 2 2 A
伏加德罗常数的值。下列说法正确的是( )
A.36.5 g HCl中电子数为8N
A
B.含1 mol Na [Ag(S O ) ]的溶液中阳离子数为4N
3 2 3 2 A
C.1 mol H SO 中含有—OH数为2N
2 4 A
D.生成2.24 L SO (已折算为标准状况)时,转移电子数为2N
2 A
答案 C
解析 36.5 g HCl(1 mol)含有的电子数为18N ,A项错误;1 mol该溶液中,溶质是配合物,自身能完全电
A
离出钠离子,但阴离子解离出银离子的能力相当小,因此溶液中的阳离子数目小于4N ,B项错误;一个
A
硫酸(H SO )分子中有两个氧原子与硫原子形成双键,另外两个氧原子与氢原子形成羟基,因此1 mol硫酸
2 4
中含有羟基的数目为2N ,C项正确;生成3 mol SO 时,转移电子数为10N ,生成2.24 L SO 时,转移电
A 2 A 2
1
子数为 N ,D项错误。
3 A
7.下列化学用语或离子方程式书写错误的是( )
A.用电子式表示MgCl 的形成过程:
2
B.用惰性电极电解MgCl 溶液:2Cl-+2H O H ↑+Cl ↑+2OH-
2 2 2 2
C.向含a mol FeBr 的溶液中通入a mol Cl :2Fe2++2Br-+2Cl ===2Fe3++Br +4Cl-
2 2 2 2
D.向Na S O 溶液中加入足量稀硝酸:3S O2- +2NO- +2H+===3S↓+3SO2- +2NO↑+H O
2 2 3 2 3 3 4 2
答案 B解析 用惰性电极电解MgCl 溶液会产生氢氧化镁沉淀,反应的离子方程式为Mg2++2Cl-+2H O
2 2
H ↑+Cl ↑+Mg(OH) ↓,故B错误;等物质的量溴化亚铁与氯气反应,亚铁离子全部被氧化,溴离子一半被
2 2 2
氧化,离子方程式为2Fe2++2Br-+2Cl ===2Fe3++Br +4Cl-,故C正确。
2 2
8.二水四氯合钴酸铵的制备反应为[CoCl (H O) ]·2H O+2NH Cl===(NH ) [CoCl (H O) ]+4H O,下列说法
2 2 4 2 4 4 2 4 2 2 2
正确的是( )
A.基态Co原子核外电子的空间运动状态有27种
B.键角:H O>H S>H Se
2 2 2
C.该反应中所涉及的元素位于p区的有4种
D.[CoCl (H O) ]·2H O中含有离子键、配位键、σ键等
2 2 4 2
答案 B
解析 基态Co原子核外电子排布式为1s22s22p63s23p63d74s2,电子的空间运动状态为15种,A错误;一般
的对于周围原子相同、中心原子不同的结构类似的分子,中心原子电负性越强,键角越大,故键角:
H O>H S>H Se,B正确;涉及元素中位于p区的有Cl、N、O三种,C错误;[CoCl (H O) ]·2H O中Co
2 2 2 2 2 4 2
与Cl原子、H O形成配位键,H O存在σ键,没有离子键,D错误。
2 2
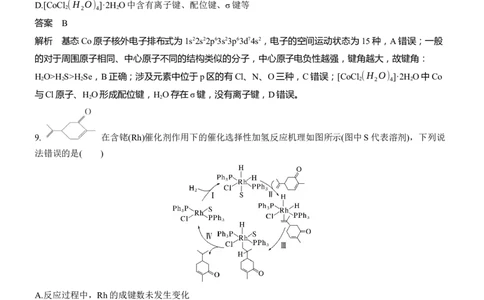
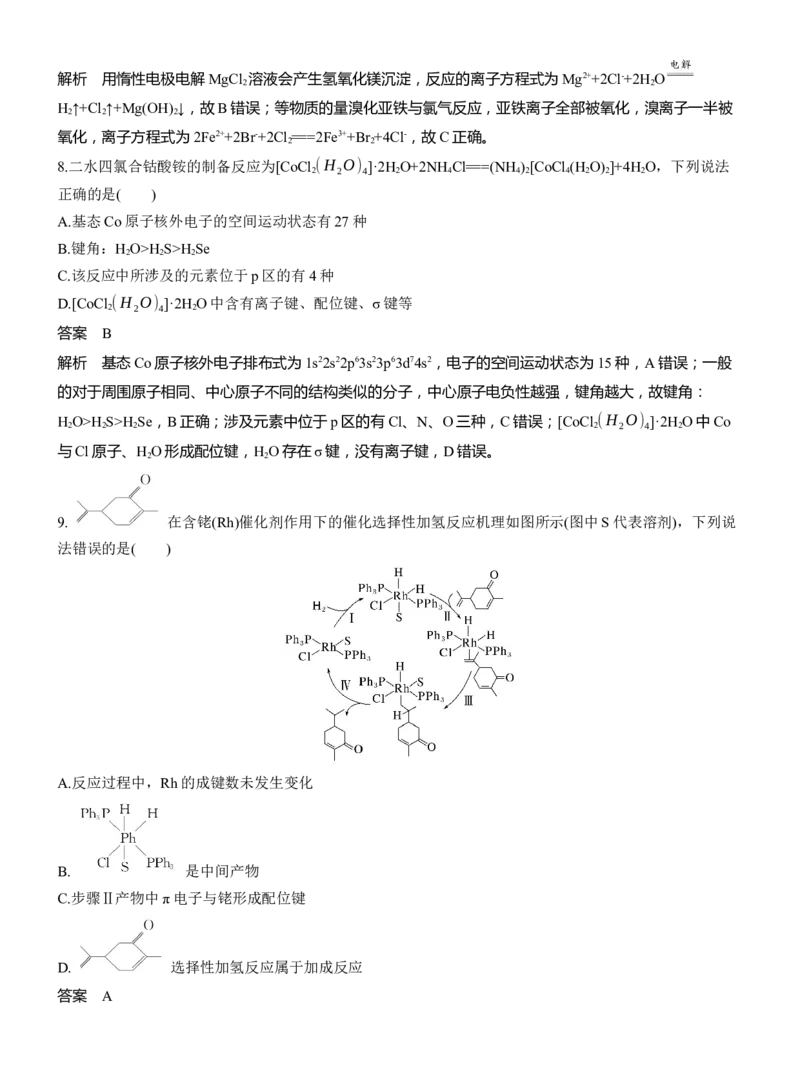
9. 在含铑(Rh)催化剂作用下的催化选择性加氢反应机理如图所示(图中S代表溶剂),下列说
法错误的是( )
A.反应过程中,Rh的成键数未发生变化
B. 是中间产物
C.步骤Ⅱ产物中π电子与铑形成配位键
D. 选择性加氢反应属于加成反应
答案 A解析 步骤Ⅰ中Rh的成键数增加了2个,步骤Ⅳ中Rh的成键数减少了2个,A错误;
是催化剂,与H 反应生成 ,其为中间产物,B正确;步骤Ⅱ中,碳碳双键提供π电子,
2
铑提供空轨道,形成配位键,C正确; 与H 的反应属于加成反应,D正确。
2
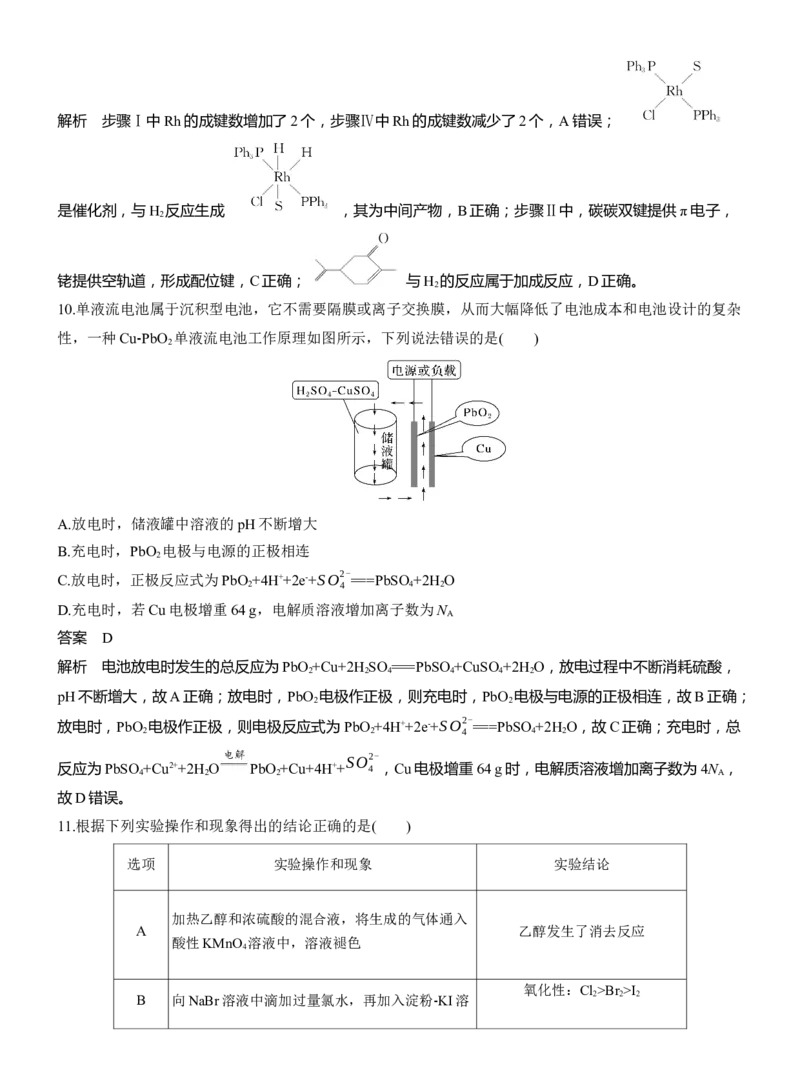
10.单液流电池属于沉积型电池,它不需要隔膜或离子交换膜,从而大幅降低了电池成本和电池设计的复杂
性,一种Cu⁃PbO
2
单液流电池工作原理如图所示,下列说法错误的是( )
A.放电时,储液罐中溶液的pH不断增大
B.充电时,PbO 电极与电源的正极相连
2
C.放电时,正极反应式为PbO +4H++2e-+SO2- ===PbSO +2H O
2 4 4 2
D.充电时,若Cu电极增重64 g,电解质溶液增加离子数为N
A
答案 D
解析 电池放电时发生的总反应为PbO +Cu+2H SO ===PbSO +CuSO +2H O,放电过程中不断消耗硫酸,
2 2 4 4 4 2
pH不断增大,故A正确;放电时,PbO 电极作正极,则充电时,PbO 电极与电源的正极相连,故B正确;
2 2
放电时,PbO 电极作正极,则电极反应式为PbO
+4H++2e-+SO2-
===PbSO +2H O,故C正确;充电时,总
2 2 4 4 2
SO2-
反应为PbSO +Cu2++2H O PbO +Cu+4H++ 4 ,Cu电极增重64 g时,电解质溶液增加离子数为4N ,
4 2 2 A
故D错误。
11.根据下列实验操作和现象得出的结论正确的是( )
选项 实验操作和现象 实验结论
加热乙醇和浓硫酸的混合液,将生成的气体通入
A 乙醇发生了消去反应
酸性KMnO 溶液中,溶液褪色
4
氧化性:Cl>Br >I
B 向NaBr溶液中滴加过量氯水,再加入淀粉 ⁃KI溶 2 2 2液,先变橙色,后变蓝色
向浓度均为0.1 mol·L-1的MgCl 、CuCl 混合溶液
2 2
C K [Mg(OH) ]>K [Cu(OH) ]
sp 2 sp 2
中逐滴加入NaOH溶液,先出现蓝色沉淀
向某无色溶液中加入稀盐酸,将产生的气体通入
原溶液中一定含有CO2-
或
3
D
澄清石灰水中,澄清石灰水变浑浊 HCO-
3
答案 C
解析 挥发的乙醇也能使酸性KMnO 溶液褪色,不能证明乙醇发生消去反应,A错误;过量氯水与KI溶
4
液直接反应,不能证明氧化性:Br >I ,B错误;相同类型的沉淀,K 小的先沉淀,故
2 2 sp
K [Mg(OH) ]>K [Cu(OH)
],C正确;原溶液中也可能含有SO2- 或HSO-
,D错误。
sp 2 sp 2 3 3
12.实验室用MnO 等原料制取KMnO 粗品的实验流程如下。下列说法正确的是( )
2 4
A.“熔融”时,应先将MnO 和KClO 混合加热一段时间后再加入KOH
2 3
B.通入CO “歧化”时,氧化剂与还原剂的物质的量之比为2∶1
2
C.“过滤”时,为加快分离速率可采用减压过滤
D.制得的KMnO 粗品可能会含有K CO ,可以向粗品中滴加盐酸观察是否有气泡来检验是否含有K CO
4 2 3 2 3
答案 C
解析 “熔融”时,先将MnO 和KClO 混合加热一段时间会反应,产生氧气和氯化钾,再加入KOH时不
2 3
反应,A错误;通入CO “歧化”时的反应,氧化剂与还原剂的物质的量之比为1∶2, B错误;“过滤”
2
时,为加快分离速率可采用减压过滤,C正确;制得的KMnO 粗品可能会含有K CO ,向粗品中滴加盐酸
4 2 3
即使没有K CO 也会产生氯气,D错误。
2 3
13.X、Y、Z、W是原子序数依次增大的短周期主族元素,X原子有两个单电子且电负性是四种元素中最大
的,Y原子的最外层电子数是X原子内层电子数的2倍,Z原子s能级上电子数与p能级上电子数之比为
2∶3,W第一电离能大于Z。下列说法正确的是( )
A.电负性:YY>W,C错误;元素的非金属性越强,其最简单氢化物的稳定性就越强,故最简单氢化物的稳
定性:SiH c(Mg2+)=c(HF)>c(H+)
答案 C
c(HF)
解析 根据lg[ ]越小,则氢离子浓度越大,根据H+(aq)+F-(aq) HF(aq),平衡正移,则氟离子浓
c(H+
)
度越小,对于MgF (s) Mg2+(aq)+2F-(aq),氟离子浓度减小,则镁离子浓度增大,则-lg c(F-)增大,-lg
2
c(HF) c(HF)
c(Mg2+)减小,因此L 代表-lg c(F-)与lg[ ]的变化曲线,L 代表-lg c(Mg2+)与lg[ ]的变化曲线,
1 c(H+
)
2 c(H+
)
c(HF)
A正确;lg[ ]=1时,-lg c(F-)=2.2,-lg c(Mg2+)=4.0,c(F-)=10-2.2 mol·L-1,c(Mg2+)=10-4 mol·L-1,根据
c(H+
)
MgF (s) Mg2+(aq)+2F-(aq),K (MgF
)=c(Mg2+)·c2(F-)=10-4×(10-2.2
)
2
=10-8.4,K(HF)=10-3.2;当c(Mg2+)=c(F-)
2 sp 2 a
时,c(Mg2+)=c(F-)=√3 K (MgF )=10-2.8,则c点的纵坐标值为2.8,B正确;MgF (s)+2H+(aq) Mg2+(aq)
sp 2 2
K (MgF )
sp 2
+2HF(aq)该反应的平衡常数K= =10-2,C错误;c点溶液中c(Mg2+)=c(F-),根据元素守恒可得
K2 (HF)
a
2c(Mg2+)=c(F-)+c(HF),则c(Mg2+)=c(F-)=c(HF),根据电荷守恒:2c(Mg2+)+c(H+)=c(F-)+c(Cl-)+c(OH-),溶液
c(HF) c(HF)
呈酸性,c(H+)>c(OH-),则c(Cl-)>c(Mg2+),c点lg [ ]>0,则 >1即c(HF)>c(H+),故溶液中存
c(H+
)
c(H+
)
在c(Cl-)>c(Mg2+)=c(HF)>c(H+),D正确。