文档内容
重难点 08 化学反应速率和化学平衡
电化学是历年高考的重要考点之一,很好的落实了宏观辨识与微观探析、证据推理与模型认知、科学精神
与社会责任等学科素养。明确原电池过程、图示中的物质转化是解题的关键。考查的内容为:提供电极材
料和电解质溶液判断能否形成原电池,原电池电极名称判断及电极反应式的书写及产物的判断和计算,,
提供反应方程式设计原电池,结合图像考查电极质量或电解质溶液质量分数的变化。展望2023年高考化学
试题呈现仍然会以我国化学领域最近取得的重大创新科研成果为载体考查考生的必备知识和关键能力,考
查社会主义核心价值观个人层面的爱国精神,落实了立德树人的教育根本任务。
一、化学反应速率的计算及影响因素
气体反应体系中充入惰性气体(不参加反应)时对反应速率的影响
恒温恒容:充入“惰性气体”→总压增大→物质浓度不变(活化分子浓度不变)→反应速率不变。
恒温恒压:充入“惰性气体”→体积增大→物质浓度减小(活化分子浓度减小)→反应速率减小。
三、化学平衡状态及化学平衡移动
1、化学平衡状态判断
是否已达
反应mA(g)+nB(g) pC(g)+qD(g)
平衡状态
各物质的物质的量或各物质的物质的量分数一定 平衡
混合物体
各物质的质量或各物质的质量分数一定 平衡
系中各组
各气体的体积或体积分数一定 平衡
分的含量
总压强、总体积、总物质的量一定 不一定平衡
在单位时间内消耗n mol B,同时生成m mol A,即v
正
平衡
=v
逆
正、逆反 在单位时间内消耗n mol B,同时生成p mol C,均指v
不一定平衡
应速率的
正
关系 v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q,v 不一定等于v 不一定平衡
正 逆
在单位时间内生成了n mol B,同时消耗q mol D,均指
不一定平衡
v
逆
压强不再变化,当m+n≠p+q时 平衡
压强
压强不再变化,当m+n=p+q时 不一定平衡混合气体
M 一定,当m+n≠p+q时 平衡
r
的平均相
对分子质
M 一定,当m+n=p+q时 不一定平衡
r
量M
r
任何化学反应都伴随着能量变化,在其他条件不变的情
温度 平衡
况下,体系的温度一定时
反应体系内有色物质的颜色不变,即有色物质的浓度不
颜色 平衡
变
体系的 若m+n=p+q,且ρ一定 不一定平衡
密度ρ
若m+n≠p+q,恒温恒压且ρ一定 平衡
混合体系 各组分的浓度一定 平衡
中各组分 各组分的浓度相等 不一定平衡
的浓度 c(A)∶c(B)∶c(C)∶c(D)=m∶n∶p∶q 不一定平衡
三、化学反应速率与化学平衡图像分析
1、速率—时间图像
反应mA(g)+nB(g) pC(g)+qD(g),m+n>p+q,且ΔH>0
(1)t 时增大反应物的浓度,正反应速率瞬间增大,然后逐渐减小,而逆反应速率逐渐增大;
1
(2)t 时升高温度,正反应和逆反应速率均增大,吸热反应的反应速率增大得快;
2
(3)t 时减小压强,容器容积增大,浓度变小,正反应速率和逆反应速率均减小,正反应的反应速率减小得
3
多;
(4)t 时使用催化剂,正反应速率和逆反应速率均瞬间增大但仍相等。
4
2. 转化率(或含量)—时间图像
反应mA(g)+nB(g) pC(g)+qD(g),m+n>p+q,且ΔH>0(1)图甲表示压强对反应物转化率的影响,对于气体反应物化学计量数之和大于气体生成物化学计量数之和
的反应,压强越大,反应物的转化率越大;
(2)图乙表示温度对反应物转化率的影响,对于吸热反应,温度越高,反应物的转化率越大;
(3)图丙表示催化剂对反应物转化率的影响,催化剂只能改变化学反应速率,不能改变反应物的转化率。
3.恒压(温)线(α表示反应物的转化率,c表示反应物的平衡浓度)
图①,若P>P>P,则正反应为气体体积减小的反应,ΔH<0;
1 2 3
图②,若T >T,则正反应为放热反应。
1 2
分析时可沿横轴作一条平行于纵轴的虚线,即为等压线或等温线,然后分析另一条件变化对该反应的
影响。
4.特殊类型图像
(1)对于化学反应mA(g)+nB(g) pC(g)+qD(g),如图所示,M点前,表示从反应物开始,v >v ;M
正 逆
点为刚达到平衡点;M点后为平衡受温度的影响情况,即升温,A的百分含量增加或C的百分含量减少,
平衡左移,故正反应ΔH<0。
(2)对于化学反应mA(g)+nB(g) pC(g)+qD(g),如图所示,L线上所有的点都是平衡点。L线的左上
方(E点),A的百分含量大于此压强时平衡体系的A的百分含量,所以E点v >v ;则L线的右下方(F
正 逆
点),v <v 。
正 逆
(3)曲线的意义是外界条件(如温度、压强等)对正、逆反应速率影响的变化趋势及变化幅度。图中交点A
是平衡状态,压强增大,正反应速率增大得快,平衡正向移动。化学平衡图像题的解答原则
(1)“定一议二”原则。
在化学平衡图像中,包括纵坐标、横坐标和曲线所表示的三个量,确定横坐标所表示的量后,讨论纵
坐标与曲线的关系或确定纵坐标所表示的量,讨论横坐标与曲线的关系。
(2)“先拐先平,数值大”原则。
在化学平衡图像中,先出现拐点的反应则先达到平衡,先出现拐点的曲线表示的温度较高或表示的压强较
大。
五、化学平衡常数、转化率的相关计算
1.K的大小只与温度有关,与反应物或生成物的起始浓度的大小无关。
代入平衡常数表达式的是平衡浓度,而不是任意时刻的浓度,更不能将物质的量代入。
同一化学反应,可以用不同的化学方程式表示,每个化学方程式都有自己的平衡常数表达式及相应的平衡
常数。因此,要注意使用与化学方程式相对应的平衡常数。
2.转化率的分析与判断
反应 的转化率分析
①若反应物起始物质的量之比等于化学计量数之比,达到平衡后,它们的转化率相等。
②若只增加A的量,平衡正向移动,B的转化率提高,A的转化率降低。
③若按原比例同倍数地增加(或降低)A、B的浓度,等效于压缩(或扩大)容器体积,气体反应物的转化率
与其化学计量数有关。
同倍增大c(A)和c(B)
1. (2023江苏卷)二氧化碳加氢制甲烷过程中的主要反应为
在密闭容器中, 、 时, 平衡转化率、在催化剂作用下反应
相同时间所测得的 实际转化率随温度的变化如题图所示。 的选择性可表示为
。下列说法正确的是A. 反应 的焓变
B. 的平衡选择性随着温度的升高而增加
C. 用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃
D. 450℃时,提高 的值或增大压强,均能使 平衡转化率达到X点的值
【答案】D
【 解 析 】 A . 由 盖 斯 定 律 可 知 反 应 的 焓 变
,A错误;
B. 为放热反应,升高温度平衡逆向移动, 的含量降低,
故 的平衡选择性随着温度的升高而降低,B错误;
C.由图可知温度范围约为450~550℃时二氧化碳实际转化率趋近于平衡转化率,此时为最适温度,温度继
续增加,催化剂活性下降,C错误;
D.450℃时,提高 的值可提高二氧化碳的平衡转化率,增大压强反应I平衡正向移动,可提
高二氧化碳的平衡转化率,均能使 平衡转化率达到X点的值,D正确。
故选D。
2.(2022年江苏卷) 乙醇-水催化重整可获得 。其主要反应为
,
,在 、
时,若仅考虑上述反应,平衡时 和CO的选择性及 的产率随温度的变化如图所示。CO的选择性 ,下列说法正确的是
A. 图中曲线①表示平衡时 产率随温度的变化
B. 升高温度,平衡时CO的选择性增大
C. 一定温度下,增大 可提高乙醇平衡转化率
D. 一定温度下,加入 或选用高效催化剂,均能提高平衡时 产率
【答案】B
【解析】
【分析】根据已知反应① ,反应②
,且反应①的热效应更大,温度升高的时候对反应①
影响更大一些,根据选择性的含义,升温时CO选择性增大,同时CO 的选择性减小,所以图中③代表CO
2
的选择性,①代表CO 的选择性,②代表H 的产率,以此解题。
2 2
【详解】A.由分析可知②代表H 的产率,故A错误;
2
B.由分析可知升高温度,平衡时CO的选择性增大,故B错误;
C.一定温度下,增大 ,可以认为开始时水蒸气物质的量不变,增大乙醇物质的量,乙醇的
平衡转化率降低,故C错误;
D.加入 或者选用高效催化剂,不会影响平衡时 产率,故D错误;
故选B。
3.(2021·江苏卷)NH 与O 作用分别生成N、NO、NO的反应均为放热反应。工业尾气中的NH 可通过
3 2 2 2 3
催化氧化为N 除去。将一定比例的NH 、O 和N 的混合气体以一定流速通过装有催化剂的反应管,NH
2 3 2 2 3
的转化率、生成N 的选择性[ 100%]与温度的关系如图所示。
2下列说法正确的是
A. 其他条件不变,升高温度,NH 平的衡转化率增大
3
B. 其他条件不变,在175~300 ℃范围,随温度的升高,出口处N 和氮氧化物的量均不断增大
2
C. 催化氧化除去尾气中的NH 应选择反应温度高于250 ℃
3
D. 高效除去尾气中的NH ,需研发低温下NH 转化率高和N 选择性高的催化剂
3 3 2
【答案】D
【解析】
【详解】A.NH 与O 作用分别生成N 、NO、NO的反应均为放热反应,根据勒夏特列原理,升高温度,
3 2 2 2
平衡向逆反应方向进行,氨气的平衡转化率降低,故A错误;
B.根据图像,在175~300 ℃范围,随温度的升高,N 的选择率降低,即产生氮气的量减少,故B错误;
2
C.根据图像,温度高于250℃ N 的选择率降低,且氨气的转化率变化并不大,浪费能源,根据图像,温
2
度应略小于225℃,此时氨气的转化率、氮气的选择率较大,故C错误;
D.氮气对环境无污染,氮的氧化物污染环境,因此高效除去尾气中的NH ,需研发低温下NH 转化率高
3 3
和N 选择性高的催化剂,故D正确;
2
答案为D。
(建议用时:45分钟)
1.(2023上·江苏连云港·高三统考期中)使用丙烯 可将汽车尾气中的 还原为 除去,主要反
应为
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
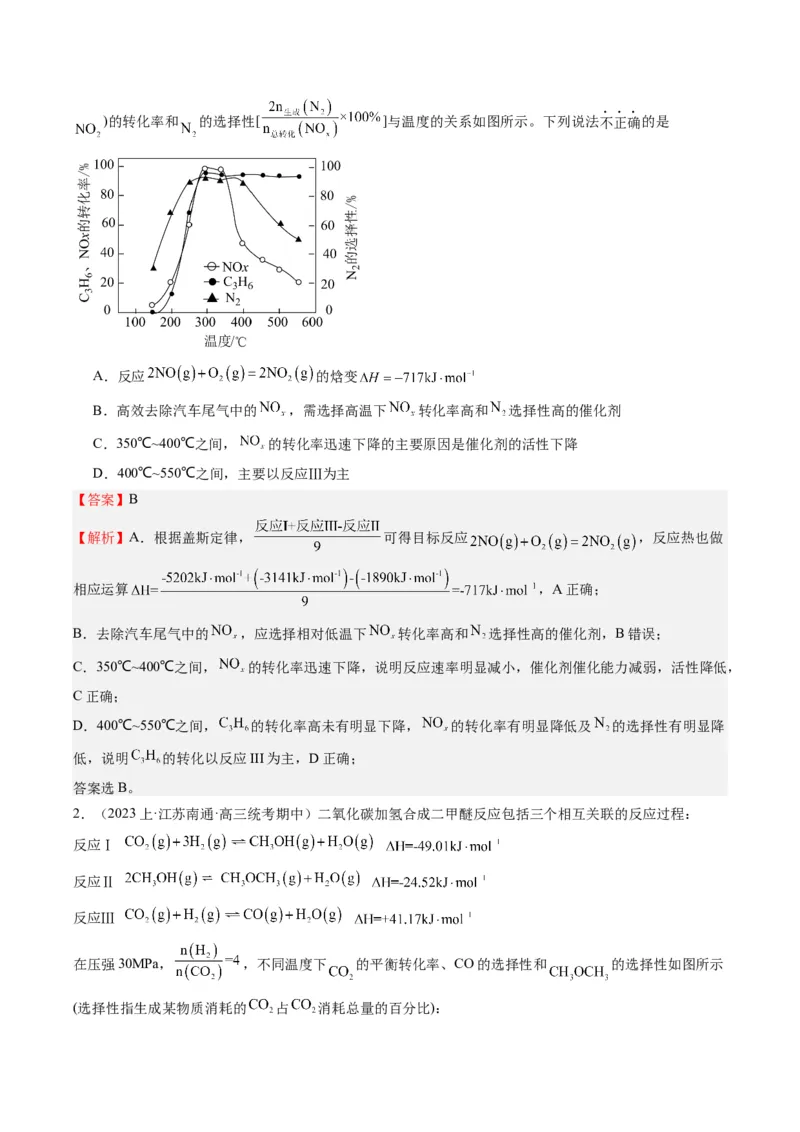
将一定比例 、 、NO、 的混合气体以一定流速通过装有催化剂的反应管, 、 (NO和)的转化率和 的选择性[ ]与温度的关系如图所示。下列说法不正确的是
A.反应 的焓变
B.高效去除汽车尾气中的 ,需选择高温下 转化率高和 选择性高的催化剂
C.350℃~400℃之间, 的转化率迅速下降的主要原因是催化剂的活性下降
D.400℃~550℃之间,主要以反应Ⅲ为主
【答案】B
【解析】A.根据盖斯定律, 可得目标反应 ,反应热也做
相应运算 ,A正确;
B.去除汽车尾气中的 ,应选择相对低温下 转化率高和 选择性高的催化剂,B错误;
C.350℃~400℃之间, 的转化率迅速下降,说明反应速率明显减小,催化剂催化能力减弱,活性降低,
C正确;
D.400℃~550℃之间, 的转化率高未有明显下降, 的转化率有明显降低及 的选择性有明显降
低,说明 的转化以反应III为主,D正确;
答案选B。
2.(2023上·江苏南通·高三统考期中)二氧化碳加氢合成二甲醚反应包括三个相互关联的反应过程:
反应Ⅰ
反应Ⅱ
反应Ⅲ
在压强30MPa, ,不同温度下 的平衡转化率、CO的选择性和 的选择性如图所示
(选择性指生成某物质消耗的 占 消耗总量的百分比):下列说法正确的是
A.曲线A表示 的选择性
B.300℃时,生成 的 平衡转化率为3%
C.220~240℃间,升高温度,比值 减小
D.为同时提高 的平衡转化率和 的选择性,应选择低温、高压的反应条件
【答案】D
【分析】由盖斯定律可知,反应Ⅰ×2+反应Ⅱ得到反应
,升高温度,平衡向逆反应方向移动,二甲醚的选择性减小,反应Ⅲ为吸热反应,升
高温度,平衡向正反应方向移动,一氧化碳的选择性增大,则曲线A表示一氧化碳的选择性、曲线B表示
二氧化碳的转化率、曲线C表示二甲醚的选择性。
【解析】A. 由分析可知,曲线C表示二甲醚的选择性,故A错误;
B.由图可知,300℃平衡时,二氧化碳的转化率为30%、二甲醚的选择性为20%,设二氧化碳的起始物质
的量为1mol,则反应生成二甲醚消耗二氧化碳的物质的量为1mol×30%×20%×2=0.12mol,则生成二甲醚的
二氧化碳的转化率为 ×100%=12%,故B错误;
C.反应Ⅰ为放热反应、反应Ⅲ为吸热反应,220~240℃间,升高温度,反应Ⅰ的平衡向正反应方向移动,
反应生成二氧化碳和氢气的物质的量比为1:3,反应Ⅲ的平衡向正反应方向移动,消耗二氧化碳和氢气的
物质的量比为1:1,则比值 增大,故C错误;
D.反应Ⅰ为气体体积减小的放热反应,反应Ⅲ为气体体积不变吸热反应,增大压强,反应Ⅰ的平衡向正
反应方向移动、反应Ⅲ的平衡不移动,则二氧化碳的转化率和甲醇的选择性都增大,降低温度,反应Ⅰ的
平衡向正反应方向移动、反应Ⅲ的平衡向逆反应方向移动,则二氧化碳的转化率和甲醇的选择性都增大,
所以为同时提高二氧化碳的平衡转化率和甲醇的选择性,应选择低温、高压的反应条件,故D正确;
故选D。
3.(2023·吉林长春·东北师大附中校考三模)反应 的速率方程为(k为速率常数,其中 , A、R为常数, 为活化能,T为开氏温
度),其半衰期反应物消耗一半所需的时间)为0.8/k。改变反应物浓度时,反应的瞬时速率如表所示。下列
说法正确的是
/ 0.25 0.5 1 0.5 1
/ 0.05 0.05 0.1 0.1 0.2
v/ 1.6 3.2 3.2
A.
B.
C.升温、加入催化剂,缩小容积(加压),均能使k增大,导致反应的瞬时速率加快
D.在过量的B存在时,A剩余12.5%所需的时间是
【答案】D
【分析】由第二组和第四组数据,A浓度相同,B浓度不同,速率相等,可知n=0,再由第一组和第二组
数据代入 可得 ,可知m=1;将第一组数据代入
,可得k=6.4×10-3,则 。
【解析】A.根据数据分析, , , ,A错误;
B.由分析可知,速率常数 ,B错误;
C.速率常数与浓度无关,缩小容积(加压)不会使k增大,C错误;
D.存在过量的B时,反应掉87.5%的A可以看作经历3个半衰期,即 ,因此所需的时
间为 ,D正确;
故选D。
4.(2023上·江苏徐州·高三徐州市第一中学校联考)利用CO 和 H 可制得甲烷,实现资源综合利用。
2 2
已知:I. -1
2 2 2 1
II. CO(g)+4H(g)=CH (g)+2HO(g) △H=-165.0 kJ·mol-1
2 2 4 2 2
在一定的温度和压力下,将按一定比例混合的CO 和H 混合气体通过装有催化剂的反应器, 反应相同时
2 2
间, CO 转化率和 CH 选择性随温度变化关系如图所示。
2 4
CH 选择性=
4下列说法不正确的是
A.反应Ⅱ:2E(C=O)+4E(H-H)<4E(C-H)+4E(H-O)(E表示键能)
B.240℃时,其他条件不变,增大压强能提高CO 的转化率
2
C.在260~300℃间, 其他条件不变, 升高温度 CH 的产率增大
4
D.320℃时CO 的转化率最大,说明反应I和反应II一定都达到了平衡状态
2
【答案】D
【分析】在两种不同催化剂作用下反应相同时间,化学反应速率越大、选择性越高,则甲烷的产率越高。
【解析】A.反应Ⅱ为放热反应,断裂化学键吸收的能量小于形成化学键放出的能量,即2E(C=O)+4E(H-
H)<4E(C-H)+4E(H-O) ,故A正确;
B.增大压强,反应Ⅱ平衡正向移动,故能提高CO 的转化率, 故B正确;
2
C.在260℃~320℃间,以为催化剂,升高温度CH 的选择性虽然基本不变,但CO 的转化率在上升,所以
4 2
CH 的产率上升,故C正确;
4
D.320℃时CO 的转化率最大,可能是因为温度过高而导致催化剂失去活性导致,从而无法判定此时的转
2
化率就是平衡转化率,则此时两个反应也不一定达到平衡状态,故D错误;
答案选D。
5.(2023上·江苏盐城·高三盐城中学校联考期中) 还原 是实现“双碳”经济的有效途径之一、
其反应有:
Ⅰ:
Ⅱ:
常压下 和 按物质的量之比 投料,某一时段内 和 的转化率随温度变化如图所示。下列
说法正确的是A.反应Ⅱ的平衡常数
B.提高 平衡转化率的条件是高温高压
C.温度高于700℃,含氢产物中 占比降低
D.1000℃时的混和体系中CO的体积百分含量约为46.7%
【答案】D
【解析】A.反应Ⅱ为: ,因此平衡常数 ,A错误;
B.两反应都为吸热反应,且反应Ⅰ为气体体积增大的反应,反应ⅠⅠ为气体体积不变的反应,因此,欲
提高 平衡转化率的条件应为高温低压,B错误;
C.由图可知,温度高于700℃,甲烷转化率增大,因此含氢产物中 占比增大,C错误;
D.由图可知,1000℃时,甲烷转化率为100%,假设起始时充入 物质的量为1mol, 物质的量为
3mol,则根据反应Ⅰ,反应结束时,消耗二氧化碳1mol,同时生成2molCO与2mol氢气,设反应Ⅱ消耗
物质的量为x mol,根据反应方程式 ,此时消耗氢气x mol,生成
CO与水蒸气各x mol,根据1000℃时, 转化率为60%,则可列 ,求得x=0.8mol,则
反应结束时,体系中含有 与氢气各1.2mol,CO2.8mol,水蒸气0.8mol,则此时CO体积分数为
,D正确;
故选D。
6.(2023上·黑龙江哈尔滨·高三哈九中校考)已知2H(g)+2NO(g) N(g)+2HO(g),N 的瞬时生成速率
2 2 2 2
,H 的瞬时生成速率 (k、k 表示速率常数)。
2 1 2
一定温度下,控制NO起始浓度为1mol/L,改变H 起始浓度,进行以上反应的实验,得到N 的生成速率
2 2
和H 起始浓度呈如图所示的直线关系。下列说法正确的是
2A.m=1
B.速率常数k=9. 375(mol/L)2·s-1
1
C.其它条件不变,增大H 浓度,正反应速率增大,逆反应速率不变
2
D.该温度下,反应的化学平衡常数K=
【答案】A
【解析】A.根据图像可知,N 的瞬时生成速率 ,与氢气的起始浓度呈直线关系,
2
则m=1,A正确;
B.由图可知,当 时, ,代入 ,
,B错误;
C.其它条件不变,增大H 浓度,正、逆反应速率都会增大,C错误;
2
D. ,根据N 的瞬时生成速率 ,H 的瞬时生成速率
2 2
, ,则 ,D错误;
故选A。
7.(2023上·江苏常州·高三统考期中)工业上用 和 的高温气相反应制备苯硫酚( ),其
主要反应为:
已知:高温下, 热解形成 和 , 与卤代苯中C-X的碳成键,首先形成中间体 ,反
应速率较慢;中间体再迅速脱去 ,形成苯硫酚,将 的混合气以一定流速(反
应停留时间45s)通过管式反应器,测得 的转化率、 与 的产率随温度的变化如图所示,
下列说法不正确的A.图中曲线①表示 的产率随温度的变化
B.反应中还可能存在二苯硫醚( )等副产物
C.一定温度下,增大 一定可提高 的产率
D.保持其他条件不变,若改用 作原料,可提高卤代苯的转化率
【答案】C
【解析】A.由题给信息可知,高温条件下氯苯与硫化氢生成硫酚的反应速率快于生成苯的反应速率,由
图可知,反应①的反应速率快于反应②,所以曲线①表示硫酚的产率随温度的变化,故A正确;
B.由题给信息可知,高温条件下氯苯与硫化氢生成硫酚的反应速率快于生成苯的反应速率,则反应生成
的硫酚可能发生取代反应生成二苯硫醚,故B正确;
C.由题给方程式可知,一定温度下,增大 的值,题给两个反应均能向正反应方向移动,则二
苯硫醚和苯的产率均可能增大,故C错误;
D.溴元素的电负性小于氯元素,碳溴键易于碳氯键断裂,则保持其他条件不变,若改用溴苯作原料,可
提高卤代苯的转化率,故D正确;
故选C。
8.(2023上·河南南阳·高三南阳中学校考)向AgCl饱和溶液(有足量AgCl固体)中滴加氨水,发生反应
和 , 与
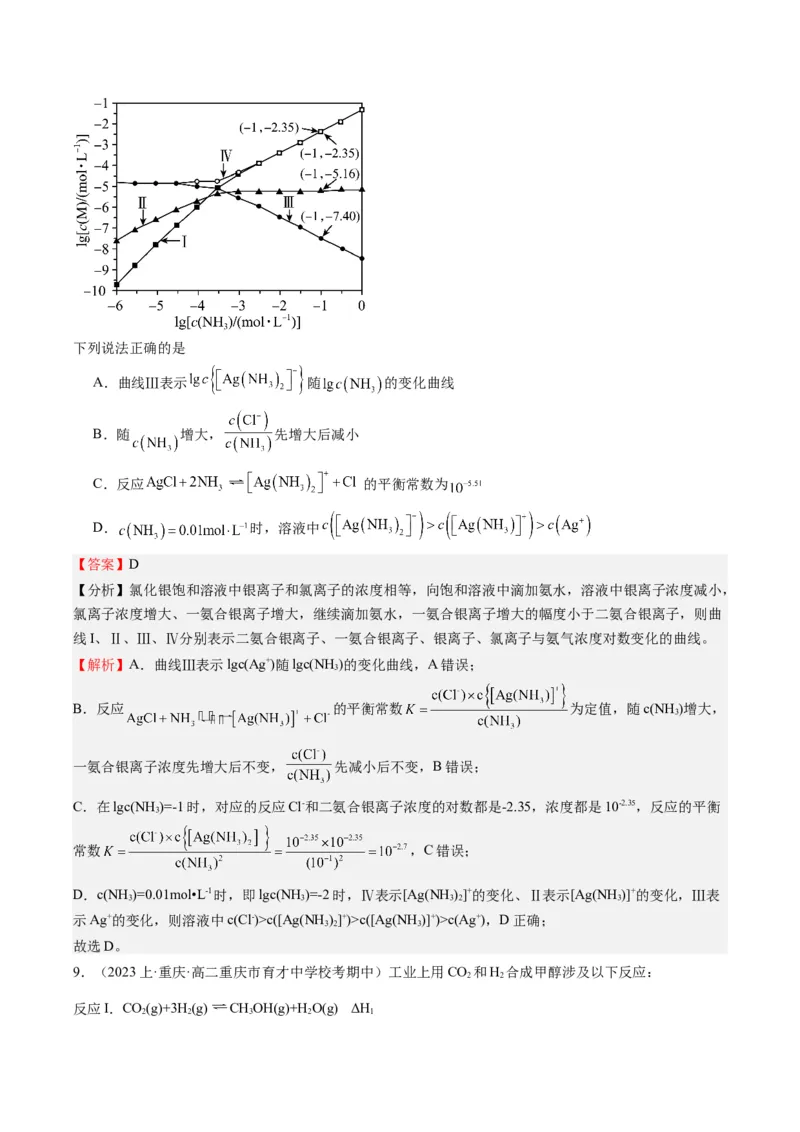
的关系如图所示{其中M代表 、 、 或 }。下列说法正确的是
A.曲线Ⅲ表示 随 的变化曲线
B.随 增大, 先增大后减小
C.反应 的平衡常数为
D. 时,溶液中
【答案】D
【分析】氯化银饱和溶液中银离子和氯离子的浓度相等,向饱和溶液中滴加氨水,溶液中银离子浓度减小,
氯离子浓度增大、一氨合银离子增大,继续滴加氨水,一氨合银离子增大的幅度小于二氨合银离子,则曲
线I、Ⅱ、Ⅲ、Ⅳ分别表示二氨合银离子、一氨合银离子、银离子、氯离子与氨气浓度对数变化的曲线。
【解析】A.曲线Ⅲ表示lgc(Ag+)随lgc(NH)的变化曲线,A错误;
3
B.反应 的平衡常数 为定值,随c(NH )增大,
3
一氨合银离子浓度先增大后不变, 先减小后不变,B错误;
C.在lgc(NH)=-1时,对应的反应Cl-和二氨合银离子浓度的对数都是-2.35,浓度都是10-2.35,反应的平衡
3
常数 ,C错误;
D.c(NH )=0.01mol•L-1时,即lgc(NH)=-2时,Ⅳ表示[Ag(NH)]+的变化、Ⅱ表示[Ag(NH)]+的变化,Ⅲ表
3 3 3 2 3
示Ag+的变化,则溶液中c(Cl-)>c([Ag(NH )]+)>c([Ag(NH )]+)>c(Ag+),D正确;
3 2 3
故选D。
9.(2023上·重庆·高二重庆市育才中学校考期中)工业上用CO 和H 合成甲醇涉及以下反应:
2 2
反应I.CO(g)+3H(g) CHOH(g)+H O(g) ΔH
2 2 3 2 1反应Ⅱ. CO(g)+H(g) CO(g)+HO(g) ΔH
2 2 2 2
在催化剂作用下,将1molCO 和2molH 的混合气体充入一恒容密闭容器中进行反应,达到平衡时,CO 的
2 2 2
转化率和容器中混合气体的平均相对分子质量随温度变化如图。下列判断正确的是
已知:平衡时甲醇的选择性为生成甲醇消耗的CO 在CO 总消耗量中占比。
2 2
A.ΔH<0
2
B.T℃,平衡时甲醇的选择性为40%
C.T℃,反应Ⅱ平衡常数
D.为同时提高CO 的平衡转化率和平衡时甲醇的选择性,应选择的反应条件为高温、高压
2
【答案】C
【解析】A.由图可知,温度越高,CO 的转化率越小,平衡逆向移动,说明逆反应是吸热反应,故反应I
2
为放热反应,反应II为吸热反应,ΔH>0,故A错误;
2
B.T℃,CO 转化率为50%,平均相对分子质量为20,混合气体总物质的量为: =2.4mol,则
2
CO 为0.5mol,设甲醇为xmol,CO为ymol,可列出以下方程:x+y=0.5,n(H )=2-(3x+y),n(H O)=x+y,
2 2 2
n(CHOH)+n(CO)+n(CO )+n(H)+n(HO)=2.4,计算n(CHOH)=0.3mol,n(CO)=0.2mol,甲醇的选择性为
3 2 2 2 3
×100%=60%,故B错误;
C.由B项分析,T℃时,反应Ⅱ中平衡n(CO)=0.5mol,n(H )=0.9mol,n(CO)=0.2mol,
2 2
n(H O)=0.3+0.2=0.5mol,反应Ⅱ平衡常数,故C正确;
2
D.由反应I为放热反应,升高温度,平衡逆向移动,故CO 的平衡转化率降低,则不能选择高温条件,
2
故D错误;
故选:C。
10.(2023上·江苏镇江·高三统考期中) 催化加氢制 的反应体系中,发生的主要反应如下:
反应1:
反应2:
恒压下,将起始 的混合气体以一定流速通过装有催化剂的反应管,测得出口处 的转化率及 和 的选择性[ ]随温度的变化如下图所示。下列说法不
正确的是
A.
B.曲线③表示CO的选择性
C.280℃时出口处 的物质的量分数比220℃时小
D.为提高 生产效率,需研发 转化率高和 选择性高的催化剂
【答案】C
【解析】A.由盖斯定律可知,反应1-反应2可得到目标热化学方程式,A项正确;
B.由选择性定义可知,CO的选择性+ 的选择性=1,由图可知,①是 的选择性,则②是
CO的选择性,B项正确;
C.虽然280℃时甲醇的选择性降低了,但是二氧化碳的转化率提高了,不能判断280℃时出口处
的物质的量分数比220℃时小,C项错误;
D.二氧化碳在高温下转化率高,但甲醇在高温下选择性低,为提高 生产效率,需研发 转化率
高和 选择性高的催化剂,D项正确;
故选C。