文档内容
重难点 10 新型电池和电解原理的应用
(建议用时:35分钟)
【真题再现】
1.(2022·广东卷)以熔融盐为电解液,以含Cu、Mg和Si等的铝合金废料为阳极进行电解,实现Al的再
生。该过程中
A.阴极发生的反应为Mg2e Mg2+ B.阴极上Al被氧化
C.在电解槽底部产生含Cu的阳极泥 D.阳极和阴极的质量变化相等
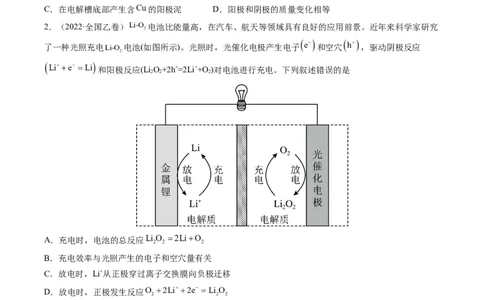
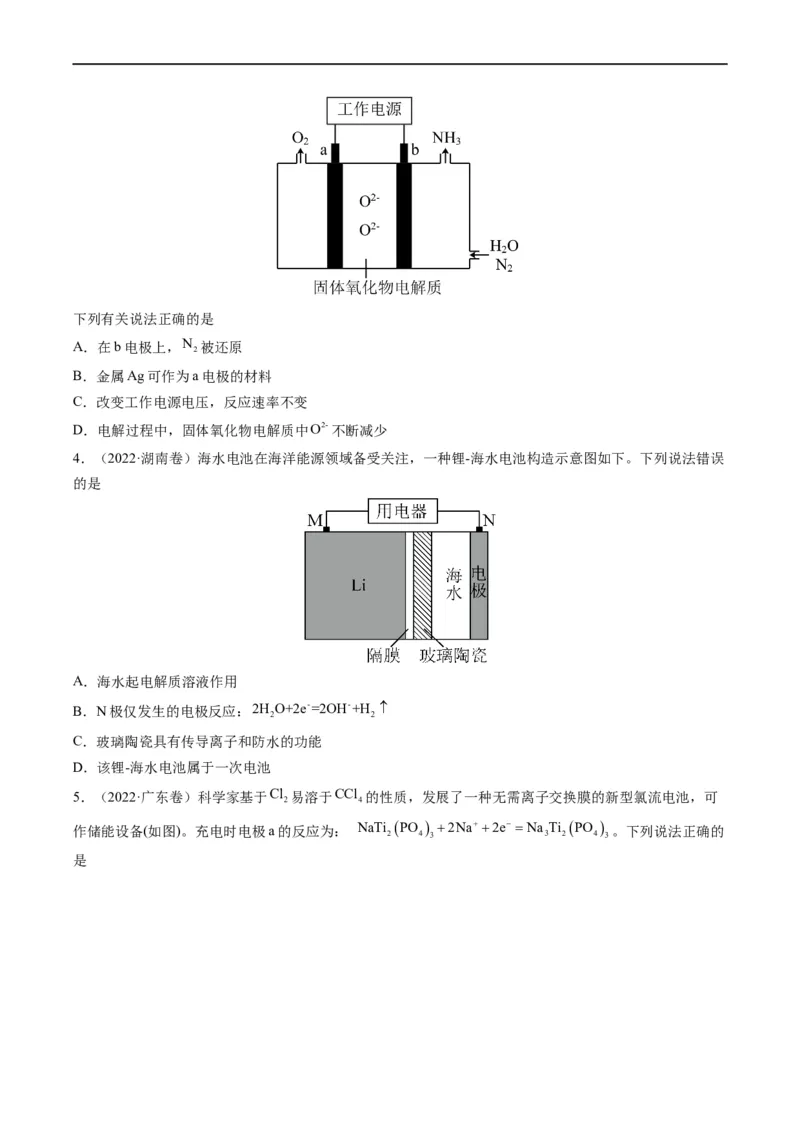
2.(2022·全国乙卷)Li-O 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科学家研究
2
了一种光照充电Li-O 电池(如图所示)。光照时,光催化电极产生电子
e
和空穴
h
,驱动阴极反应
2
Li e Li 和阳极反应(Li O+2h+=2Li++O )对电池进行充电。下列叙述错误的是
2 2 2
A.充电时,电池的总反应Li O 2LiO
2 2 2
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应O 2Li 2e Li O
2 2 2
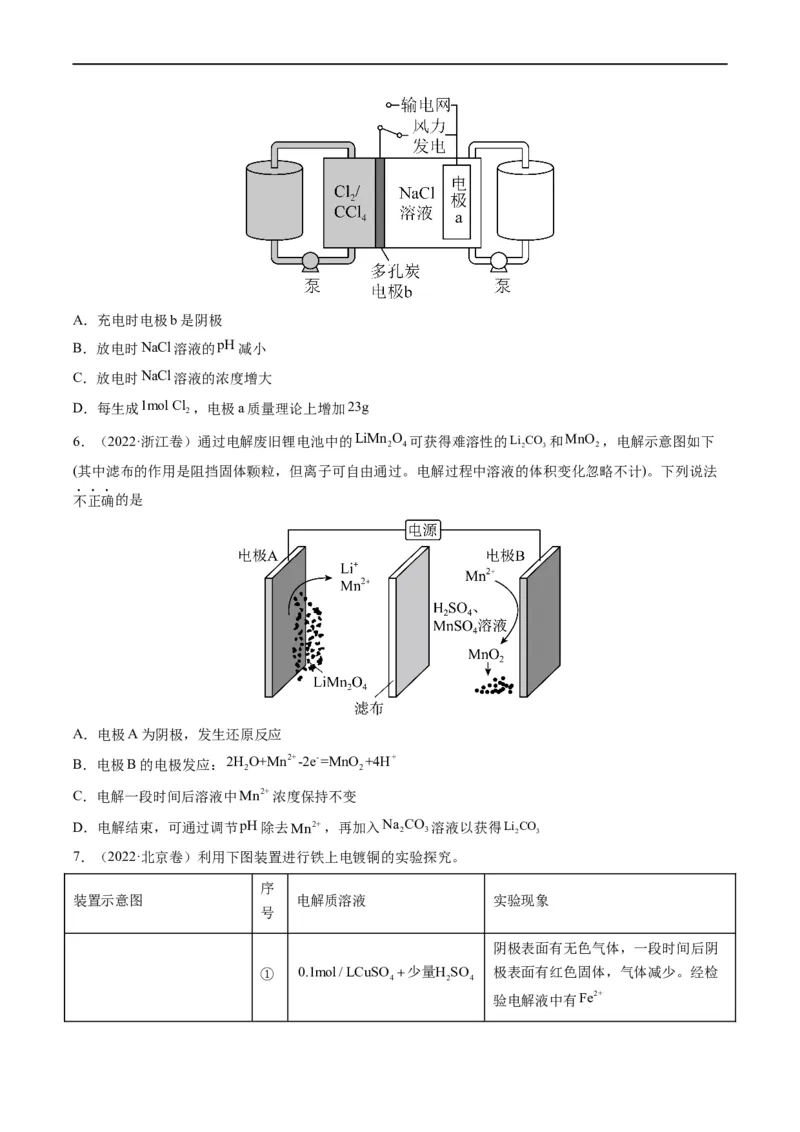
3.(2022·海南卷)一种采用H O(g)和N (g)为原料制备NH (g)的装置示意图如下。
2 2 3下列有关说法正确的是
A.在b电极上,N 被还原
2
B.金属Ag可作为a电极的材料
C.改变工作电源电压,反应速率不变
D.电解过程中,固体氧化物电解质中O2-不断减少
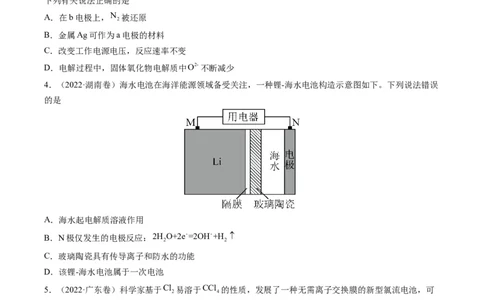
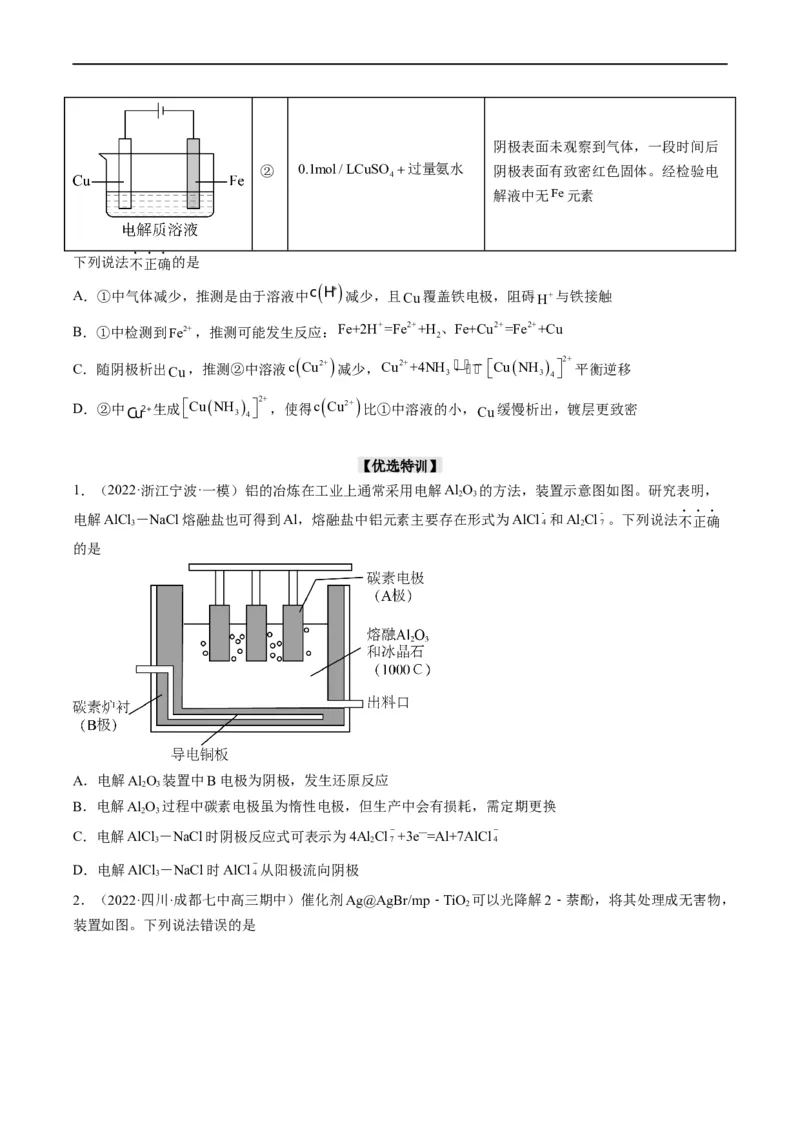
4.(2022·湖南卷)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错误
的是
A.海水起电解质溶液作用
B.N极仅发生的电极反应:2H O+2e-=2OH-+H
2 2
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池
5.(2022·广东卷)科学家基于Cl 易溶于CCl 的性质,发展了一种无需离子交换膜的新型氯流电池,可
2 4
作储能设备(如图)。充电时电极a的反应为: NaTi PO 2Na2e Na Ti PO 。下列说法正确的
2 4 3 3 2 4 3
是A.充电时电极b是阴极
B.放电时NaCl溶液的pH减小
C.放电时NaCl溶液的浓度增大
D.每生成1mol Cl ,电极a质量理论上增加23g
2
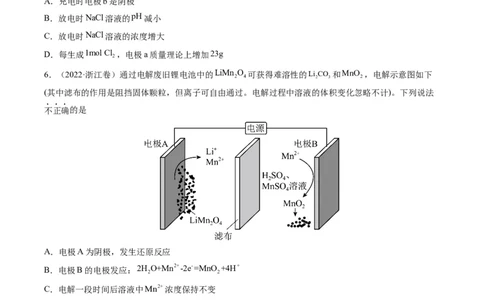
6.(2022·浙江卷)通过电解废旧锂电池中的LiMn O 可获得难溶性的Li CO 和MnO ,电解示意图如下
2 4 2 3 2
(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。下列说法
不正确的是
A.电极A为阴极,发生还原反应
B.电极B的电极发应:2H O+Mn2+-2e-=MnO +4H+
2 2
C.电解一段时间后溶液中Mn2+浓度保持不变
D.电解结束,可通过调节pH除去Mn2+,再加入Na
2
CO
3
溶液以获得Li
2
CO
3
7.(2022·北京卷)利用下图装置进行铁上电镀铜的实验探究。
序
装置示意图 电解质溶液 实验现象
号
阴极表面有无色气体,一段时间后阴
① 0.1mol/LCuSO 少量H SO 极表面有红色固体,气体减少。经检
4 2 4
验电解液中有Fe2+阴极表面未观察到气体,一段时间后
② 0.1mol/LCuSO 过量氨水 阴极表面有致密红色固体。经检验电
4
解液中无Fe元素
下列说法不正确的是
A.①中气体减少,推测是由于溶液中c
H+
减少,且Cu覆盖铁电极,阻碍H+与铁接触
B.①中检测到Fe2+,推测可能发生反应:Fe+2H+=Fe2++H 、Fe+Cu2+=Fe2++Cu
2
C.随阴极析出Cu,推测②中溶液c Cu2+ 减少,Cu2++4NH 3 CuNH 3 4 2+ 平衡逆移
D.②中 Cu2+生成 CuNH 3 4 2+ ,使得c Cu2+ 比①中溶液的小,Cu缓慢析出,镀层更致密
【优选特训】
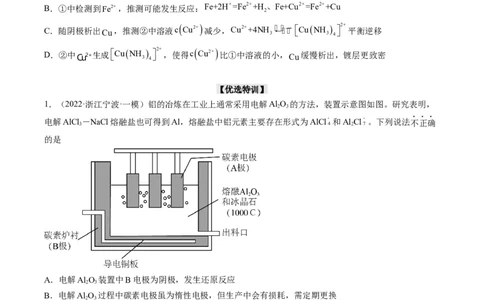
1.(2022·浙江宁波·一模)铝的冶炼在工业上通常采用电解Al O 的方法,装置示意图如图。研究表明,
2 3
电解AlCl
3
-NaCl熔融盐也可得到Al,熔融盐中铝元素主要存在形式为AlCl-
4
和Al
2
Cl-
7
。下列说法不正确
的是
A.电解Al O 装置中B电极为阴极,发生还原反应
2 3
B.电解Al O 过程中碳素电极虽为惰性电极,但生产中会有损耗,需定期更换
2 3
C.电解AlCl -NaCl时阴极反应式可表示为4Al Cl+3e—=Al+7AlCl
3 2 7 4
D.电解AlCl -NaCl时AlCl从阳极流向阴极
3 4
2.(2022·四川·成都七中高三期中)催化剂Ag@AgBr/mp﹣TiO 可以光降解2﹣萘酚,将其处理成无害物,
2
装置如图。下列说法错误的是A.该装置将光能和化学能转化为电能
B.工作时的负极发生反应: ﹣46e﹣+23O2﹣=10CO ↑+4H O
2 2
C.工作时,O2﹣从正极迁移到负极
D.b极电势高于a极
3.(2022·浙江温州·模拟预测)一种新型的高性能、低成本的钠型双离子可充电电池,其结构如图所示。
采用锡箔(不参与电极反应)作为电池电极及集流体,石墨(C )为另一极,电解液为NaPF 作为电解质的溶
n 6
液。下列有关说法不正确的是中
A.放电时,锡箔与钠的合金为负极
B.充电时,图中所示的正八面体形离子嵌入石墨电极
C.电池总反应:xNaC PF xNaPF C
n 6 x 6 n
D.当外电路通过nmol电子时,锡钠极板质量应减少23ng
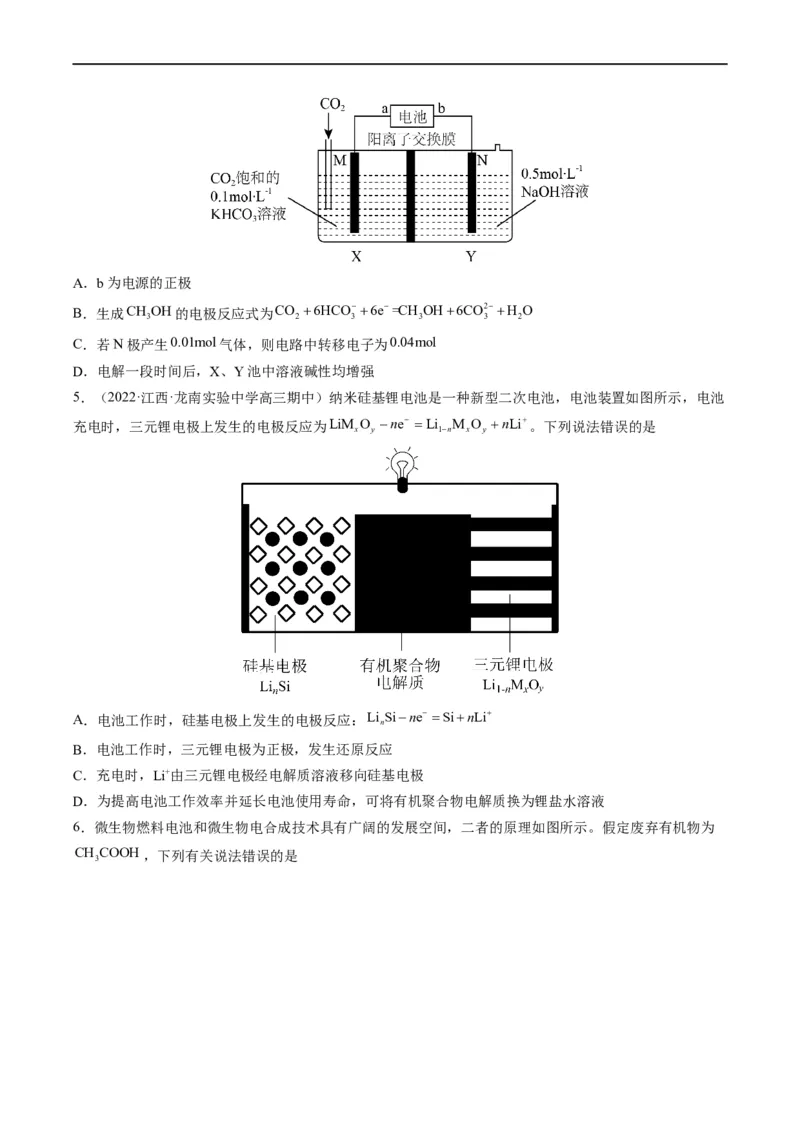
4.电解CO 饱和的0.1molL1的KHCO 溶液,含碳产物主要为CH OH,还有少量CO、HCOOH和
2 3 3
HCHO,实验装置如图,其中M、N均为TiO 纳米电极。下列说法错误的是
2A.b为电源的正极
B.生成CH OH的电极反应式为CO 6HCO6e=CH OH6CO2H O
3 2 3 3 3 2
C.若N极产生0.01mol气体,则电路中转移电子为0.04mol
D.电解一段时间后,X、Y池中溶液碱性均增强
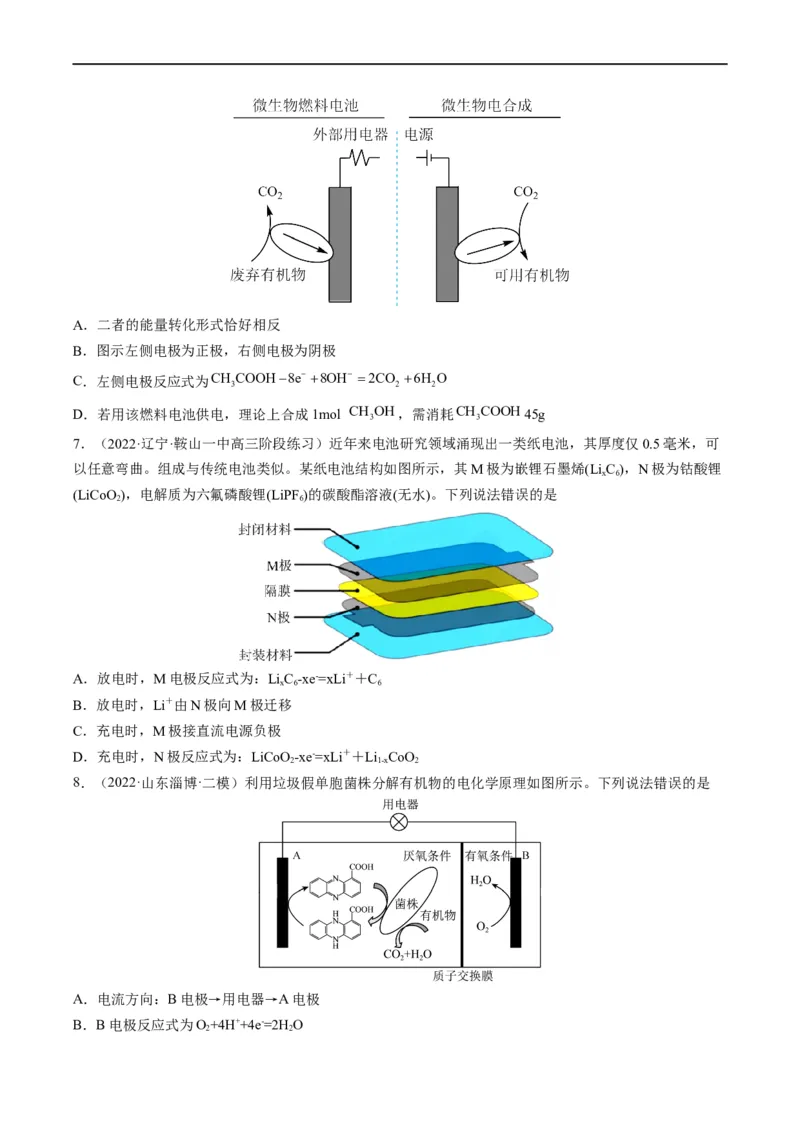
5.(2022·江西·龙南实验中学高三期中)纳米硅基锂电池是一种新型二次电池,电池装置如图所示,电池
充电时,三元锂电极上发生的电极反应为LiM O ne Li M O nLi 。下列说法错误的是
x y 1n x y
A.电池工作时,硅基电极上发生的电极反应:Li Sine SinLi
n
B.电池工作时,三元锂电极为正极,发生还原反应
C.充电时,Li+由三元锂电极经电解质溶液移向硅基电极
D.为提高电池工作效率并延长电池使用寿命,可将有机聚合物电解质换为锂盐水溶液
6.微生物燃料电池和微生物电合成技术具有广阔的发展空间,二者的原理如图所示。假定废弃有机物为
CH COOH,下列有关说法错误的是
3A.二者的能量转化形式恰好相反
B.图示左侧电极为正极,右侧电极为阴极
C.左侧电极反应式为CH COOH8e8OH 2CO 6H O
3 2 2
D.若用该燃料电池供电,理论上合成1mol CH OH,需消耗CH COOH45g
3 3
7.(2022·辽宁·鞍山一中高三阶段练习)近年来电池研究领域涌现出一类纸电池,其厚度仅0.5毫米,可
以任意弯曲。组成与传统电池类似。某纸电池结构如图所示,其M极为嵌锂石墨烯(Li C ),N极为钴酸锂
x 6
(LiCoO ),电解质为六氟磷酸锂(LiPF )的碳酸酯溶液(无水)。下列说法错误的是
2 6
A.放电时,M电极反应式为:LiC -xe-=xLi++C
x 6 6
B.放电时,Li+由N极向M极迁移
C.充电时,M极接直流电源负极
D.充电时,N极反应式为:LiCoO -xe-=xLi++Li CoO
2 1-x 2
8.(2022·山东淄博·二模)利用垃圾假单胞菌株分解有机物的电化学原理如图所示。下列说法错误的是
A.电流方向:B电极→用电器→A电极
B.B电极反应式为O+4H++4e-=2H O
2 2C.A电极反应式为: -4e-→ +4H+
D.若有机物为葡萄糖C H O,处理0.25mol时,会有6molH+透过质子交换膜迁移
6 12 6
9.(2022·广东韶关·二模)我国科学家设计了一种表面锂掺杂的锡纳米粒子催化剂s-SnLi实现安培级CO
2
电合成甲酸盐,同时释放电能,实验原理如图所示。下列说法不正确的是
A.放电时,正极电极周围pH升高
B.充电时,阴极反应式为ZnOH2-+2e=Zn+4OH-
4
C.使用催化剂Sn或者s-SnLi均能有效减少副产物CO的生成
D.使用Sn催化剂,中间产物更不稳定
10.(2022·广西南宁·二模)KIO 广泛用于化工、医学和生活中,工业上制备KIO 的工作原理如图所示,
3 3
下列说法正确的是
A.a为正极,B极上发生氧化反应
B.电子流向:A→a→b→B
C.X气体是H,每转移2mole-,可产生22.4LX气体
2
D.A极的电极反应式为:I-+6OH--6e-=IO+3H O
3 2
11.(2022·福建·模拟预测)微生物电解池(MEC)产甲烷技术是一种有望成为缓解能源危机与温室效应的
重要新型途径。它以外界输入的较小电能为能量来源,以微生物为催化剂,MEC耦合厌氧消化系统产甲烷
的工作原理如图。下列有关说法错误的是A.a为电源的正极,b为电源的负极
B.电子的移动方向:从b→导线→Y电极,再经X→导线→a
C.Y电极发生的反应:CO+8H++8e-=CH +2H O、8H++8e-=4H 、CO+4H =CH +2H O
2 4 2 2 2 2 4 2
D.若用铅酸电池为电源,理论上消耗98gHSO 时,此装置中有2molH+发生迁移
2 4