文档内容
高考解密 03 离子反应
A 组 基础练
1.(2022·河南·焦作市第一中学模拟预测)现有一包粉末样品,可能由 中
的两种或三种组成。现进行如下实验:
ⅰ.取适量固体样品于试管中,加足量蒸馏水充分振荡,溶液变浑浊;ⅱ.将ⅰ中的混合物过滤、洗涤;ⅲ.
向滤渣中加入足量稀盐酸,滤渣部分溶解并产生刺激性气味的气体。
则该样品中一定存在的物质是
A. B.
C. D.
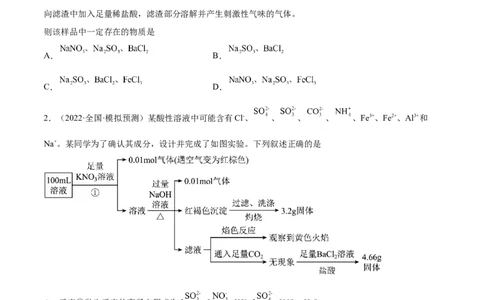
2.(2022·全国·模拟预测)某酸性溶液中可能含有Cl-、 、 、 、 、Fe3+、Fe2+、Al3+和
Na+。某同学为了确认其成分,设计并完成了如图实验。下列叙述正确的是
A.反应①发生反应的离子方程式为3 +2 +2H+=3 +2NO↑+HO
2
B. 、 、Na+一定存在, 、Al3+一定不存在
C.溶液中可能含有Fe3+,一定含有Fe2+,可取少量原溶液加入KSCN溶液检验
D.溶液中至少有6种离子大量存在,其中Cl-一定存在,且c(Cl-)>0.6mol•L-1
3.(2022·天津·耀华中学模拟预测)25℃时,下列各组离子在指定溶液中能大量共存的是
A.Na+、K+、MnO 、Cl-B.与Al反应能放出H 的溶液中:Fe2+、K+、NO 、SO
2
C.中性溶液:Fe3+、Cl-、Na+、SO
D.弱碱性溶液:Na+、K+、Cl-、HCO
4.(2022·吉林·长春十一高模拟预测)将已污染的空气通入某溶液,测其导电性的变化,能获得某种污染
气体的含量。如果把含Cl 的空气通入NaOH溶液,导电性稍有变化,但溶液吸收Cl 的容量大;若用蒸馏
2 2
水则吸收容量不大而导电性变化很大。现要测量空气中的HS含量,能兼顾吸收容量和导电性变化的灵敏
2
度的吸收溶液是
A.CuSO 溶液 B.稀硫酸 C.稀溴水 D.浓氨水
4
5.(2022·吉林·长春十一高模拟预测)某溶液中可能存在Br-、CO 、SO 、Al3+、I-、Mg2+、Na+7种离
子中的某几种。现取该溶液进行实验,得到如下现象:(已知:5Cl+I +6H O=10HCl+2HIO )
2 2 2 3
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;②向所得橙色溶液中加入足量BaCl 溶液,
2
无沉淀生成;③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
根据以上信息,下列对溶液的组成判断正确的是
A.一定不含有Al3+、Mg2+、SO 、I- B.一定含有Na+、CO 、Br-
C.可能含有Na+、SO 、Br-、I- D.可能含有Na+、I-
6.(2022·河北·霸州市第一中学模拟预测)下列各组中的两种物质相互反应时,无论哪种过量,都可用同
一个离子方程式表示的是
①氯化铝溶液与氢氧化钠溶液
②过氧化钠与水
③碘化亚铁溶液与氯水
④碳酸氢钙溶液与澄清石灰水
A.①② B.①③ C.③④ D.②④
7.(2022·浙江·模拟预测)下列物质不属于电解质的是
A.氨基酸 B.锌单质 C.硫酸钡 D.氯化铝
8.(2022·北京市第十中学三模)下列解释事实的方程式不正确的是
A.小苏打在水溶液中发生水解:B.84消毒液与洁厕灵混用产生有毒气体:
C.用食醋清洗水垢:
D.用硫化钠除去废水中的汞离子:
9.(2022·重庆·一模)按要求书写方程式:
(1)已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。在一氧化还原反应的体系
中,共有KCl、 、浓 、 、 、 、 七种物质。
①写出一个包含上述七种物质的氧化还原反应方程式,并配平:___________。
②在反应后的溶液中加入 (不溶于冷水),溶液又变为紫红色, 反应后变为无色的 。写出该
实验中涉及反应的离子方程式:___________。
(2)+6价铬的毒性很强,具有一定的致癌作用,需要转化为低毒的 ,再转化为不溶物除去,废水中含有
的 可以用绿矾( )除去。测得反应后的溶液中含 、 、 、 等阳离子。写出
该反应的离子方程式:___________。
(3)已知:① (绿色)(强碱性条件);② (强酸性条
件)。
将 溶液滴入NaOH溶液中微热,得到透明的绿色溶液,写出反应的离子方程式:___________。
(4)由硫可得多硫化钠 ,x值一般为2~6,已知 与NaClO反应的化学方程式:
,试配平上述方程式,将系数填写
出来。___________
10.(2021·安徽合肥·一模)钒性能优良,用途广泛,有金属“维生素”之称。完成下列填空:
(1)将废钒催化剂(主要成分VO)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的化
2 5
学方程式是____。
(2)向上述所得溶液中加入KClO 溶液,完善并配平反应的离子方程式______。
3ClO + VO2++ = Cl-+ VO +
(3) V O 能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与NaSO 溶液反应被吸收,则 、Cl-、
2 5 2 3
VO2+还原性由大到小的顺序是____。
(4)在20.00 mL 0.1 mol.L-1 溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是 ___。
a.VO2+ b. c. V2+ d.V
B 组 提升练
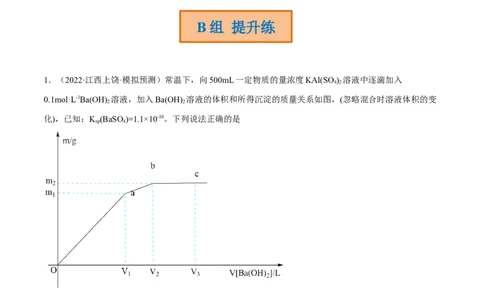
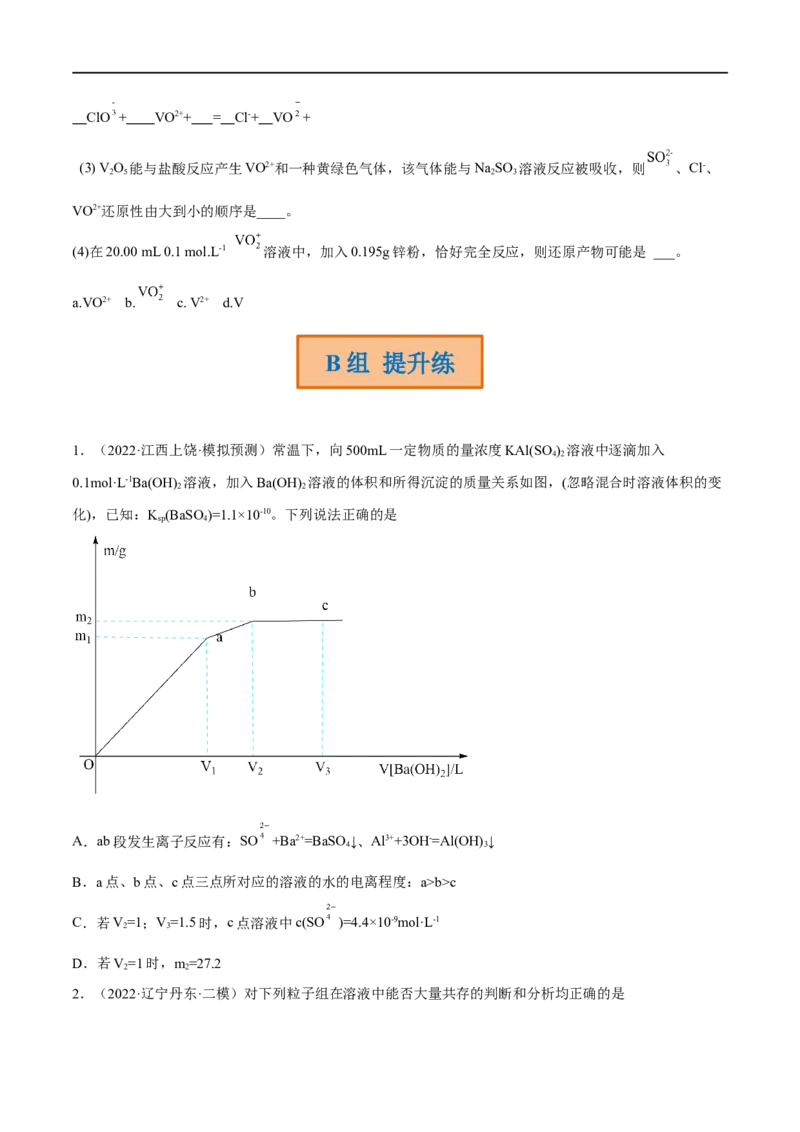
1.(2022·江西上饶·模拟预测)常温下,向500mL一定物质的量浓度KAl(SO ) 溶液中逐滴加入
4 2
0.1mol·L-1Ba(OH) 溶液,加入Ba(OH) 溶液的体积和所得沉淀的质量关系如图,(忽略混合时溶液体积的变
2 2
化),已知:K (BaSO)=1.1×10-10。下列说法正确的是
sp 4
A.ab段发生离子反应有:SO +Ba2+=BaSO ↓、Al3++3OH-=Al(OH) ↓
4 3
B.a点、b点、c点三点所对应的溶液的水的电离程度:a>b>c
C.若V=1;V=1.5时,c点溶液中c(SO )=4.4×10-9mol·L-1
2 3
D.若V=1时,m=27.2
2 2
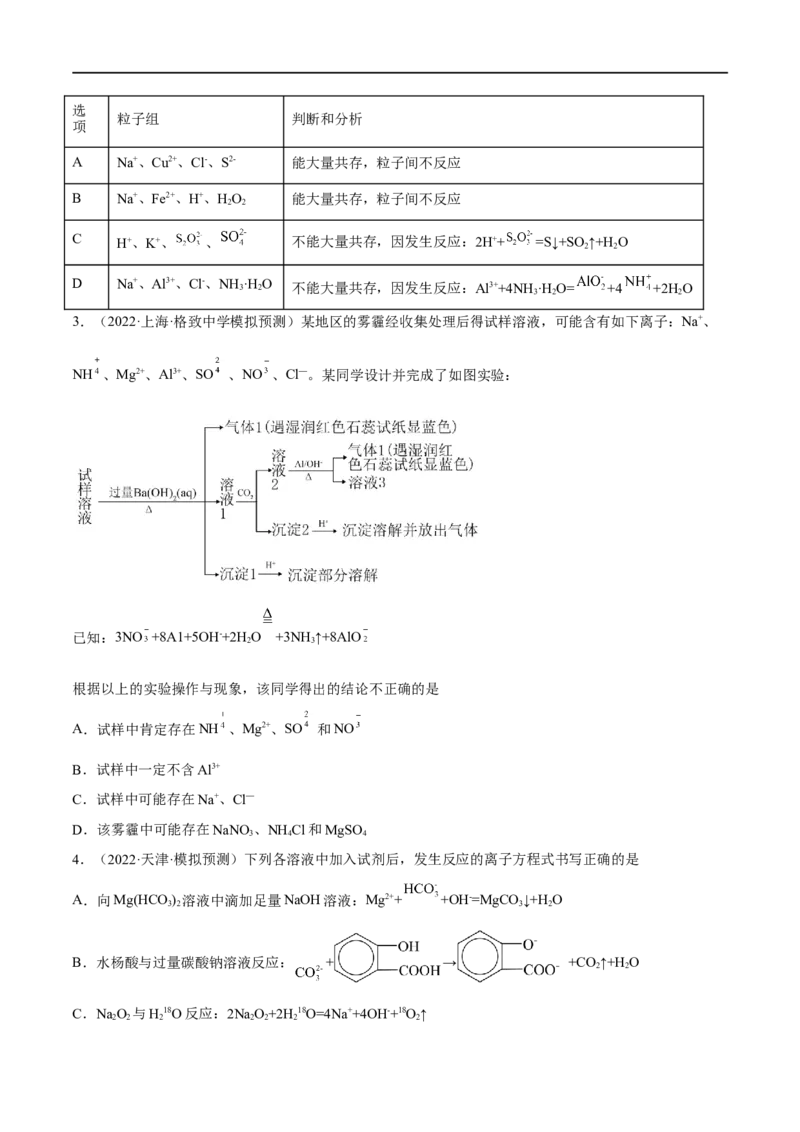
2.(2022·辽宁丹东·二模)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是选
粒子组 判断和分析
项
A Na+、Cu2+、Cl-、S2- 能大量共存,粒子间不反应
B Na+、Fe2+、H+、HO 能大量共存,粒子间不反应
2 2
C H+、K+、 、 不能大量共存,因发生反应:2H++ =S↓+SO ↑+H O
2 2
D Na+、Al3+、Cl-、NH 3 ·H 2 O 不能大量共存,因发生反应:Al3++4NH·H O= +4 +2H O
3 2 2
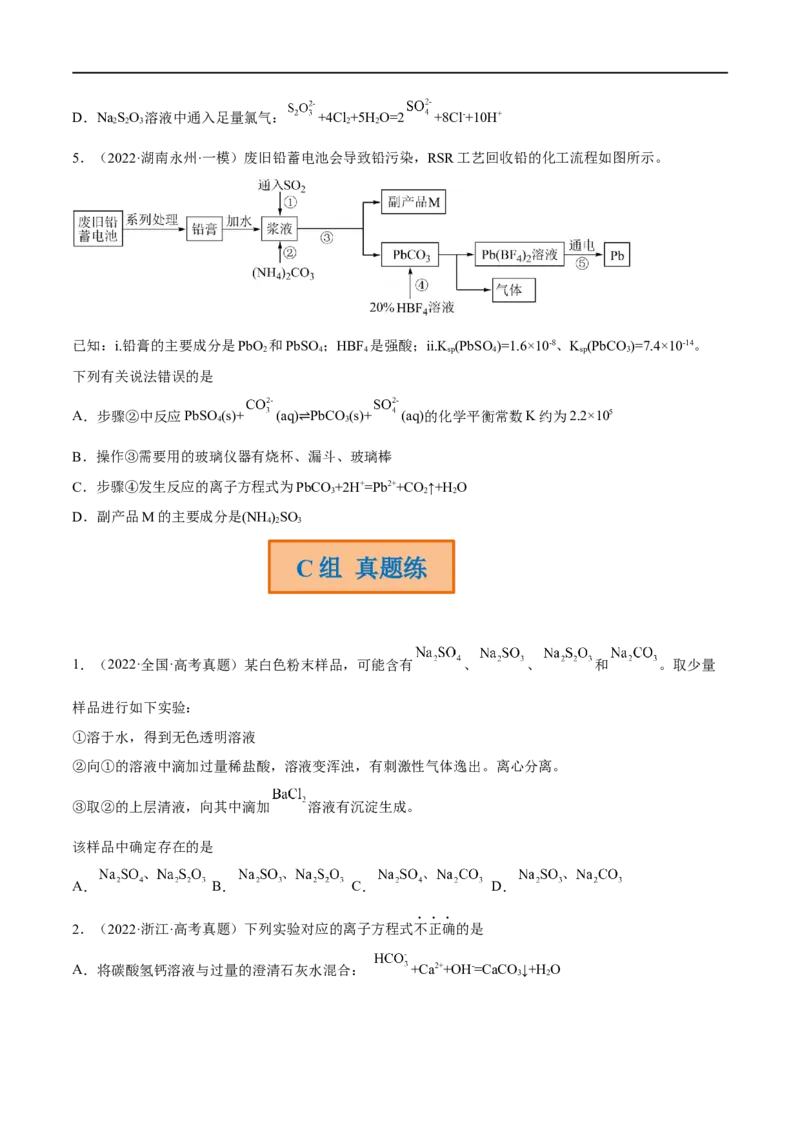
3.(2022·上海·格致中学模拟预测)某地区的雾霾经收集处理后得试样溶液,可能含有如下离子:Na+、
NH 、Mg2+、Al3+、SO 、NO 、Cl—。某同学设计并完成了如图实验:
已知:3NO +8A1+5OH-+2H O +3NH↑+8AlO
2 3
根据以上的实验操作与现象,该同学得出的结论不正确的是
A.试样中肯定存在NH 、Mg2+、SO 和NO
B.试样中一定不含Al3+
C.试样中可能存在Na+、Cl—
D.该雾霾中可能存在NaNO 、NH Cl和MgSO
3 4 4
4.(2022·天津·模拟预测)下列各溶液中加入试剂后,发生反应的离子方程式书写正确的是
A.向Mg(HCO ) 溶液中滴加足量NaOH溶液:Mg2++ +OH-=MgCO↓+H O
3 2 3 2
B.水杨酸与过量碳酸钠溶液反应: + → +CO ↑+H O
2 2
C.NaO 与H18O反应:2NaO+2H 18O=4Na++4OH-+18O↑
2 2 2 2 2 2 2D.NaSO 溶液中通入足量氯气: +4Cl+5H O=2 +8Cl-+10H+
2 2 3 2 2
5.(2022·湖南永州·一模)废旧铅蓄电池会导致铅污染,RSR工艺回收铅的化工流程如图所示。
已知:i.铅膏的主要成分是PbO 和PbSO ;HBF 是强酸;ii.K (PbSO )=1.6×10-8、K (PbCO )=7.4×10-14。
2 4 4 sp 4 sp 3
下列有关说法错误的是
A.步骤②中反应PbSO (s)+ (aq) PbCO (s)+ (aq)的化学平衡常数K约为2.2×105
4 3
⇌
B.操作③需要用的玻璃仪器有烧杯、漏斗、玻璃棒
C.步骤④发生反应的离子方程式为PbCO +2H+=Pb2++CO ↑+H O
3 2 2
D.副产品M的主要成分是(NH )SO
4 2 3
C 组 真题练
1.(2022·全国·高考真题)某白色粉末样品,可能含有 、 、 和 。取少量
样品进行如下实验:
①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加 溶液有沉淀生成。
该样品中确定存在的是
A. B. C. D.
2.(2022·浙江·高考真题)下列实验对应的离子方程式不正确的是
A.将碳酸氢钙溶液与过量的澄清石灰水混合: +Ca2++OH-=CaCO ↓+H O
3 2B.将少量NO 通入NaOH溶液:2NO +2OH-= + +H O
2 2 2
C.将少量SO 通入NaClO溶液:SO +H O+2ClO-= +2HClO
2 2 2
D.向氨水中滴入少量硝酸银溶液:Ag++2NH·H O= +2H O
3 2 2
3.(2021·重庆·高考真题)25°时, 下列各组离子在指定溶液中一定能大量共存的是
A.1.0 mol·L-1氯化钡溶液中: Mg2+、K+、Br-、
B.1.0 mol·L-1硫酸中: A13+、 Na+、Cl-、
C.pH=1l 的氨水中: Fe2+、 Na+、 、ClO-
D.pH=1的硝酸中: Fe3+、K+、I-、
4.(2022·江苏·高考真题)周期表中ⅣA族元素及其化合物应用广泛,甲烷具有较大的燃烧热
,是常见燃料;Si、Ge是重要的半导体材料,硅晶体表面 能与氢氟酸(HF,弱酸)反应
生成 ( 在水中完全电离为 和 );1885年德国化学家将硫化锗 与 共热制得了门
捷列夫预言的类硅—锗;下列化学反应表示正确的是
A. 与HF溶液反应:
B.高温下 还原 :
C.铅蓄电池放电时的正极反应:
D.甲烷的燃烧:
5.(2012·上海·高考真题)碳酸氢铵是一种重要的铵盐。实验室中,将二氧化碳通入氨水可制得碳酸氢铵,
用碳酸氢铵和氯化钠可制得纯碱。完成下列填空:
(1)二氧化碳通入氨水的过程中,先有__晶体(填写化学式)析出,然后晶体溶解,最后析出NH HCO 晶体。
4 3
(2)含0.800 mol NH 的水溶液质量为54.0 g,向该溶液通入二氧化碳至反应完全,过滤,得到滤液31.2g,
3
则NH HCO 的产率为____%。
4 3(3)粗盐(含Ca2+、Mg2+)经提纯后,加入碳酸氢铵可制得碳酸钠。实验步骤依次为:①粗盐溶解;②加入试
剂至沉淀完全,煮沸;③__;④加入盐酸调pH;⑤加入__;⑥过滤;⑦灼烧,冷却,称重。
(4)上述步骤②中所加入的试剂为__、__。
(5)上述步骤④中加盐酸调pH的目的是__。
(6)为探究NH HCO 和NaOH的反应,设计实验方案如下:含0.1 mol NH HCO 的溶液中加入0.1 mol
4 3 4 3
NaOH,反应完全后,滴加氯化钙稀溶液。若有沉淀,则NH HCO 与NaOH的反应可能为_____(写离子方
4 3
程式);若无沉淀,则NH HCO 与NaOH的反应可能为______(写离子方程式)。该实验方案有无不妥之处?
4 3
若有,提出修正意见_____。