文档内容
高考解密04 氧化还原反应
考点热度 ★★★★☆
考点1、氧化还原反应的概念辨析
1.(2022·浙江·高考真题)关于反应 ,下列说法正确的是
A. 发生还原反应
B. 既是氧化剂又是还原剂
C.氧化产物与还原产物的物质的量之比为2∶1
D. 发生反应,转移 电子
考点2、氧化还原反应的规律及其应用
(2022·全国·高考真题)由实验操作和现象,可得出相应正确结论的是
实验操作 现象 结论
氧化性:
A 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液 先变橙色,后变蓝色
向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的
B 无砖红色沉淀 蔗糖未发生水解
悬浊液
气体中含有不饱和
C 石蜡油加强热,将产生的气体通入 的 溶液 溶液红棕色变无色
烃
试管口润湿的蓝色石蕊 氯乙烯加聚是可逆
D 加热试管中的聚氯乙烯薄膜碎片
试纸变红 反应
A.A B.B C.C D.D
考点3、氧化还原反应的书写及简单计算
(2020·江苏·高考真题)次氯酸钠溶液和二氯异氰尿酸钠(C NOClNa)都是常用的杀菌消毒剂。 NaClO可
3 3 3 2
用于制备二氯异氰尿酸钠.
(1)NaClO溶液可由低温下将Cl 缓慢通入NaOH溶液中而制得。制备 NaClO的离子方程式为__________;
2用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,将会导致消毒作用
减弱,其原因是__________________。
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标
准。实验检测原理为
准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸
和过量KI溶液,密封在暗处静置5min;用 NaSO 标准溶液滴定至溶液呈微黄色,加入淀粉
2 2 3
指示剂继续滴定至终点,消耗NaSO 溶液20.00mL。
2 2 3
①通过计算判断该样品是否为优质品_______。(写出计算过程,
)
②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值____________(填“偏高”或“偏低”)。
1、对点核心素养
(1)宏观辨识与微观探析:能从元素和原子、分子、电子转移的角度认识物质的性质和变化。
(2)变化观念与平衡思想:知道化学变化需要一定的条件,并遵循质量、元素、电子守恒,能多角度、动态分析
氧化还原反应,运用其原理解决实际问题。
(3)证据推理与模型认知:通过分析、推理等方法认识氧化还原反应的本质特征,能运用反应原理解释化学现
象,揭示现象的本质和规律。
(4)科学探究与创新意识:利用氧化还原反应对物质进行定性研究或判断,能发现和提出有探究价值的问题。
2、对点命题分析
氧化还原反应是高中化学的核心理论,贯穿整个高中化学的始终,它是历年高考的必考的热点和重点
内容,选择题、主观填空题均有可能出现,近三年的高考中,选择题主要考查氧化还原反应的概念与本质;
判断氧化剂与还原剂、氧化产物与还原产物,被氧化元素与被还原元素;比较氧化剂(还原剂)的氧化性(还
原性)的强弱;主观填空题主要考查氧化还原反应方程式的书写及简单计算。预计氧化还原反应在 2023年
高考中考查形式有:(1)出现在阿伏伽德罗常数的正误判断的选择题中。在阿伏伽德罗常数的正误判断中,
计算得失电子数目是常考查的一种角度,在这儿需要掌握高中一些重要物质的性质,如氯气是强氧化剂,
但1molCl 在化学反应中,不一定得2mole—,如它与NaOH溶液的反应,转移电子的物质的量为1mol,还
2
有NaO,它与水的反应中,也是既作氧化剂又作还原剂,有 2mol的NaO 参加反应,电子转移数为2NA。
2 2 2 2
(2)出现在离子共存问题的选择题中。具有氧化性的微粒有Cl 、NaO 和H+、NO —(相当于HNO)、Fe3+、
2 2 2 3 3
MnO —,具有还原性的离子还有SO 2—、S2—、Fe2+。(3)出现在离子方程式的正误判断的选择题中。(4)出现
4 3
在主观填空题中的陌生的氧化还原反应方程式的书写成为近年来考查的亮点,需要重点关注。能力要求高,
难度较大。核心考点一 氧化还原反应的基本概念
1.依据框图理清4对概念之间的关系
2.正确理解氧化还原反应的实质
概念理解抓实质,解题应用靠特征,即从氧化还原反应的实质——电子转移去分析理解有关概念,而
在实际解题过程中,应从分析元素化合价有无变化这一氧化还原反应的特征入手。具体方法是找变价、判
类型、分升降、定其他。其中“找变价”是非常关键的一步,特别是不同反应物中含有同种元素的氧化还
原反应,必须弄清元素化合价的变化情况。
3.氧化还原反应电子转移的表示方法
(1)双线桥法:①标变价,②画箭头,③算数目,④说变化。
(2)单线桥法:箭头由失电子原子指向得电子原子,线桥上只标电子转移的数目,不标“得”“失”字样。
4.氧化性及还原性的强弱比较
物质的氧化性或还原性的强弱只取决于得到或失去电子的难易程度,与得失电子的数目无关。如:Na、
Mg、Al的还原性强弱依次为Na>Mg>Al;浓HNO、稀HNO 的氧化性强弱为浓HNO>稀HNO。
3 3 3 3
(1)根据氧化还原反应原理:氧化剂氧化性强于氧化产物,还原剂还原性强于还原产物。
(2)根据元素的化合价:如果物质中某元素具有最高价,该元素只有氧化性;物质中某元素具有最低价,该
元素只有还原性;物质中某元素具有中间价态,该元素既有氧化性又有还原性。元素化合价升高被氧化,
发生氧化反应,元素化合价降低被还原,发生还原反应。
(3)根据活动性顺序:在金属活动性顺序表中,位置越靠前,其还原性就越强,其阳离子的氧化性就越弱。
一般来说,越活泼的非金属,得到电子还原成非金属阴离子越容易,其阴离子失电子氧化成单质越难,还
原性越弱。
(4)根据元素周期表:同周期元素,随着核电荷数的递增,氧化性逐渐增强,还原性逐渐减弱;同主族元素,
随着核电荷数的递增,氧化性逐渐减弱,还原性逐渐增强。
(5)根据反应的难易程度:氧化还原反应越容易进行(表现为反应所需条件越低),则氧化剂的氧化性和还原剂的还原性就越强。不同的还原剂(或氧化剂)与同一氧化剂(或还原剂)反应时,条件越易或者氧化剂(或还
原剂)被还原(或被氧化)的程度越大,则还原剂(或氧化剂)的还原性(或氧化性)就越强。
(6)根据电化学原理判断:两种不同的金属构成原电池的两极,负极金属是电子流出的极,正极金属是电子
流入的极,负极还原性强于正极。用惰性电极电解混合液时,若混合液中存在多种金属阳离子时,在阴极
先放电的阳离子的氧化性较强(相应的金属单质的还原性较弱),若混合液中存在多种阴离子,在阳极先放
电的阴离子的还原性较强(相应的非金属单质的氧化性较弱)。
(7)根据影响因素判断氧化性、还原性强弱的方法
①浓度:同一种物质浓度越大,氧化性(或还原性)越强。如氧化性:浓 HSO >稀HSO ,浓HNO>稀
2 4 2 4 3
HNO,还原性:浓HCl>稀HCl。
3
②温度:同一种物质,温度越高其氧化性越强。如热的浓硫酸的氧化性比冷的浓硫酸的氧化性强。
③酸碱性:同一种物质,所处环境酸(碱)性越强其氧化性(还原性)越强。
如酸性条件:2MnO+6H++5SO===2Mn2++5SO+3HO
2
中性条件:2MnO+HO+3SO===2MnO+3SO+2OH-
2 2
碱性条件:2MnO+2OH-+SO===2MnO+SO+HO
2
其氧化性为KMnO (酸性)>KMnO (中性)>KMnO (碱性)。
4 4 4
5.辨析氧化还原反应基本概念常出现的“6个误区”
(1)误认为有单质参与或生成的反应一定是氧化还原反应。如O 与O 的转化为非氧化还原反应。
2 3
(2)误认为元素由化合态变为游离态一定被还原,其实不一定。如 HCl→Cl ,氯元素被氧化;CuO→Cu,铜
2
元素被还原。
(3)误认为氧化还原反应中有一种元素被氧化,则一定有另一种元素被还原,其实不一定。如 Cl +
2
HOHCl+ HClO中,被氧化和被还原的都是氯元素。
2
(4)误认为具有氧化性的物质和具有还原性的物质一定都能发生化学反应,其实不一定。如 SO 具有还原性,
2
浓HSO 具有氧化性,但二者不发生氧化还原反应。
2 4
(5)误认为同种元素的高价态的物质一定比低价态物质的氧化性强,其实不一定。如 HClO的氧化性高于
HClO。
4
(6)误认为得电子难的物质一定易失电子,如第ⅣA族和稀有气体既不容易得到电子也不容易失去电子。
核心考点二 氧化还原反应的基本规律
1.氧化还原反应的四大规律及其应用
1)守恒规律:
(1)内容:化合价有升必有降,电子有得必有失。对于一个完整氧化还原反应,化合价升高的总数与降
低的总数相等;氧化剂得到的电子数一定等于还原剂失去的电子数
(2)应用:①用于氧化还原反应的某些量的计算;②用于氧化还原反应方程式的配平;③判断反应是否
属于氧化还原反应。
2)表现性质规律:
(1)内容:元素处于最高价,只有氧化性;元素处于最低价,只有还原性;元素处于中间价态,既有氧
化性又有还原性,但主要呈现一种性质。物质若含有多种元素,其性质是这些元素的综合体现。
(2)应用:判断元素或物质氧化性或还原性的有无。3)由强到弱规律:
(1)内容:氧化还原反应中,较强氧化性的氧化剂跟较强还原性的还原剂反应,生成弱还原性的还原产
物和弱氧化性的氧化产物,即同一反应中,氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物.
(2)应用:①在适宜条件下,用氧化性较强的物质制备氧化性较弱的物质,或用还原性较强的物质制备
还原性较弱的物质;
②判断氧化还原反应能否进行;
③比较微粒氧化性或还原性强弱应用:A.比较物质间氧化性或还原性的强弱;B.在适宜条件下,用氧化性
强的物质制备氧化性弱的物质或用还原性强的物质制备还原性弱的物质。
4)转化律
(1)内容:在一般情况下,①氧化还原反应中,以元素相邻价态间的转化最容易;②同种元素不同价态之间
的氧化还原反应,化合价的变化遵循:高价+低价 ──→ 中间价(归中反应);中间价──→高价+低
价(歧化反应)③同种元素,相邻价态间不发生氧化还原反应。
(2)应用:①分析判断氧化还原反应能否发生。②判断氧化还原反应的氧化产物和还原产物。
5)难易律
(1)内容:越易失电子的物质,失去电子后就越难得电子,越易得电子的物质,得到后就越难失电子,一种
氧化剂同时和几种还原剂相遇时,还原性最强的优先发生反应;同理,一种还原剂同时和几种氧化剂相遇
时,氧化性最强的优先发生反应。
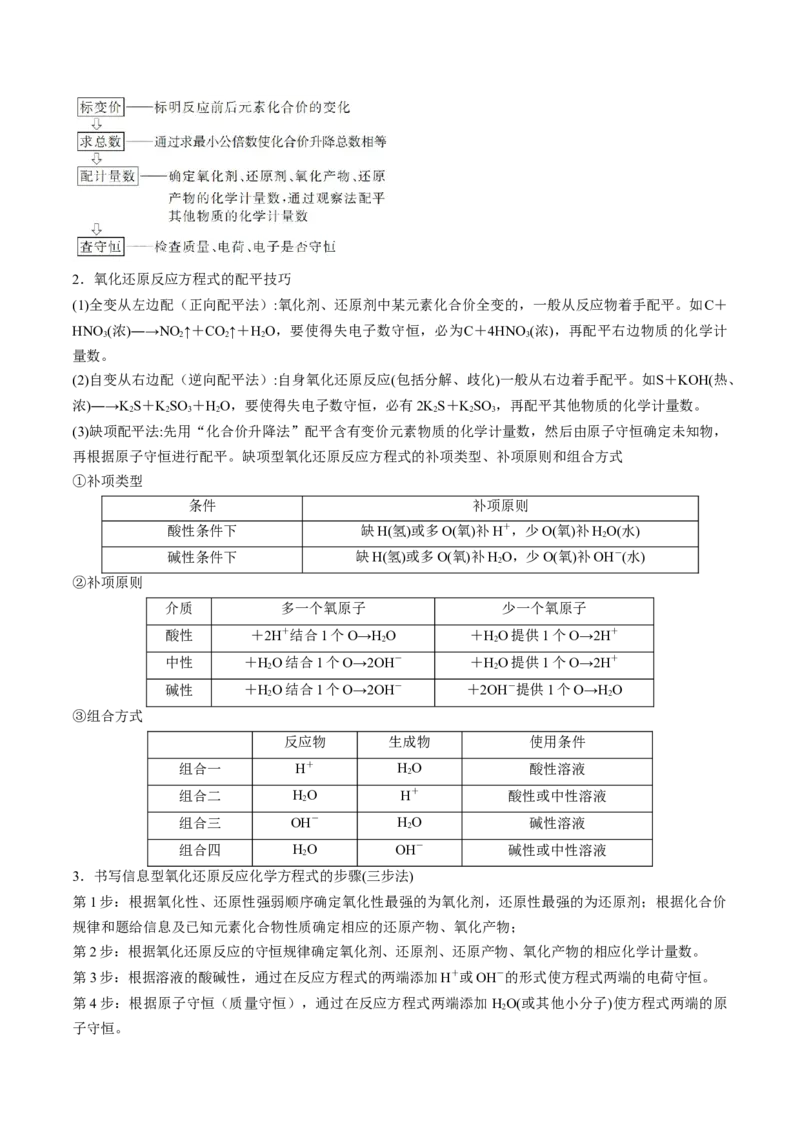
可把常见微粒的氧化性、还原性按强弱以位置前后的形式排列:
(2)应用:①判断物质的稳定性;②判断物质反应的先后顺序,即左上方的一种氧化剂可氧化它右下方的还
原性微粒.若有多种,则优先氧化较右下方的微粒;③选择合适的氧化剂或还原剂,如要氧化Fe2+而Br-
不被氧化,则可选择Br ;④判断氧化性微粒、还原性微粒能否共成。虚线所指两种微粒一定能发生反应,
2
故不共存;实线所指微粒能共存.
2.熟记两串微粒的反应先后顺序
(1)同一还原剂与多种氧化剂发生氧化还原反应的先后顺序:KMnO (H+)>Cl>Br >Fe3+>Cu2+>H+。
4 2 2
(2)同一氧化剂与多种还原剂发生氧化还原反应的先后顺序:S2->SO(或HSO)>I->Fe2+>Br->Cl-。
3.利用相关规律解答氧化还原反应问题的三步骤
(1)准确判断氧化剂、还原剂、氧化产物、还原产物,并根据方程式确定其强弱。
(2)氧化还原反应按照“先强后弱”的反应顺序进行。
(3)灵活应用“化合价升降总数相等”“电荷守恒”及“得失电子守恒”进行简单计算。
核心考点三 氧化还原反应方程式的书写、配平与计算
1.一般氧化还原反应方程式的配平——化合价升降法步骤:
标变价→列变化→求总数→配系数→细检查2.氧化还原反应方程式的配平技巧
(1)全变从左边配(正向配平法):氧化剂、还原剂中某元素化合价全变的,一般从反应物着手配平。如C+
HNO(浓)―→NO↑+CO↑+HO,要使得失电子数守恒,必为C+4HNO(浓),再配平右边物质的化学计
3 2 2 2 3
量数。
(2)自变从右边配(逆向配平法):自身氧化还原反应(包括分解、歧化)一般从右边着手配平。如S+KOH(热、
浓)―→KS+KSO+HO,要使得失电子数守恒,必有2KS+KSO,再配平其他物质的化学计量数。
2 2 3 2 2 2 3
(3)缺项配平法:先用“化合价升降法”配平含有变价元素物质的化学计量数,然后由原子守恒确定未知物,
再根据原子守恒进行配平。缺项型氧化还原反应方程式的补项类型、补项原则和组合方式
①补项类型
条件 补项原则
酸性条件下 缺H(氢)或多O(氧)补H+,少O(氧)补HO(水)
2
碱性条件下 缺H(氢)或多O(氧)补HO,少O(氧)补OH-(水)
2
②补项原则
介质 多一个氧原子 少一个氧原子
酸性 +2H+结合1个O→H O +HO提供1个O→2H+
2 2
中性 +HO结合1个O→2OH- +HO提供1个O→2H+
2 2
碱性 +HO结合1个O→2OH- +2OH-提供1个O→H O
2 2
③组合方式
反应物 生成物 使用条件
组合一 H+ HO 酸性溶液
2
组合二 HO H+ 酸性或中性溶液
2
组合三 OH- HO 碱性溶液
2
组合四 HO OH- 碱性或中性溶液
2
3.书写信息型氧化还原反应化学方程式的步骤(三步法)
第1步:根据氧化性、还原性强弱顺序确定氧化性最强的为氧化剂,还原性最强的为还原剂;根据化合价
规律和题给信息及已知元素化合物性质确定相应的还原产物、氧化产物;
第2步:根据氧化还原反应的守恒规律确定氧化剂、还原剂、还原产物、氧化产物的相应化学计量数。
第3步:根据溶液的酸碱性,通过在反应方程式的两端添加H+或OH-的形式使方程式两端的电荷守恒。
第4步:根据原子守恒(质量守恒),通过在反应方程式两端添加 HO(或其他小分子)使方程式两端的原
2
子守恒。【特别提醒】①注意特殊物质中元素的化合价:如CuFeS 中铜、铁元素的化合价都为+2,硫元素的化合价为
2
-2;FeS 中硫元素的化合价为-1;KFeO 中铁元素的化合价为+6等。②配平化学方程式时,化学计量数
2 2 4
“1”也必须填写在空格里。③依据电子得失守恒列等式时不要忽略变价原子的个数。
4.氧化还原反应计算中重要的解题方法——电子守恒法
(1)应用电子守恒解题的三步骤。
“一找各物质”:找出氧化剂、还原剂及相应的还原产物和氧化产物。
“二定得失数”:确定一个原子或离子得失电子数(注意化学式中的原子个数)。
“三列关系式”:根据题中物质的物质的量和得失电子守恒列出关系式:
n(氧化剂)×变价原子个数×化合价变化值=n(还原剂)×变价原子个数×化合价变化值
(2)多步反应得失电子守恒问题
有的试题反应过程多,涉及的氧化还原反应也多,数量关系较为复杂,若用常规方法求解比较困难,
若抓住失电子总数等于得电子总数这一关系,则解题就变得很简单。解多步连续进行的氧化还原反应这类
试题时,注意不要遗漏某个氧化还原反应,只要中间各步反应过程中电子没有损耗,可直接找出起始物和最
终产物,略去中间产物,建立起始物和最终产物之间的电子守恒关系,从而快速求解。
考点1、考查氧化还原反应中的基本概念
【高考解密】氧化还原反应中存在许多概念,如氧化剂与还原剂、氧化反应与还原反应(或被氧化与被还
原)、氧化产物与还原产物、氧化性与还原性、转移电子数、得或失电子数等,这也是对氧化还原反应概
念考查的主要内容。主要以选择题或主观题的形式出现。解答的办法就是熟练运用元素的金属性或非金属
性强弱关系判断元素价态的正负及数值,也可直接利用常见元素的价态推知不常见元素的价态,然后抓住
概念内容即可解答此类问题。
例1.(2022·吉林·抚松县第一中学模拟预测)四氧化钌 是金黄色针状晶体,微溶于水,有强氧化性,
能氧化浓盐酸生成 和 。在稀硫酸环境中,可利用 与NaClO反应制备 ,其化学方程
式为 。下列说法正确的是
A.该反应中NaCl是氧化产物, 是还原产物
B.该反应中硫酸既表现酸性又表现氧化性
C.酸性介质中氧化性:
D.该反应中的稀硫酸不能用浓盐酸代替
【变式训练1】(考查氧化还原反应的概念辨析)(2022·浙江温州·模拟预测)关于反应3SiO+6C+2N
2 2
Si N+6CO,下列说法正确的是
3 4
A.C在反应过程中被还原 B.Si N 既是氧化产物又是还原产物
3 4
C.氧化剂和还原剂质量之比为1:3 D.每生成14.0g Si N 共转移1.2mol电子
3 4
【变式训练2】(考查氧化还原反应的判断)(2023·广东·深圳市光明区高级中学模拟预测)古医典中富含化
学知识,下列描述与氧化还原反应无关的是。A.汞的性质:汞得硫则赤如丹
B.强水(硝酸):用水入五金皆成水
C.熬制胆矾:熬胆矾铁釜,久之亦化为铜
D.制取黄铜:红铜(Cu)六斤、倭铅(Zn)四斤,先后入罐熔化,冷定取出,即成黄铜
【变式训练3】(考查氧化还原反应与四种基本反应类型关系)(2022·江苏连云港·模拟预测)NaClO可用于
回收光盘金属层中的少量Ag,反应为4Ag+4NaClO+2HO=4AgCl+4NaOH+O↑。下列说法正确的是
2 2
A.AgCl属于弱电解质 B.反应中NaClO作还原剂
C.该反应属于复分解反应 D.反应中有极性键和非极性键的形成
考点2、考查氧化还原反应的规律及灵活应用
【高考解密】氧化还原反应中存在许多规律,如电子守恒规律、价态规律、强弱规律、先后规律、价态变
化不交叉等规律,其中电子守恒规律是氧化还原反应方程式配平的理论基础,是解答氧化还原反应计算的
主要策略,也是理解或解答电化学反应原理问题的知识基础;价态规律用来判断物质的氧化性或还原性及
理解歧化反应、归中反应发生的原因;强弱规律、先后规律是用来判断反应的先后或电化学中离子放电的
先后等。
例2.(2022·浙江·模拟预测)关于反应 ,下列说法不正确的是
A. , B.该化学反应中HCl仅体现出了酸性
C.通过该反应可知氧化性: D.该反应生成1mol水,转移 个电子
【变式训练1】(考查氧化性、还原性强弱的判断)(2022·甘肃武威·高三阶段练习)在常温下,发生下列几
个反应:
①2KMnO +16HCl=2KCl+2MnCl +5Cl↑+8H O
4 2 2 2
②Cl+2NaBr=2NaCl+Br
2 2
③Br +2FeBr =2FeBr
2 2 3
根据上述反应,下列结论正确的是
A.还原性强弱顺序为:Br->Fe2+>Cl-
B.氧化性强弱顺序为:MnO >Cl>Br >Fe3+
2 2
C.溶液中可发生反应:2Fe3++2Cl-=2Fe2++Cl↑
2
D.反应①中,氧化剂与还原剂的物质的量之比为1:8
【变式训练2】(考查氧化还原反应中反应的先后顺序)[(2022·河北·石家庄二中实验学校高三开学考试)在
离子浓度都为0.1mol•L-1的下列溶液中,加入(或通入)某物质后,发生反应的先后顺序正确的是
A.在含Fe3+、Cu2+、H+的溶液中加入锌粉:Cu2+、Fe3+、H+
B.在含I—、SO 、Br—的溶液中不断通入氯气:I—、Br—、SO
C.在含AlO 、SO 、OH—的溶液中逐滴加入硫酸氢钠溶液:OH—、AlO 、SO
D.在含Fe3+、H+、NH 的溶液中逐渐加入烧碱溶液:Fe3+、NH 、H+
考点3、考查有关氧化还原反应的书写及计算【高考解密】陌生的氧化还原反应方程式的书写成为近年来考查的亮点,需要重点关注。书写提供信息的
陌生的氧化还原反应(或离子)方程式时,应利用所给的信息并按氧化还原反应或离子反应规律预测产物,
再加以配平,即可得氧化还原反应的化学方程式。氧化还原反应是化学计算的主要命题点,常以分析物质
的组成、含量、转化率等问题中出现,有时也渗透在电化学计算、氧化还原反应滴定中。计算时可以先利
用电子守恒配平化学方程式再计算,也可以直接利用电子守恒寻找关系来计算。
例3.(2022·江西·模拟预测)ClO 广泛用于水处理、纸浆漂白等。
2
(1)制备ClO 原料有NaClO 等,产生的ClO (g)用蒸馏水吸收得到吸收液A。
2 2 2
①ClO 中氯元素的化合价为___。
2
②NaClO 与盐酸在微热条件下生成ClO 气体(及少量副产物Cl),写出其反应生成ClO 、NaCl和水的化学
2 2 2 2
方程式:___。
(2)碘量法测定ClO 吸收液A中ClO 和Cl 的浓度的主要实验步骤如下:
2 2 2
步骤1.向锥形瓶中加入50mL蒸馏水、25mL100g·L-1KI溶液(足量),再向其中加入5.00mLClO 吸收液(发生
2
反应:2ClO +2KI=2KClO +I ,Cl+2KI=2KCl+I )。
2 2 2 2 2
步骤2.用0.1000mol·L-1NaSO 标准溶液滴定(2Na SO+I =2NaI+Na SO)至浅黄色,再加入1mL淀粉溶液,
2 2 3 2 2 3 2 2 4 6
继续滴定至蓝色刚好消失,消耗NaSO 溶液6.00mL。
2 2 3
步骤3.向步骤2的溶液中加入5mL2mol·L-1硫酸溶液酸化,发生反应:
KClO+4KI+2H SO =KCl+2K SO +2I +2H O。
2 2 4 2 4 2 2
步骤4.重复步骤2操作,第二次滴定又消耗0.1000mol·L-1NaSO 溶液20.00mL。
2 2 3
根据上述数据,计算ClO 吸收液A中ClO 和Cl 的浓度___(单位g·L-1,写出计算过程)。
2 2 2
【变式训练1】(考查信息陌生氧化还原反应方程式的书写与配平)(2022·河北·霸州市第一中学模拟预测)
(节选)铬及其化合物在工业生产中应用广泛。某铬铁矿的主要成分为 ,另外还含有FeO、 、
MgO等杂质。一种液相氧化法制备 的工艺路线如图:
回答下列问题:
(2)“加压碱浸”中,发生的主要反应为 转化为铬酸钠,其化学方程式为_______。
(5)在“溶解还原”过程中,有 生成,发生反应的离子方程式为_______。
【变式训练2】(考查有关氧化还原反应的计算)(2022·江西·丰城九中高三开学考试)将一定量 通入
质量分数为 的 溶液中,制成含有 和 的混合溶液。用此溶液吸收
标准状况下 ,恰好形成中性溶液(假设气体均完全反应),请计算:
(1) 溶液中 ___________ 。
(2)已知混合溶液中 ,则混合溶液中 ___________。(3)所通 在标准状况下的体积为___________L。