文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(上海
专用)
黄金卷02
(考试时间:60分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Al 27 S 32 Cl 35.5 Fe 56 Cu
64
一、亚硝酸钠的制取(本题共25分)
亚硝酸钠(NaNO)主要用于医药、染料和漂白等行业,也常用于食品保鲜剂。
2
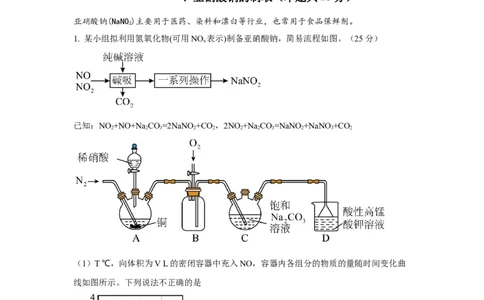
1. 某小组拟利用氮氧化物(可用NO 表示)制备亚硝酸钠,简易流程如图。(25分)
x
已知:NO +NO+Na CO=2NaNO +CO ,2NO +Na CO=NaNO +NaNO +CO
2 2 3 2 2 2 2 3 2 3 2
(1)T ℃,向体积为V L的密闭容器中充入NO,容器内各组分的物质的量随时间变化曲
线如图所示。下列说法不正确的是
A.X是NO
21
B.0~3 min内,v(NO )= mol·(L· min)-1
2
3V
C.T ℃时该反应的平衡常数为1
D.NO 和X的浓度相等不可以作为判断反应到达平衡的标志
2
(2)利用饱和NH Cl溶液和饱和NaNO 溶液在加热条件下反应可制得N,该反应的化学方
4 2 2
程式为 ;实验时装置B中应间断性通入适量
的O,其目的是 。
2
(3)装置C中盛装饱和NaCO 溶液的仪器的名称是
2 3
;NO不能单独被纯碱溶液吸收,为了使NO 完全被纯碱溶液吸收且产品纯度最高,x=
x
。
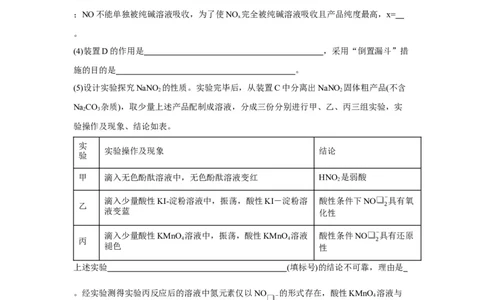
(4)装置D的作用是 ,采用“倒置漏斗”措
施的目的是 。
(5)设计实验探究NaNO 的性质。实验完毕后,从装置C中分离出NaNO 固体粗产品(不含
2 2
NaCO 杂质),取少量上述产品配制成溶液,分成三份分别进行甲、乙、丙三组实验,实
2 3
验操作及现象、结论如表。
实
实验操作及现象 结论
验
甲 滴入无色酚酞溶液中,无色酚酞溶液变红 HNO 是弱酸
2
滴入少量酸性KI-淀粉溶液中,振荡,酸性KI-淀粉溶 酸性条件下NO❑ −具有氧
乙 2
液变蓝 化性
滴入少量酸性KMnO 溶液中,振荡,酸性KMnO 溶液 酸性条件NO❑ −具有还原
丙 4 4 2
褪色 性
上述实验 (填标号)的结论不可靠,理由是
。经实验测得实验丙反应后的溶液中氮元素仅以NO 的形式存在,酸性KMnO 溶液与
❑ − 4
3
NO 反应的离子方程式为 。
−
❑
2
(6)吸光光度法是借助分光光度计测定溶液的吸光度,根据朗伯-比耳定律确定物质溶液的
浓度。亚硝酸钠标准曲线数据如表所示。(已知:稀溶液的吸光度与浓度成正比)
标准使用液浓度/(μg•mL-1) 取标准液体积/mL 相当于亚硝酸钠的质量/μg 吸光度A
1 4.00 4 2.7045取0.001gNaNO 样品溶于蒸馏水配成1000mL稀溶液,取4.00mL该稀溶液测得吸光度为
2
2.7000,对比标准曲线数据可知,该亚硝酸钠产品纯度为
(列出计算式即可,已知1μg=10-6g)。
二、燃煤发电厂二氧化碳的处理(本题共20分)
法可用于吸收燃煤发电厂的 ,同时获得产品 。反应的原理为:
NH −CaSO CO (NH ) SO
3 4 2 4 2 4
❑ 。
CO +CaSO ⋅2H O(s)+2NH →CaCO (s)+(NH ) SO +H O
2 4 2 3 3 4 2 4 2
2. 实验室根据上述反应原理,模拟生产硫酸铵。完成下列填空:(20分)
(1)搭建如图装置,先通入NH 。通入NH 的仪器采用干燥管替代长导管的目的是
3 3
;然后通入CO ,当液体由红色变为浅红色时,立即停止实验,此时溶液的pH范围为
2
,不继续通入CO 直至过量的可能原因是 。
2
(2)已知 的溶解度曲线如图。将反应后的混合液进行如下实验:过滤、蒸发浓缩、
(NH ) SO
4 2 4
冷却结晶、过滤、洗涤烘干。两次过滤依次得到的物质分别为
和 ;实验时,烘干温度不易过高,其原因
为 。
(3)实验所得 的量较少,为提高其产量,工业上可采取的措施是
(NH ) SO
4 2 4
。(任写一条即可)
为了测定样品中 的纯度,进行实验。取1.500g硫酸铵在碱性溶液中反应,蒸馏出
(NH ) SO
4 2 4生成的氨气,用25.00mL0.500mol⋅L−1硫酸标准液吸收,再用氢氧化钠标准溶液滴定吸
收氨气后过量的硫酸。
(4)若滴定时消耗了0.200mol⋅L−1的NaOH溶液20.00mL,则该硫酸铵产品的纯度为
%。
(5)若蒸馏出的氨气中含有较多水蒸气,则实验结果将
(选填“偏大”“偏小”或“无影响”)。
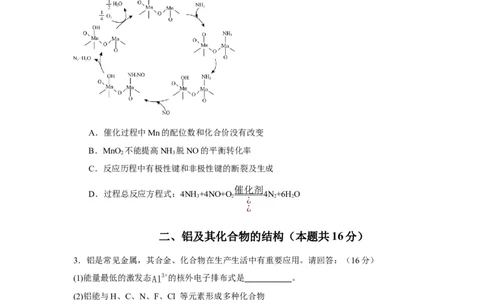
(6) NH 脱NO的一种MnO 催化机理示意图如图。下列说法错误的是
3 2
A.催化过程中Mn的配位数和化合价没有改变
B.MnO 不能提高NH 脱NO的平衡转化率
2 3
C.反应历程中有极性键和非极性键的断裂及生成
催化剂
D.过程总反应方程式:4NH +4NO+O 4N+6H O
3 2 2 2
¿
¿
二、铝及其化合物的结构(本题共16分)
3.铝是常见金属,其合金、化合物在生产生活中有重要应用。请回答:(16分)
(1)能量最低的激发态Al3+的核外电子排布式是 。
(2)铝能与H、C、N、F、Cl 等元素形成多种化合物
①下列说法不正确的是 。
A.NaAlH 中Al原子的杂化方式是sp2
4
B.化学键中离子键成分的百分数:AlF >AlBr
3 3
C.AlNH 分子中有6对共用电子对
6
D.Na AlF 中所有原子或离子满足8 电子稳定结构
3 6
②常温下 AlCl 在四氯化碳中的溶解度大于MgCl ,理由是 。
3 2
③三乙基铝是一种金属有机物,结构简式为Al(C H),可做高能火箭燃料,原因是
2 5 3。
(3)AlP 晶胞结构如下图所示:
①磷化铝晶胞沿着 y轴的投影图为 (填选项字母)。
A. B. C. D.
②若磷化铝的晶胞边长为 apm,N 表示阿伏加德罗常数的值,则 AlP晶体的密度为
A
g∙cm−3(1pm=1.0×10−12m用含 N 、a 的最简代数式表示)。
A
四、化学合成山梨酸正丁酯(本题共17分)
山梨酸酯具有解毒作用,可以减轻肝脏负担,促进肝细胞修复,保护肝脏健康。
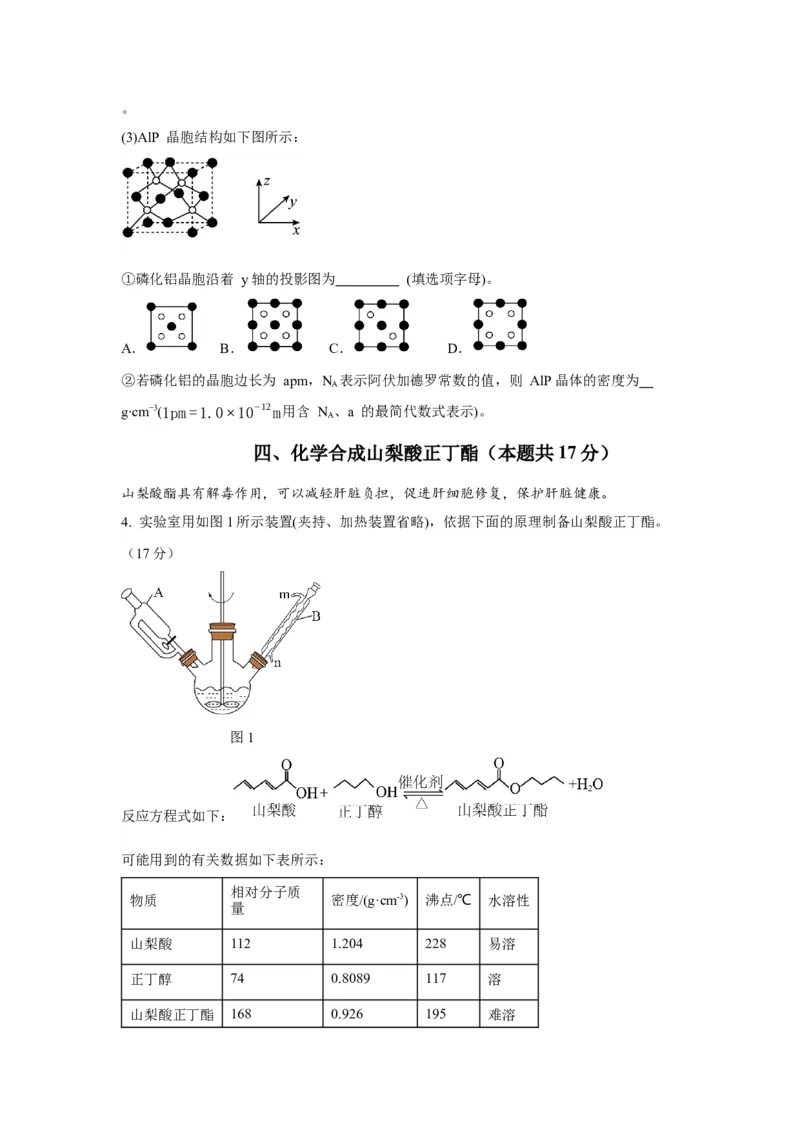
4. 实验室用如图1所示装置(夹持、加热装置省略),依据下面的原理制备山梨酸正丁酯。
(17分)
图1
反应方程式如下:
可能用到的有关数据如下表所示:
相对分子质
物质 密度/(g·cm-3) 沸点/℃ 水溶性
量
山梨酸 112 1.204 228 易溶
正丁醇 74 0.8089 117 溶
山梨酸正丁酯 168 0.926 195 难溶乙醚 74 0.714 34.6 难溶
环己烷 84 0.779 80.7 难溶
实验步骤:
①在三颈烧瓶中加入16.8g山梨酸、7.4g正丁醇、少量催化剂和几粒沸石,水浴加热三颈
烧瓶,使反应体系保持微沸。
②回流4小时后停止加热和搅拌,反应液冷却至室温。
③滤去催化剂和沸石,将滤液倒入200mL水中,加入50mL乙醚,倒入分液漏斗中,分液。
④分离出的有机层先用ρ=10mg/L的NaHCO 溶液洗涤至中性,再用水洗涤分液,收集有机
3
层。
⑤在有机层中加入少量无水MgSO ,静置片刻,过滤。
4
⑥将滤液进行蒸馏,除去杂质得到纯净的山梨酸正丁酯6.0g。回答下列问题:
(1)仪器A的名称是 ;仪器B的作用是 ,冷却水由
(填“m”或“n”)口通入。
(2)洗涤、分液过程中,加入ρ=10mg/L的NaHCO 溶液的目的是 ,
3
若改为加入NaOH的浓溶液,是否可行 (填“是”或“否”),原
因是: 。
(3)在实验步骤④中加入少量无水MgSO₄的目的是
(4)在实验步骤⑥中进行蒸馏,蒸馏至120℃除去的杂质是 。
A.乙醚和正丁醇 B. 山梨酸 C.环己烷 D.水
(5)为了提高反应正向进行的程度,实验室常使用如图2所示装置(夹持、加热装置已略去)
代替图1装置制备山梨酸正丁酯以提高产物的产率,请结合环己烷的物理性质,解释在该
装置中环己烷的主要作用 。图2
五、硫酸铝铵的综合利用及溶液离子浓度(本题共22分)
NHAl(SO) 常用作食品加工中的食品添加剂,用于焙烤食品;NHHSO 在分析试剂、医药、
4 4 2 4 4
电子工业中用途广泛。
5. 请回答下列问题:
(1)NH Al(SO ) 可用作净水剂,其原理是 (用离子方程式说明)。
4 4 2
(2)相同条件下,0.1mol•L-1NH Al(SO ) 溶液中的c(NH ) (填“等于”“大于”或
4 4 2 ❑ +
4
“小于”)0.1mol•L-1NH HSO 溶液中的c(NH )。
4 4 ❑ +
4
(3)几种均为0.1mol•L-1的电解质溶液的pH随温度变化的曲线如图所示。
①其中符合0.1mol•L-1NH Al(SO ) 溶液的pH随温度变化的曲线是 (填数字),导致
4 4 2
NH Al(SO ) 溶液的pH随温度变化的原因是 。
4 4 2
②20℃时,0.1mol•L-1NH Al(SO ) 溶液中2c(SO )—c(NH )—3c(Al3+)= (列计算
4 4 2 2- +
❑ ❑
4 4
式不必化简)mol•L-1。
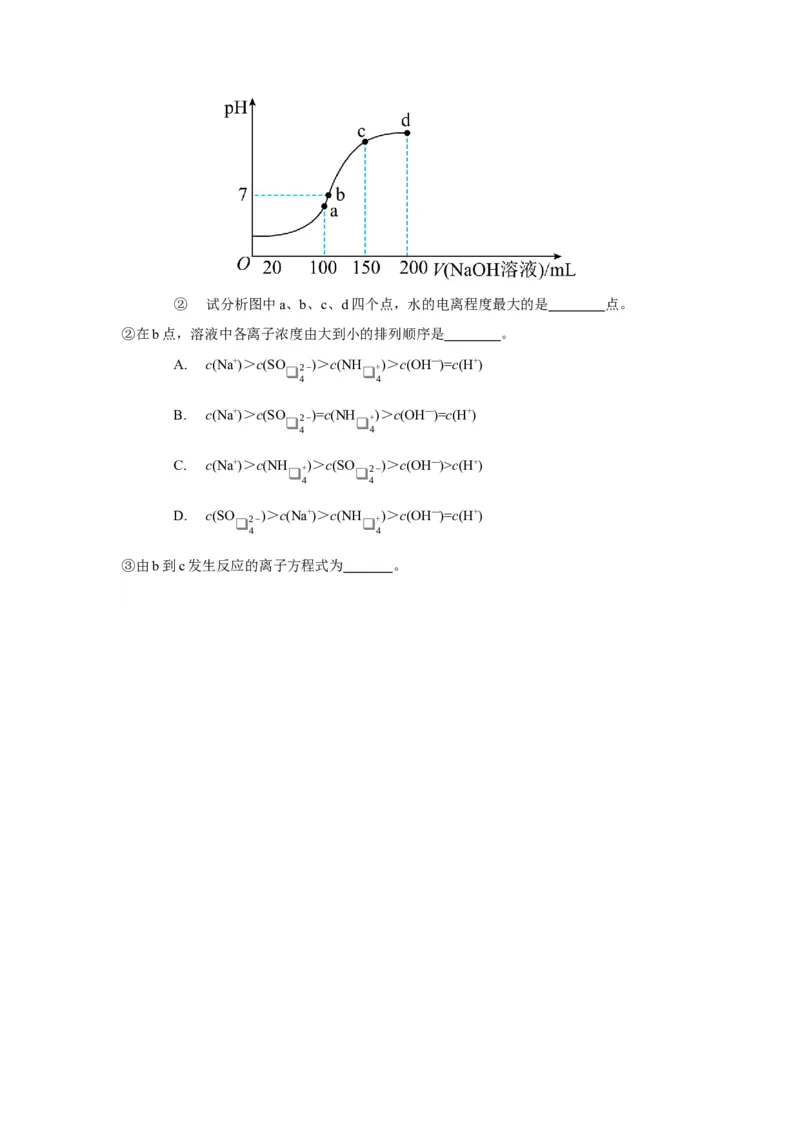
(4)室温时,向100mL0.1mol•L-1NH HSO 溶液中滴加0.1mol•L-1NaOH溶液,溶液pH与加入
4 4
NaOH溶液体积的关系曲线如图所示。② 试分析图中a、b、c、d四个点,水的电离程度最大的是 点。
②在b点,溶液中各离子浓度由大到小的排列顺序是 。
A. c(Na+)>c(SO )>c(NH )>c(OH—)=c(H+)
2− +
❑ ❑
4 4
B. c(Na+)>c(SO )=c(NH )>c(OH—)=c(H+)
2− +
❑ ❑
4 4
C. c(Na+)>c(NH )>c(SO )>c(OH—)>c(H+)
+ 2−
❑ ❑
4 4
D. c(SO )>c(Na+)>c(NH )>c(OH—)=c(H+)
2− +
❑ ❑
4 4
③由b到c发生反应的离子方程式为 。