文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(福建专用)
黄金卷02
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Ti-48 V-51 Ga-70
第Ⅰ卷
1.一带一路是中国提出的经济发展战略,也是一项全球性的合作倡议,涉及亚洲、欧洲和非洲等60多个
国家和地区。下列“一带一路”各成员国的特色贸易商品中,主要有机成分不属于糖类的是
A.吉尔吉斯坦蜂蜜 B.蒙古羊绒 C.新疆棉花 D.泰国大米
2.奥司他韦是目前治疗甲型流感的常用药物。其结构如图所示,下列有关奥司他韦的说法错误的是
A.难溶于水
B.分子式为C H NO
16 27 2 4
C.可发生加成反应、水解反应、氧化反应
D.分子中满足sp3杂化轨道类型的原子对应的元素有3种
3.解耦电解水可实现用电低谷期的过剩电力向氢能的高效转化,一种以多硫化物离子为介质的转化关系
如下图所示。设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.用电低谷期生成1molS 得到电子数目为2N
A
B.1mol的硫酸分子中含有σ键数目为4N
A
C.1L 0.1mol•L-1 NaS溶液中含阴离子的数目小于0.lN
2 A
D.用电高峰期1molH O发生还原反应生成11.2L H
2 2
4.下列实验能达到实验目的的是
A.图1装置可制备HS气体
2
B.图2装置可准确测定醋酸溶液的浓度
C.图3装置可验证碳酸氢钠与柠檬酸反应的热效应
D.图4装置可验证非金属性Cl>C>Si
5.前四周期元素M、Q、W、X、Y、Z原子序数依次增大。M的单质常用作保护气,W是元素周期表中
电负性最大的元素,X与Y形成化合物的化学式为YX且其焰色试验为紫色(透过蓝色钴玻璃),Z的原子序
数为28,下列说法正确的是A.键角: B.X是其所在周期第一电离能最大的元素
C.简单氢化物沸点: D.化合物甲(晶胞示意图如上图甲)的化学式为YQ
2
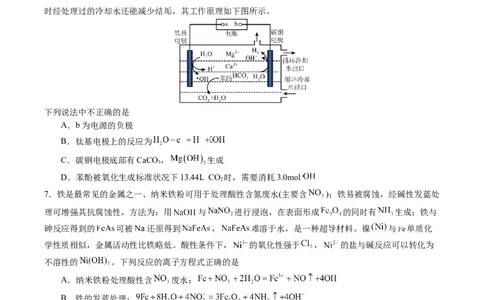
6.用电化学方法可以去除循环冷却水[含有 、 、 、 (苯酚)等]中的有机污染物,同
时经处理过的冷却水还能减少结垢,其工作原理如下图所示。
下列说法中不正确的是
A.b为电源的负极
B.钛基电极上的反应为
C.碳钢电极底部有CaCO , 生成
3
D.苯酚被氧化生成标准状况下13.44L CO 时,需要消耗3.0mol
2
7.铁是最常见的金属之一、纳米铁粉可用于处理酸性含氮废水(主要含 );铁易被腐蚀,经碱性发蓝处
理可增强其抗腐蚀性,方法为:用 与 进行浸泡,在表面形成 的同时有 生成;铁与
砷反应得到的 可被 还原得到 , 难溶于水,是一种超导材料。镍 与 单质化
学性质相似,金属活动性比铁略低。酸性条件下, 的氧化性强于 , 的盐与碱反应可以转化为
不溶性的 。下列反应的离子方程式正确的是
A.纳米铁粉处理酸性含 废水:
B.铁的发蓝处理:
C. 溶液中加少量氨水:
D. 与浓盐酸反应:
8.乙二醇在生产、生活中有着广泛的用途,某工艺制取乙二醇所涉及的反应如下:
反应Ⅰ
反应Ⅱ
在压强一定的条件下,将 、 按1:3进料比通入装有催化剂的反应器中,测得的转化率与 、 的选择性[
]。
下列说法正确的是
A.曲线a表示 转化率
B.195℃时,反应Ⅰ的平衡常数约为2904
C.190~198℃范围内,温度升高, 的值减小
D.其它条件相同时,增大压强和升高温度均可以提高平衡时 的产量
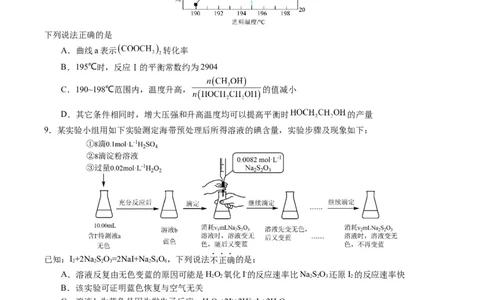
9.某实验小组用如下实验测定海带预处理后所得溶液的碘含量,实验步骤及现象如下:
已知:I+2Na SO=2NaI+Na SO,下列说法不正确的是:
2 2 2 3 2 4 6
A.溶液反复由无色变蓝的原因可能是HO 氧化I-的反应速率比NaSO 还原I 的反应速率快
2 2 2 2 3 2
B.该实验可证明蓝色恢复与空气无关
C.溶液b为蓝色是因为发生了反应:HO+2I-+2H+=I +2H O
2 2 2 2
D.上述实验不能准确测定待测液中的碘含量,应补充实验步骤:滴定前向溶液b中加少量MnO ,反
2
应至不再产生气泡,过滤,对滤液进行滴定
10.常温下,向10.0mL浓度均为0.1mol/L的 和 混合溶液中加入NaOH固体,溶液中金属元素
有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b两点溶液的pH分别
为3.0,4.3.已知:① ;
② ,298K, 。
下列叙述正确的是
A.曲线Ⅱ代表
B.常温下,
C.c点铁铝元素主要存在形式为 和
D. 的平衡常数K为 数量级
第Ⅱ卷
二、非选择题:共4题,共60分。
11.(19分)综合利用炼锌矿渣[主要含铁酸镓 、铁酸锌 、偏钛酸亚铁 ]获得钛
白( )和单质镓,部分工艺流程如图
已知:①镓和铝同主族,化学性质相似;
②常温下, , , ;
③酸浸时,钛元素以 形式存在,室温下 极易水解;
④金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见下表。
金属离子
萃取率(%) 0 99 0 97~98.5
(1)步骤Ⅰ,“浸出”时 发生反应的离子方程式为 。
(2)下列有关说法正确的是 。
A.步骤Ⅰ:将炼锌矿渣粉碎和适当提高硫酸浓度提高浸出速率
B.操作1包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等一系列操作
C.步骤Ⅱ,调节pH的目的是沉淀 和D.步骤Ⅳ,加大萃取剂用量,一次完成萃取以提高萃取效率
E.步骤Ⅴ,溶液直接电解制得粗镓的电极反应式为
(3)Ga可形成[Ga(NH )Cl]Cl、[Ga(NH )Cl]Cl 、[Ga(NH )]Cl 等一系列配合物。
3 4 2 3 5 2 3 6 3
①组成该配合物的元素Ga、N、Cl的第一电离能由大到小的顺序为 。
②[Ga(NH)Cl]Cl中的中心体是 。
3 4 2
(4)GaN、GaP、GaAs都是很好的半导体材料,晶体类型与晶体硅类似,熔点如下表所示,分析其变化
原因 。
GaN GaP GaAs
熔 1480
1700℃ 1238℃
点 ℃
(5)GaN晶胞结构如图1所示。已知六棱柱底边边长为a cm,阿伏伽德罗常数的值为N 。
A
①晶胞中Ga原子采用六方最密堆积方式,每个Ga原子周围距离最近的Ga原子数目为 ;
②从GaN晶体中“分割”出的平行六面体如图2。若该平行六面体的体积为 a3cm3,GaN晶体的密度为
g/cm3(用a、N 表示)。
A
图1 图2
(6)测定钛白中 的含量可用滴定分析法:称取mg样品放入锥形瓶中,加入 和 混合
溶液,加热使样品溶解。冷却后,加入足量稀盐酸(Ti元素存在形式变为 )。加入过量铝粉将 充
分还原[ (未配平)],待过量金属铝完全溶解并冷却后,滴加2~3滴指示剂,用
cmol/L的 标准溶液进行滴定( 能将 氧化成四价钛的化合物),重复上述滴定操作2~3
次,平均消耗 标准溶液VmL。
①过量铝粉的作用除了还原 外,另一个作用是 。
②上述滴定过程中应选用指示剂为 。
③下列关于滴定分析的操作,不正确的是 。
A.用托盘天平称量 样品mg
B.滴定管用蒸馏水洗涤时,洗涤液应从滴定管下端放出
C.滴定时,通常用左手控制旋塞滴加溶液,右手摇动锥形瓶,使溶液向同一方向旋转
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.滴定前滴定管尖嘴内无气泡,滴定后尖嘴内有气泡,则测得 的含量测定结果偏高
④钛白中 质量分数为 。(写出最简表达式即可)。
12.(14分)硫酸氧矾( )对高血糖症具有一定的治疗作用。制备 的实验流程如下,实验装置如图所示(夹持及加热装置已省略)。
溶液(橙红色) 溶液(蓝黑色) 晶体(纯蓝
色)
回答下列问题;
(1)仪器b的名称为 。仪器a中发生反应生成 的化学方程式为 。
(2)常温下, 是一种黄色固体粉末,微溶于水,溶于硫酸。溶于硫酸过程中温度与产物的产率之间
的关系如图所示,则最适宜的加热方式为 (填“直接加热”或“水浴加热”)。
(3)加入草酸前,为防止草酸受热分解,需对反应液采取的措施是 。反应液由橙红色变为蓝
黑色,反应的离子方程式为 。操作a包括 、冷却结晶、过滤、洗涤、干燥。
(4)硫酸氧钒中钒含量的测定(硫酸氧钒中钒含量 ):
Ⅰ.制备 溶液
称取 ,并量取一定体积的浓硫酸、水,加入一定量的草酸,置于图1装置中反应至溶液呈蓝
黑色。
Ⅱ.滴定预处理
步骤①:将制得的蓝黑色 溶液用250mL容量瓶定容。
步骤②:取定容后的蓝黑色 溶液15.00mL于锥形瓶中,滴加足量酸性 溶液(可将 氧化
为 )至反应完全。
步骤③:加入2mL尿素溶液,振荡,使其充分反应;然后在酸性条件下滴加 溶液,至溶液不再产
生气泡[已知: ]。
Ⅲ.滴定过程
加入10mL硫酸和磷酸的混合酸,调节pH=0,滴入几滴指示剂,用硫酸亚铁铵[ ]标准溶液
滴定至终点( )。得到处理后的数据如下:
次数 1 2 3
换算得到250mL蓝黑色 溶液中钒元素的质量m(V)/g 0.2441 0.2685 0.2439则步骤③中加入尿素的目的是 ,测得硫酸氧钒中钒含量为 (列出计算式)。
13.(14分) 和 是重要的化工原料,其综合利用具有重要意义。
(1) 与 经催化重整,制得合成气:
①已知上述反应中相关的化学键键能数据如下:
化学键
键能/ 413 745 436 1075
则该反应的 。
②按一定体积比加入 和 ,在恒压下发生反应,温度对CO和 产率的影响如图所示。此反应优选
温度为900℃的原因是 。
(2)工业上常用甲烷水蒸气重整制备氢气,体系中发生如下反应:
I.
Ⅱ.
①某温度下,体积为1L的密闭容器中, 和 反应达平衡时, 的转化率为
, 的物质的量为 ,则反应I的平衡常数 。(写出含有 、b的计算式)
②在允许 自由迁移的固体电解质燃料电池中, 放电的电极反应式为 。
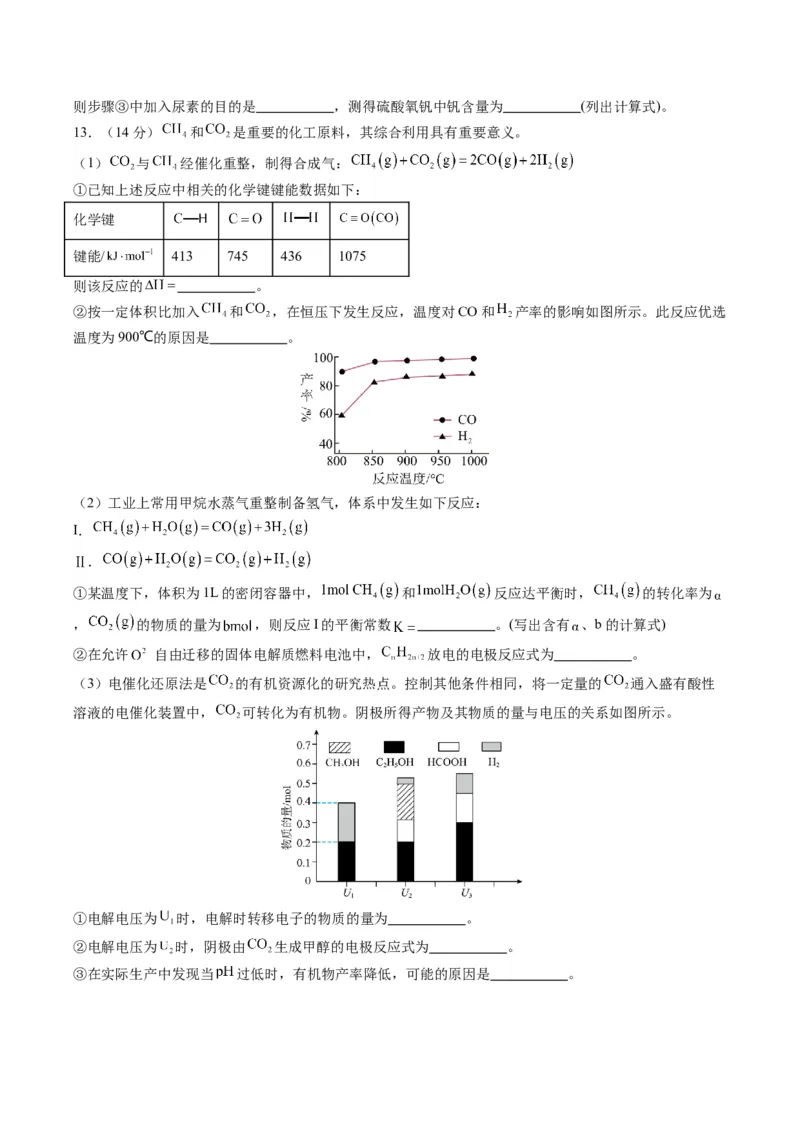
(3)电催化还原法是 的有机资源化的研究热点。控制其他条件相同,将一定量的 通入盛有酸性
溶液的电催化装置中, 可转化为有机物。阴极所得产物及其物质的量与电压的关系如图所示。
①电解电压为 时,电解时转移电子的物质的量为 。
②电解电压为 时,阴极由 生成甲醇的电极反应式为 。
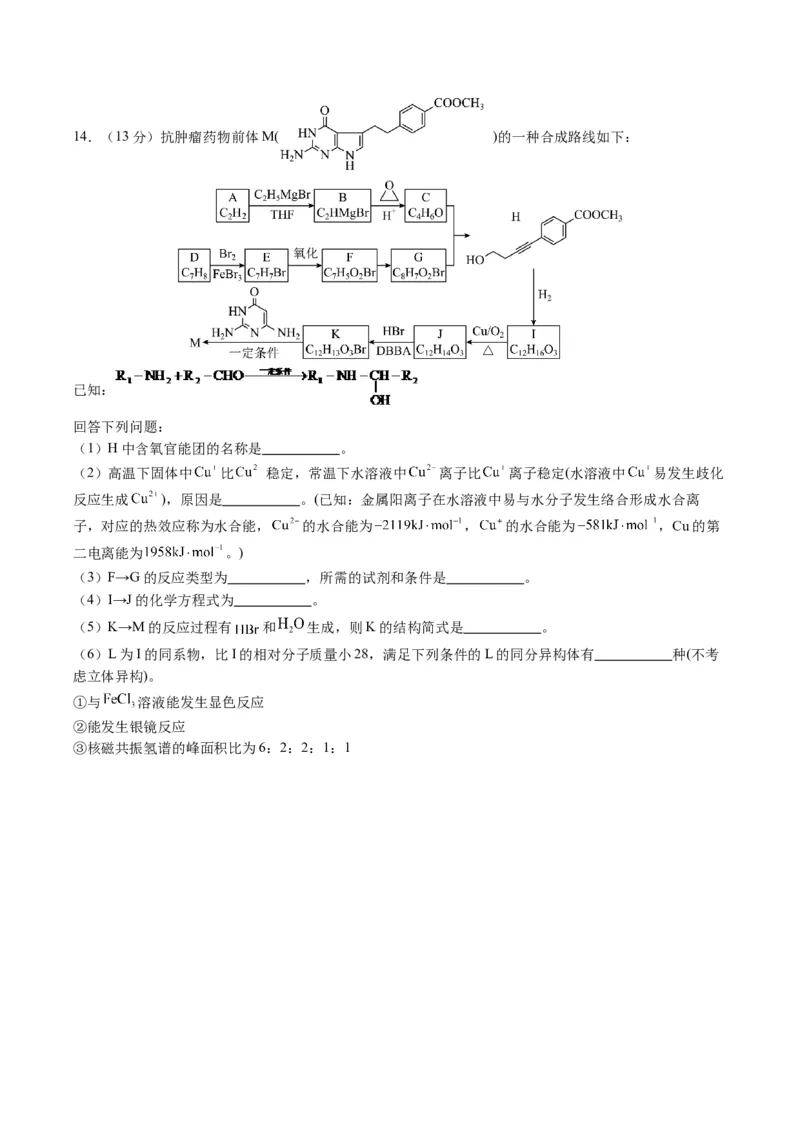
③在实际生产中发现当 过低时,有机物产率降低,可能的原因是 。14.(13分)抗肿瘤药物前体M( )的一种合成路线如下:
已知:
回答下列问题:
(1)H中含氧官能团的名称是 。
(2)高温下固体中 比 稳定,常温下水溶液中 离子比 离子稳定(水溶液中 易发生歧化
反应生成 ),原因是 。(已知:金属阳离子在水溶液中易与水分子发生络合形成水合离
子,对应的热效应称为水合能, 的水合能为 , 的水合能为 ,Cu的第
二电离能为 。)
(3)F→G的反应类型为 ,所需的试剂和条件是 。
(4)I→J的化学方程式为 。
(5)K→M的反应过程有 和 生成,则K的结构简式是 。
(6)L为I的同系物,比I的相对分子质量小28,满足下列条件的L的同分异构体有 种(不考
虑立体异构)。
①与 溶液能发生显色反应
②能发生银镜反应
③核磁共振氢谱的峰面积比为6:2:2:1:1