文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(福建专用)
黄金卷03
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Fe-56 Zn-65
第Ⅰ卷
一、单项选择题:共10题,每题4分,共40分。每题只有一个选项最符合题意。
1.室温常压超导材料LK-99(改性铅磷灰石),其化学式为Pb Cu (PO )O,x=0.9~1.0.LK-99材料属于
10-x x 4 6
A.金属材料 B.无机非金属材料 C.有机合成材料 D.半导体材料
2.设 是阿伏加德罗常数的值,催化氧化脱硫的工作原理: ,
时, 。下列说法正确的是
A. 水中含有的氢键数为2
B.每生成 , 失去的电子数为
C.氢氧化铁的悬浊液中,若 时,悬浊液中的 数目为
D.反应中每产生 ,消耗 数目
3.英国皇家化学学会(RSC)、华威大学和苏黎世IBM研究所的科学家们合作研发出结构酷似奥运五环的新
分子,因此被命名为“奥林匹克烯”,其结构如图所示。下列说法错误的是
A.“奥林匹克烯”的分子式为
B.“奥林匹克烯”可以发生加成反应
C.分子中所有的原子共平面
D.其一氯代物有6种
4.原子序数依次递增的X、Y、Z、W、M五种主族元素位于短周期,Y、Z、W位于同周期,基态X、
Y、Z、W原子的未成对电子数之和是基态M原子的价层电子数的2倍。X、Y、Z、W元素组成的物质存
在如图所示的转化关系。下列说法错误的是
A.第一电离能
B.M的单质属于共价晶体
C.离子半径:
D.X、Y、Z、W形成的化合物中可能含有离子键
5.室温下,下列实验探究方案能达到探究目的的是选项 探究方案 探究目的
向甲、乙两支试管中分别加入 溶液,向甲试 探究反应物浓度对水解平衡
A
的影响
管中加入少量 晶体,振荡、静置,对比观察溶液颜色变化
用pH计分别测定等体积的 溶液和 溶液的 探究键的极性对羧酸酸性的
B
影响
pH
向圆底烧瓶中加入2.0gNaOH、15mL无水乙醇、碎瓷片和5mL1-溴
C 探究1—溴丁烷的消去产物
丁烷,微热,将产生的气体通入酸性 溶液,观察现象
探究 与 氧化性强
D 向 溶液中滴入硫酸酸化的 溶液,观察溶液颜色变化
弱
6. 的KOH溶液称为奈斯勒(Nessler)试剂,其制备流程及特色反应如图所示。
下列说法错误的是
A.反应①的离子方程式为:
B.由反应②可知用KI溶液可除去 中的
C.反应③中消耗的 和 的物质的量之比为1:4
D.可用奈斯勒试剂检验 中微量的
7.为探究 在盐酸中与 、 的反应,某实验小组设计如图实验。
已知: ,实验Ⅰ中得到的黑色固体为 。下列说法正确的是
A.实验Ⅰ、Ⅱ中生成 白色沉淀的原理不相同
B. 在实验Ⅰ、Ⅱ中呈现的化学性质一致
C.实验Ⅰ通入 时反应的离子方程式为
2
原创精品资源学科网独家享有版权,侵权必究!D.实验Ⅱ若消耗 ,则生成 个
8.用黄铁矿为原料制硫酸产生的硫酸渣(含 、 、 、MgO等)提取铁红( )的过程如图所
示。下列有关离子反应方程式判断和书写错误的是
A.酸溶过程中 溶解的离子反应方程式为
B.滤渣A溶解于NaOH溶液的离子方程式为
C.“还原”过程产物之一为 ,发生的离子反应方程式为
D.“氧化”过程发生的离子反应方程式为
9.电解硫酸钠溶液制取电池正极材料 的前驱体 ,其工作原理如图所示:
下列说法不正确的是
A.a是直流电源的正极,石墨电极发生氧化反应
B.交换膜A是阴离子交换膜,通电一段时间,Ⅰ室pH降低
C.当产生 的 时,标准状况下纯钛电极上至少产生 气体
D.若将纯钛电极直接放入Ⅱ室,则纯钛电极上会有金属与前驱体附着而使产率降低
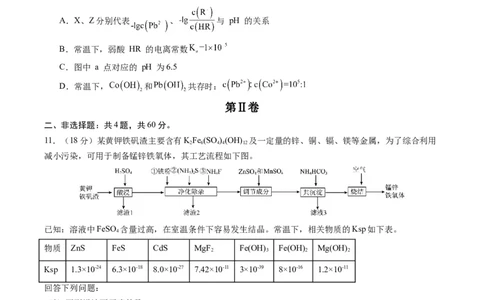
10.常温下,向 、 和 HR 的混合液中滴加 NaOH 溶液,pM 与 pH 的关系如图所
示。已知:pM=-lgc(M),c(M)代表 、 或 , 。下列叙述错误的是
A.X、Z分别代表 、 与 pH 的关系
B.常温下,弱酸 HR 的电离常数
C.图中 a 点对应的 pH 为6.5
D.常温下, 和 共存时:
第Ⅱ卷
二、非选择题:共4题,共60分。
11.(18分)某黄钾铁矾渣主要含有KFe (SO )(OH) 及一定量的锌、铜、镉、镁等金属,为了综合利用
2 6 4 4 12
减小污染,可用于制备锰锌铁氧体,其工艺流程如下图。
已知:溶液中FeSO 含量过高,在室温条件下容易发生结晶。常温下,相关物质的Ksp如下表。
4
物质 ZnS FeS CdS MgF Fe(OH) Fe(OH) Mg(OH)
2 3 2 2
Ksp 1.3×10-24 6.3×10-18 8.0×10-27 7.42×10-11 3×10-39 8×10-16 1.2×10-11
回答下列问题:
(1)下列说法不正确的是___________。
A.酸浸时,可通过增大酸的浓度及加热的方式加快酸浸速率
B.浸出液中的Fe3+极易形成Fe(OH) 胶体造成过滤困难和带入大量杂质,因而需要加铁粉进行还原
3
C.净化除杂过程中加入(NH )S的目的是除去溶液中的Cd2+,加入NH F的目的是除去溶液中的Mg2+
4 2 4
D.将滤液3蒸发结晶、过滤可获得纯净的(NH )SO 晶体
4 2 4
(2)基态铁原子的外围电子排布式为 。 和 可形成如图所示的配合物离子,其中铁的
一个配体为茂环阴离子( ),该配体以π电子参与配位,配合物离子中与铁形成配位键的电子共有
个,S元素的杂化方式为 。
4
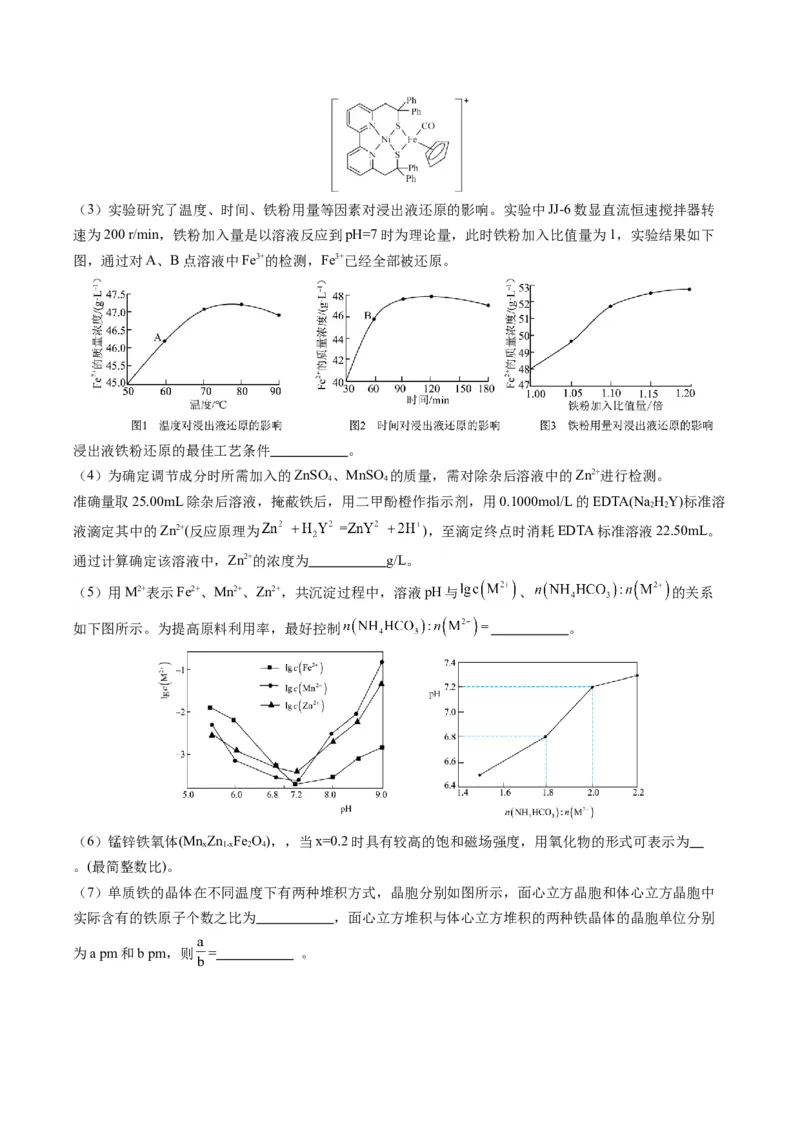
原创精品资源学科网独家享有版权,侵权必究!(3)实验研究了温度、时间、铁粉用量等因素对浸出液还原的影响。实验中JJ-6数显直流恒速搅拌器转
速为200 r/min,铁粉加入量是以溶液反应到pH=7时为理论量,此时铁粉加入比值量为1,实验结果如下
图,通过对A、B点溶液中Fe3+的检测,Fe3+已经全部被还原。
浸出液铁粉还原的最佳工艺条件 。
(4)为确定调节成分时所需加入的ZnSO、MnSO 的质量,需对除杂后溶液中的Zn2+进行检测。
4 4
准确量取25.00mL除杂后溶液,掩蔽铁后,用二甲酚橙作指示剂,用0.1000mol/L的EDTA(Na HY)标准溶
2 2
液滴定其中的Zn2+(反应原理为 ),至滴定终点时消耗EDTA标准溶液22.50mL。
通过计算确定该溶液中,Zn2+的浓度为 g/L。
(5)用M2+表示Fe2+、Mn2+、Zn2+,共沉淀过程中,溶液pH与 、 的关系
如下图所示。为提高原料利用率,最好控制 。
(6)锰锌铁氧体(Mn Zn Fe O),,当x=0.2时具有较高的饱和磁场强度,用氧化物的形式可表示为
x 1-x 2 4
。(最简整数比)。
(7)单质铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,面心立方晶胞和体心立方晶胞中
实际含有的铁原子个数之比为 ,面心立方堆积与体心立方堆积的两种铁晶体的晶胞单位分别
为a pm和b pm,则 = 。12.(14分)某小组同学探究不同条件下 与三价铬( )化合物的反应。
资料:ⅰ、 (墨绿色)、 (墨绿色)、 (蓝色)、 (黄色)、 (橙色)、 (砖
红色)。
ⅱ、
ⅲ、 ;
室温下,向 溶液中滴加 溶液或 溶液分别配制不同 的 (Ⅲ)溶液;取
配制后的溶液各 ,分别加入足量30% 溶液。
实验 ① ② ③ ④
4.10 6.75 8.43 13.37
加 前
现 蓝色浊
墨绿色溶液 蓝色浊液 墨绿色溶液
象 液
现 黄色溶
加 后 墨绿色溶液 黄绿色溶液 砖红色溶液
象 液
(1)结合加 前的实验现象,可推测 具有 (填“碱性”、“酸性”或“两性”)。
(2)实验①中,加 后无明显现象的原因可能是 。
(3)实验②中,蓝色浊液变为黄绿色溶液的原因可能是 。
(4)取实验③中黄色溶液,加入一定量稀硫酸,可观察到,溶液迅速变为橙色,最终变为绿色,观察到
有无色气体产生。结合化学用语解释上述实验现象 。
(5)已知 中 为+5价。实验④中,加入 后发生反应的离子方程式为 。
(6)取少量实验④的砖红色溶液,加热,随着温度的升高,溶液最终变为黄色。针对溶液的颜色变化,
该小组同学提出如下猜想。
猜想1:加热条件下, 发生自身氧化还原反应,生成 ;
猜想2: 。
针对上述猜想,该小组同学另取少量实验④的砖红色溶液, ,溶液由砖红色变为黄色,由此
得出猜想1成立。
(7)综合以上实验,影响 与三价铬化合物反应的因素除了 ,还有 。
13.(14分)甲醇重整制氢的主要反应如下:
6
原创精品资源学科网独家享有版权,侵权必究!反应i:
反应ⅱ:
反应iii:
(1)已知在标态和温度为T条件下,由稳定态单质生成1mo1化合物的焓变叫做该物质在T时的标准摩尔
生成熔(符号是ΔH ϴ)。几种物质在298K时的标准摩尔生成焓如下表所示,据此计算ΔH=
1 m 1
kJ·mol-1。
物质 CHOH(g) HO(g) CO(g) H(g)
3 2 2 2
ΔH ϴ /(kJ
1 m
-190.7 -241.8 -393.5 0
mol-1)
(2)一定条件下,向某恒容密闭容器中通入CHOH(g)和HO(g),在铜基催化剂上发生反应i,可能反应
3 2
机理如图所示:
①根据图中反应机理分析,HC=O与Cu2+催化剂之间形成的化学键类型为 。
2
A.σ键 B.π键 C.配位键 D.离子键
②在反应i过程中,不断分离出CO 有利于提高反应速率的原因 。
2
③能表明反应达到平衡状态的是 (填序号);
A.c(CO)=3c(H ) B.混合气体的平均相对分子质量不变
2 2
C.3v (H O)=v (H ) D.混合气体的密度不变
正 2 逆 2
(3)一定温度下,向体积为2L的刚性容器中充入2 mol CHOH(g)和1mol HO(g)发生上述反应i、ii、
3 2
iii。
①反应过程中,CO 的浓度随者温度的升高先增大后减小,其原因为 。
2
②已知反应进行10min时,容器中含碳产物的选择性[例如 ]随温
度变化如图所示:若500K时,反应进行到10min时达到平衡,其中CHOH(g)的平衡转化率为60%,则0~10min内,
3
v(CHOCH )=
3 3
m ol·L-1·min-1。此时,HO(g)的平衡转化率为 ;由以上数据分析反应ii的平衡常数
2
K = (用分数表示)。
ii
14.(16分)我国科学家利用N—苯基甘氨酸(E)中的 键在氧气作用下构建 键,实现了喹啉并
内酯(L)的高选择性制备,其合成路线如下图。
已知:①F的核磁共振氢谱有3组峰。
②RCHO
③ROH ROR'
(1)K中官能团的名称为 。
(2)C→D的过程中通常要加入稍过量的C,可能的原因是 。
(3)F→G的反应类型为 。
(4)I→J的化学方程式为 。
(5)E的同分异构体中同时满足下列条件的有 种(不考虑立体异构)。
①苯环上有2个取代基;
②能发生水解反应和银镜反应;
③结构中既无氮氧键也无醚键。
其中1 mol能消耗2 mol NaOH的同分异构体的结构简式为 (任写一种)。
(6)E和K反应得到L的流程如下图所示(无机试剂及条件已略去):
8
原创精品资源学科网独家享有版权,侵权必究!已知:
结合已知反应信息,写出中间产物的结构简式 。