文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(广东专用)
黄金卷06
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:C -12 O -16 H- 1 P-31 S-32 N-14 Ti-48
第Ⅰ卷
一、选择题:本题共16个小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在
每小题给出的四个选项中,只有一项是符合题目要求的。
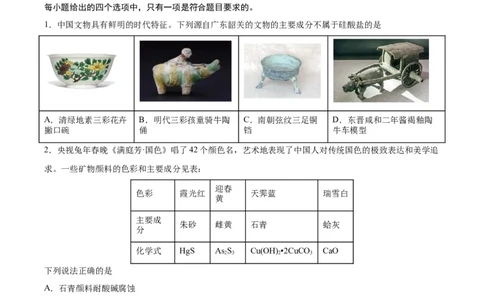
1.中国文物具有鲜明的时代特征。下列源自广东韶关的文物的主要成分不属于硅酸盐的是
A.清绿地素三彩花卉 B.明代三彩孩童骑牛陶 C.南朝弦纹三足铜 D.东晋咸和二年酱褐釉陶
撇口碗 俑 铛 牛车模型
2.央视兔年春晚《满庭芳·国色》唱了42个颜色名,艺术地表现了中国人对传统国色的极致表达和美学追
求。一些矿物颜料的色彩和主要成分见表:
迎春
色彩 霞光红 天霁蓝 瑞雪白
黄
主要成
朱砂 雌黄 石青 蛤灰
分
化学式 HgS As S Cu(OH) •2CuCO CaO
2 3 2 3
下列说法正确的是
A.石青颜料耐酸碱腐蚀
B.蛤灰加水后会放出大量的热
C.朱砂能化为汞涉及蒸发操作
D.《遁斋闲览》中记载:有误字,以雌黄灭之,为其与纸色相类。利用了雌黄的化学性质
3.科学家利用 等放射性核素释放的射线育种。下列说法正确的是
A. 的核电荷数为35 B. 和 的中子数相同C. 和 互为同位素 D. 与水反应生成
4.下列有关物质性质与用途对应关系错误的是
物质性质 物质用途
A NaO 吸收CO 产生O NaO 用作呼吸面具供氧剂
2 2 2 2 2 2
B Al O 熔融状态可电离 电解熔融Al O 制取单质Al
2 3 2 3
C 铁比铜金属性强 FeCl 腐蚀Cu刻制印刷电路板
3
D HF与SiO 反应 HF在玻璃器皿上刻蚀标记
2
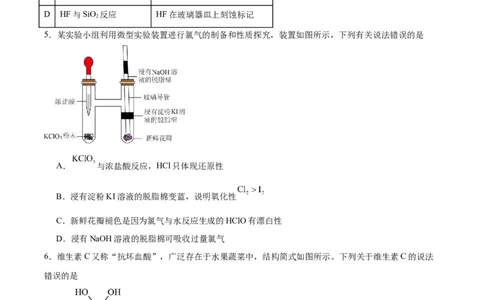
5.某实验小组利用微型实验装置进行氯气的制备和性质探究,装置如图所示,下列有关说法错误的是
A. 与浓盐酸反应,HCl只体现还原性
B.浸有淀粉KI溶液的脱脂棉变蓝,说明氧化性
C.新鲜花瓣褪色是因为氯气与水反应生成的HClO有漂白性
D.浸有NaOH溶液的脱脂棉可吸收过量氯气
6.维生素C又称“抗坏血酸”,广泛存在于水果蔬菜中,结构简式如图所示。下列关于维生素C的说法
错误的是
A.分子式为C HO
6 8 6
B.能与金属钠反应
C.能发生酯化反应
D.不能使酸性高锰酸钾溶液褪色
7.溴甲基蓝(用HBb表示)指示剂是一元弱酸,HBb为黄色,Bb-为蓝色。下列叙述正确的是A.0.01mol·L-1HBb溶液的pH=2
B.HBb溶液的pH随温度升高而减小
C.向NaOH溶液中滴加HBb指示剂,溶液显黄色
D.0.01mol·L-1NaBb溶液中,c(H+)+c(Na+)=c(Bb-)+c(HBb)
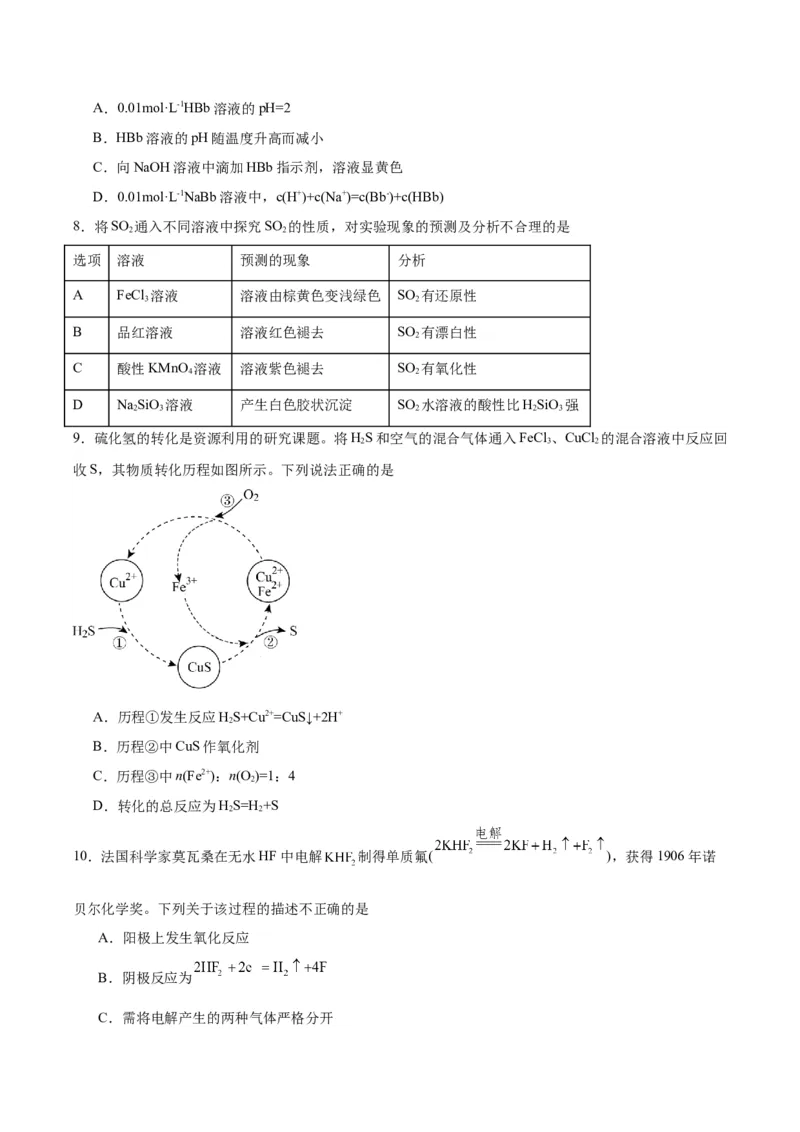
8.将SO 通入不同溶液中探究SO 的性质,对实验现象的预测及分析不合理的是
2 2
选项 溶液 预测的现象 分析
A FeCl 溶液 溶液由棕黄色变浅绿色 SO 有还原性
3 2
B 品红溶液 溶液红色褪去 SO 有漂白性
2
C 酸性KMnO 溶液 溶液紫色褪去 SO 有氧化性
4 2
D NaSiO 溶液 产生白色胶状沉淀 SO 水溶液的酸性比HSiO 强
2 3 2 2 3
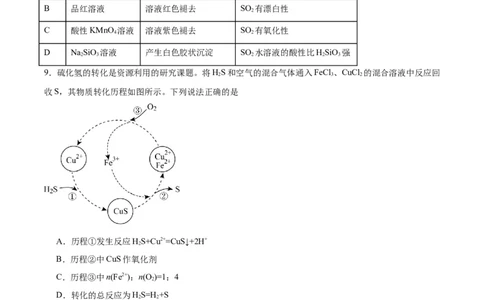
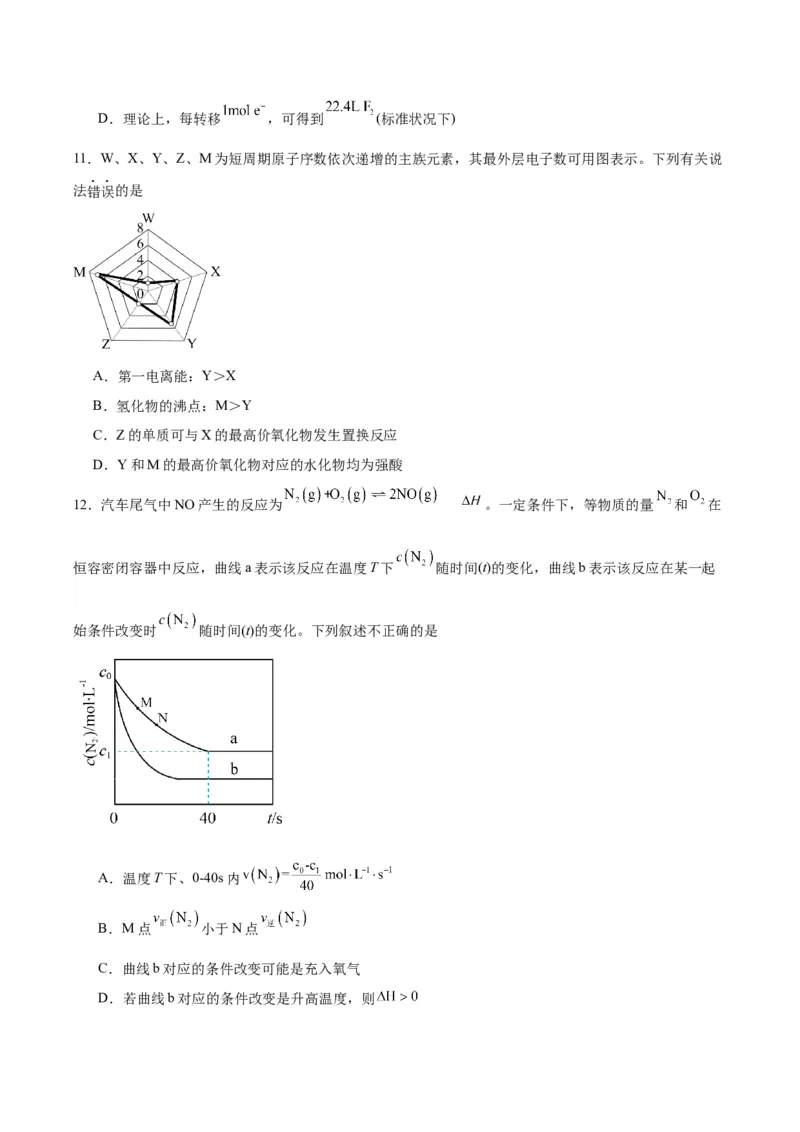
9.硫化氢的转化是资源利用的研究课题。将HS和空气的混合气体通入FeCl 、CuCl 的混合溶液中反应回
2 3 2
收S,其物质转化历程如图所示。下列说法正确的是
A.历程①发生反应HS+Cu2+=CuS↓+2H+
2
B.历程②中CuS作氧化剂
C.历程③中n(Fe2+):n(O )=1:4
2
D.转化的总反应为HS=H+S
2 2
10.法国科学家莫瓦桑在无水HF中电解 制得单质氟( ),获得1906年诺
贝尔化学奖。下列关于该过程的描述不正确的是
A.阳极上发生氧化反应
B.阴极反应为
C.需将电解产生的两种气体严格分开D.理论上,每转移 ,可得到 (标准状况下)
11.W、X、Y、Z、M为短周期原子序数依次递增的主族元素,其最外层电子数可用图表示。下列有关说
法错误的是
A.第一电离能:Y>X
B.氢化物的沸点:M>Y
C.Z的单质可与X的最高价氧化物发生置换反应
D.Y和M的最高价氧化物对应的水化物均为强酸
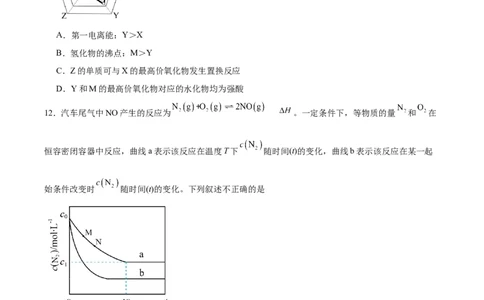
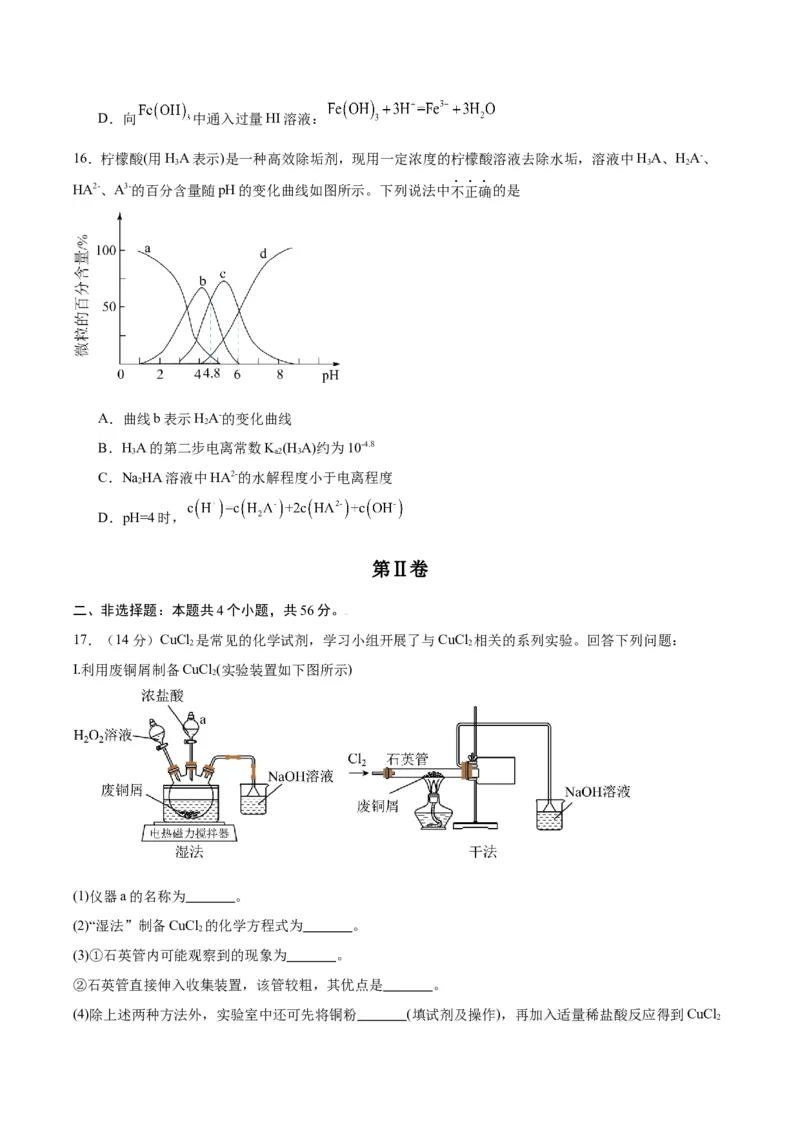
12.汽车尾气中NO产生的反应为 。一定条件下,等物质的量 和 在
恒容密闭容器中反应,曲线a表示该反应在温度T下 随时间(t)的变化,曲线b表示该反应在某一起
始条件改变时 随时间(t)的变化。下列叙述不正确的是
A.温度T下、0-40s内
B.M点 小于N点
C.曲线b对应的条件改变可能是充入氧气
D.若曲线b对应的条件改变是升高温度,则13.下列实验对应的现象和结论都正确的是
选项 实验 现象 结论
向食品脱氧剂样品(含还原铁粉)中加入硫酸后滴 食品脱氧剂样品中含
A 紫红色褪去
加酸性 溶液
向 溶液中滴入 溶液,再滴加 溶 加入 后溶液变成 既有氧化性又有
B
液 血红色 还原性
溶液变蓝、有黑色固
C 向 溶液加入铜片 金属铁比铜活泼
体出现
D 向 溶液中加入 溶液后滴加几滴淀粉溶液 溶液变为蓝色 氧化性:
14.新型Li-Mg双离子可充电电池是一种高效、低成本的储能电池,其工作原理如图所示。放电时电极a
的反应为: ;下列说法不正确的是
A.充电时, 极为阴极
B.放电时, 从I室向II室迁移
C.放电时,II室 溶液的浓度增大
D.每消耗 ,电极a质量理论上增加
15.宏观辨识与微观探析是化学核心素养之一,下列有关离子方程式的书写正确的是
A.向 溶液中通入过量 :
B.用惰性电极电解NaCl溶液:
C.将铜丝插入稀硝酸溶液中:D.向 中通入过量HI溶液:
16.柠檬酸(用HA表示)是一种高效除垢剂,现用一定浓度的柠檬酸溶液去除水垢,溶液中HA、HA-、
3 3 2
HA2-、A3-的百分含量随pH的变化曲线如图所示。下列说法中不正确的是
A.曲线b表示HA-的变化曲线
2
B.HA的第二步电离常数K (H A)约为10-4.8
3 a2 3
C.NaHA溶液中HA2-的水解程度小于电离程度
2
D.pH=4时,
第Ⅱ卷
二、非选择题:本题共4个小题,共56分。
17.(14分)CuCl 是常见的化学试剂,学习小组开展了与CuCl 相关的系列实验。回答下列问题:
2 2
I.利用废铜屑制备CuCl (实验装置如下图所示)
2
(1)仪器a的名称为 。
(2)“湿法”制备CuCl 的化学方程式为 。
2
(3)①石英管内可能观察到的现象为 。
②石英管直接伸入收集装置,该管较粗,其优点是 。
(4)除上述两种方法外,实验室中还可先将铜粉 (填试剂及操作),再加入适量稀盐酸反应得到CuCl
2溶液。
II.探究Al与CuCl 溶液的反应
2
将铝片放入盛有0.1mol·L-1CuCl 溶液的试管中,观察到现象为:铝片表面析出疏松的紫红色固体,产生无
2
色无味气体,溶液颜色变浅。
(5)紫红色固体为 (填化学式)。
(6)经检验产生的气体为H 在CuCl 溶液中存在Cu2++2H O=Cu(OH) +2H+、2A1+6H+=2A13++3H ↑,小组成
2. 2 2 2 2
员认为应产生Cu(OH) ,但实际实验中并未观察到蓝色沉淀。于是他们提出了以下两种猜测并进行相关验
2
证。完成下列表格:
猜测 实验 现象 结论
取少量Cu(OH) 悬浊液,加入打磨过的 猜想i不
i.① 。 2 无明显现象
铝片,振荡 成立
ii.Cu(OH) 与Al3+发生了 固体立即溶解,溶液呈 猜想ii成
2 ② 。
反应 浅绿色 立
③在猜测ii成立的基础上,该小组成员查阅文献发现体系中可能存在反应:2Al3+
+3Cu(OH) =2Al(OH) +3Cu2+,列式计算平衡常数分析该反应进行的趋势 。(已知:
2 3
K [Cu(OH) ]=2.2×10-20;K [Al(OH) ]=1.3×10-33。一般认为,K>105时反应进行较完全,K<10-5时反应难以
sp 2 sp 3
进行)文献显示生成的Al(OH) 可能以胶体形式存在,这是未观察到白色沉淀的可能原因,但仍需进一步深
3
入研究。
18.(14分)某湿法炼锌的萃余液中含有 及二价钴离子( )、镍离子( )、镉
离子( )和 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
已知:
沉淀物(1)“氧化、调 ”时,先加入适量的石灰石调节pH为1.0,加入适量的 ,再加入石灰石 为
4.0,
①“沉渣”的主要成分除 外还有_______________。
②若加入过量的 ,钴元素会被氧化进入“沉渣”中,则溶液中残留 的浓度为__________
。
(2)“沉锌”时,在近中性条件下加入 可得碱式碳酸锌 固体,同时产生大
量的气体,试分析产生大量气体的原因是_____________________________。
(3)由碱式碳酸锌生成氧化锌的化学方程式为______________________________。
(4)沉锌后的滤液经过一系列操作后得到的副产品为________________________(填化学式)。
(5) 的晶胞结构如图,则锌的配位数为___________;已知晶胞参数为a cm,该晶体的密度为
___________ (写出计算式,阿佛加德罗常数的值为 )。
19.氨气是基础有机合成工业和化肥工业的重要原料。
(1)诺贝尔奖获得者埃特尔提出了合成氨反应吸附解离的机理,通过实验测得合成氨势能如图所示:
在合成氨吸附解离的过程中,下列状态最稳定的是 (填选项)。A. B.NH (g) C.NH(ad)+2H(ad) D.N(ad)+3H(ad)
3
其中,NH (ad) NH (g) ∆H= kJ·mol-1,若要使该平衡正向移动,可采取的措施是
3 3
(填选项)。
A.升高温度 B.降低温度 C.增大压强 D.减小压强
(2)在上述实验条件下,向一密闭容器中通入 1molN 和 3molH 充分反应,达到平衡时放出 46kJ 热量,计
2 2
算该条件下 H 的转化率 。
2
(3)在 t ℃、压强为 3.6 MPa 条件下,向一恒压密闭容器中通入氢氮比[c(H):c(N)] 为 3 的混合气体,
2 2
体系中气体的含量与时间变化关系如图所示:
反应 20 min 达到平衡,试求 0~20 min 内氨气的平均反应速率 v(NH )= MPa·min-1。若起始
3
条件一样,在恒容容器中发生反应,则达到平衡时 H 的含量符合上图中 点(填
2
“d”、“e”、“f”或“g”)。
(4)在合成氨工艺中,未反应的气体(含不参与反应的惰性气体)可多次循环使用。当氢氮比[c(H):c(N)]为
2 2
3 时,平衡时氨气的含量关系式为:ω (NH)=0.325·K ·P·(1-i ) 2,(K :平衡常数;P:平衡体系压强;i:
3 P P
惰性气体体积分数)。当温度为 500℃,不含惰性气体时,平衡体系压强为 2.4MPa,氨气的含量为 ω ,
若此时增大压强,K 将(填“变大”、“变小”或“不变”)。若温度不变,体系中有 20%的
p
惰性气体,欲使平衡时氨气的含量仍为 ω ,应将压强调整至 MPa。
20.(14分)某研究小组以物质A和乙烯为原料,按如图路线合成用于治疗冠心病及高血压药物尼群地平。已知:① →R-CHO+H O
2
②R CHO+ +无机小分子
1
③2 +ROH
请回答:
(1)物质H中官能团的名称是 。
(2)反应Ⅲ的反应类型为 。
(3)下列说法正确的是___________。
A.反应Ⅰ需要用FeCl 做催化剂 B.化合物C能发生银镜反应
3
C.D分子中所有碳原子共平面 D.尼群地平的分子式是C H NO
18 19 2 6
(4)写出D+H→E的化学方程式 。
(5)化合物X是式量比化合物D大14的同系物,同时符合下列条件的化合物X所有同分异构体共
种,写出其中一种能直接氧化得到醛的结构简式为 。
①能与FeCl 溶液发生显色反应;
3
②HNMR谱显示分子中有4种氢原子;
③IR谱表明分子中含-C≡N键,无-O-O-、C-O-C-键
(6)设计以乙醇为原料合成H的路线(用流程图表示,无机试剂任选) 。