文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(上海专
用)
黄金卷07
(考试时间:60分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
一、 氮及其化合物的结构及其应用(19分)
氮是空气中最多的元素,在自然界中存在十分广泛,在生物体内亦有极大作用,是组
成氨基酸的基本元素之一。氮在自然界主要以双原子分子的形式存在于大气中,因而工业
上由液态空气分馏来获得氮气。产品通常储存在钢瓶中出售。从空气分馏得到的氮气纯度
约为99% ,其中含少量的氧气、氩气及水等杂质。
1.氮的化合物应用广泛。
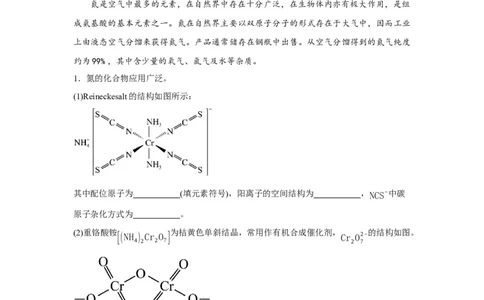
(1)Reineckesalt的结构如图所示:
其中配位原子为 (填元素符号),阳离子的空间结构为 ,NCS−中碳
原子杂化方式为 。
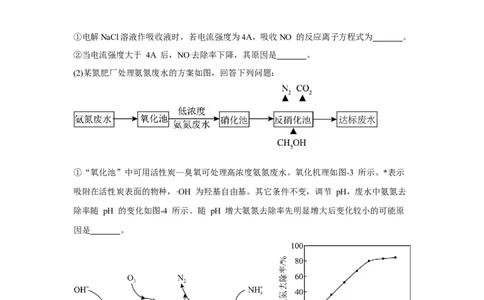
(2)重铬酸铵 为桔黄色单斜结晶,常用作有机合成催化剂, 的结构如图。
[(NH ) Cr O ] Cr O2−
4 2 2 7 2 7
中N、O、Cr三种元素第一电离能由大到小的顺序是 (填元素符号)
(NH ) Cr O
4 2 2 7
[Zn(IMI) ](ClO ) Zn2+ IMI IMI
4 4 2
(3) 是 的一种配合物, 的结构为 。 的某种衍生物与甘氨酸形成的离子化合物 常温下为液态而非
固态,原因是 。
(4)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电
子可在多个原子间运动,形成“离域 键”(或大 键)。大 键可用 表示,其中m、n
π π π Πn
m
分别代表参与形成大 键的原子个数和电子数,如苯分子中大 键表示为 。
π π Π6
6
①下列微粒中存在“离域Π键”的是 。
A. CH =CH−CH=CH B. CCl C. H O D.SO
2 2 4 2 2
② 中阴离子 与 互为等电子体,均为直线型结构, 中的2个大 键可表示为
NaN N− CO N− π
3 3 2 3
。
(5)符号“3p ”没有给出的信息是___________。
x
A.能层 B.能级
C.电子云在空间的伸展方向 D.电子的自旋方向
(6)下列实验事实不能用氢键来解释的是___________。
A.CH 比SiH 稳定
4 4
B.乙醇能与水以任意比互溶
C.邻羟基苯甲醛的沸点低于对羟基苯甲醛
D.接近沸点的水蒸气的相对分子质量测量值大于18
二、氮氧化物的处理(21分)
NO 是空气的污染物,废水中的氨氮(以NH、NH 存在)和硝态氮(以NO 、NO 存
x 3 + - -
❑ ❑ ❑
4 2 3
在)会引起水体富营养化,需经处理后才能排放。
1.电解氧化吸收法可将废气中的 NO 转变为NO 。
x -
❑
3
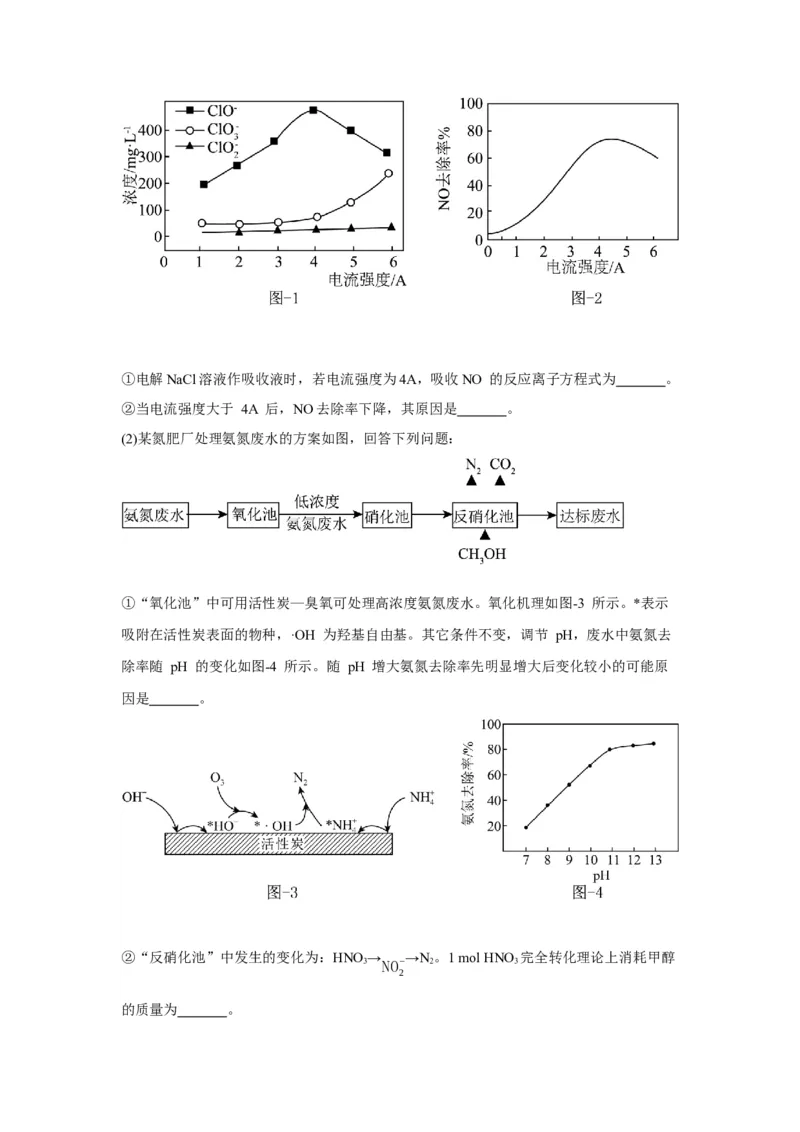
(1)电解 0.1 mol·L-1NaCl 溶液时,溶液中相关成分的浓度变化与电流强度的关系如图-1
所示。向 0.1 mol·L-1NaCl 溶液中通入 NO,测得电流强度与 NO 的脱除率的关系如图-2
所示。①电解NaCl溶液作吸收液时,若电流强度为4A,吸收NO 的反应离子方程式为 。
②当电流强度大于 4A 后,NO去除率下降,其原因是 。
(2)某氮肥厂处理氨氮废水的方案如图,回答下列问题:
①“氧化池”中可用活性炭—臭氧可处理高浓度氨氮废水。氧化机理如图-3 所示。*表示
吸附在活性炭表面的物种,·OH 为羟基自由基。其它条件不变,调节 pH,废水中氨氮去
除率随 pH 的变化如图-4 所示。随 pH 增大氨氮去除率先明显增大后变化较小的可能原
因是 。
②“反硝化池”中发生的变化为:HNO→ →N。1 mol HNO 完全转化理论上消耗甲醇
3 NO− 2 3
2
的质量为 。(3)纳米Fe 可还原去除水中的硝酸盐污染物。
已知:i.纳米 Fe 具有很高的活性,易被氧化使表面形成氧化层
ii.纳米 Fe 将 还原为 的转化关系如下:
NO− NH+
3 4
NO− Fe NO− Fe NH+
3 → 2 → 4
①纳米 Fe 的制备原理:FeSO +2NaBH +6HO=2B(OH) +Fe+7H↑+NaSO ; 已知电负
4 4 2 3 2 2 4
性 H>B,则该反应中氧化剂是 (填化学式) 。
②检验还原后的溶液中存在
NH+
的实验方法是 。
4
③溶液初始 pH 较低有利于 的去除,其可能的原因是 。
NO−
3
三、 氢能(19分)
氢能,氢和氧进行化学反应释放出的化学能,是一种二次清洁能源,被誉为“21世纪
终极能源”,也是在碳达峰、碳中和的大背景下,加速开发利用的一种清洁能源。
3.绿色能源是未来能源发展的方向。可以用以下方法制备氢气。
I.甲烷和水蒸气催化制氢气。主要反应如下:
i.CH(g)+HO(g)❑CO(g)+3H(g) △H=+206.2kJ•mol-1
4 2 2
⇌
ii.CO(g)+HO(g)❑CO(g)+H(g) △H=-41.2kJ•mol-1
2 2 2
⇌
(1)反应CH(g)+CO (g)❑2CO(g)+2H(g)的△H= kJ•mol-1。
4 2 2
⇌
(2)在容积不变的绝热密闭容器中发生反应i,下列能说明反应达到平衡状态的是 (填
标号)。
A.气体混合物的密度不再变化
B.CH 消耗速率和H 的生成速率相等
4 2
C.CO的浓度保持不变
D.气体平均相对分子质量不再变化
E.体系的温度不再发生变化
(3)恒定压强为PMPa时,将n(CH):n(H O)=1:3的混合气体投入反应器中发生反应i和
0 4 2
ii,平衡时,各组分的物质的量分数与温度的关系如图所示。①图中表示CO 的物质的量分数与温度的变化曲线是 (填字母)。
2
②结合图中数据,其他条件不变,若要H 的产量最大,最适宜的反应温度是 (填标
2
号)。
A.550~600℃ B.650~700℃ C.750~800℃
在其他条件不变的情况下,向体系中加入CaO可明显提高平衡体系中H 的含量,原因是
2
。
③600℃时,反应ii的平衡常数的计算式为K= (K 是以分压表示的平衡常数,分压=
p p
总压×物质的量分数)。
Ⅱ.电解法制氢气。某科研小组设计如图所示电解池,利用CO 和HO在碱性电解液中制
2 2
备水煤气(H 、CO),产物中H 和CO的物质的量之比为1∶1。
2 2
(4)电极B是 极,生成水煤气的电极反应式为 。
四、氨氮废水的处理(19分)
研究人员合成了一种普鲁士蓝(PB)改性的生物炭(BC)复合材料(BC-PB),并将其应用于
氨氮废水(含 、 )的处理。
NH NH+
3 4
4. 资料:①普鲁士蓝(PB)是亚铁氰化铁的俗称,化学式为 ,难溶于水。
Fe [Fe(CN) ]
4 6 3
②BC-PB中,PB负载在BC表面,没有产生新化学键,各自化学性质保持不变。
Ⅰ.复合材料BC-PB的合成
(1)下列关于ⅰ中HCN参与反应的说法正确的是 (填字母)。
a.提供H+,与Fe反应
b.提供H+,与OH−反应
c.提供CN−,与Fe2+配位
d.提供CN−,与K+反应
(2)ⅱ中分离得到 的操作包括加热浓缩、 。
K [Fe(CN) ]⋅3H O
4 6 2
(3)ⅲ中生成普鲁士蓝反应的离子方程式为 。
(4)添加造孔剂可以增加BC的孔道数目和容量。造孔剂的造孔原理之一是在一定条件下分
解产生气体。700℃时,KHCO 造孔原理的化学方程式为 。
3
Ⅱ.氨氮废水处理
用NH Cl溶液模拟氨氮废水。实验发现pH=2时,在BC-PB体系中加入H O ,可将氨氮转
4 2 2
化为无毒气体N ,提高氮氮的去除率。其原理为:
2
ⅰ. Fe [Fe(CN) ] +3H O +3H+=3Fe[Fe(CN) ]+Fe3++3⋅OH+3H O
4 6 3 2 2 6 2
ⅱ.·OH将氨氮氧化为N
2
(5)ⅱ的离子方程式为 。
(6)用BC-PB和H O混合处理1000L某氨氦含量(以NH Cl质量计算)为120mg⋅L−1的废水。
2 4
实验结束后,收集到22.4L N (已折算成标准状况)。
2
①实验中消耗的H O 的质量至少为 g。
2 2
②处理后的废水中氨氮含量为 mg⋅L−1(废水体积变化忽略不计),达到了污水
排放标准要求(≤15mg⋅L−1)。
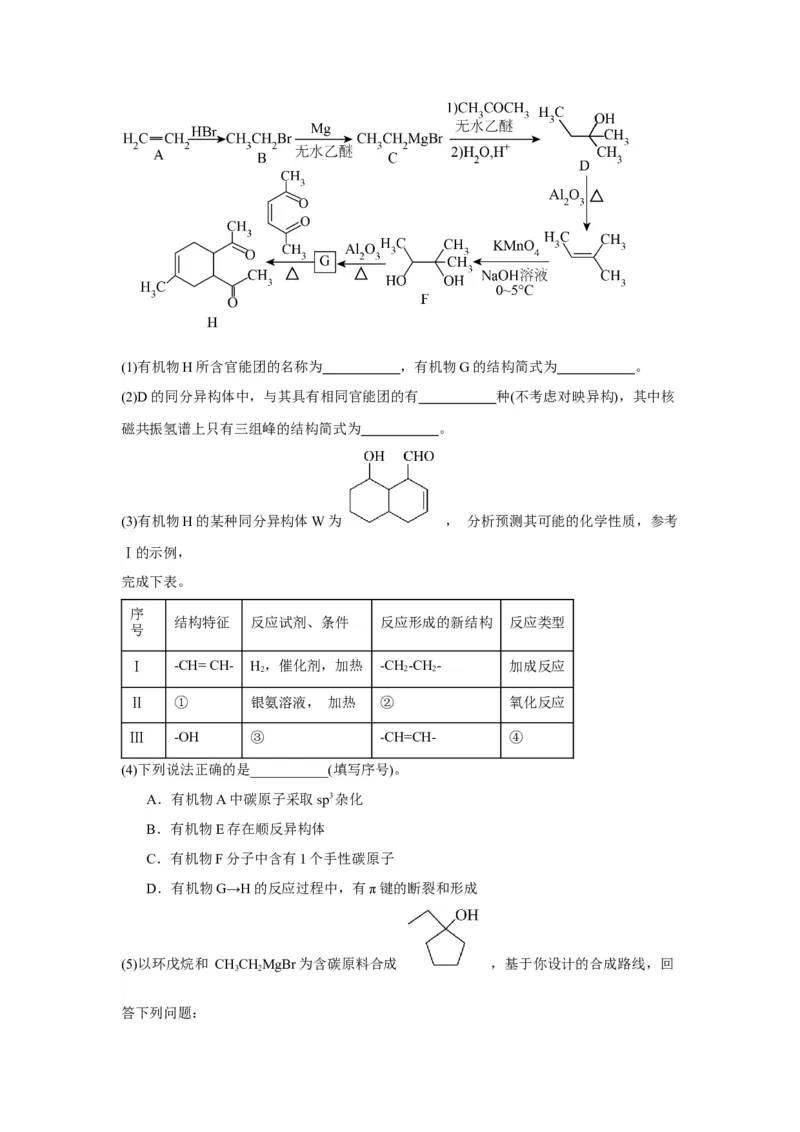
五、乙烯合成二酮(22分)
5.以乙烯为原料合成二酮H的路线如下:(1)有机物H所含官能团的名称为 ,有机物G的结构简式为 。
(2)D的同分异构体中,与其具有相同官能团的有 种(不考虑对映异构),其中核
磁共振氢谱上只有三组峰的结构简式为 。
(3)有机物H的某种同分异构体W为 , 分析预测其可能的化学性质,参考
Ⅰ的示例,
完成下表。
序
结构特征 反应试剂、条件 反应形成的新结构 反应类型
号
Ⅰ -CH= CH- H,催化剂,加热 -CH-CH- 加成反应
2 2 2
Ⅱ ① 银氨溶液, 加热 ② 氧化反应
Ⅲ -OH ③ -CH=CH- ④
(4)下列说法正确的是___________(填写序号)。
A.有机物A中碳原子采取sp3杂化
B.有机物E存在顺反异构体
C.有机物F分子中含有1个手性碳原子
D.有机物G→H的反应过程中,有π键的断裂和形成
(5)以环戊烷和 CHCHMgBr为含碳原料合成 ,基于你设计的合成路线,回
3 2
答下列问题:①除已给含碳原料外,最后一步反应物为 (写结构简式)。
②相关步骤涉及到卤代烃到醇的转化,其反应条件为 。
③从环戊烷出发,第一步的化学方程式为 (注明反应条件)。