文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(上海专
用)
黄金卷07
(考试时间:60分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
一、 氮及其化合物的结构及其应用(19分)
氮是空气中最多的元素,在自然界中存在十分广泛,在生物体内亦有极大作用,是组
成氨基酸的基本元素之一。氮在自然界主要以双原子分子的形式存在于大气中,因而工业
上由液态空气分馏来获得氮气。产品通常储存在钢瓶中出售。从空气分馏得到的氮气纯度
约为99% ,其中含少量的氧气、氩气及水等杂质。
1.氮的化合物应用广泛。
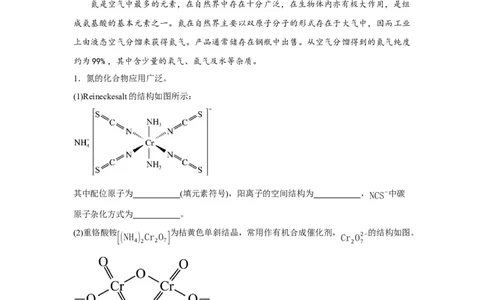
(1)Reineckesalt的结构如图所示:
其中配位原子为 (填元素符号),阳离子的空间结构为 ,NCS−中碳
原子杂化方式为 。
(2)重铬酸铵 为桔黄色单斜结晶,常用作有机合成催化剂, 的结构如图。
[(NH ) Cr O ] Cr O2−
4 2 2 7 2 7
中N、O、Cr三种元素第一电离能由大到小的顺序是 (填元素符号)
(NH ) Cr O
4 2 2 7
[Zn(IMI) ](ClO ) Zn2+ IMI IMI
4 4 2
(3) 是 的一种配合物, 的结构为 。 的某种衍生物与甘氨酸形成的离子化合物 常温下为液态而非
固态,原因是 。
(4)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电
子可在多个原子间运动,形成“离域 键”(或大 键)。大 键可用 表示,其中m、n
π π π Πn
m
分别代表参与形成大 键的原子个数和电子数,如苯分子中大 键表示为 。
π π Π6
6
①下列微粒中存在“离域Π键”的是 。
A. CH =CH−CH=CH B. CCl C. H O D.SO
2 2 4 2 2
② 中阴离子 与 互为等电子体,均为直线型结构, 中的2个大 键可表示为
NaN N− CO N− π
3 3 2 3
。
(5)符号“3p ”没有给出的信息是___________。
x
A.能层 B.能级
C.电子云在空间的伸展方向 D.电子的自旋方向
(6)下列实验事实不能用氢键来解释的是___________。
A.CH 比SiH 稳定
4 4
B.乙醇能与水以任意比互溶
C.邻羟基苯甲醛的沸点低于对羟基苯甲醛
D.接近沸点的水蒸气的相对分子质量测量值大于18
【答案】(1) Cr 正四面体形 sp杂化
(2)N>O>Cr
(3)阴阳离子半径较大,所带电荷较小,导致形成的离子键键能小,熔点低
(4) AD
π4
3
(5)D
(6)A
【解析】(1)由图可知,配位原子为 Cr,阳离子为 ,价层电子对数为
NH+
45-1-1×4
4+ =4,无孤对电子,其空间结构为正四面体型,NCS-的结构式为[N≡C-S]-,
2
碳原子杂化方式为sp杂化,故答案为:Cr;正四面体型;sp杂化;
(2)金属元素的第一电离能较小,N的第一电离能大于O,所以(NH )Cr O 中N、O、Cr
4 2 2 7
三种元素第一电离能由大到小的顺序是N>O>Cr;
(3)该化合物常温下为液态而非固态,原因是:阴阳离子半径较大,所带电荷较小,导致
形成的离子键键能小,熔点低;
(4)①根据多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p
电子可在多个原子间运动,形成“离域π键(或大π键),故A、D符合,B为正四面体结构,
C中H原子和O原子没有平行的p轨道,故答案为:AD;
② 与CO 互为等电子体,等电子体之间结构相似, 的结构式为[N=N=N]-,该离子中两
N- 2 N-
3 3
边的N原子提供1个电子,中间N原子提供2个电子,形成大π键,所以形成的大π键为:
;
π4
3
(5)3p 表示原子核外第3能层(电子层)p能级(电子亚层)轨道,其中p轨道应有3个不同
x
伸展方向的轨道,可分别表示为p、p、p,同一个原子轨道中最多含有2个自旋相反的电
x y z
子,所以从符号“3p”中不能看出电子的自旋方向,故答案为:D;
x
(6)A.氢化物稳定性与共价键的强弱有关,与氢键无关,且二者均不能形成氢键,故A
正确;
B.乙醇能与水形成氢键,所以和水以任意比互溶,故B错误;
C.邻羟基苯甲醛形成分子内氢键,对羟基苯甲醛形成分子间氢键,所以邻羟基苯甲醛的
沸点低于对羟基苯甲醛,故C错误;
D.水蒸气分子之间除了存在分之间作用力外还存在氢键,使水蒸气分之间间隙变小,导
致其相对分子质量测量值大于18,故D错误;
故答案为:A。
二、氮氧化物的处理(21分)
NO 是空气的污染物,废水中的氨氮(以NH、NH 存在)和硝态氮(以NO 、NO 存
x 3 + - -
❑ ❑ ❑
4 2 3
在)会引起水体富营养化,需经处理后才能排放。1.电解氧化吸收法可将废气中的 NO 转变为NO 。
x -
❑
3
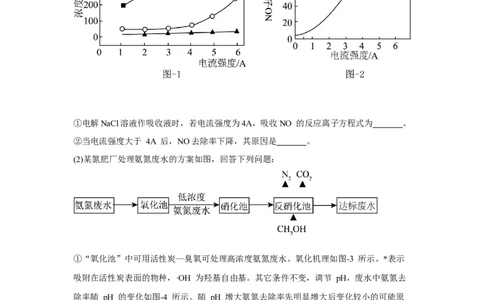
(1)电解 0.1 mol·L-1NaCl 溶液时,溶液中相关成分的浓度变化与电流强度的关系如图-1
所示。向 0.1 mol·L-1NaCl 溶液中通入 NO,测得电流强度与 NO 的脱除率的关系如图-2
所示。
①电解NaCl溶液作吸收液时,若电流强度为4A,吸收NO 的反应离子方程式为 。
②当电流强度大于 4A 后,NO去除率下降,其原因是 。
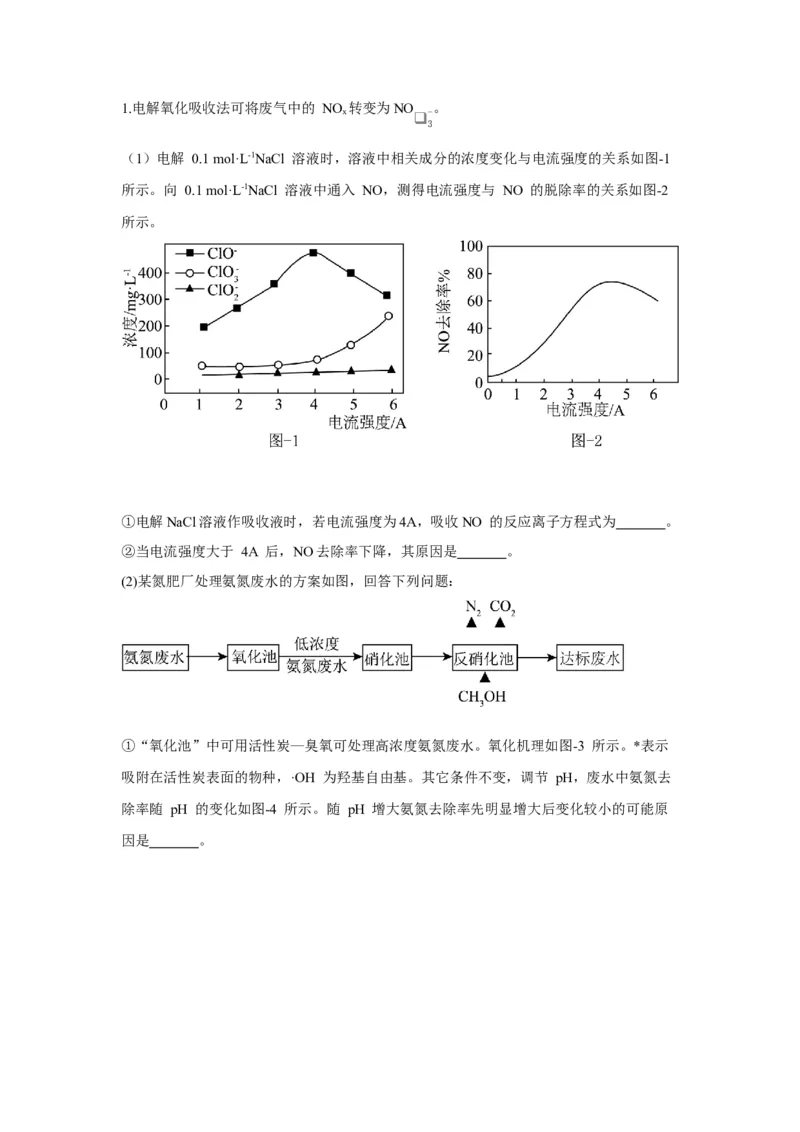
(2)某氮肥厂处理氨氮废水的方案如图,回答下列问题:
①“氧化池”中可用活性炭—臭氧可处理高浓度氨氮废水。氧化机理如图-3 所示。*表示
吸附在活性炭表面的物种,·OH 为羟基自由基。其它条件不变,调节 pH,废水中氨氮去
除率随 pH 的变化如图-4 所示。随 pH 增大氨氮去除率先明显增大后变化较小的可能原
因是 。②“反硝化池”中发生的变化为:HNO→ →N。1 mol HNO 完全转化理论上消耗甲醇
3 NO− 2 3
2
的质量为 。
(3)纳米Fe 可还原去除水中的硝酸盐污染物。
已知:i.纳米 Fe 具有很高的活性,易被氧化使表面形成氧化层
ii.纳米 Fe 将 还原为 的转化关系如下:
NO− NH+
3 4
NO− Fe NO− Fe NH+
3 → 2 → 4
①纳米 Fe 的制备原理:FeSO +2NaBH +6HO=2B(OH) +Fe+7H↑+NaSO ; 已知电负
4 4 2 3 2 2 4
性 H>B,则该反应中氧化剂是 (填化学式) 。
②检验还原后的溶液中存在
NH+
的实验方法是 。
4
③溶液初始 pH 较低有利于 的去除,其可能的原因是 。
NO−
3
【答案】(1) 随着电流强度的增大,导致
3ClO−+2NO+2OH−=3Cl−+2NO+H O
2
次氯酸根转化(歧化)为氯酸根离子、氯酸根离子氧化性比次氯酸根离子弱
(2) 随pH增大,活性炭上吸附的OH−增多,生成⋅OH增多;pH继续增大时,OH−将
160
NH+转化为NH ,不利于活性炭对氨氮的吸附 g
4 3 6
(3) FeSO 、H O 取少量样品与试管中,加入氢氧化钠浓溶液并加热,在试管口
4 2
用湿润的红色石蕊试纸检验放出气体,试纸由红变蓝,证明有 NH+ pH 越低,酸性越
4强,则 氧化性越强
NO−
3
【解析】(1)①根据题意,ClO-氧化吸收NO生成硝酸根,本身还原为氯离子,且溶液为
碱性,离子方程式: ;
3ClO−+2NO+2OH−=3Cl−+2NO+H O
2
②当电流强度大于 4A 后,NO去除率下降,其原因:根据图可知电流强度增大到4A之后,
次氯酸根的浓度会下降,而氧化性较弱的氯酸根离子浓度增大,从而导致NO去除率下降,
而只有温度较高时才会有氯酸根生成,所以答案为:随着电流强度的增大,导致次氯酸根
转化(歧化)为氯酸根离子、氯酸根离子氧化性比次氯酸根离子弱;
(2)①随pH增大,活性炭上吸附的 增多,生成 增多;pH继续增大时, 将
OH− ⋅OH OH− NH+
4
转化为NH ,不利于活性炭对氨氮的吸附;
3
②1 mol HNO 完全转化为N,氮元素从+5价降为0价,则转移电子的物质的量为5mol;
3 2
甲醇分子中H化合价为+1价,O为-2价,则C为-2价,甲醇在反应中作还原剂,被氧化为
二氧化碳,元素化合价从-2升高到+4价,结合得失电子守恒,需要消耗甲醇物质的量:
1mol×5 5 5 160
= mol,消耗甲醇质量: mol×32g/mol= g;
6 6 6 6
(3)①NaBH 中H为-1价,升高到0价,Fe2+由+2价将为0价,水中部分H元素由+1价
4
降低到0价,则该反应中FeSO 和H O都是氧化剂;
4 2
②检验还原后的溶液中存在 的实验方法:取少量样品与试管中,加入氢氧化钠浓溶液
NH+
4
并加热,在试管口用湿润的红色石蕊试纸检验放出气体,试纸由红变蓝,证明有 ;
NH+
4
③溶液初始 pH 较低有利于 的去除,其可能的原因:pH 越低,酸性越强,则 氧
NO− NO−
3 3
化性越强;
三、 氢能(19分)
氢能,氢和氧进行化学反应释放出的化学能,是一种二次清洁能源,被誉为“21世纪
终极能源”,也是在碳达峰、碳中和的大背景下,加速开发利用的一种清洁能源。
3.绿色能源是未来能源发展的方向。可以用以下方法制备氢气。I.甲烷和水蒸气催化制氢气。主要反应如下:
i.CH(g)+HO(g)❑CO(g)+3H(g) △H=+206.2kJ•mol-1
4 2 2
⇌
ii.CO(g)+HO(g)❑CO(g)+H(g) △H=-41.2kJ•mol-1
2 2 2
⇌
(1)反应CH(g)+CO (g)❑2CO(g)+2H(g)的△H= kJ•mol-1。
4 2 2
⇌
(2)在容积不变的绝热密闭容器中发生反应i,下列能说明反应达到平衡状态的是 (填
标号)。
A.气体混合物的密度不再变化
B.CH 消耗速率和H 的生成速率相等
4 2
C.CO的浓度保持不变
D.气体平均相对分子质量不再变化
E.体系的温度不再发生变化
(3)恒定压强为PMPa时,将n(CH):n(H O)=1:3的混合气体投入反应器中发生反应i和
0 4 2
ii,平衡时,各组分的物质的量分数与温度的关系如图所示。
①图中表示CO 的物质的量分数与温度的变化曲线是 (填字母)。
2
②结合图中数据,其他条件不变,若要H 的产量最大,最适宜的反应温度是 (填标
2
号)。
A.550~600℃ B.650~700℃ C.750~800℃
在其他条件不变的情况下,向体系中加入CaO可明显提高平衡体系中H 的含量,原因是
2
。
③600℃时,反应ii的平衡常数的计算式为K= (K 是以分压表示的平衡常数,分压=
p p
总压×物质的量分数)。Ⅱ.电解法制氢气。某科研小组设计如图所示电解池,利用CO 和HO在碱性电解液中制
2 2
备水煤气(H 、CO),产物中H 和CO的物质的量之比为1∶1。
2 2
(4)电极B是 极,生成水煤气的电极反应式为 。
【答案】(1)+247.4
(2)CDE
(3) n B CaO为碱性氧化物,能吸收酸性氧化物CO,导致CO 浓度减小,
2 2
25
促使反应ii平衡正向移动,导致CO浓度减小,引起反应i平衡也正向移动
12
(4) 阳 CO+2H O+2e-=H +CO+2OH-
2 2 2
【解析】(1)由题干信息已知,反应i.CH
4
(g)+H
2
O(g)⇌CO(g)+3H
2
(g) Δ
H=+206.2kJ•mol-1,反应ii.CO(g)+H
2
O(g)⇌CO
2
(g)+H
2
(g) ΔH=-41.2kJ•mol-1,反应i-反应ii
可得反应CH
4
(g)+CO
2
(g) ⇌2CO(g)+2H
2
(g),根据盖斯定律可知,ΔH=(+206.2kJ/mol)-
(-41.2kJ/mol)=+247.4kJ•mol-1,故答案为:+247.4;
(2)A.由题干信息可知,反应i反应体系均为气体,则反应过程中气体质量不变,容器
体积不变,则气体混合物的密度始终不变,则气体混合物的密度不再变化,不能说明反应
达到化学平衡,A不合题意;
B.CH 消耗速率和H 的生成速率均表示正反应速率,且二者系数不相等,故CH 消耗速
4 2 4
率和H 的生成速率相等,不能说明反应达到化学平衡,B不合题意;
2
C.化学平衡的特征之一为各组分的浓度保持不变,故CO的浓度保持不变,说明反应达到
化学平衡,C符合题意;
D.由题干信息可知,反应i前后气体的物质的量发生改变,气体质量不变,则气体平均相
对分子质量一直在改变,故气体平均相对分子质量不再变化,说明反应达到化学平衡,D
符合题意;E.由于反应容器是一个绝热密闭容器,故体系的温度不再发生变化,说明反应达到化学
平衡,E符合题意;
故答案为:CDE;
(3)①随反应进行,二氧化碳和氢气的量增加,故甲烷和水蒸气的量减小,将n(CH):
4
n(H O)=1:3的混合气体投入反应器中,故p为表示平衡时水蒸气的物质的量分数随温度
2
的变化,随着温度升高反应i正向移动,反应ii逆向移动,故CO随温度升高而增大,即m
表示平衡时CO的物质的量分数随温度的变化,则n表示CO 的物质的量分数随温度的变
2
化,故答案为:n;
②结合图中数据,其他条件不变,当温度达到650℃时,CH 的转化率几乎为100%,H 的
4 2
物质的量分数达到最大,再升高温度,H 的物质的量分数不再增大,CH 的转化率也增大
2 4
不大,且增大能源投入,故若要H 的产量最大,最适宜的反应温度是650~700℃,CaO为
2
碱性氧化物,能吸收酸性氧化物CO,导致CO 浓度减小,促使反应ii平衡正向移动,导
2 2
致CO浓度减小,引起反应i平衡也正向移动,故在其他条件不变的情况下,向体系中加入
CaO可明显提高平衡体系中H 的含量,原因是故答案为:B;CaO为碱性氧化物,能吸收
2
酸性氧化物CO,导致CO 浓度减小,促使反应ii平衡正向移动,导致CO浓度减小,引
2 2
起反应i平衡也正向移动;
③由题干图像信息可知,600℃平衡时,H 的物质的量分数为:50%,HO(g)的物质的量分
2 2
数为32%,CH 的物质的量分数为4%,设投入CH 为1mol、HO为3mol,根据三段式分
4 4 2
析:
CO+3H
2
CH 4 +H 2 O ⇌ ¿转化量(mol)¿x¿x¿¿平衡量(mol)¿1-x¿3-x¿¿ 0 0
起始量(mol) 1 ¿ x 3x
x 3x
CO +H
2 2
CO +H 2 O ⇌ ¿转化量(mol)¿y¿y¿¿平衡量(mol)¿x-y¿3-x-y¿¿ 0 3x
起始量(mol) x ¿ y y
y 3x+y
1-x 3x+y
则有 =0.04,解得x=0.78mol, =0.5,解得y=0.45mol,CO物质的量分数为:
4+2x 4+2x0.78-0.45 0.45
×100%=6%,CO 的物质的量分数为 ×100%=8%,600℃时,反应ii
2
4+2×0.78 4+2×0.78
的平衡常数的计算式为K= p(CO )p(H ) = 0.08P MPa×0.50P MPa =25,故答案为:
p 2 2 0 0
p(CO)p(H O) 0.06P MPa×0.32P MPa 12
2 0 0
25
;
12
(4)由题干电解池装置图可知,电解B产生氧气,电解反应为:4OH- -4e-=O ↑+2H O,发
2 2
生氧化反应,故电极B是阳极,则A电极为阴极,发生还原反应,生成水煤气即CO和
H,该电极的电极反应式为CO+2H O+2e-=H +CO+2OH-,故答案为:阳;CO+2H O+2e-
2 2 2 2 2 2
=H +CO+2OH-。
2
四、氨氮废水的处理(19分)
研究人员合成了一种普鲁士蓝(PB)改性的生物炭(BC)复合材料(BC-PB),并将其应用于
氨氮废水(含 、 )的处理。
NH NH+
3 4
4. 资料:
①普鲁士蓝(PB)是亚铁氰化铁的俗称,化学式为 ,难溶于水。
Fe [Fe(CN) ]
4 6 3
②BC-PB中,PB负载在BC表面,没有产生新化学键,各自化学性质保持不变。
Ⅰ.复合材料BC-PB的合成
(1)下列关于ⅰ中HCN参与反应的说法正确的是 (填字母)。
a.提供H+,与Fe反应
b.提供H+,与OH−反应
c.提供CN−,与Fe2+配位
d.提供CN−,与K+反应
(2)ⅱ中分离得到 的操作包括加热浓缩、 。
K [Fe(CN) ]⋅3H O
4 6 2
(3)ⅲ中生成普鲁士蓝反应的离子方程式为 。
(4)添加造孔剂可以增加BC的孔道数目和容量。造孔剂的造孔原理之一是在一定条件下分解产生气体。700℃时,KHCO 造孔原理的化学方程式为 。
3
Ⅱ.氨氮废水处理
用NH Cl溶液模拟氨氮废水。实验发现pH=2时,在BC-PB体系中加入H O ,可将氨氮转
4 2 2
化为无毒气体N ,提高氮氮的去除率。其原理为:
2
ⅰ. Fe [Fe(CN) ] +3H O +3H+=3Fe[Fe(CN) ]+Fe3++3⋅OH+3H O
4 6 3 2 2 6 2
ⅱ.·OH将氨氮氧化为N
2
(5)ⅱ的离子方程式为 。
(6)用BC-PB和H O混合处理1000L某氨氦含量(以NH Cl质量计算)为120mg⋅L−1的废水。
2 4
实验结束后,收集到22.4L N (已折算成标准状况)。
2
①实验中消耗的H O 的质量至少为 g。
2 2
②处理后的废水中氨氮含量为 mg⋅L−1(废水体积变化忽略不计),达到了污水
排放标准要求(≤15mg⋅L−1)。
【答案】(1)ac
(2)冷却结晶、过滤、洗涤、干燥
(3)3[Fe(CN) ]4-+4Fe3+=
6 Fe [Fe(CN) ] ↓
4 6 3
Δ
(4)2KHCO ==K CO +H O+CO ↑
3 2 3 2 2
❑
(5)6·OH+ =N ↑+6H O+2H+
2NH+ 2 2
4
(6) 204 13
【分析】反应ⅰ中铁粉转化为亚铁离子,KOH溶液和HCN气体、铁粉反应生成
K[Fe(CN) ],K[Fe(CN) ]溶液蒸发浓缩、冷却结晶得到K[Fe(CN) ] •3H O,K[Fe(CN) ]
4 6 4 6 4 6 2 4 6
•3H O和氯化铁溶液、生物炭反应生成 。
2 Fe [Fe(CN) ]
4 6 3
【解析】(1)ⅰ中铁粉和HCN反应转化为亚铁离子,同时HCN提供CN−,形成配位键,
故HCN作用为提供H+,与Fe反应;提供CN−,与Fe2+配位,故选ac。
(2)ⅱ中从溶液分离得到 的操作包括加热浓缩、冷却结晶、过滤、洗
K [Fe(CN) ]⋅3H O
4 6 2
涤、干燥。(3)ⅲ中生成普鲁士蓝反应的离子方程式为3[Fe(CN) ]4-+4Fe3+= 。。
6 Fe [Fe(CN) ]
4 6 3
Δ
(4)700℃时,KHCO 造孔原理的化学方程式为2KHCO ==K CO +H O+CO ↑ 。
3 3 2 3 2 2
❑
(5)ⅱ的离子方程式为6·OH+ =N ↑+6H O+2H+。
2NH+ 2 2
4
(6)由反应ⅰ、ⅱ可得总反应为:
。
2Fe [Fe(CN) ] +6H O +4H++2NH+=6Fe[Fe(CN) ]+2Fe3++N ↑+12H O
4 6 3 2 2 4 6 2 2
①标准状况下22.4LN 物质的量为1mol,则实验中消耗的H O 的质量至少为6mol×34g/
2 2 2
mol=204g。
120mg⋅L−1×1000L
②该废水氨氮总质量为 =120g,反应消耗铵根离子为2mol,处理后
1000mg/g
120g-53.5g/mol×2mol
的废水中氨氮含量为 =13mg/L,达到了污水排放标准要求(
1000L
≤15mg⋅L−1)。
五、乙烯合成二酮(22分)
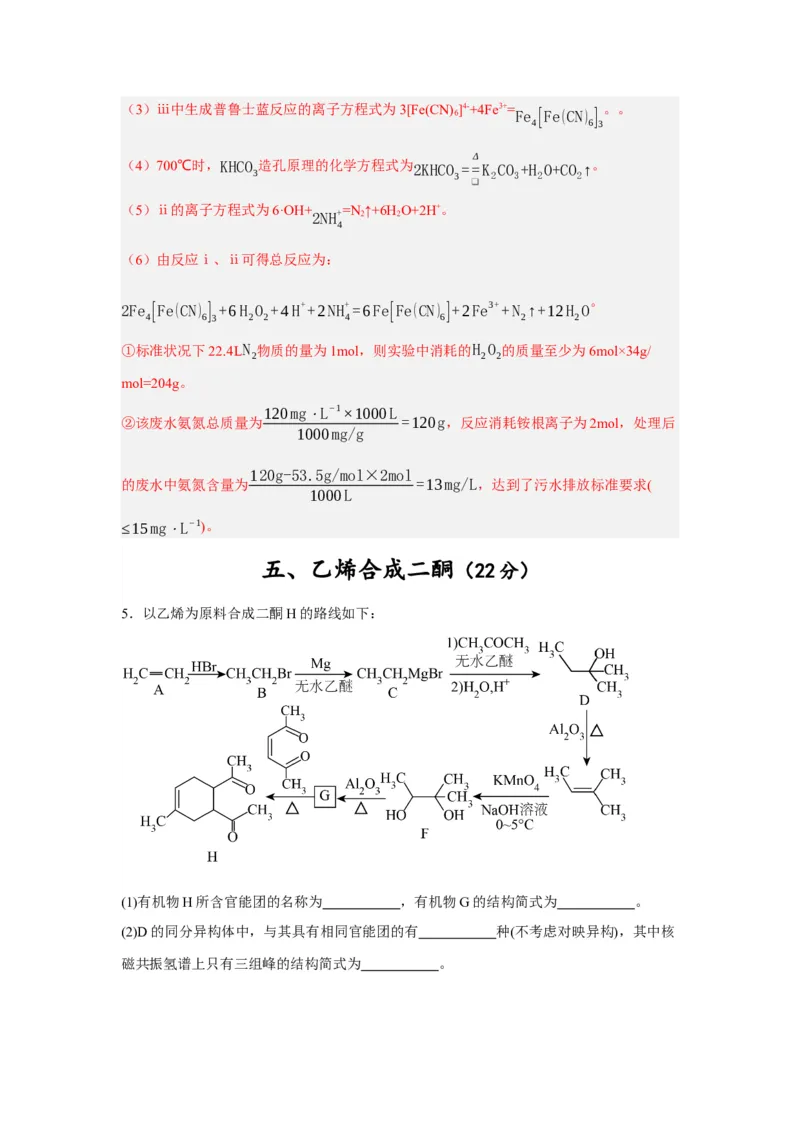
5.以乙烯为原料合成二酮H的路线如下:
(1)有机物H所含官能团的名称为 ,有机物G的结构简式为 。
(2)D的同分异构体中,与其具有相同官能团的有 种(不考虑对映异构),其中核
磁共振氢谱上只有三组峰的结构简式为 。(3)有机物H的某种同分异构体W为 , 分析预测其可能的化学性质,参考
Ⅰ的示例,
完成下表。
序
结构特征 反应试剂、条件 反应形成的新结构 反应类型
号
Ⅰ -CH= CH- H,催化剂,加热 -CH-CH- 加成反应
2 2 2
Ⅱ ① 银氨溶液, 加热 ② 氧化反应
Ⅲ -OH ③ -CH=CH- ④
(4)下列说法正确的是___________(填写序号)。
A.有机物A中碳原子采取sp3杂化
B.有机物E存在顺反异构体
C.有机物F分子中含有1个手性碳原子
D.有机物G→H的反应过程中,有π键的断裂和形成
(5)以环戊烷和 CHCHMgBr为含碳原料合成 ,基于你设计的合成路线,回
3 2
答下列问题:
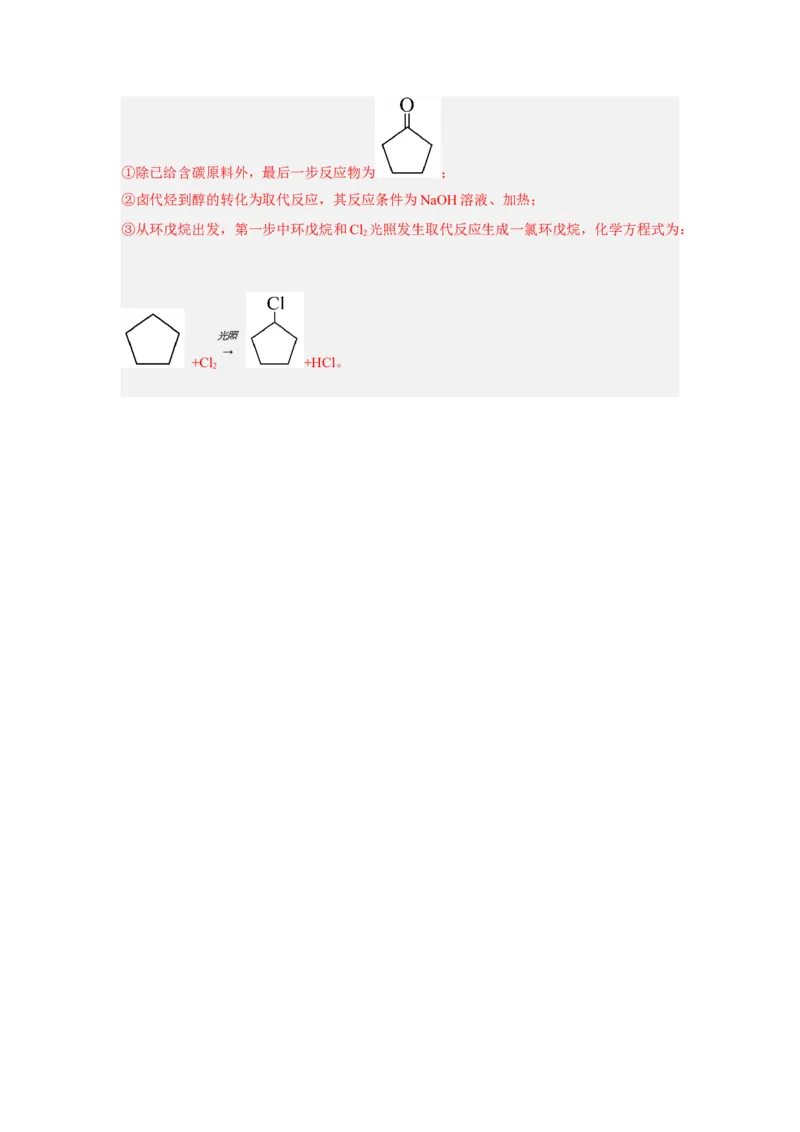
①除已给含碳原料外,最后一步反应物为 (写结构简式)。
②相关步骤涉及到卤代烃到醇的转化,其反应条件为 。
③从环戊烷出发,第一步的化学方程式为 (注明反应条件)。
【答案】(1) 碳碳双键、酮(羰)基
(2) 7
(3) -CHO -COONH 浓硫酸、加热 消去反应
4
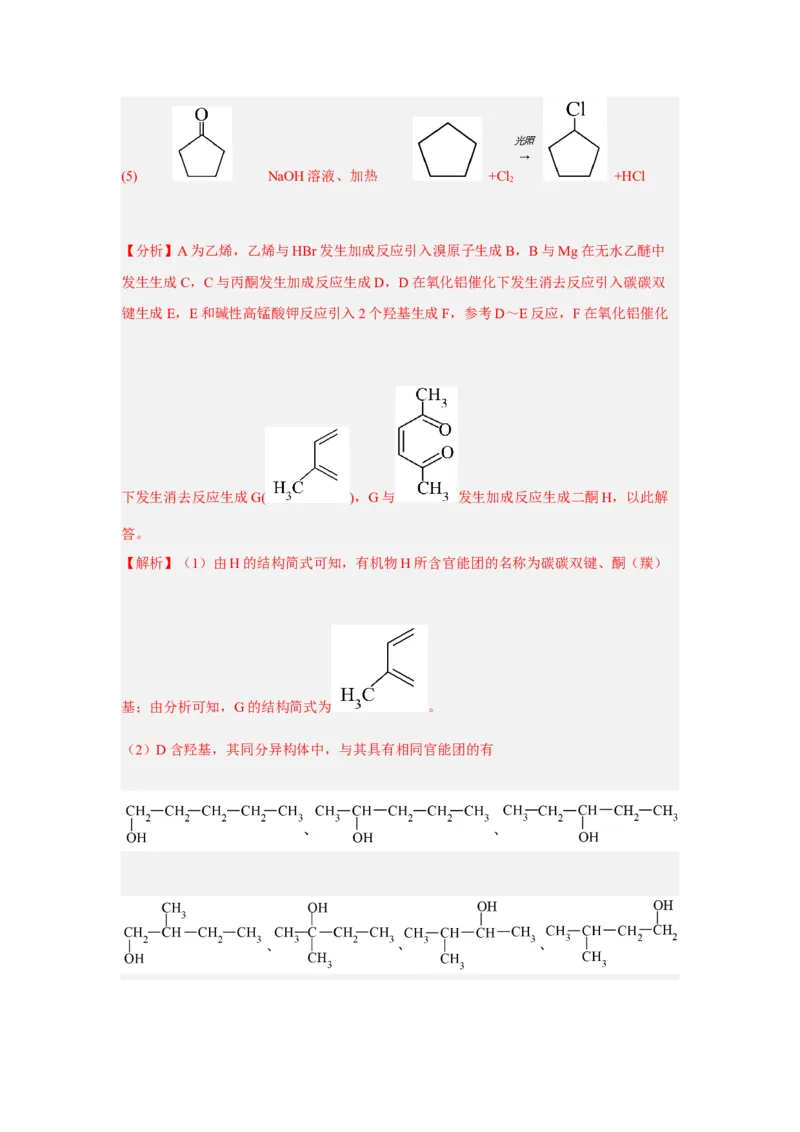
(4)CD光照
→
(5) NaOH溶液、加热 +Cl +HCl
2
【分析】A为乙烯,乙烯与HBr发生加成反应引入溴原子生成B,B与Mg在无水乙醚中
发生生成C,C与丙酮发生加成反应生成D,D在氧化铝催化下发生消去反应引入碳碳双
键生成E,E和碱性高锰酸钾反应引入2个羟基生成F,参考D~E反应,F在氧化铝催化
下发生消去反应生成G( ),G与 发生加成反应生成二酮H,以此解
答。
【解析】(1)由H的结构简式可知,有机物H所含官能团的名称为碳碳双键、酮(羰)
基;由分析可知,G的结构简式为 。
(2)D含羟基,其同分异构体中,与其具有相同官能团的有,共8种(不考虑立体异构),除去其本身,还有7种;其中核
磁共振氢谱有三组峰,峰面积之比为9∶2∶1的为 。
(3)W中含有-CHO,可以和银氨溶液发生氧化反应生成-COONH ,W中含有-OH,可以
4
在浓硫酸、加热的条件下发生消去反应,-OH转化为-CH=CH-。
(4)A.有机物A中含碳碳双键,碳原子采取sp2杂化,故A错误;
B.有机物E中,碳碳双键上连接3个甲基,不存在顺反异构,故B错误;
C.有机物F分子中,连接-OH的碳原子为手性碳原子,故C正确;
D.F→G为消去反应,G的结构为 ,有机物G→H的反应过程
中,有π键的断裂和形成,故D正确;
故选CD。
(5)环戊烷和Cl 光照发生取代反应生成一氯环戊烷,一氯环戊烷在NaOH溶液,加热条
2
件下发生取代反应生成醇,醇催化氧化生成 , 与CHCHMgBr反应合成
3 2
;①除已给含碳原料外,最后一步反应物为 ;
②卤代烃到醇的转化为取代反应,其反应条件为NaOH溶液、加热;
③从环戊烷出发,第一步中环戊烷和Cl 光照发生取代反应生成一氯环戊烷,化学方程式为:
2
光照
→
+Cl +HCl。
2