文档内容
【赢在高考·黄金8卷】
2024年普通高中学业水平等级性考试模拟(北京专用)
黄金卷07
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.作答时,务必将答案写在答题卡上。写在本试卷及草稿纸上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量: H 1 C 12 N 14 O 16 S 32 Fe 56 Ce 140
第一部分
本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
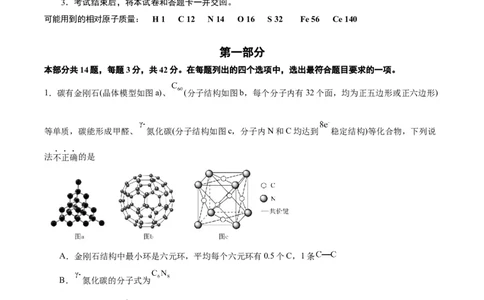
1.碳有金刚石(晶体模型如图a)、 (分子结构如图b,每个分子内有32个面,均为正五边形或正六边形)
等单质,碳能形成甲醛、 氮化碳(分子结构如图c,分子内N和C均达到 稳定结构)等化合物,下列说
法不正确的是
A.金刚石结构中最小环是六元环,平均每个六元环有0.5个C,1条
B. 氮化碳的分子式为
C.甲醛中C为 杂化
D. 分子中有16个五元环和16个六元环
2.下列化学用语或图示表达正确的是
A. 的电子式为 B. 的VSEPR模型:C. 电子云轮廓图为: D.基态 的简化电子排布式:
3.下列“类推”合理的是
A.Na与HO反应生成NaOH和H,则Fe与HO反应生成Fe(OH) 和H
2 2 2 3 2
B.SO 可与水反应生成HSO ,则SiO 可与水反应生成HSiO
2 2 3 2 2 3
C.铁与硫加热反应生成FeS,则铜与硫加热反应生成Cu S
2
D.Cl 与HO反应生成HCl和HClO,则F 与HO反应生成HF和HFO
2 2 2 2
4.采取下列措施对增大化学反应速率有明显效果的是
A.铁与稀硫酸反应,滴入几滴硫酸铜溶液
B. 与无水乙醇反应时增大无水乙醇的用量
C. 与 两溶液反应时,增大压强
D. 与稀盐酸反应,加入少量醋酸钠粉末
5.化学在环境保护中起着十分重要的作用,电化学降解法可用于治理水中硝酸盐的污染其原理如图所示,
下列说法不正确的是
A.Pt电极为电解池的阴极
B.电解时,质子从Pt电极转移到Ag-Pt电极
C.电解池的总反应方程式为2HO+4NO N↑+5O ↑+4OH-
2 2 2
D.当交换膜右室电解液的质量减少 时,电子转移数目为4N
A
6.不能正确表示下列变化的离子方程式是
A. 溶于盐酸:
B. 浴液腐蚀铜板:C.Fe和稀盐酸反应:
D. 气体通入溴水中:
7.下列关于实验操作的说法正确的是
A.取用药品时,剩余药品均不得放回原试剂瓶
B.中和热测定时,只需记录溶液的初始温度和最高温度
C.稀硫酸、 溶液等沾到皮肤上应立即用大量清水冲洗
D.酸碱中和滴定时,不能加入蒸馏水,以免溶液稀释产生误差
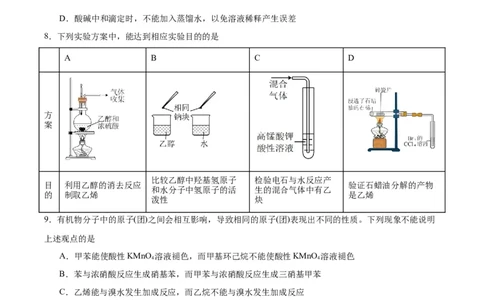
8.下列实验方案中,能达到相应实验目的的是
A B C D
方
案
比较乙醇中羟基氢原子 检验电石与水反应产
目 利用乙醇的消去反应 验证石蜡油分解的产物
和水分子中氢原子的活 生的混合气体中有乙
的 制取乙烯 是乙烯
泼性 炔
9.有机物分子中的原子(团)之间会相互影响,导致相同的原子(团)表现出不同的性质。下列现象不能说明
上述观点的是
A.甲苯能使酸性KMnO 溶液褪色,而甲基环己烷不能使酸性KMnO 溶液褪色
4 4
B.苯与浓硝酸反应生成硝基苯,而甲苯与浓硝酸反应生成三硝基甲苯
C.乙烯能与溴水发生加成反应,而乙烷不能与溴水发生加成反应
D.苯酚具有酸性,而环己醇( )没有酸性
10.硫代碳酸钠能用于处理废水中的重金属离子,可通过如下反应制备:
下列说法错误的是
A. 具有还原性 B. 是直线形非极性分子C.该反应中 是氧化产物 D.电负性:
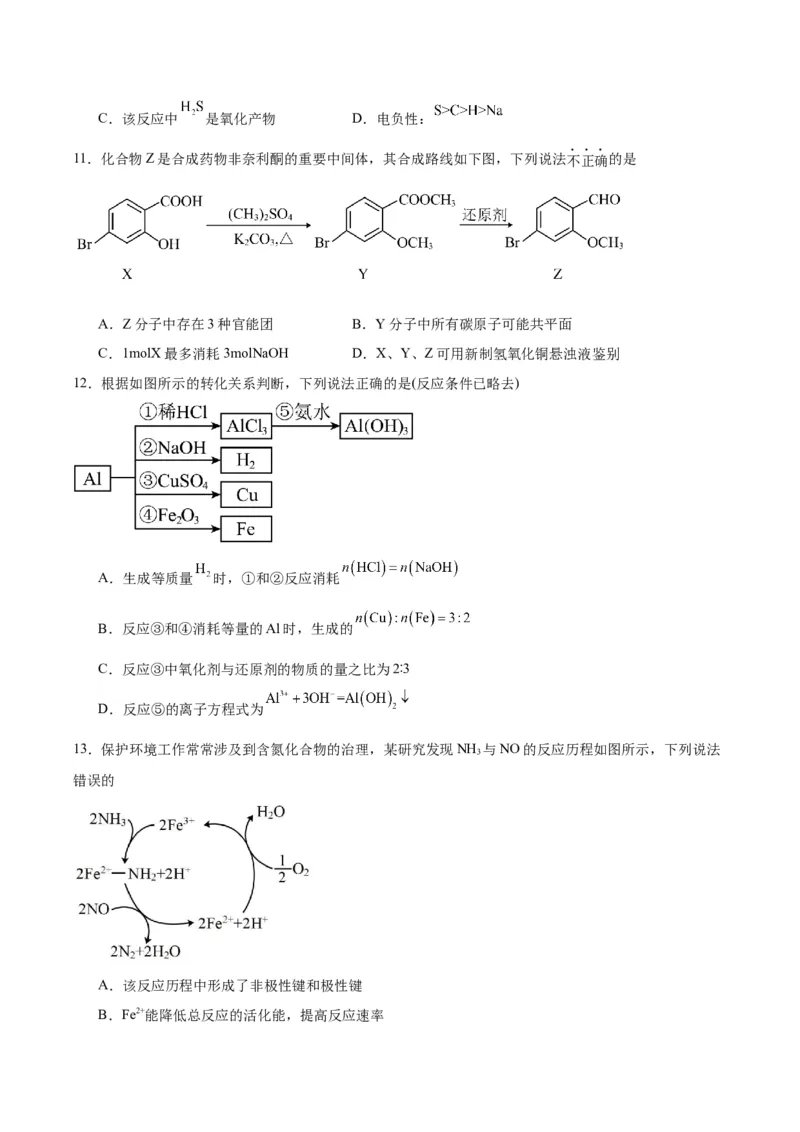
11.化合物Z是合成药物非奈利酮的重要中间体,其合成路线如下图,下列说法不正确的是
A.Z分子中存在3种官能团 B.Y分子中所有碳原子可能共平面
C.1molX最多消耗3molNaOH D.X、Y、Z可用新制氢氧化铜悬浊液鉴别
12.根据如图所示的转化关系判断,下列说法正确的是(反应条件已略去)
A.生成等质量 时,①和②反应消耗
B.反应③和④消耗等量的Al时,生成的
C.反应③中氧化剂与还原剂的物质的量之比为2∶3
D.反应⑤的离子方程式为
13.保护环境工作常常涉及到含氮化合物的治理,某研究发现NH 与NO的反应历程如图所示,下列说法
3
错误的
A.该反应历程中形成了非极性键和极性键
B.Fe2+能降低总反应的活化能,提高反应速率C.每生成2molN ,转移的电子总数为6N
2 A
D.该反应历程中存在:NO+Fe2+-NH =Fe2++N ↑+H O
2 2 2
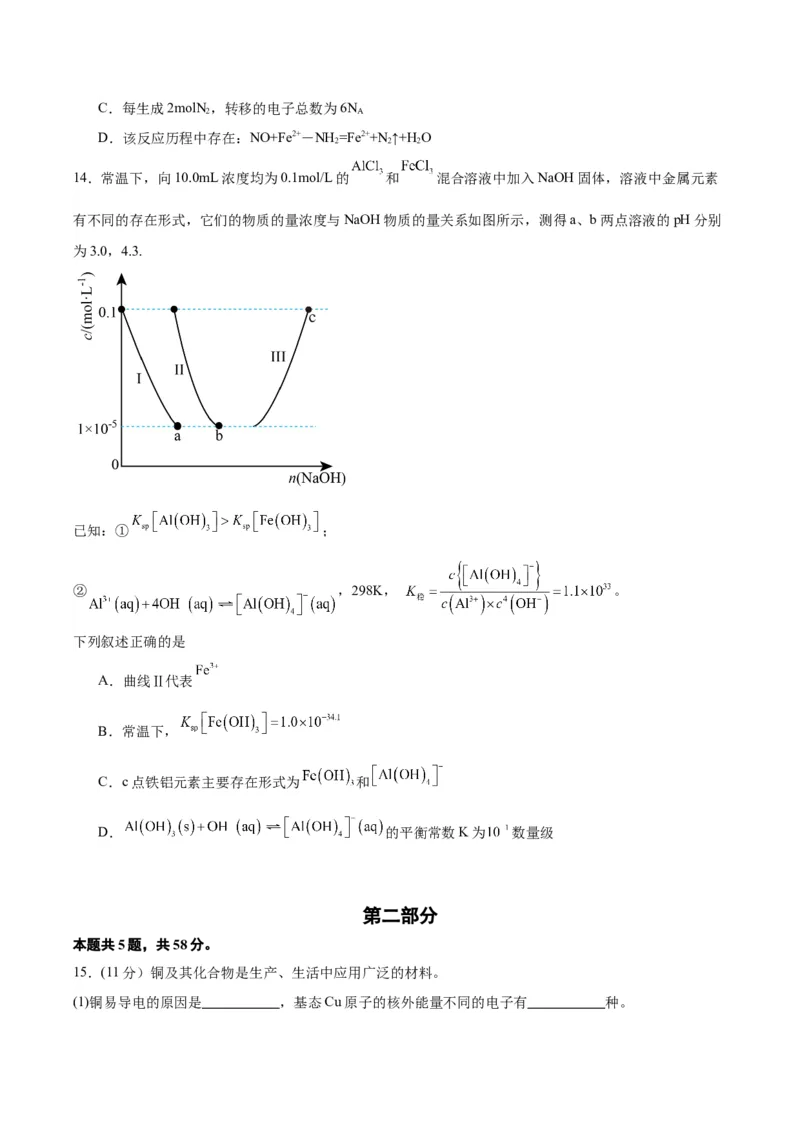
14.常温下,向10.0mL浓度均为0.1mol/L的 和 混合溶液中加入NaOH固体,溶液中金属元素
有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b两点溶液的pH分别
为3.0,4.3.
已知:① ;
② ,298K, 。
下列叙述正确的是
A.曲线Ⅱ代表
B.常温下,
C.c点铁铝元素主要存在形式为 和
D. 的平衡常数K为 数量级
第二部分
本题共5题,共58分。
15.(11分)铜及其化合物是生产、生活中应用广泛的材料。
(1)铜易导电的原因是 ,基态Cu原子的核外能量不同的电子有 种。(2)铜的第二电离能 (填“>”、“<”或“=”)锌的第二电离能,其主要原因是 。
(3)合成氨工业常用醋酸二氨合铜 溶液吸收对合成氨反应的催化剂有毒害的气体CO。
①写出一个与CO互为等电子体的离子: 。
②醋酸二氨合铜水解生成的醋酸(HA)的结构式为 ,则HAc分子中π键和σ键的数目之比
为 ,HAc中碳原子的杂化类型为 ,分子中键角α (填“>”“<”或“=”)
键角β。
(4)晶胞有两个基本要素。
①原子坐标参数:表示晶胞内部各微粒的相对位置。下图是CuI的晶胞结构图,其坐标参数如下:A(0,
0,0),B(1,0,0),C(1,1,1)。则D处微粒的坐标参数为 。
②晶胞参数:描述晶胞的大小和形状。若 最短距离为anm,则晶胞的边长为 nm,该化
合物的密度为 (设 为阿伏加德罗常数的值,用含a、 的代数式表示)。
16.(11分)一种用于治疗高血脂的新药I的合成路线如图:
已知:①RCHO+CH3CHO RCH=CHCHO;②
回答下列问题:
(1)B的化学名称为 ;H的分子式为 。
(2)E的结构简式为 ;G中所含官能团的名称是 。
(3)②的反应类型是 ;写出反应①的化学方程式 。
(4)化合物W的相对分子质量比化合物C大14,且满足下列条件的W的结构有 种,其中核磁
共振氢谱显示有5种不同化学环境的氢,峰面积之比为2:2:2:1:1的W的结构简式为 。
①遇 溶液显紫色②属于芳香族化合物③能发生银镜反应
(5)设计用乙醇为原料制备 的合成路线,其他无机试剂任选。
17.(12分)工业上利用软锰矿(主要成分为 ,含 等元素)与纤维素制备
,工艺如下图所示。
(1)基态 原子的价电子排布式 ;为利用纤维素“酸浸”相较于 酸浸法,除了原料来源丰富、
耗能低,还具有的优点为 。
(2)“酸浸”时,由纤维素水解得到的葡萄糖与软锰矿反应,该反应的离子方程式为 。
(3)“中和”时,相关离子形成氢氧化物沉淀的 范围如下:
金属离子
开始沉淀的 1.5 3.0 8.9 6.0 8.1
完全沉淀的 2.8 4.7 10.9 8.0 10.1
“中和”步骤要调节溶液 ,最适宜的 范围是 。(4)“净化”时,加入 是为了将 转化为 和 沉淀除去,还能除去 (填元
素符号)。
(5)“沉锰”时,主要生成 和 沉淀,其中生成 的离子方程式为 。
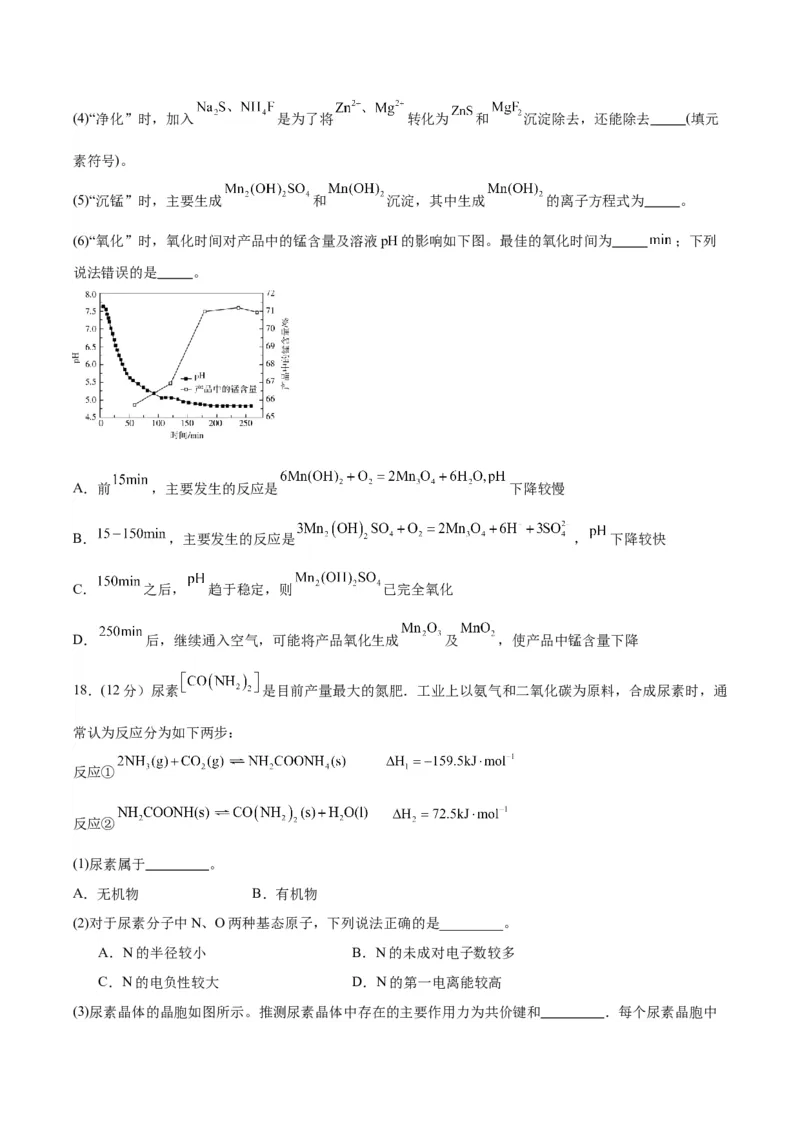
(6)“氧化”时,氧化时间对产品中的锰含量及溶液pH的影响如下图。最佳的氧化时间为 ;下列
说法错误的是 。
A.前 ,主要发生的反应是 下降较慢
B. ,主要发生的反应是 , 下降较快
C. 之后, 趋于稳定,则 已完全氧化
D. 后,继续通入空气,可能将产品氧化生成 及 ,使产品中锰含量下降
18.(12分)尿素 是目前产量最大的氮肥.工业上以氨气和二氧化碳为原料,合成尿素时,通
常认为反应分为如下两步:
反应①
反应②
(1)尿素属于 。
A.无机物 B.有机物
(2)对于尿素分子中N、O两种基态原子,下列说法正确的是_________。
A.N的半径较小 B.N的未成对电子数较多
C.N的电负性较大 D.N的第一电离能较高
(3)尿素晶体的晶胞如图所示。推测尿素晶体中存在的主要作用力为共价键和 .每个尿素晶胞中含有 个尿素分子。
(4)写出反应①的化学平衡常数表达式, 。
(5)反应①能自发进行,条件是 。
A.较高温度 B.较低温度 C. 较高温度或较低温度
(6)已知反应①的反应速率远大于反应②。如图能表示上述两步反应能量变化的是_________。
A. B. C. D.
(7)恒温恒容时,将 和 充入 反应器中合成尿素,经 测得反应器内气体压强变为
起始的80%(已知此时尿素为固态,水为液态),则从反应开始至 时, 的平均反应速率
。
(8)与铵态氮肥相比,写出施用尿素的两个优点 、 。
19.(12分)某实验小组欲探究 和 的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。
于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A受热分解的化学方程式为
。
(2)称取两种固体各2g,分别加入两个小烧杯中,再各加10mL蒸馏水,振荡,测量温度变化;待固体充分
溶解,恢复至室温,向所得溶液中各滴入2滴酚酞溶液。
①发现 固体完全溶解,而 固体有剩余,由此得出结论: 。
②同学们在两烧杯中还观察到以下现象。其中,盛放 的烧杯中出现的现象是 (填字母
序号)
a.溶液温度升高 b.溶液温度下降c.滴入酚酞后呈浅红色 d.滴入酚酞后呈红色
(3)如图所示,在气密性良好的装置I和II中分别放入药品,将气球内的固体同时倒入试管中。
①两试管中均产生气体, 的反应程度更为剧烈。(填“I”或“II”)
②反应结束后,恢复至室温,下列说法正确的是 。
a.装置I的气球体积较大 b.装置II的气球体积较大
c.生成气体的体积根据盐酸计算 d.生成气体的体积根据固体计算
(4)同学们将两种固体分别配制成 的溶液,设计如下方案并对反应现象做出预测:
预测现
实验方案 预测依据
象
操作1:向 溶液中滴加
无白色
溶液中的 浓度很小,不能与 反应
溶液 沉淀
操作2:向 溶液中滴加 有白色 溶液中的 浓度较大,能与 发生反
溶液 沉淀 应 (写出该反应的离子方程式)
实施实验后,发现操作1的现象与预测有差异:产生白色沉淀和二氧化碳气体。则该条件下, 溶
液与 溶液反应的离子方程式为 。