文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(广东专用)
黄金卷08
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Mn 55 Co 59
第Ⅰ卷
一、选择题:本题共16个小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在
每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列广东传统民俗文化艺术品中,涉及的主要物质不属于有机高分子的是
A.高州牛角雕刻 B.广州木刻版画 C.云浮玉雕 D.茂名剪纸
2.化学科学在“国之重器”的打造中发挥着重要作用。下列有关叙述正确的是
A.“墨子号”卫星成功发射实现了光纤量子通信,生产光纤的原料为晶体硅
B.实现海上首飞的“鲲龙”水陆两栖飞机的燃料为航空煤油,其组成元素与生物柴油相同
C.长征五号火箭的箭体蒙皮材料2219-铝合金,可一定程度上减轻火箭的质量
D.“奋斗者”号载人潜水器成功坐底,深度10909m,所用硬质合金潜孔钻头属于复合材料
3.进行化学实验时应规范实验操作,强化安全意识。下列做法正确的是
A.金属钠失火使用湿毛巾盖灭
B.酒精灯加热平底烧瓶时不垫石棉网
C. 萃取碘水实验完成后的废液直接排入下水道中
D.制取硝基苯用到的试剂苯应与浓硝酸分开放置并远离火源
4.化学与生产生活密切相关。下列物质的用途没有运用相应化学原理的是
选项 用途 化学原理
A 氧化铝用于制作坩埚 氧化铝的熔点高
B 碳酸氢钠用于制作泡沫灭火器 碳酸氢钠受热易分解
C 以油脂为原料制肥皂 油脂可以发生皂化反应
D 用浓氨水检查氯气管道是否漏气 具有还原性
5.下列图示或化学用语错误的是A.羟基的电子式:
B.HO的VSEPR模型:
2
C.Mn2+的价电子的轨道表示式:
D.中子数为5的铍原子:
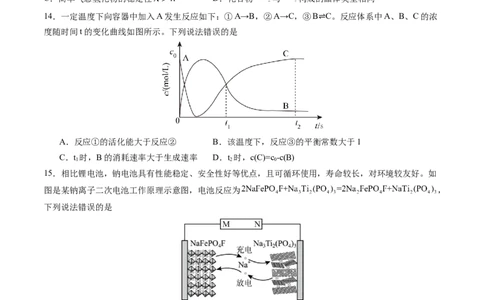
6.物质类别和元素价态,是学习元素及其化合物性质的重要认识视角。结合硫元素的“价—类”二维图
分析,下列有关说法正确的是
A.在酸性条件下,将e和f的钠盐溶液混合,会有d生成
B.若上图中盐为钠的正盐,则图中既有氧化性又有还原性的物质有3种
C.将b的稀溶液滴加到品红溶液中,品红溶液褪色,体现了b的强氧化性
D.将c的浓溶液滴加在胆矾晶体上,晶体由蓝色变成白色,体现了c的脱水性
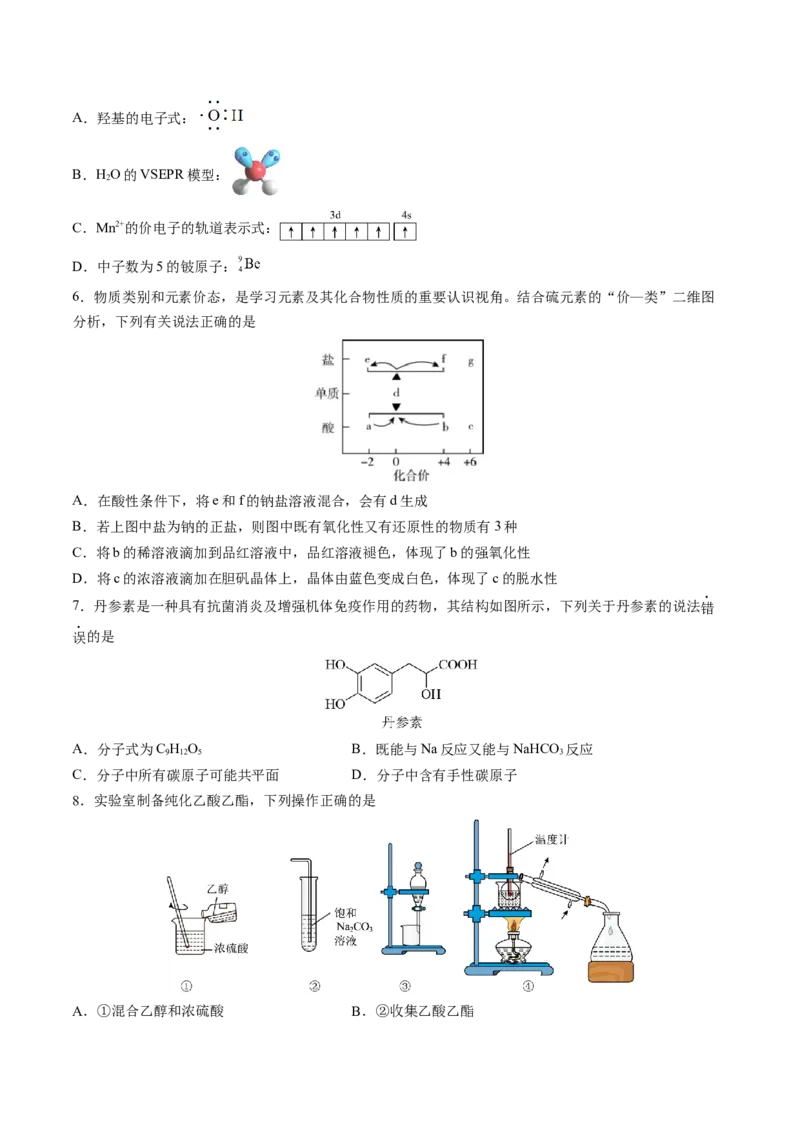
7.丹参素是一种具有抗菌消炎及增强机体免疫作用的药物,其结构如图所示,下列关于丹参素的说法错
误的是
A.分子式为C H O B.既能与Na反应又能与NaHCO 反应
9 12 5 3
C.分子中所有碳原子可能共平面 D.分子中含有手性碳原子
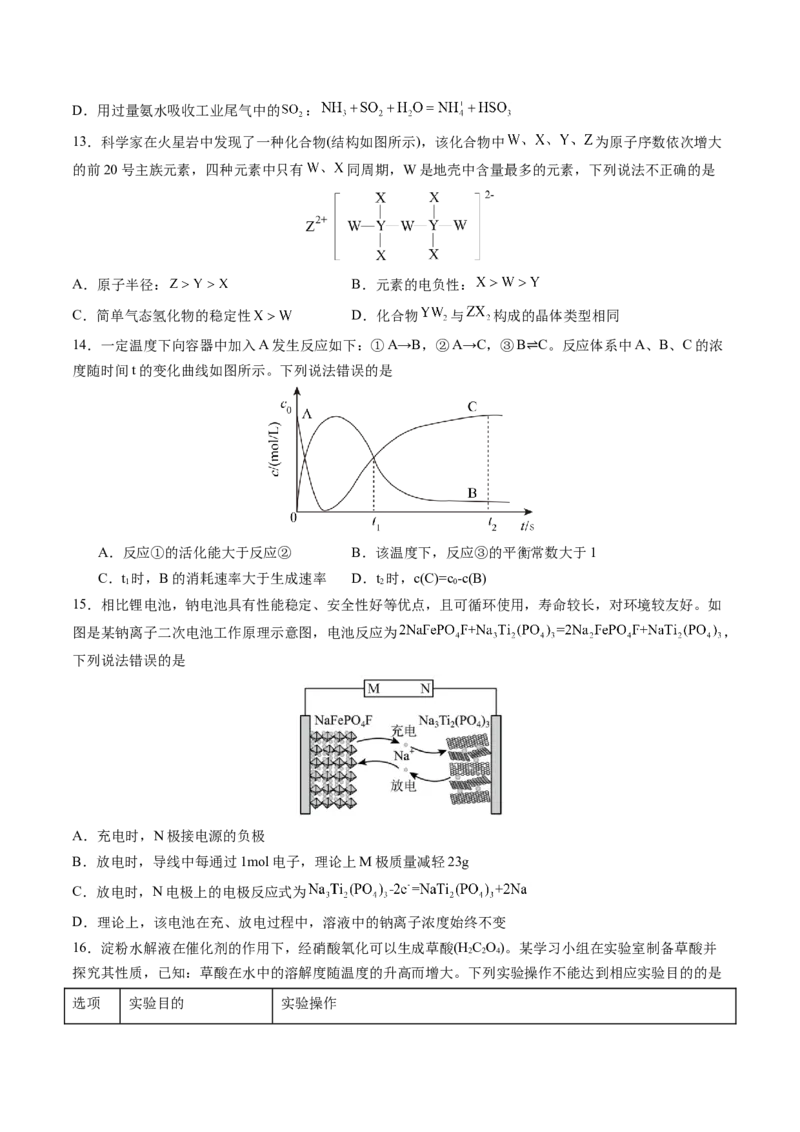
8.实验室制备纯化乙酸乙酯,下列操作正确的是
A.①混合乙醇和浓硫酸 B.②收集乙酸乙酯C.③分离乙酸乙酯和饱和碳酸钠溶液 D.④提纯乙酸乙酯
9.CO与 在铁催化剂表面进行如下两步反应:
第一步: (慢)
第二步: (快)
其相对能量与反应历程如下图所示,下列说法错误的是
A.在整个反应历程中,有极性键的断裂和生成
B.总反应的反应速率由第一步反应决定
C.两步反应均为放热反应
D. FeO*和Fe *均为反应的催化剂
10.铬离子能形成多种配位化合物,下列关于 说法正确的是
A. 中 的化合价为
B. 中铬离子的配位数是5
C. 的沸点比 低
D. 与 的键角相同
11.常温下,用0.1mol·L-1氨水滴定10mL浓度均为0.1mol·L-1的HCl和CHCOOH的混合液,已知醋酸的
3
电离常数为K =1.8×10-5,下列说法错误的是
a
A.在氨水滴定前,混合溶液c(Cl-)>c(CHCOOH)
3
B.在氨水滴定前,混合溶液c(CHCOO-)≈Ka
3
C.当滴入氨水10mL时,c( )+c(NH ·H O)=c(CHCOOH)+c(CHCOO-)
3 2 3 3
D.当溶液呈中性时,氨水滴入量等于20mL,且c( )<c(Cl-)
12.下列离子方程式表示正确的是
A.侯氏制碱法中制取 :
B.用 溶液预处理水垢中的 :
C.泡沫灭火器的灭火原理:D.用过量氨水吸收工业尾气中的 :
13.科学家在火星岩中发现了一种化合物(结构如图所示),该化合物中 为原子序数依次增大
的前20号主族元素,四种元素中只有 同周期,W是地壳中含量最多的元素,下列说法不正确的是
A.原子半径: B.元素的电负性:
C.简单气态氢化物的稳定性 D.化合物 与 构成的晶体类型相同
14.一定温度下向容器中加入A发生反应如下:①A→B,②A→C,③B C。反应体系中A、B、C的浓
度随时间t的变化曲线如图所示。下列说法错误的是
⇌
A.反应①的活化能大于反应② B.该温度下,反应③的平衡常数大于1
C.t 时,B的消耗速率大于生成速率 D.t 时,c(C)=c -c(B)
1 2 0
15.相比锂电池,钠电池具有性能稳定、安全性好等优点,且可循环使用,寿命较长,对环境较友好。如
图是某钠离子二次电池工作原理示意图,电池反应为 ,
下列说法错误的是
A.充电时,N极接电源的负极
B.放电时,导线中每通过1mol电子,理论上M极质量减轻23g
C.放电时,N电极上的电极反应式为
D.理论上,该电池在充、放电过程中,溶液中的钠离子浓度始终不变
16.淀粉水解液在催化剂的作用下,经硝酸氧化可以生成草酸(H C O)。某学习小组在实验室制备草酸并
2 2 4
探究其性质,已知:草酸在水中的溶解度随温度的升高而增大。下列实验操作不能达到相应实验目的的是
选项 实验目的 实验操作A 制备淀粉水解液 向烧瓶中加入淀粉和稀硫酸溶液,加热
向草酸粗产品中加入适量水,加热溶解,趁热过滤,冷却结晶,过滤,
B 提纯草酸晶体
冰水洗涤,干燥
C 验证草酸为二元弱酸 用NaOH标准溶液滴定草酸溶液,消耗NaOH的物质的量为草酸的2倍
D 验证草酸的还原性 取酸性KMnO 溶液于试管中,滴加草酸溶液,溶液颜色逐渐褪去
4
第Ⅱ卷
二、非选择题:本题共4个小题,共56分。
17.(14分)实验室以 为原料,用两种方法制备高锰酸钾。已知: 在浓强碱溶液中可稳
定存在,溶液呈墨绿色,当溶液碱性减弱时易发生反应:
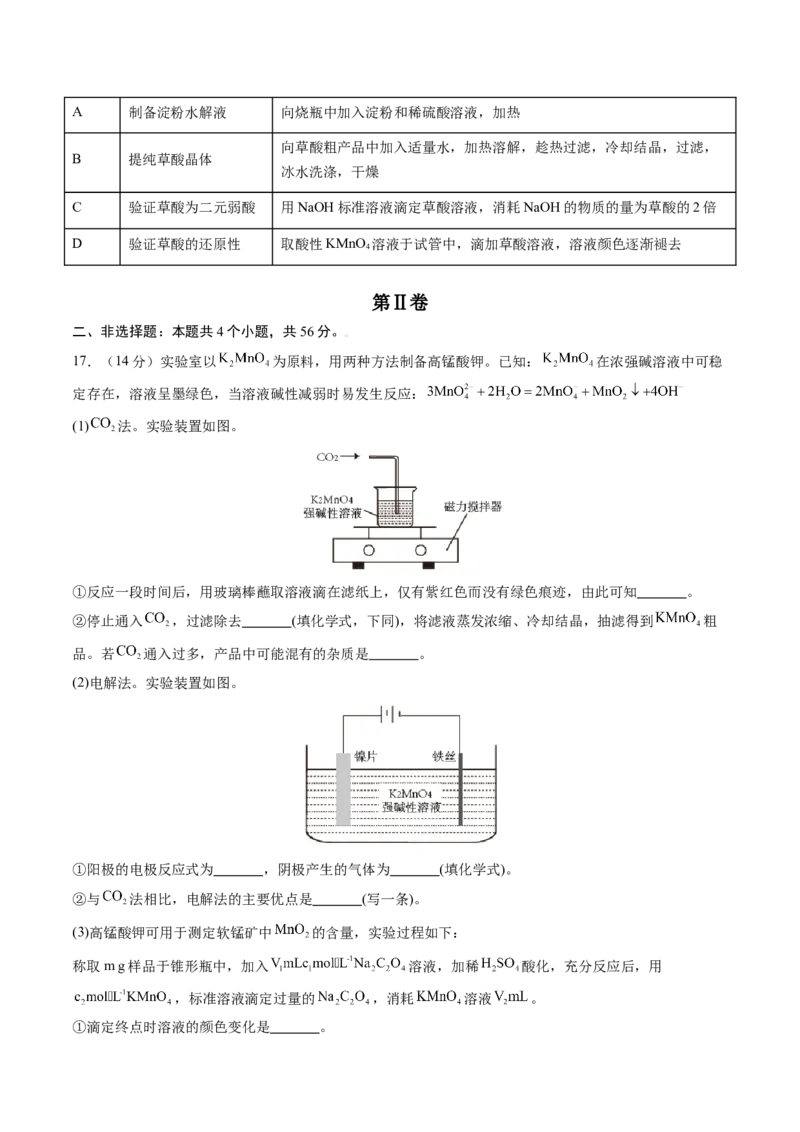
(1) 法。实验装置如图。
①反应一段时间后,用玻璃棒蘸取溶液滴在滤纸上,仅有紫红色而没有绿色痕迹,由此可知 。
②停止通入 ,过滤除去 (填化学式,下同),将滤液蒸发浓缩、冷却结晶,抽滤得到 粗
品。若 通入过多,产品中可能混有的杂质是 。
(2)电解法。实验装置如图。
①阳极的电极反应式为 ,阴极产生的气体为 (填化学式)。
②与 法相比,电解法的主要优点是 (写一条)。
(3)高锰酸钾可用于测定软锰矿中 的含量,实验过程如下:
称取m g样品于锥形瓶中,加入 溶液,加稀 酸化,充分反应后,用
,标准溶液滴定过量的 ,消耗 溶液 。
①滴定终点时溶液的颜色变化是 。②软锰矿中 的质量分数表达式为 。
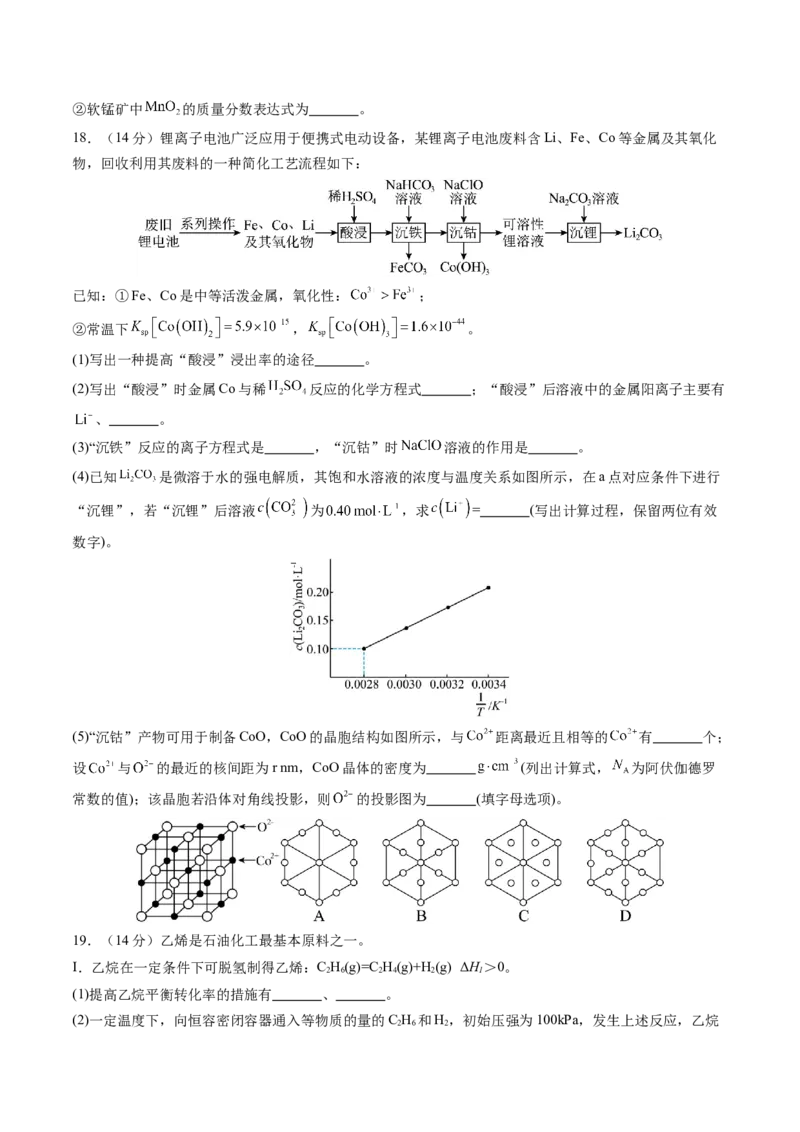
18.(14分)锂离子电池广泛应用于便携式电动设备,某锂离子电池废料含Li、Fe、Co等金属及其氧化
物,回收利用其废料的一种简化工艺流程如下:
已知:①Fe、Co是中等活泼金属,氧化性: ;
②常温下 , 。
(1)写出一种提高“酸浸”浸出率的途径 。
(2)写出“酸浸”时金属Co与稀 反应的化学方程式 ;“酸浸”后溶液中的金属阳离子主要有
、 。
(3)“沉铁”反应的离子方程式是 ,“沉钴”时 溶液的作用是 。
(4)已知 是微溶于水的强电解质,其饱和水溶液的浓度与温度关系如图所示,在a点对应条件下进行
“沉锂”,若“沉锂”后溶液 为 ,求 = (写出计算过程,保留两位有效
数字)。
(5)“沉钴”产物可用于制备CoO,CoO的晶胞结构如图所示,与 距离最近且相等的 有 个;
设 与 的最近的核间距为r nm,CoO晶体的密度为 (列出计算式, 为阿伏伽德罗
常数的值);该晶胞若沿体对角线投影,则 的投影图为 (填字母选项)。
19.(14分)乙烯是石油化工最基本原料之一。
I.乙烷在一定条件下可脱氢制得乙烯:C H(g)=C H(g)+H(g) ΔH>0。
2 6 2 4 2 1
(1)提高乙烷平衡转化率的措施有 、 。
(2)一定温度下,向恒容密闭容器通入等物质的量的C H 和H,初始压强为100kPa,发生上述反应,乙烷
2 6 2的平衡转化率为20%。平衡时体系的压强为 kPa,该反应的平衡常数K = kPa (用平衡分压
p
代替平衡浓度计算,分压=总压×物质的量分数)。
II.在乙烷中引入O 可以降低反应温度,减少积碳。涉及如下反应:
2
a.2C H(g)+ O (g)= 2C H(g) + 2HO(g) H<0
2 6 2 2 4 2 2
b.2C H(g) + 5O(g)= 4CO(g) + 6H O(g) H<0
2 6 2 2 △ 3
c.C H(g)+ 2O (g)= 2CO(g) + 2H O(g) H<0
2 4 2 2 △4
(3)根据盖斯定律,反应a的△H= (写出代数式)。
2 △
(4)氧气的引入可能导致过度氧化。为减少过度氧化,需要寻找催化剂降低反应 (选填“a、b、c”)的
活化能。
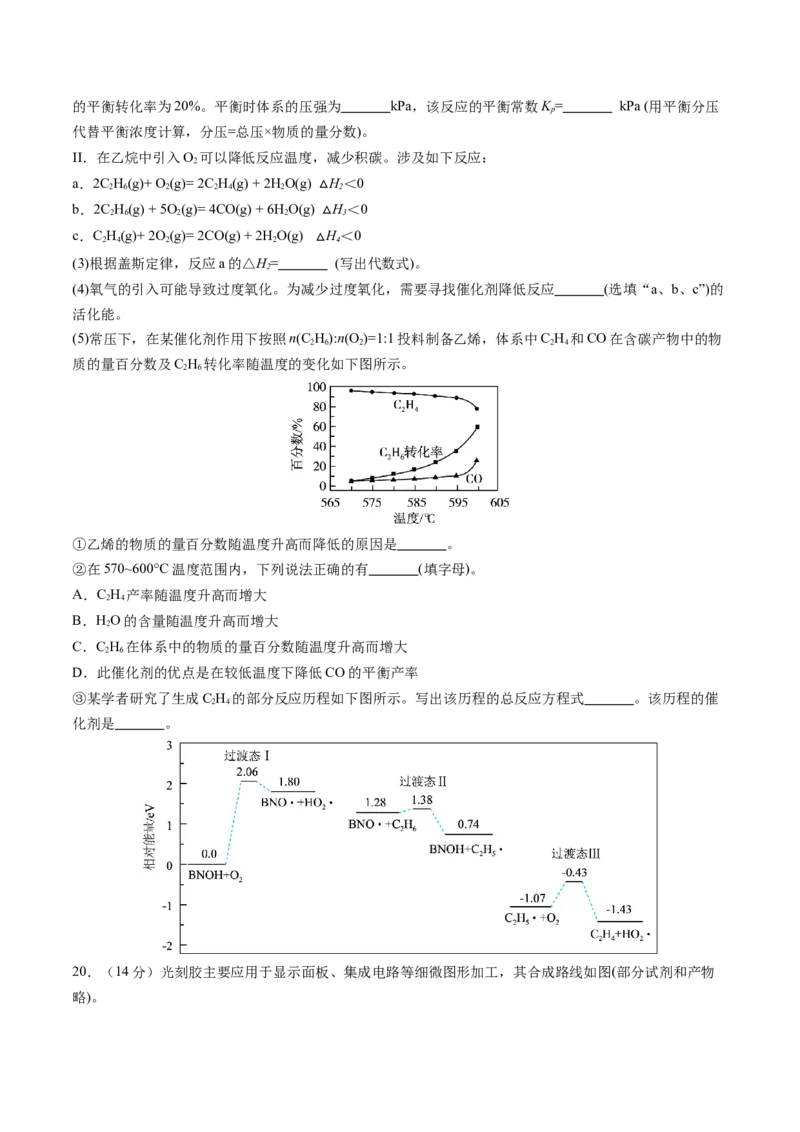
(5)常压下,在某催化剂作用下按照n(C H):n(O )=1:1投料制备乙烯,体系中C H 和CO在含碳产物中的物
2 6 2 2 4
质的量百分数及C H 转化率随温度的变化如下图所示。
2 6
①乙烯的物质的量百分数随温度升高而降低的原因是 。
②在570~600°C温度范围内,下列说法正确的有 (填字母)。
A.C H 产率随温度升高而增大
2 4
B.HO的含量随温度升高而增大
2
C.C H 在体系中的物质的量百分数随温度升高而增大
2 6
D.此催化剂的优点是在较低温度下降低CO的平衡产率
③某学者研究了生成C H 的部分反应历程如下图所示。写出该历程的总反应方程式 。该历程的催
2 4
化剂是 。
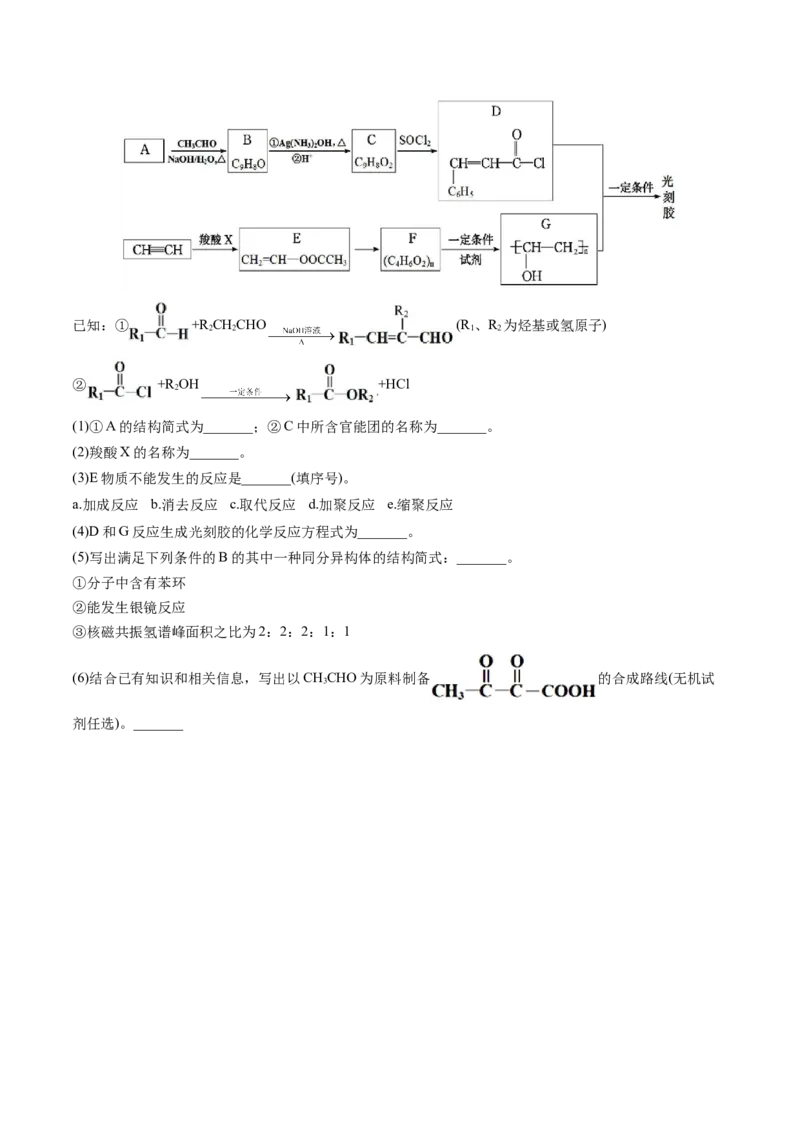
20.(14分)光刻胶主要应用于显示面板、集成电路等细微图形加工,其合成路线如图(部分试剂和产物
略)。已知:① +R CHCHO (R 、R 为烃基或氢原子)
2 2 1 2
② +R OH +HCl
2
(1)①A的结构简式为_______;②C中所含官能团的名称为_______。
(2)羧酸X的名称为_______。
(3)E物质不能发生的反应是_______(填序号)。
a.加成反应 b.消去反应 c.取代反应 d.加聚反应 e.缩聚反应
(4)D和G反应生成光刻胶的化学反应方程式为_______。
(5)写出满足下列条件的B的其中一种同分异构体的结构简式:_______。
①分子中含有苯环
②能发生银镜反应
③核磁共振氢谱峰面积之比为2:2:2:1:1
(6)结合已有知识和相关信息,写出以CHCHO为原料制备 的合成路线(无机试
3
剂任选)。_______