文档内容
课堂检测·素养达标
1.根据元素在周期表中的位置判断,下列正确的是 ( )
A.金属性:Na>K B.非金属性:S>Cl
C.酸性:H PO >HNO D.碱性:KOH>Mg(OH)
3 4 3 2
2.X、Y、Z三种元素的电子层数相同,它们的最高价氧化物分别为酸性氧化物、
碱性氧化物和两性氧化物,则三种元素的原子序数的大小顺序是 ( )
A.X>Y>Z B.Y>Z>X C.X>Z>Y D.Z>X>Y
3.(2019·福州一中月考)X、Y两元素是同周期的非金属主族元素,如果X原子
半径比Y的大,下面说法正确的是 ( )
A.最高价氧化物对应水化物的酸性,X的比Y的强
B.X的非金属性比Y的强
C.X的阴离子比Y的阴离子还原性强
D.X的气态氢化物比Y的稳定
【补偿训练】
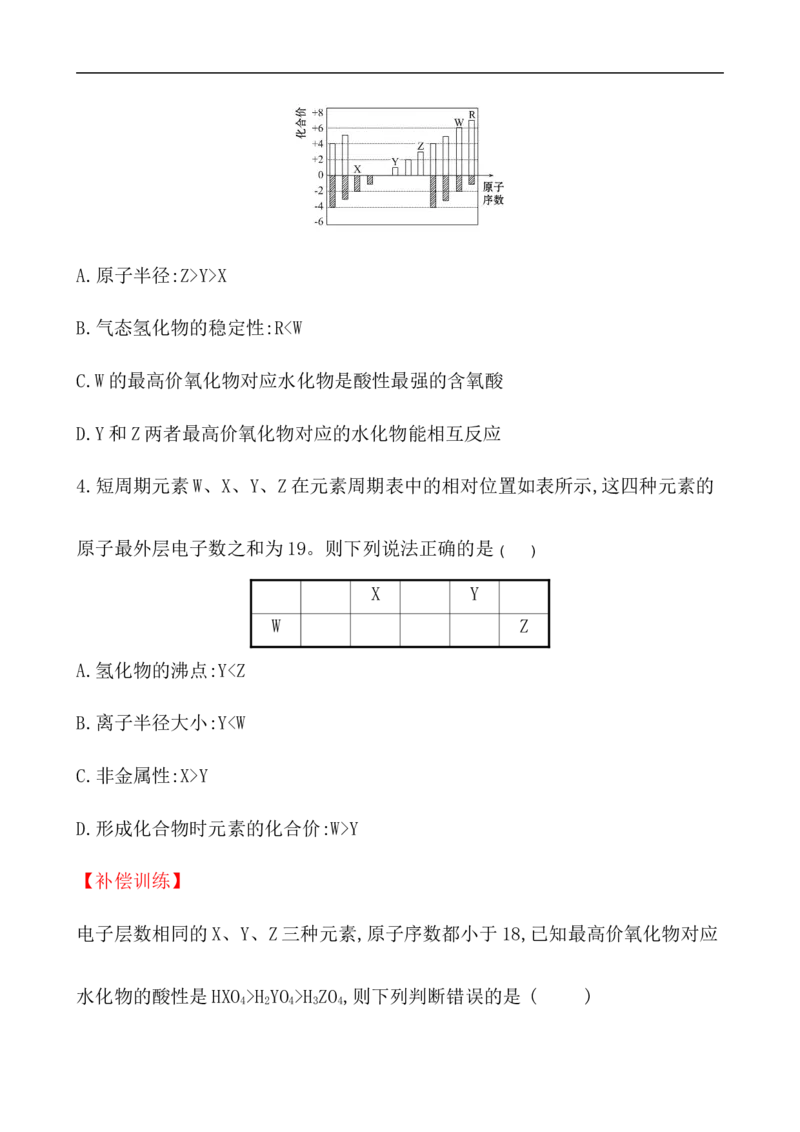
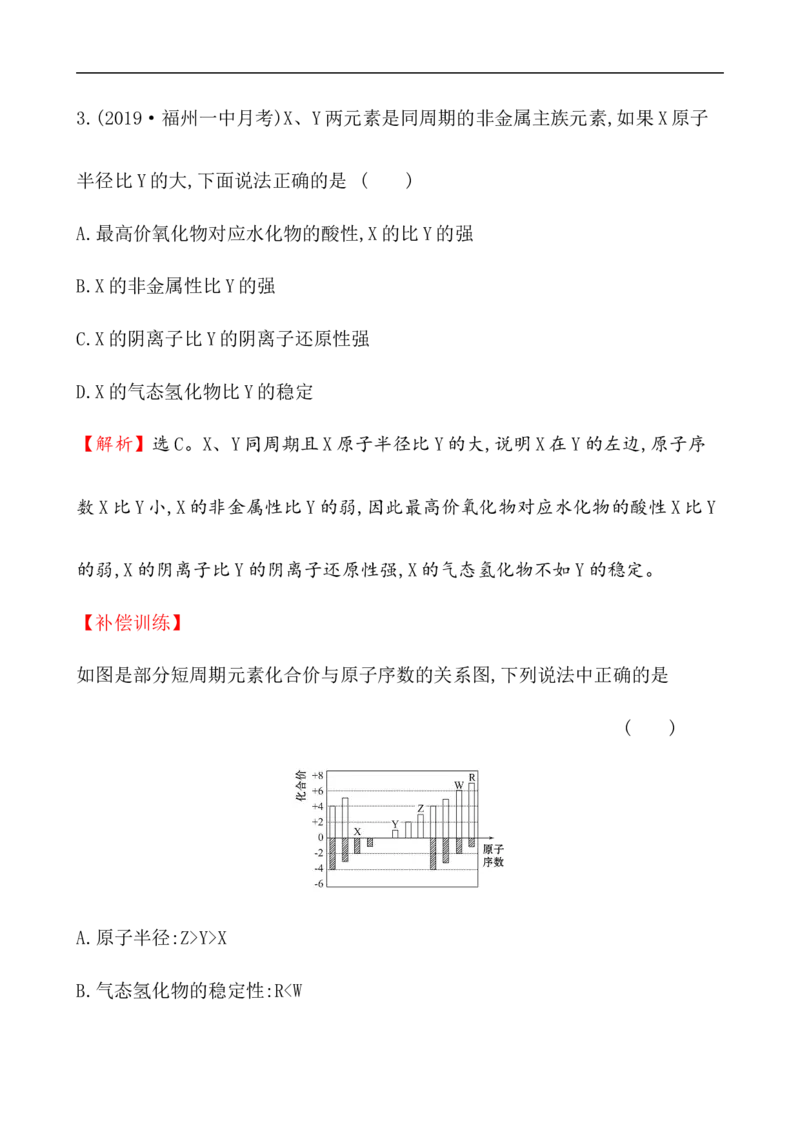
如图是部分短周期元素化合价与原子序数的关系图,下列说法中正确的是
( )A.原子半径:Z>Y>X
B.气态氢化物的稳定性:RY
D.形成化合物时元素的化合价:W>Y
【补偿训练】
电子层数相同的X、Y、Z三种元素,原子序数都小于18,已知最高价氧化物对应
水化物的酸性是HXO >H YO >H ZO ,则下列判断错误的是 ( )
4 2 4 3 4A.原子半径:X>Y>Z
B.气态氢化物的稳定性:HX>H Y>ZH
2 3
C.非金属性:X>Y>Z
D.阴离子的还原性:Z3->Y2->X-
5.(新思维·新考向)我们生活在化学世界中,某些元素在人体的细胞、组织和
体液中大量富集,如大脑中含有丰富的Na、Mg、K,骨筋和骨组织中含有丰富的
Li、Mg、K等。
(1)Li、Na、Mg、K原子半径大小关系是什么?
(2)Li、Na、Mg、K元素的金属性强弱顺序是什么?课堂检测·素养达标
1.根据元素在周期表中的位置判断,下列正确的是 ( )
A.金属性:Na>K B.非金属性:S>Cl
C.酸性:H PO >HNO D.碱性:KOH>Mg(OH)
3 4 3 2
【解析】选D。同主族自上而下金属性逐渐增强,A错误;同周期从左到右非金属
性逐渐增强,同主族自下而上,最高价氧化物对应水化物的酸性逐渐增强,B、C
错误;由同主族元素的最高价氧化物的水化物碱性递变规律可得:KOH>NaOH,由
同周期元素的最高价氧化物的水化物碱性递变规律可得NaOH>Mg(OH) ,则碱
2
性:KOH>Mg(OH) ,D正确。
2
2.X、Y、Z三种元素的电子层数相同,它们的最高价氧化物分别为酸性氧化物、
碱性氧化物和两性氧化物,则三种元素的原子序数的大小顺序是 ( )
A.X>Y>Z B.Y>Z>X C.X>Z>Y D.Z>X>Y
【解析】选C。大多数金属氧化物属于碱性氧化物,大多数非金属氧化物属于酸
性氧化物,电子层数相同的元素从左到右按照先金属、后非金属的顺序排列。
即最高价氧化物从左向右依次是碱性氧化物、两性氧化物、酸性氧化物,所以X
的原子序数最大,Y的原子序数最小。3.(2019·福州一中月考)X、Y两元素是同周期的非金属主族元素,如果X原子
半径比Y的大,下面说法正确的是 ( )
A.最高价氧化物对应水化物的酸性,X的比Y的强
B.X的非金属性比Y的强
C.X的阴离子比Y的阴离子还原性强
D.X的气态氢化物比Y的稳定
【解析】选C。X、Y同周期且X原子半径比Y的大,说明X在Y的左边,原子序
数X比Y小,X的非金属性比Y的弱,因此最高价氧化物对应水化物的酸性X比Y
的弱,X的阴离子比Y的阴离子还原性强,X的气态氢化物不如Y的稳定。
【补偿训练】
如图是部分短周期元素化合价与原子序数的关系图,下列说法中正确的是
( )
A.原子半径:Z>Y>X
B.气态氢化物的稳定性:RZ>X,A项错误;非金属性越强,对应气态氢化物就越稳定,
所以HCl比H S稳定,B项错误;C项中硫酸的酸性小于高氯酸,C项错误;Y和Z的
2
最高价氧化物对应的水化物分别是NaOH和Al(OH) ,因Al(OH) 为两性氢氧化物,
3 3
既能与酸反应又能与强碱反应,D项正确。
4.短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的
原子最外层电子数之和为19。则下列说法正确的是
( )
X Y
W Z
A.氢化物的沸点:YY
D.形成化合物时元素的化合价:W>Y【解析】选D。W、X、Y、Z均为短周期主族元素,由位置关系可知,X、Y处于第
2周期,W、Z处于第3周期,设W原子最外层电子数为a,则X、Y、Z最外层电子
数依次为a+2、a+4、a+5,四种元素的原子最外层电子数之和为19,则a+a+2+a+
4+a+5=19,解得a=2,则W为镁元素,故X为碳元素、Y为氧元素、Z为氯元素;A
项,H O分子间有氢键,常温下是液态,而HCl常温下是气态,可知H O的沸点大于
2 2
HCl,故A错误;B项,O2-与Mg2+的电子层结构相同,Mg的核电荷数大,Mg2+半径小,
故B错误;C项,同周期从左到右,非金属性逐渐增强,故C错误;D项,Mg是金属,
形成化合物时化合价是+2,O形成化合物时化合价通常为-1或-2,故D正确。
【补偿训练】
电子层数相同的X、Y、Z三种元素,原子序数都小于18,已知最高价氧化物对应
水化物的酸性是HXO >H YO >H ZO ,则下列判断错误的是 ( )
4 2 4 3 4
A.原子半径:X>Y>Z
B.气态氢化物的稳定性:HX>H Y>ZH
2 3
C.非金属性:X>Y>Z
D.阴离子的还原性:Z3->Y2->X-【解析】选A。由三种元素最高价氧化物的水化物的分子式知X、Y、Z的最高
正价分别为+7、+6、+5,因为F没有+7价,所以X一定是Cl,则Y是S,Z是P。因
为非金属性:Cl>S>P,所以气态氢化物的稳定性:HCl>H S>PH ,阴离子的还原
2 3
性:P3->
S2->Cl-,故B、C、D选项都正确。因为电子层数相同的原子,随着原子序数的递
增,原子半径减小,所以原子半径:P>S>Cl,故A选项错误。
5.(新思维·新考向)我们生活在化学世界中,某些元素在人体的细胞、组织和
体液中大量富集,如大脑中含有丰富的Na、Mg、K,骨筋和骨组织中含有丰富的
Li、Mg、K等。
(1)Li、Na、Mg、K原子半径大小关系是什么?
提示:原子半径:LiNa>Li>Mg。