文档内容
课时素养评价 二十三
元素性质的周期性变化规律
(40分钟 70分)
一、选择题(本题包括10小题,每小题4分,共40分)
1.(2019·莆田高一检测)下列关于元素周期律的叙述正确的是 ( )
A.随着元素原子序数的递增,原子最外层电子数总是从1到8重复出现
B.元素的性质随着原子序数的递增而呈周期性变化
C.随着元素原子序数的递增,元素的最高化合价从+1到+7,最低化合价从-7到-1
重复出现
D.元素性质的周期性变化是指原子核外电子排布的周期性变化、原子半径的周
期性变化及元素主要化合价的周期性变化
【补偿训练】
下列说法正确的是 ( )
A.原子序数越大,原子半径一定越大
B.电子层数多的原子半径一定比电子层数少的原子半径大
C.元素性质的周期性变化不是元素性质的简单重复D.按C、N、O、F的顺序,元素的最高正化合价依次升高
2.(2019·沧州高一检测)已知铍(Be)的原子序数为4。下列对铍及其化合物的
叙述中正确的是 ( )
A.铍的原子半径大于硼的原子半径
B.相同条件下,单质铍与酸反应比单质锂与酸反应剧烈
C.氢氧化铍碱性比氢氧化钙的强
D.单质铍跟冷水反应产生氢气
3.(2019·临沂高一检测)门捷列夫对化学这一学科发展的最大贡献在于发现了
化学元素周期律。下列事实不能用元素周期律解释的只有 ( )
A.碱性:KOH>Ca(OH) >Mg(OH)
2 2
B.稳定性:H O>H S>H Se
2 2 2
C.挥发性:HNO >H PO >H SO
3 3 4 2 4
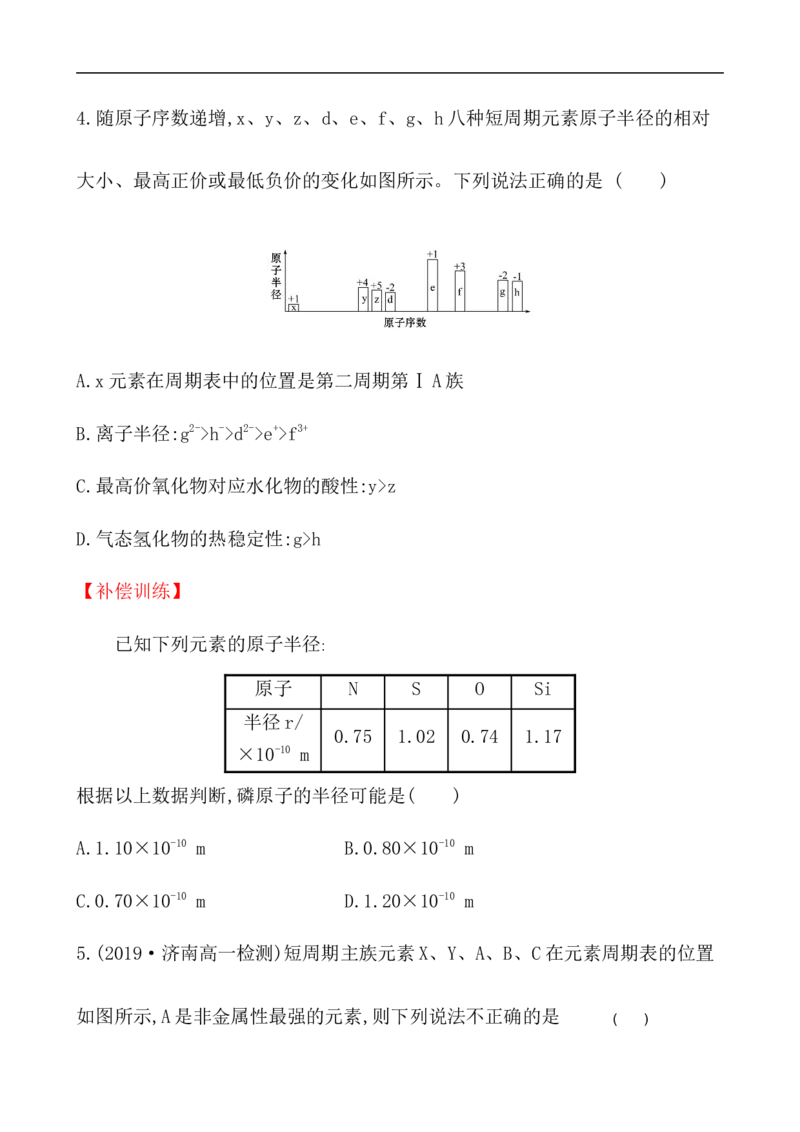
D.原子半径:P>S>Cl4.随原子序数递增,x、y、z、d、e、f、g、h八种短周期元素原子半径的相对
大小、最高正价或最低负价的变化如图所示。下列说法正确的是 ( )
A.x元素在周期表中的位置是第二周期第ⅠA族
B.离子半径:g2->h->d2->e+>f3+
C.最高价氧化物对应水化物的酸性:y>z
D.气态氢化物的热稳定性:g>h
【补偿训练】
已知下列元素的原子半径
:
原子 N S O Si
半径r/
0.75 1.02 0.74 1.17
×10-10 m
根据以上数据判断,磷原子的半径可能是( )
A.1.10×10-10 m B.0.80×10-10 m
C.0.70×10-10 m D.1.20×10-10 m
5.(2019·济南高一检测)短周期主族元素X、Y、A、B、C在元素周期表的位置
如图所示,A是非金属性最强的元素,则下列说法不正确的是
( )X A
Y C B
A.原子半径由小到大的顺序为AMg
Na比Mg剧烈
Ca(OH) 的碱性
2
B 金属性:Ca>Mg
强于Mg(OH)
2
H SO 的酸
2 3
C 非金属性:S>C
性比H CO 强
2 3
HCl热稳定性
D 非金属性:Cl>S
比H S强
2
7.(改编题)六六六是一种有机氯杀虫剂。代森锌、代森锰、福美铁、福美锌等
都属于有机硫农药。硫和氯为农药的发展做出巨大贡献,但二者的非金属性有
较大差异。为说明氯比硫的非金属性强,下列事实可作依据的是 ( )
A.HCl的溶解性强于H S
2
B.氯的最高价为+7价
C.H S中的S2-能被Cl 氧化
2 2
D.HClO的氧化性强于H SO
2 4
8.(2019·沈阳高一检测)如图是部分短周期元素原子(用字母表示)最外层电子
数与原子序数的关系。下列说法正确的是 ( )
A.X和R在同一周期
B.原子半径:W>R>X
C.气态氢化物的稳定性:YY
B.氢化物稳定性H X>HY
2
C.原子核内质子数R丁
D.丙所形成的单质可能互为同位素14.(2019·北京高考)2019年是元素周期表发表150周年,期间科学家为完善周
期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟( In)等9
49
种元素相对原子质量的新值,被采用为国际新标准。铟与铷( Rb)同周期。下列
37
说法不正确的是 ( )
A.In是第五周期第ⅢA族元素
B In的中子数与电子数的差值为17
C.原子半径:In>Al
D.碱性:In(OH) >RbOH
3
二、非选择题(本题包括1小题,共12分)
15.我国的纳米技术基础研究能力已跻身世界前列,例如曾作为我国十大科技成
果之一的就是一种合成纳米材料,化学式为RN。RN与NH 中氮元素的价态相同,
3
则:
(1)RN中氮元素显________价,该化合物中的Rn+核外有28个电子。则R元素位
于元素周期表的 ( )A.第三周期ⅤA族
B.第四周期ⅢA族
C.第五周期ⅢA族
D.第四周期ⅤA族
(2)请画出R原子的结构示意图。
【补偿训练】
下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元
素的有关性质)。
(1)把与下面元素有关性质相符的曲线标号填入相应的空格中:
①第ⅡA族元素的价电子数________。
②第三周期元素的最高化合价________。
③F-、Na+、Mg2+、Al3+的离子半径________。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原
子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回
答:
①X为________________________(名称),Y为__________________(元素符
号),Z原子结构示意图为________________________________。
②N的最高价氧化物的水化物的化学式为______________________。
③M的最高价氧化物的化学式为________________________。课时素养评价 二十三
元素性质的周期性变化规律
(40分钟 70分)
一、选择题(本题包括10小题,每小题4分,共40分)
1.(2019·莆田高一检测)下列关于元素周期律的叙述正确的是 ( )
A.随着元素原子序数的递增,原子最外层电子数总是从1到8重复出现
B.元素的性质随着原子序数的递增而呈周期性变化
C.随着元素原子序数的递增,元素的最高化合价从+1到+7,最低化合价从-7到-1
重复出现
D.元素性质的周期性变化是指原子核外电子排布的周期性变化、原子半径的周
期性变化及元素主要化合价的周期性变化
【解析】选B。A项中,只有一层电子时最外层电子数是从1到2;C项中,O、F没
有正价,最低负价也不是从-7开始出现;D项中,不包括核外电子排布的周期性变
化。
【补偿训练】
下列说法正确的是 ( )A.原子序数越大,原子半径一定越大
B.电子层数多的原子半径一定比电子层数少的原子半径大
C.元素性质的周期性变化不是元素性质的简单重复
D.按C、N、O、F的顺序,元素的最高正化合价依次升高
【解析】选C。原子半径随原子序数的递增呈周期性变化,故A项错误。氯原子
比锂原子多一个电子层,但原子半径r(Li)>r(Cl),故B项错误。元素性质的周
期性变化不是简单的重复变化,变化的程度不同,变化的起点和终点也不同,故C
项正确。氟是最活泼的非金属元素,它只有负价,没有正价;氧的非金属性也很
强,中学阶段一般只讲负价,故D项错误。
2.(2019·沧州高一检测)已知铍(Be)的原子序数为4。下列对铍及其化合物的
叙述中正确的是 ( )
A.铍的原子半径大于硼的原子半径
B.相同条件下,单质铍与酸反应比单质锂与酸反应剧烈
C.氢氧化铍碱性比氢氧化钙的强D.单质铍跟冷水反应产生氢气
【解析】选A。A项,Be、B同周期,根据“序大径小”可知原子半径:Be>B;B项,
金属性:Li>Be,故单质锂与酸反应比单质铍与酸反应剧烈;C项,金属性:Ca>Be,
故碱性:Ca(OH) >Be(OH) ;D项,活泼性:Mg>Be,Mg与冷水反应缓慢,故Be与冷水
2 2
不反应。
3.(2019·临沂高一检测)门捷列夫对化学这一学科发展的最大贡献在于发现了
化学元素周期律。下列事实不能用元素周期律解释的只有 ( )
A.碱性:KOH>Ca(OH) >Mg(OH)
2 2
B.稳定性:H O>H S>H Se
2 2 2
C.挥发性:HNO >H PO >H SO
3 3 4 2 4
D.原子半径:P>S>Cl
【解析】选C。元素的金属性越强,其原子失电子能力越强,其最高价氧化物对
应的水化物碱性越强,金属性K>Ca>Mg,则碱性:KOH>Ca(OH) >Mg(OH) ,A可以;元
2 2
素的非金属性越强,其对应的气态氢化物越稳定,同主族元素非金属性O>S>Se,
则稳定性:H O>H S>H Se,B可以;挥发性与物质的结构无关,C不可以;同周期元素
2 2 2
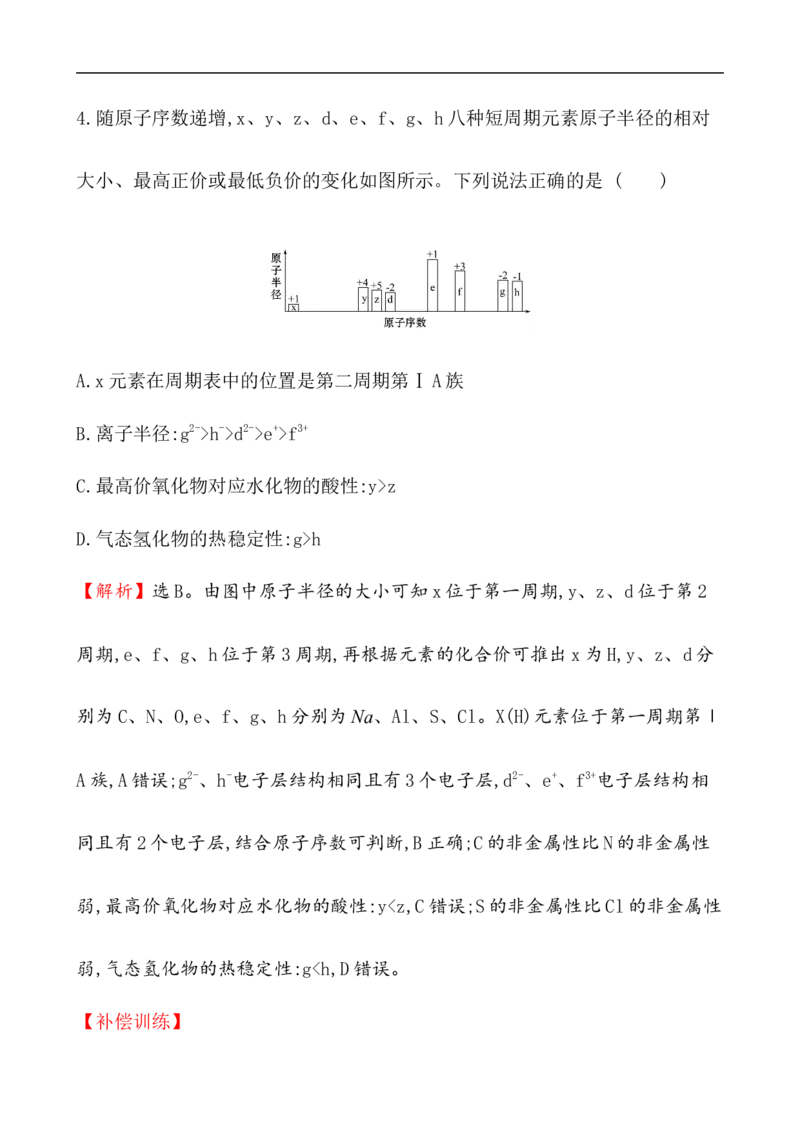
从左到右原子半径逐渐减小,D可以。4.随原子序数递增,x、y、z、d、e、f、g、h八种短周期元素原子半径的相对
大小、最高正价或最低负价的变化如图所示。下列说法正确的是 ( )
A.x元素在周期表中的位置是第二周期第ⅠA族
B.离子半径:g2->h->d2->e+>f3+
C.最高价氧化物对应水化物的酸性:y>z
D.气态氢化物的热稳定性:g>h
【解析】选B。由图中原子半径的大小可知x位于第一周期,y、z、d位于第2
周期,e、f、g、h位于第3周期,再根据元素的化合价可推出x为H,y、z、d分
别为C、N、O,e、f、g、h分别为Na、Al、S、Cl。X(H)元素位于第一周期第Ⅰ
A族,A错误;g2-、h-电子层结构相同且有3个电子层,d2-、e+、f3+电子层结构相
同且有2个电子层,结合原子序数可判断,B正确;C的非金属性比N的非金属性
弱,最高价氧化物对应水化物的酸性:yHCl,B项错误;X、Y位于同一
主族,随原子序数的增大,非金属性逐渐减弱,最高价氧化物对应的水化物的酸
性逐渐减弱,故酸性由弱到强的顺序为H YO Mg
Na比Mg剧烈
Ca(OH) 的碱性
2
B 金属性:Ca>Mg
强于Mg(OH)
2
H SO 的酸
2 3
C 非金属性:S>C
性比H CO 强
2 3
HCl热稳定性
D 非金属性:Cl>S
比H S强
2
【解析】选C。用与水反应的剧烈程度判断元素金属性的强弱,与冷水反应,Na
比Mg剧烈,说明Na的金属性比Mg强,A项正确;用对应碱的碱性判断元素金属性
的强弱,Ca(OH) 的碱性强于Mg(OH) ,金属性:Ca>Mg,B项正确;亚硫酸不是最高
2 2
价含氧酸,亚硫酸的酸性比碳酸的酸性强,不能说明S与C的非金属性的强弱,C项错误;用气态氢化物的热稳定性判断非金属性的强弱,热稳定性HCl>H S,说明
2
非金属性Cl>S,D项正确。
7.(改编题)六六六是一种有机氯杀虫剂。代森锌、代森锰、福美铁、福美锌等
都属于有机硫农药。硫和氯为农药的发展做出巨大贡献,但二者的非金属性有
较大差异。
为说明氯比硫的非金属性强,下列事实可作依据的是 ( )
A.HCl的溶解性强于H S
2
B.氯的最高价为+7价
C.H S中的S2-能被Cl 氧化
2 2
D.HClO的氧化性强于H SO
2 4
【解析】选C。溶解性的强弱与分子的极性有关,属于物理性质,不能用于比较
非金属性强弱,故A错误;化合价的高低与原子最外层电子数有关,不能用于比较
非金属性的强弱,故B错误;元素的非金属性越强,对应单质的氧化性越强,H S中
2
的S2-能被Cl 氧化,氯气与H S能发生置换反应,说明氯气的氧化性大于S,元素
2 2的非金属性Cl大于S,故C正确;比较非金属性的强弱不能根据含氧酸的氧化性
强弱,如F不存在含氧酸,但F的非金属性最强,故D错误。
8.(2019·沈阳高一检测)如图是部分短周期元素原子(用字母表示)最外层电子
数与原子序数的关系。下列说法正确的是 ( )
A.X和R在同一周期
B.原子半径:W>R>X
C.气态氢化物的稳定性:YCl>O,B项错误;非金属性越强,对应气态氢化物越稳
定,HF>H O,C项错误;F的非金属性比S强,还原性:F-Y
B.氢化物稳定性H X>HY
2
C.原子核内质子数RY,非金属性:Y>X,氢化物稳定性:HY>H X,B错误,A正确;
2
R与冷水即可反应,M与热水反应缓慢,说明R、M的金属性:MP>Si,故
NH 的稳定性大于SiH 的稳定性。
3 4
答案:(1)7 K O、K O (KO 也可以)
2 2 2 2(2)氯(或Cl) +7价 (3)Al 两性 (4)Na
(5)NH SiH
3 4
12.(15分)哲学有云:万事万物的诞生发展运动变化都是有规律的,是严格按照
事物运动发展变化的内部法则进行的,宇宙是一个整体,没有超越这个整体而独
立存在的事物,这叫“诸行有常”。“诸行有常”的“诸”含义是“所有事
物”,“行”指所有事物的运动变化,“常”指“常态”“规律”“法则”“轨
迹”。元素性质存在周期性变化。
(1)短周期元素中最高价氧化物的水化物酸性最强的是哪一种?
提示:HClO 。
4
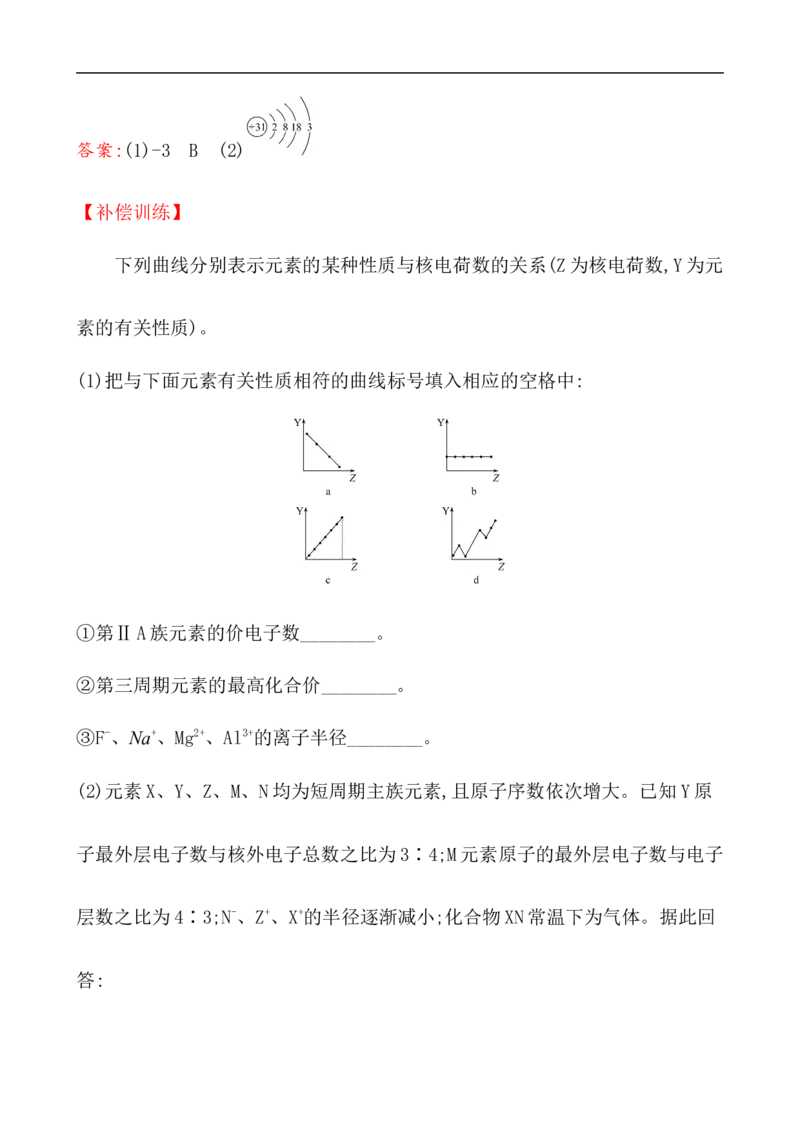
(2)Cl和C中哪种元素非金属性强?下列实验能否证明?
提示:Cl的非金属性强。本实验证明盐酸酸性强于碳酸,但不能证明Cl的非金
属性强于C。(20分钟 30分)
一、选择题(本题包括2小题,每小题9分,共18分)
13.(2019·长沙高一检测)短周期元素甲、乙、丙、丁的原子半径依次增大,其
氢化物中甲、乙、丙、丁的化合价如表所示。下列说法中正确的是
( )
元素 甲 乙 丙 丁
化合价 -2 -3 -4 -2
A.含氧酸的酸性:乙<丁
B.元素非金属性:甲<乙
C.氢化物的稳定性:甲>丁
D.丙所形成的单质可能互为同位素
【解析】选C。根据元素周期律中的原子半径规律和化合价规律判断甲是氧元
素,乙是氮元素,丙是碳元素,丁是硫元素,N的含氧酸有HNO 、HNO ,S的含氧酸
2 3
有H SO 、H SO ,酸性强弱无法判断,A项错误;O的非金属性大于N的非金属性,B
2 3 2 4
项错误;O的非金属性大于S,氢化物的稳定性:H O>H S,C项正确;C的单质可能为
2 2
同素异形体,同位素是同种元素不同原子的互称,D项错误。14.(2019·北京高考)2019年是元素周期表发表150周年,期间科学家为完善周
期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟( In)等9
49
种元素相对原子质量的新值,被采用为国际新标准。铟与铷( Rb)同周期。下列
37
说法不正确的是 ( )
A.In是第五周期第ⅢA族元素
B In的中子数与电子数的差值为17
C.原子半径:In>Al
D.碱性:In(OH) >RbOH
3
【解析】选D。In为49号元素,根据元素周期表中元素的排布规律,In是第五
周期第ⅢA族元素,故A正确 In的中子数为115-49=66,电子数为49,中子数
与电子数的差值为66-49=17,故B正确;In是第五周期第ⅢA族元素,Al为第三
周期第ⅢA族元素,依据元素周期律,原子半径:In>Al,故C正确;In是第五周期
第ⅢA族元素,Rb为第五周期第ⅠA族元素,金属性InNa+>Mg2+>Al3+,a符合。
(2)已知Y原子最外层电子数与核外电子总数之比为3∶4,则Y为O。M元素原子
的最外层电子数与电子层数之比为4∶3,则M为Si。由X、Y、Z、M、N的原子
序数关系和N、Z、X的简单离子形式可知,N为Cl,Z为Na,X为H。
答案:(1)①b ②c ③a
(2)①氢 O ②HClO ③SiO
4 2