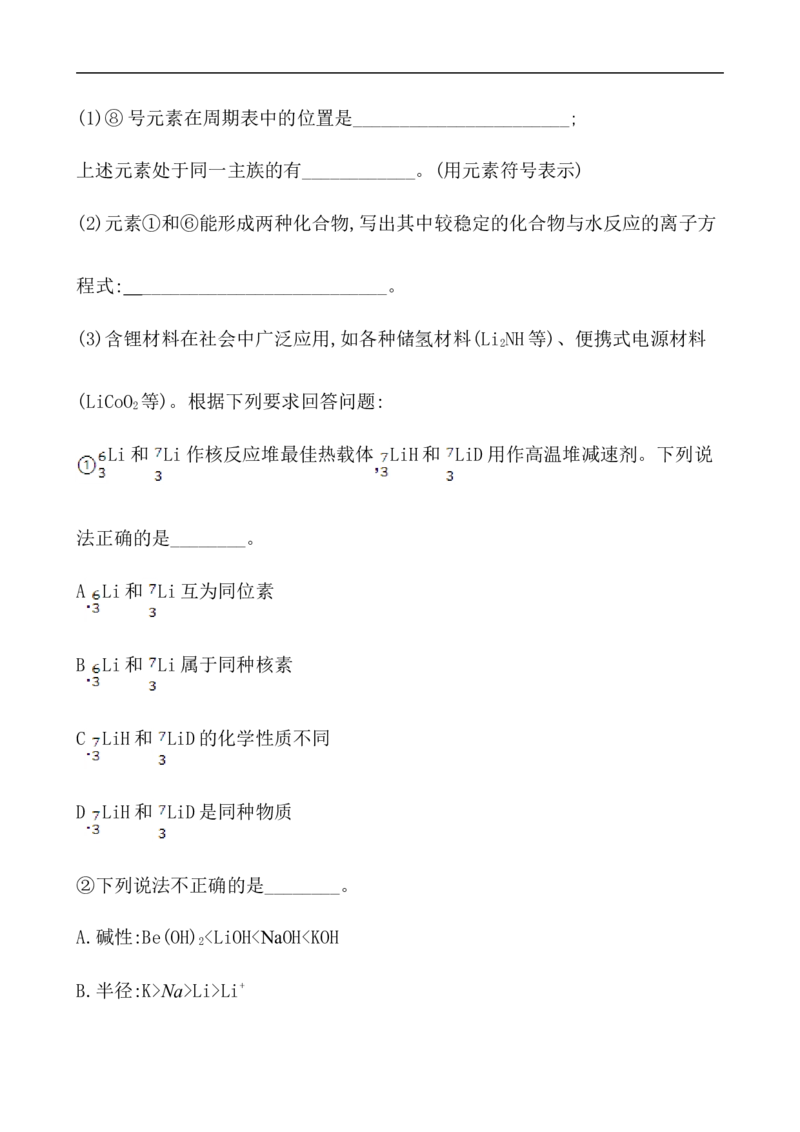文档内容
课时素养评价 二十四
元素周期表和元素周期律的应用
(40分钟 70分)
一、选择题(本题包括10小题,每小题4分,共40分)
1.(2019·北京西城区高一检测)英国研究人员认为,全球将有1.4亿人因为用水
受到砷中毒之害,导致更多的人患癌症。下列对砷(As)的有关判断正确的是
( )
A.砷原子序数为33,它与铝同主族
B.砷的原子半径小于磷的原子半径
C.砷化氢的稳定性比溴化氢的强
D.砷酸的酸性比硫酸的弱
【补偿训练】
已知 As、 Br位于同一周期。下列关系正确的是 ( )
33 35
A.原子半径:As>Cl>PB.热稳定性:HCl>AsH >HBr
3
C.还原性:As3->S2->Cl-
D.酸性:H AsO >H SO >H PO
3 4 2 4 3 4
2.某元素原子M层电子数是K层电子数的3.5倍,则该元素最高价氧化物对应水
化物的化学式为 ( )
A.HNO B.H PO
3 3 4
C.H SO D.HClO
2 4 4
3.(2019·青岛高一检测)根据原子结构及元素周期律的知识,下列推断正确的
是
( )
A.同主族元素含氧酸的酸性随核电荷数的增加而减弱
B.核外电子排布相同的微粒化学性质也相同
C.Cl-、S2-、Ca2+、K+半径逐渐减小
D Cl与 Cl得电子能力相同
【补偿训练】
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说
法不合理的是 ( )A.由水溶液的酸性:HCl>HF,不能推断出元素的非金属性:Cl>F
B.人们可以在周期表的过渡元素中寻找催化剂和耐腐蚀、耐高温的合金材料
C.短周期元素正化合价数值和其族序数相同
D.短周期元素形成的微粒X2-和Y2+核外电子排布相同,离子半径:X2->Y2+
4.下列说法正确的是 ( )
A.N和As属于第ⅤA族元素,氮原子得电子能力比砷原子强
B.族序数等于其周期序数的元素一定是金属元素
C.元素周期表中,位于金属和非金属交界线附近的元素属于过渡元素
D.Si、S、Cl的最高价氧化物都能与水反应生成相应的酸,且酸性依次增强
5.(2019·济南高一检测)已知某原子最外层有7个电子,推测下列选项不正确的
是 ( )
A.单质有氧化性
B.最高正价一定为+7价
C.是非金属元素
D.同周期元素中原子半径最小6.镓是1871年俄国化学家门捷列夫在编制元素周期表时曾预言的“类铝”元素。
镓的原子序数为31,属ⅢA族。镓的熔点为29.78 ℃,沸点高达2 403 ℃。镓
有过冷现象(即冷至熔点下不凝固),它可过冷到-120 ℃。
由此判断下列有关镓的性质及其用途的叙述不正确的是( )
A.镓是制造高温温度计的上佳材料
B.镓能溶于强酸和强碱中
C.镓与锌、锡、铟等金属制成的合金,可用在自动救火的水龙头中
D.近年来,镓成为电子工业的新宠,其主要用途是制造半导体材料,被誉为“半
导体家族的新成员”,这是利用了镓的导电性介于导体和绝缘体之间的性质
7.(2019·贵阳高一检测)不能作为判断硫、氯两种元素非金属性强弱的依据是
( )
A.单质氧化性的强弱
B.单质沸点的高低
C.单质与氢气化合的难易
D.最高价氧化物对应的水化物酸性的强弱8.锗是一种重要的半导体材料,用于制造晶体管及各种电子装置。门捷列夫把
它命名为类硅,处于周期表中金属区与非金属区的交界线上。
下列叙述正确的是 ( )
A.锗是一种金属性很强的元素
B.锗的单质具有半导体的性能
C.锗化氢(GeH )稳定性很强
4
D.锗酸是难溶于水的强酸
9.(2019·大连高一检测)X、Y、Z、W为周期表中前20号元素中的四种,原子序
数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3
倍,Y、Z位于同周期,Z单质是一种良好的半导体。W能与冷水剧烈反应,Y、Z原
子的最外层电子数之和与X、W原子的最外层电子数之和相等。下列说法正确的
是
( )
A.原子半径:W>Y>Z>XB.气态氢化物的稳定性:XW
D.Y、Z的氧化物均为两性氧化物
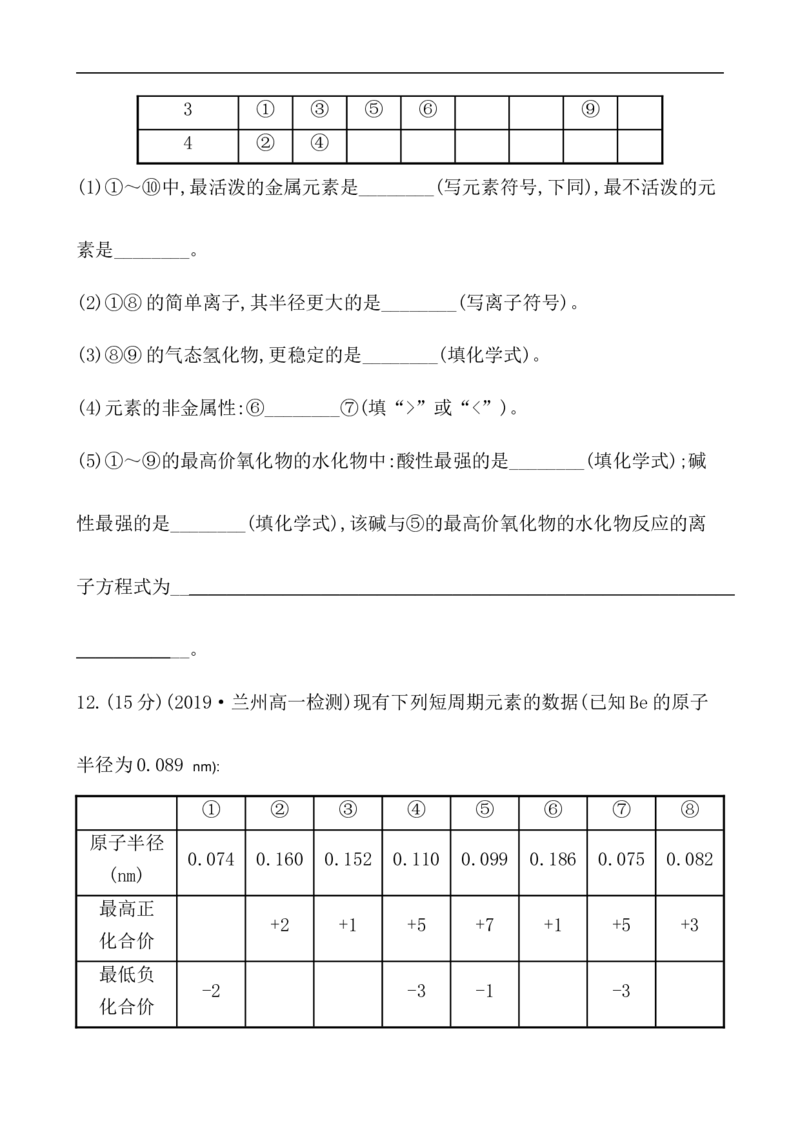
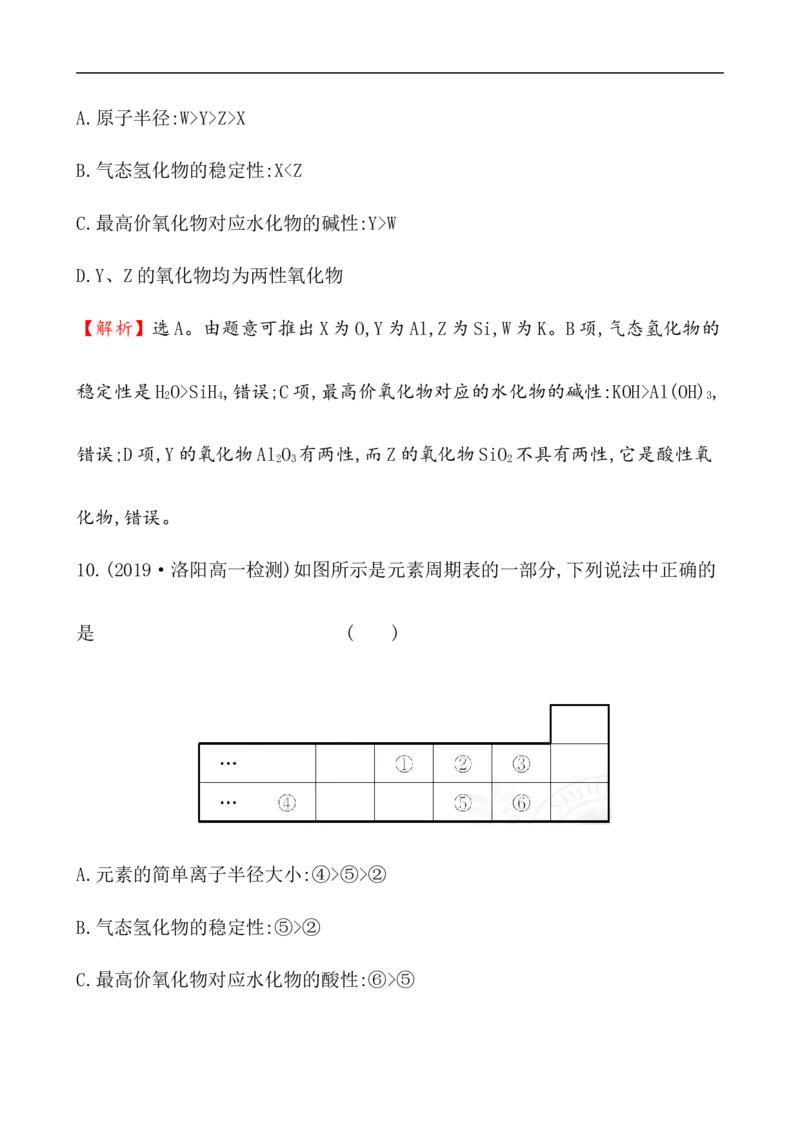
10.(2019·洛阳高一检测)如图所示是元素周期表的一部分,下列说法中正确的
是 ( )
A.元素的简单离子半径大小:④>⑤>②
B.气态氢化物的稳定性:⑤>②
C.最高价氧化物对应水化物的酸性:⑥>⑤
D.元素的最高正化合价:③=⑥
二、非选择题(本题包括2小题,共30分)
11.(15分)(2019·襄樊高一检测)下表为元素周期表的一部分,表中序号分别代
表某一元素。请回答下列问题。
族
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
周期
2 ⑦ ⑧ ⑩3 ① ③ ⑤ ⑥ ⑨
4 ② ④
(1)①~⑩中,最活泼的金属元素是________(写元素符号,下同),最不活泼的元
素是________。
(2)①⑧的简单离子,其半径更大的是________(写离子符号)。
(3)⑧⑨的气态氢化物,更稳定的是________(填化学式)。
(4)元素的非金属性:⑥________⑦(填“>”或“<”)。
(5)①~⑨的最高价氧化物的水化物中:酸性最强的是________(填化学式);碱
性最强的是________(填化学式),该碱与⑤的最高价氧化物的水化物反应的离
子方程式为__
__。
12.(15分)(2019·兰州高一检测)现有下列短周期元素的数据(已知Be的原子
半径为0.089
nm):
① ② ③ ④ ⑤ ⑥ ⑦ ⑧
原子半径
0.074 0.160 0.152 0.110 0.099 0.186 0.075 0.082
(nm)
最高正
+2 +1 +5 +7 +1 +5 +3
化合价
最低负
-2 -3 -1 -3
化合价(1)⑧号元素在周期表中的位置是_______________________;
上述元素处于同一主族的有____________。(用元素符号表示)
(2)元素①和⑥能形成两种化合物,写出其中较稳定的化合物与水反应的离子方
程式: __________________________。
(3)含锂材料在社会中广泛应用,如各种储氢材料(Li NH等)、便携式电源材料
2
(LiCoO 等)。根据下列要求回答问题:
2
Li和 Li作核反应堆最佳热载体 LiH和 LiD用作高温堆减速剂。下列说
法正确的是________。
A Li和 Li互为同位素
B Li和 Li属于同种核素
C LiH和 LiD的化学性质不同
D LiH和 LiD是同种物质
②下列说法不正确的是________。
A.碱性:Be(OH) Na>Li>Li+C.氧化性:Li+Rb>K>Na>Li>Be
(20分钟 30分)
一、选择题(本题包括2小题,每小题9分,共18分)
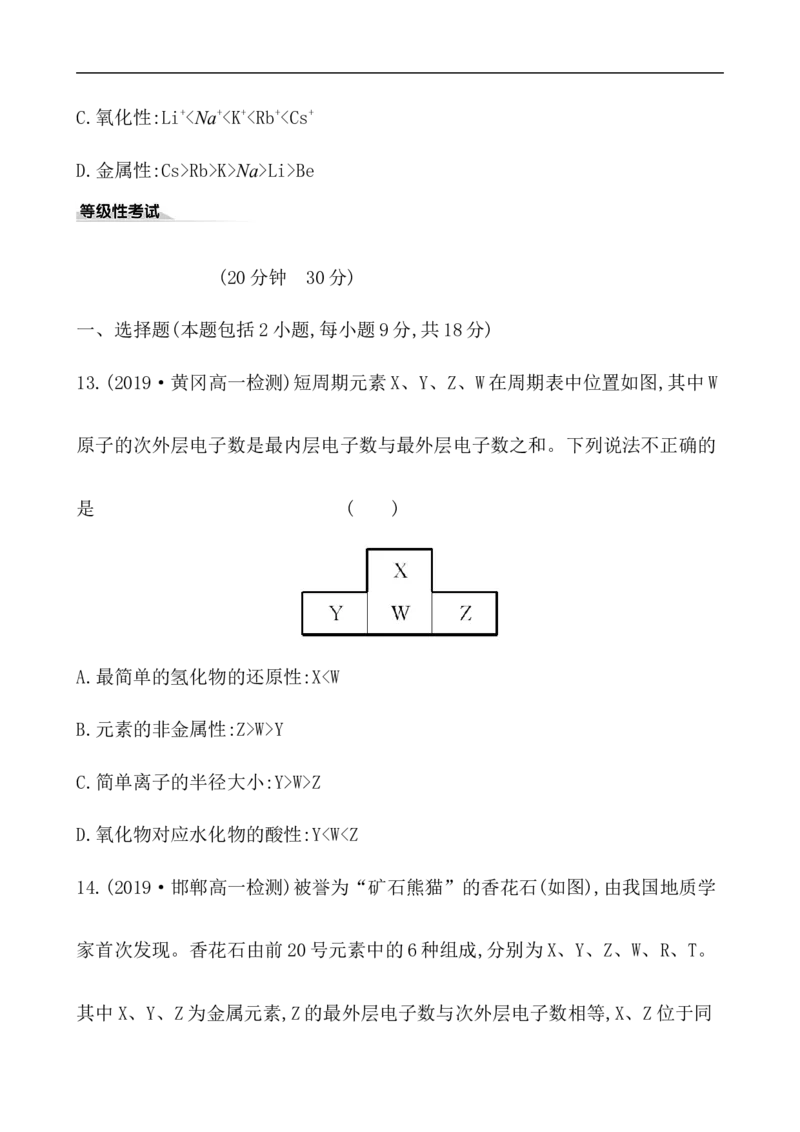
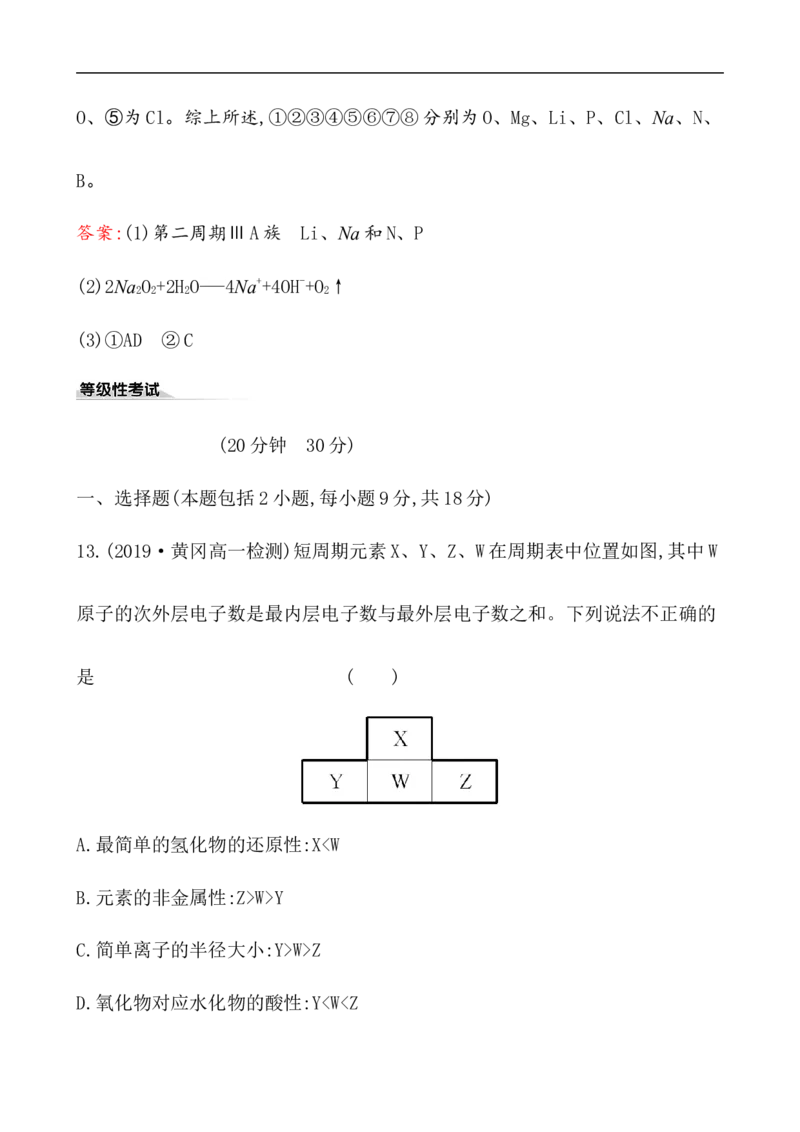
13.(2019·黄冈高一检测)短周期元素X、Y、Z、W在周期表中位置如图,其中W
原子的次外层电子数是最内层电子数与最外层电子数之和。下列说法不正确的
是 ( )
A.最简单的氢化物的还原性:XW>Y
C.简单离子的半径大小:Y>W>Z
D.氧化物对应水化物的酸性:YZ>R>T
B.气态氢化物的稳定性:WZ
D.XR 、WR 两种化合物中R的化合价相同
2 2
二、非选择题(本题包括1小题,共12分)
15.我国著名化学家张青莲精确地测定了锗(Ge)、锌等九种元素的相对原子质
量,得到的新值被作为国际新标准。已知锗的原子序数为32。
(1)锗位于元素周期表中第________周期__________________族。
(2)锗类似于铝,能溶于氢氧化钠溶液,其主要原因是
_。
①它与硅位于同一主族
②它与铝位于对角线位置,且性质相似
③它位于周期表中金属与非金属分界线附近④它位于边界线附近
⑤它是两性物质
(3)材料科学是目前全世界研究的热点,为了寻找半导体材料,科学家应在元素
周期表中某区域寻找元素组成材料,该区域是________。
A.左上角
B.右上角
C.过渡元素
D.金属与非金属分界线附近课时素养评价 二十四
元素周期表和元素周期律的应用
(40分钟 70分)
一、选择题(本题包括10小题,每小题4分,共40分)
1.(2019·北京西城区高一检测)英国研究人员认为,全球将有1.4亿人因为用水
受到砷中毒之害,导致更多的人患癌症。下列对砷(As)的有关判断正确的是
( )
A.砷原子序数为33,它与铝同主族
B.砷的原子半径小于磷的原子半径
C.砷化氢的稳定性比溴化氢的强
D.砷酸的酸性比硫酸的弱
【解析】选D。砷原子序数为33,位于第ⅤA族,A错;砷、磷同主族,砷的原子
半径大于磷的原子半径,B错;砷、溴同周期,砷的非金属性比溴弱,因此砷化氢的稳定性比溴化氢的弱,C错;由于非金属性S>P>As,因此砷酸的酸性比硫酸的弱,
D对。
【补偿训练】
已知 As、 Br位于同一周期。下列关系正确的是 ( )
33 35
A.原子半径:As>Cl>P
B.热稳定性:HCl>AsH >HBr
3
C.还原性:As3->S2->Cl-
D.酸性:H AsO >H SO >H PO
3 4 2 4 3 4
【解析】选C。A项,原子半径As>P>Cl;B项,非金属性Cl>Br>As,所以热稳定性
HCl>HBr>AsH ;D项,非金属性S>P>As,故酸性H SO >H PO >H AsO 。
3 2 4 3 4 3 4
2.某元素原子M层电子数是K层电子数的3.5倍,则该元素最高价氧化物对应水
化物的化学式为 ( )
A.HNO B.H PO
3 3 4
C.H SO D.HClO
2 4 4
【解析】选D。某元素原子M层电子数是K层电子数的3.5倍,则该原子M层电
子数为7,故M为氯元素;最高正化合价为+7,该元素最高价氧化物对应水化物的
化学式为HClO ,D正确。
43.(2019·青岛高一检测)根据原子结构及元素周期律的知识,下列推断正确的
是
( )
A.同主族元素含氧酸的酸性随核电荷数的增加而减弱
B.核外电子排布相同的微粒化学性质也相同
C.Cl-、S2-、Ca2+、K+半径逐渐减小
D Cl与 Cl得电子能力相同
【解析】选D。A项,同主族的非金属元素,从上到下非金属性逐渐减弱,其最高
价含氧酸的酸性依次减弱;B项,K+、Ca2+、S2-、Cl-的核外电子排布相同,但化学
性质不同,如S2-、Cl-具有还原性,而K+、Ca2+具有氧化性,错误;C项,具有相同电
子层结构的离子,核电荷数越大其微粒半径越小,则半径:S2->Cl->K+>Ca2+,错误;D
项, Cl属于同种元素,具有相同的核外电子排布,化学性质相同,原子
得电子能力相同,正确。
【补偿训练】
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说
法不合理的是 ( )A.由水溶液的酸性:HCl>HF,不能推断出元素的非金属性:Cl>F
B.人们可以在周期表的过渡元素中寻找催化剂和耐腐蚀、耐高温的合金材料
C.短周期元素正化合价数值和其族序数相同
D.短周期元素形成的微粒X2-和Y2+核外电子排布相同,离子半径:X2->Y2+
【解析】选C。A项,非金属性的强弱,应根据对应最高价氧化物对应水化物的酸
性比较,不能根据氢化物的酸性进行比较,HF的酸性比HCl弱,但非金属性F大
于Cl,正确;B项,优良的催化剂及耐高温和耐腐蚀的合金材料(如镍、铂等),大
多属于过渡元素,正确;C项,短周期元素正化合价数值和其族序数不一定相同,
如C有+2、+4价,错误;D项,微粒X2-与Y2+核外电子排布相同,核电荷数:Y>X,核
电荷数越大,离子半径越小,故离子半径:X2->Y2+,正确。
4.下列说法正确的是 ( )
A.N和As属于第ⅤA族元素,氮原子得电子能力比砷原子强
B.族序数等于其周期序数的元素一定是金属元素
C.元素周期表中,位于金属和非金属交界线附近的元素属于过渡元素
D.Si、S、Cl的最高价氧化物都能与水反应生成相应的酸,且酸性依次增强
【解析】选A。N和As属于第ⅤA族元素,同主族元素自上而下非金属性逐渐减
弱,所以氮原子得电子能力比砷原子强,A正确;族序数等于其周期序数的元素不一定是金属元素,如第一周期第ⅠA族的氢元素是非金属元素,B不正确;元素周
期表中,位于金属和非金属交界线附近的元素一般既具有金属性,还具有非金属
性。过渡元素是指周期表中第3~12列的元素,C不正确;二氧化硅与水不反
应,D不正确。
5.(2019·济南高一检测)已知某原子最外层有7个电子,推测下列选项不正确的
是 ( )
A.单质有氧化性
B.最高正价一定为+7价
C.是非金属元素
D.同周期元素中原子半径最小
【解析】选B。某原子的最外层有7个电子,说明位于第ⅦA族,ⅦA族元素得到
一个电子达到稳定结构,其单质具有强氧化性,故A说法正确;F没有正价,故B
说法错误;第ⅦA族为非金属元素,故C说法正确;同周期从左向右原子半径逐渐
减小(稀有气体除外),因此卤族元素的原子半径是同周期中最小的,故D说法正
确。6.镓是1871年俄国化学家门捷列夫在编制元素周期表时曾预言的“类铝”元素。
镓的原子序数为31,属ⅢA族。镓的熔点为29.78 ℃,沸点高达2 403 ℃。镓
有过冷现象(即冷至熔点下不凝固),它可过冷到-120 ℃。
由此判断下列有关镓的性质及其用途的叙述不正确的是( )
A.镓是制造高温温度计的上佳材料
B.镓能溶于强酸和强碱中
C.镓与锌、锡、铟等金属制成的合金,可用在自动救火的水龙头中
D.近年来,镓成为电子工业的新宠,其主要用途是制造半导体材料,被誉为“半
导体家族的新成员”,这是利用了镓的导电性介于导体和绝缘体之间的性质
【解析】选D。镓的熔点为29.78 ℃,沸点高达2 403 ℃;镓有过冷现象(即冷
至熔点下不凝固),它可过冷到-120 ℃,因此A、C两项正确。铝能溶于强酸和强
碱中,铝是电的良导体而不是半导体,镓是“类铝”元素,所以镓能溶于强酸和
强碱中,镓是电的良导体而不是半导体,即B项正确,D项不正确。
7.(2019·贵阳高一检测)不能作为判断硫、氯两种元素非金属性强弱的依据是( )
A.单质氧化性的强弱
B.单质沸点的高低
C.单质与氢气化合的难易
D.最高价氧化物对应的水化物酸性的强弱
【解析】选B。元素的非金属性越强,其单质获得电子的能力就越强,因此单质
氧化性就越强,故可以通过比较单质氧化性的强弱,判断元素的非金属性的强弱,
A正确。S单质,Cl 都是分子晶体,分子之间通过分子间作用力结合,分子间作用
2
力越大,物质的熔沸点就越高,这与元素的非金属性强弱无关,B错误。元素的非
金属性越强,其单质与氢气化合形成氢化物就越容易,形成的氢化物的稳定性就
越强,因此,可以比较元素的非金属性的强弱,C正确。元素的非金属性越强,其
最高价氧化物对应的水化物的酸性就越强,因此可以通过比较硫、氯两种元素
最高价氧化物对应的水化物酸性的强弱比较元素的非金属性的强弱,D正确。
8.锗是一种重要的半导体材料,用于制造晶体管及各种电子装置。门捷列夫把
它命名为类硅,处于周期表中金属区与非金属区的交界线上。下列叙述正确的是 ( )
A.锗是一种金属性很强的元素
B.锗的单质具有半导体的性能
C.锗化氢(GeH )稳定性很强
4
D.锗酸是难溶于水的强酸
【解析】选B。锗处于金属区与非金属区的交界线上,元素金属性和非金属性都
较弱,反应中既不易得电子,也不易失去电子,常用作半导体材料;锗化氢(GeH )
4
稳定性很弱;锗和硅处于同一主族,主族元素的非金属性从上到下逐渐减弱,则
硅的非金属性大于锗,非金属性越强,对应的最高价氧化物的水化物的酸性越强,
所以酸性比硅酸弱,为弱酸,碳酸溶于水,硅酸不溶于水,推知锗酸应难溶于水,
故D错误。
【方法规律】推断陌生元素性质的“3”个角度
(1)与同周期前、后元素相比较,根据同周期元素性质的递变规律推测元素的性
质。(2)与同主族上、下元素相比较,依据同主族元素性质的递变规律推测元素的性
质。
(3)比较不同周期、不同主族元素的性质时,可借助“三角”规律推断
若A、B、C三种元素位于元素周期表中如图所示位置,有关元素的各种性质均可
排出顺序(但D不能参与排序)。
①原子半径:C>A>B;
②金属性:C>A>B;
③非金属性:B>A>C。
9.(2019·大连高一检测)X、Y、Z、W为周期表中前20号元素中的四种,原子序
数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3
倍,Y、Z位于同周期,Z单质是一种良好的半导体。W能与冷水剧烈反应,Y、Z原
子的最外层电子数之和与X、W原子的最外层电子数之和相等。下列说法正确的
是
( )A.原子半径:W>Y>Z>X
B.气态氢化物的稳定性:XW
D.Y、Z的氧化物均为两性氧化物
【解析】选A。由题意可推出X为O,Y为Al,Z为Si,W为K。B项,气态氢化物的
稳定性是H O>SiH ,错误;C项,最高价氧化物对应的水化物的碱性:KOH>Al(OH) ,
2 4 3
错误;D项,Y的氧化物Al O 有两性,而Z的氧化物SiO 不具有两性,它是酸性氧
2 3 2
化物,错误。
10.(2019·洛阳高一检测)如图所示是元素周期表的一部分,下列说法中正确的
是 ( )
A.元素的简单离子半径大小:④>⑤>②
B.气态氢化物的稳定性:⑤>②
C.最高价氧化物对应水化物的酸性:⑥>⑤D.元素的最高正化合价:③=⑥
【解析】选C。元素①~⑥分别为N、O、F、Al、S、Cl。离子半径:S2->O2-
>Al3+,A项错误;非金属性越强则对应气态氢化物越稳定,最高价氧化物对应水化
物的酸性也越强,故稳定性:H O>H S,酸性:HClO >H SO ,B项错误,C项正确;F无
2 2 4 2 4
正价,D项错误。
二、非选择题(本题包括2小题,共30分)
11.(15分)(2019·襄樊高一检测)下表为元素周期表的一部分,表中序号分别代
表某一元素。请回答下列问题。
族
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
周期
2 ⑦ ⑧ ⑩
3 ① ③ ⑤ ⑥ ⑨
4 ② ④
(1)①~⑩中,最活泼的金属元素是________(写元素符号,下同),最不活泼的元
素是________。
(2)①⑧的简单离子,其半径更大的是________(写离子符号)。
(3)⑧⑨的气态氢化物,更稳定的是________(填化学式)。
(4)元素的非金属性:⑥________⑦(填“>”或“<”)。(5)①~⑨的最高价氧化物的水化物中:酸性最强的是________(填化学式);碱
性最强的是________(填化学式),该碱与⑤的最高价氧化物的水化物反应的离
子方程式为__
__。
【解析】(1)由表知最活泼的金属元素是在元素周期表中第ⅠA族,最下方的②
为K,最不活泼的元素在元素周期表中的0族,由表知⑩为Ne。(2)由表知①为
Na、⑧为F,它们的简单离子Na+、F-的核外电子排布相同,且钠的原子序数比氟
大,所以r(Na+)Na>Li>Li+
C.氧化性:Li+Rb>K>Na>Li>Be
【解析】由题中及表中数据可知,①②③④⑤⑥⑦⑧分别位于第ⅥA、第ⅡA、
第ⅠA、第ⅤA、第ⅦA、第ⅠA、第ⅤA、第ⅢA族。Be的原子半径为0.089
nm,Be的最高价为+2,②的最高价也是+2、半径比Be大,则②为Mg;③是最高价
为+1、半径比Mg小,则③是Li;⑥是最高价为+1、半径比Mg大,则⑥为Na;④
和⑦的最高价都是+5、最低价都是-3,则它们为第ⅤA族元素,因为④的半径较
大,故④为P、⑦为N;根据同周期元素的原子半径逐渐减小,可知⑧为B、①为O、⑤为Cl。综上所述,①②③④⑤⑥⑦⑧分别为O、Mg、Li、P、Cl、Na、N、
B。
答案:(1)第二周期ⅢA族 Li、Na和N、P
(2)2Na O +2H O 4Na++4OH-+O ↑
2 2 2 2
(3)①AD ②C
(20分钟 30分)
一、选择题(本题包括2小题,每小题9分,共18分)
13.(2019·黄冈高一检测)短周期元素X、Y、Z、W在周期表中位置如图,其中W
原子的次外层电子数是最内层电子数与最外层电子数之和。下列说法不正确的
是 ( )
A.最简单的氢化物的还原性:XW>Y
C.简单离子的半径大小:Y>W>Z
D.氧化物对应水化物的酸性:YW>Y,B正确;具有相同电子排布的离子中,原子序数大的离
子半径小,则简单离子的半径大小:Y>W>Z,C正确;非金属性越强,对应最高价含
氧酸的酸性越强,不是最高价含氧酸无此规律,如硫酸为强酸,HClO为弱酸,D错
误。
14.(2019·邯郸高一检测)被誉为“矿石熊猫”的香花石(如图),由我国地质学
家首次发现。香花石由前20号元素中的6种组成,分别为X、Y、Z、W、R、T。
其中X、Y、Z为金属元素,Z的最外层电子数与次外层电子数相等,X、Z位于同
族,Y、Z、R、T位于同周期,R最外层电子数是次外层的3倍,T无正价,X与R原
子序数之和是W的2倍。下列说法错误的是 ( )
A.原子半径:Y>Z>R>TB.气态氢化物的稳定性:WZ
D.XR 、WR 两种化合物中R的化合价相同
2 2
【解析】选D。“矿石熊猫”香花石由前20号元素中的6种组成,其中R原子最
外层电子数为其次外层电子数的3倍,R原子只能有2个电子层,最外层电子数
为6,则R为O;Y、Z、R、T位于同周期,即处于第二周期,T无正价,则T为F;Z
的最外层电子数与次外层电子数相等,则Z为Be;Y为金属元素,则Y为Li;X、Z
位于同主族,则X为Mg或Ca,若X为镁元素,则由X与R原子序数之和是W的2
倍,则 =10,推出W为氖元素不符合题意,若X为钙元素,则由X与R原子序数
之和是W的2倍,则 =14,推出W为Si,符合题意。Y为锂元素、Z为铍元素、
R为氧元素、T为氟元素,位于同周期,元素的原子半径从左向右半径在减小,即
原子半径:Y>Z>R>T,选项A正确;W为硅元素、R为氧元素、T为氟元素,非金属
性F>O>Si,则气态氢化物的稳定性WBe,则最高价氧化物对应的水化物的碱性:氢氧化钙>氢氧化铍,选项C正确;XR 、WR 两化合物分别为CaO 、SiO ,CaO 中O为-1价,SiO 中O为-2价,
2 2 2 2 2 2
选项D错误。
二、非选择题(本题包括1小题,共12分)
15.我国著名化学家张青莲精确地测定了锗(Ge)、锌等九种元素的相对原子质
量,得到的新值被作为国际新标准。已知锗的原子序数为32。
(1)锗位于元素周期表中第________周期__________________族。
(2)锗类似于铝,能溶于氢氧化钠溶液,其主要原因是
_。
①它与硅位于同一主族
②它与铝位于对角线位置,且性质相似
③它位于周期表中金属与非金属分界线附近
④它位于边界线附近
⑤它是两性物质
(3)材料科学是目前全世界研究的热点,为了寻找半导体材料,科学家应在元素
周期表中某区域寻找元素组成材料,该区域是________。
A.左上角
B.右上角C.过渡元素
D.金属与非金属分界线附近
【解析】根据元素周期表的结构可知,锗属于第四周期第ⅣA族元素。锗位于元
素周期表中金属与非金属分界线附近,它具有某些金属元素的性质,又具有某些
非金属元素的性质,它是金属元素,但不能说锗是两性物质,因两性物质是指既
能溶于强酸又能溶于强碱且都生成盐和水的物质,如氧化铝、氢氧化铝。
答案:(1)四 ⅣA (2)②③ (3)D