文档内容
课堂检测·素养达标
1.(教材改编)下列各组物质中,每种物质都是既有离子键又有共价键的一组是
( )
A.NaOH H SO (NH ) SO
2 4 4 2 4
B.MgO Na SO HNO
2 4 3
C.Na O KOH Na PO
2 2 3 4
D.HCl Na O MgCl
2 2
2.(2019·济南高一检测)关于共价键的说法正确的是 ( )
A.金属原子在化学反应中只能失去电子,因而不能形成共价键
B.由共价键形成的分子可以是单质分子,也可以是化合物分子
C.共价键只能在不同原子之间形成
D.稀有气体分子中只存在共价键
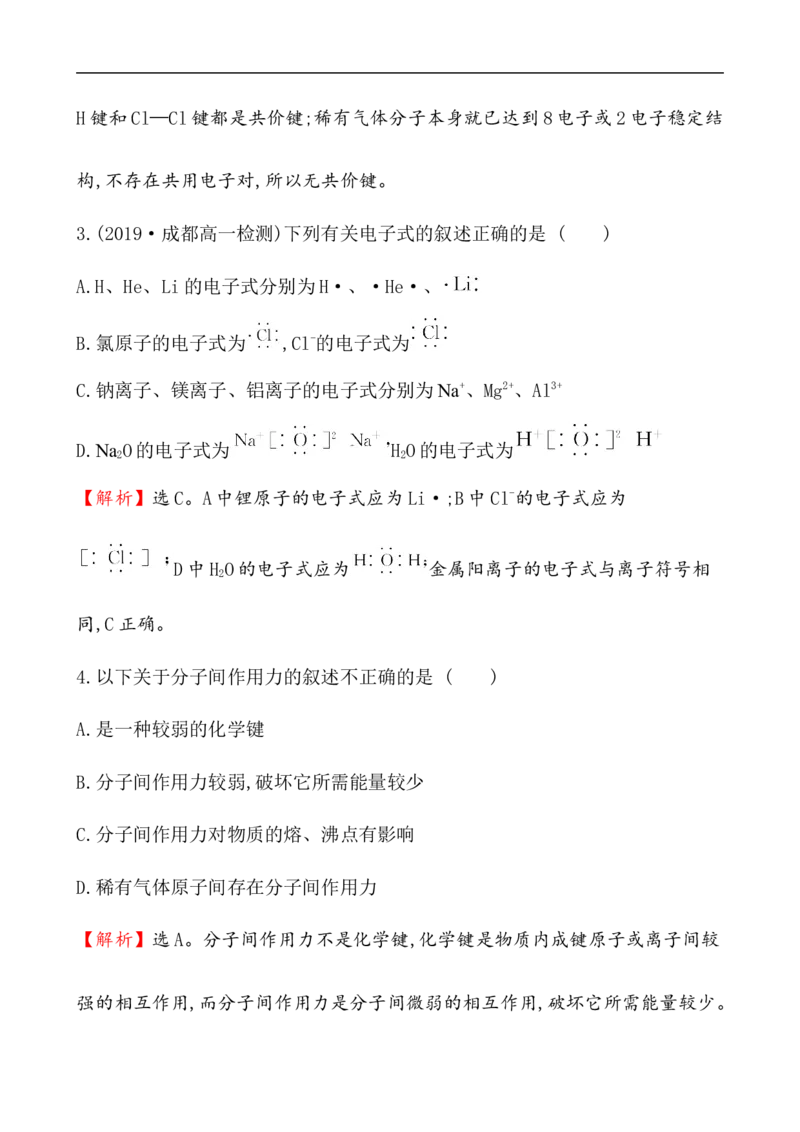
3.(2019·成都高一检测)下列有关电子式的叙述正确的是 ( )
A.H、He、Li的电子式分别为H·、·He·、
B.氯原子的电子式为 ,Cl-的电子式为
C.钠离子、镁离子、铝离子的电子式分别为Na+、Mg2+、Al3+
D.Na O的电子式为 H O的电子式为
2 2
4.以下关于分子间作用力的叙述不正确的是 ( )A.是一种较弱的化学键
B.分子间作用力较弱,破坏它所需能量较少
C.分子间作用力对物质的熔、沸点有影响
D.稀有气体原子间存在分子间作用力
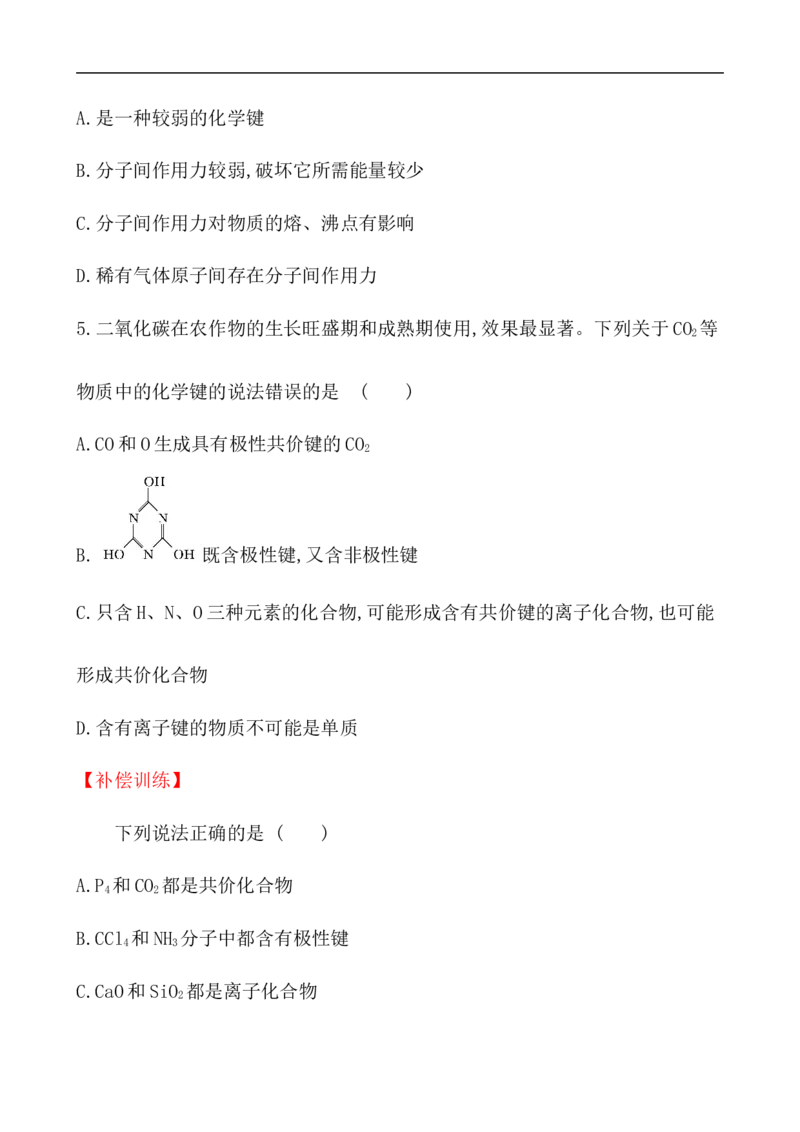
5.二氧化碳在农作物的生长旺盛期和成熟期使用,效果最显著。下列关于CO 等
2
物质中的化学键的说法错误的是 ( )
A.CO和O生成具有极性共价键的CO
2
B. 既含极性键,又含非极性键
C.只含H、N、O三种元素的化合物,可能形成含有共价键的离子化合物,也可能
形成共价化合物
D.含有离子键的物质不可能是单质
【补偿训练】
下列说法正确的是 ( )
A.P 和CO 都是共价化合物
4 2
B.CCl 和NH 分子中都含有极性键
4 3
C.CaO和SiO 都是离子化合物
2D.NaOH是离子化合物,只含有离子键
6.(新思维·新考向)某汽车安全气囊的产气药剂主要含有NaN 、Fe O 、
3 2 3
KClO 、NaHCO 等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速
4 3
膨胀,从而起到保护作用。
(1)NaN 是气体发生剂,受热分解产生N 和Na,NaN 属于离子化合物还是共价化
3 2 3
合物?并写出N 的电子式。
2
(2)Fe O 是主氧化剂,与Na发生置换反应,其还原产物是什么?
2 3
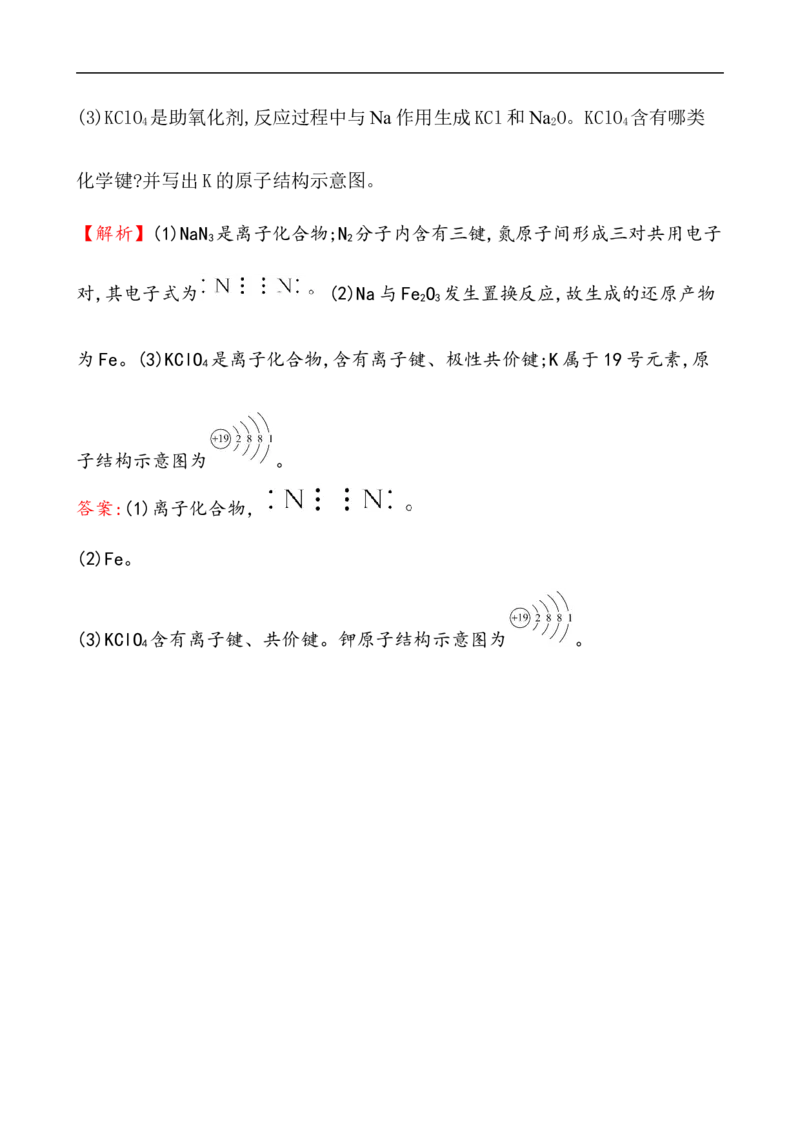
(3)KClO 是助氧化剂,反应过程中与Na作用生成KCl和Na O。KClO 含有哪类
4 2 4
化学键?并写出K的原子结构示意图。课堂检测·素养达标
1.(教材改编)下列各组物质中,每种物质都是既有离子键又有共价键的一组是
( )
A.NaOH H SO (NH ) SO
2 4 4 2 4
B.MgO Na SO HNO
2 4 3
C.Na O KOH Na PO
2 2 3 4
D.HCl Na O MgCl
2 2
【解析】选C。H SO 中只有共价键,A错误;MgO中只有离子键,HNO 中只有共价
2 4 3
键,B错误;各物质中既有离子键又有共价键,C正确;HCl中只有共价键,Na O、
2
MgCl 中只有离子键,D错误。
2
2.(2019·济南高一检测)关于共价键的说法正确的是 ( )
A.金属原子在化学反应中只能失去电子,因而不能形成共价键
B.由共价键形成的分子可以是单质分子,也可以是化合物分子
C.共价键只能在不同原子之间形成
D.稀有气体分子中只存在共价键
【解析】选B。金属和非金属化合时也能形成共价键,如AlCl 分子中的Al—Cl
3
键是共价键;在H 、O 、N 、HCl、NH 分子中均存在共价键;H 、Cl 分子中的H—
2 2 2 3 2 2H键和Cl—Cl键都是共价键;稀有气体分子本身就已达到8电子或2电子稳定结
构,不存在共用电子对,所以无共价键。
3.(2019·成都高一检测)下列有关电子式的叙述正确的是 ( )
A.H、He、Li的电子式分别为H·、·He·、
B.氯原子的电子式为 ,Cl-的电子式为
C.钠离子、镁离子、铝离子的电子式分别为Na+、Mg2+、Al3+
D.Na O的电子式为 H O的电子式为
2 2
【解析】选C。A中锂原子的电子式应为Li·;B中Cl-的电子式应为
D中H O的电子式应为 金属阳离子的电子式与离子符号相
2
同,C正确。
4.以下关于分子间作用力的叙述不正确的是 ( )
A.是一种较弱的化学键
B.分子间作用力较弱,破坏它所需能量较少
C.分子间作用力对物质的熔、沸点有影响
D.稀有气体原子间存在分子间作用力
【解析】选A。分子间作用力不是化学键,化学键是物质内成键原子或离子间较
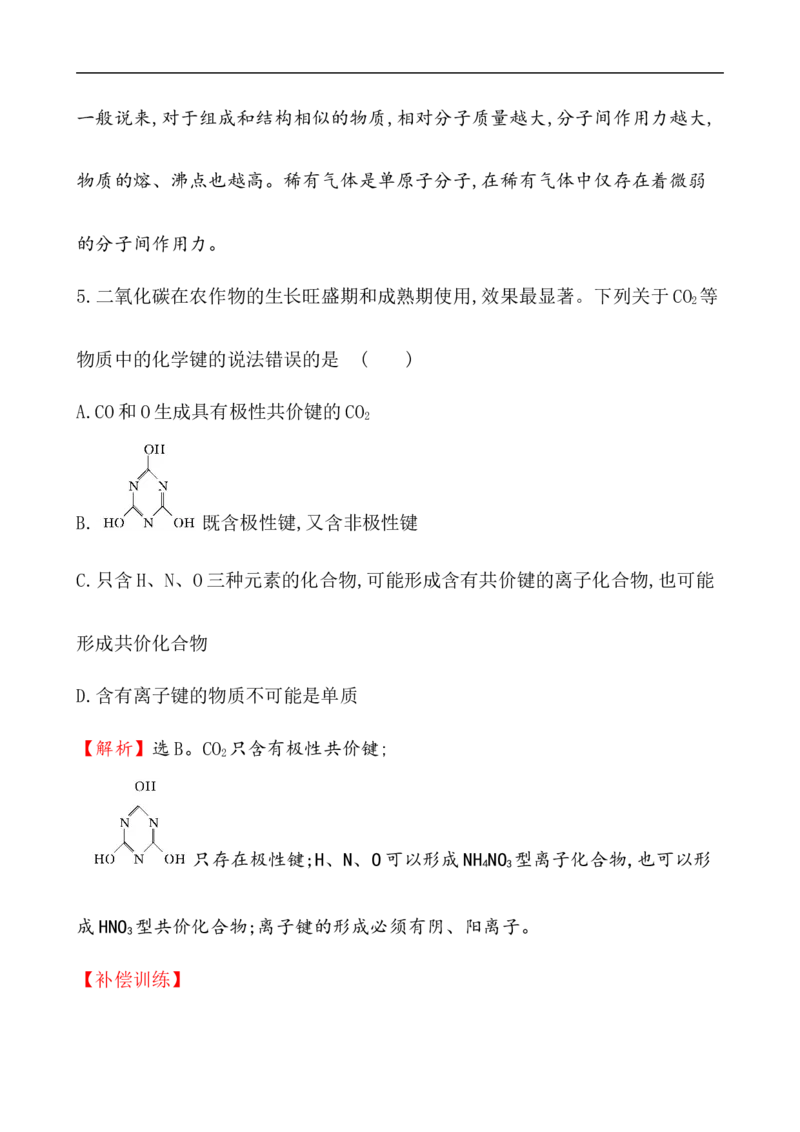
强的相互作用,而分子间作用力是分子间微弱的相互作用,破坏它所需能量较少。一般说来,对于组成和结构相似的物质,相对分子质量越大,分子间作用力越大,
物质的熔、沸点也越高。稀有气体是单原子分子,在稀有气体中仅存在着微弱
的分子间作用力。
5.二氧化碳在农作物的生长旺盛期和成熟期使用,效果最显著。下列关于CO 等
2
物质中的化学键的说法错误的是 ( )
A.CO和O生成具有极性共价键的CO
2
B. 既含极性键,又含非极性键
C.只含H、N、O三种元素的化合物,可能形成含有共价键的离子化合物,也可能
形成共价化合物
D.含有离子键的物质不可能是单质
【解析】选B。CO 只含有极性共价键;
2
只存在极性键;H、N、O可以形成NH NO 型离子化合物,也可以形
4 3
成HNO 型共价化合物;离子键的形成必须有阴、阳离子。
3
【补偿训练】下列说法正确的是 ( )
A.P 和CO 都是共价化合物
4 2
B.CCl 和NH 分子中都含有极性键
4 3
C.CaO和SiO 都是离子化合物
2
D.NaOH是离子化合物,只含有离子键
【解析】选B。P 和CO 分子中都含有共价键,但P 是磷的单质,A项错误;CCl 、
4 2 4 4
NH 分子中都含有极性键,B项正确;CaO是离子化合物,SiO 是共价化合物,C项错
3 2
误;NaOH中既含有离子键,又含有共价键,D项错误。
6.(新思维·新考向)某汽车安全气囊的产气药剂主要含有NaN 、Fe O 、
3 2 3
KClO 、NaHCO 等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速
4 3
膨胀,从而起到保护作用。
(1)NaN 是气体发生剂,受热分解产生N 和Na,NaN 属于离子化合物还是共价化
3 2 3
合物?并写出N 的电子式。
2
(2)Fe O 是主氧化剂,与Na发生置换反应,其还原产物是什么?
2 3(3)KClO 是助氧化剂,反应过程中与Na作用生成KCl和Na O。KClO 含有哪类
4 2 4
化学键?并写出K的原子结构示意图。
【解析】(1)NaN 是离子化合物;N 分子内含有三键,氮原子间形成三对共用电子
3 2
对,其电子式为 (2)Na与Fe O 发生置换反应,故生成的还原产物
2 3
为Fe。(3)KClO 是离子化合物,含有离子键、极性共价键;K属于19号元素,原
4
子结构示意图为 。
答案:(1)离子化合物,
(2)Fe。
(3)KClO 含有离子键、共价键。钾原子结构示意图为 。
4