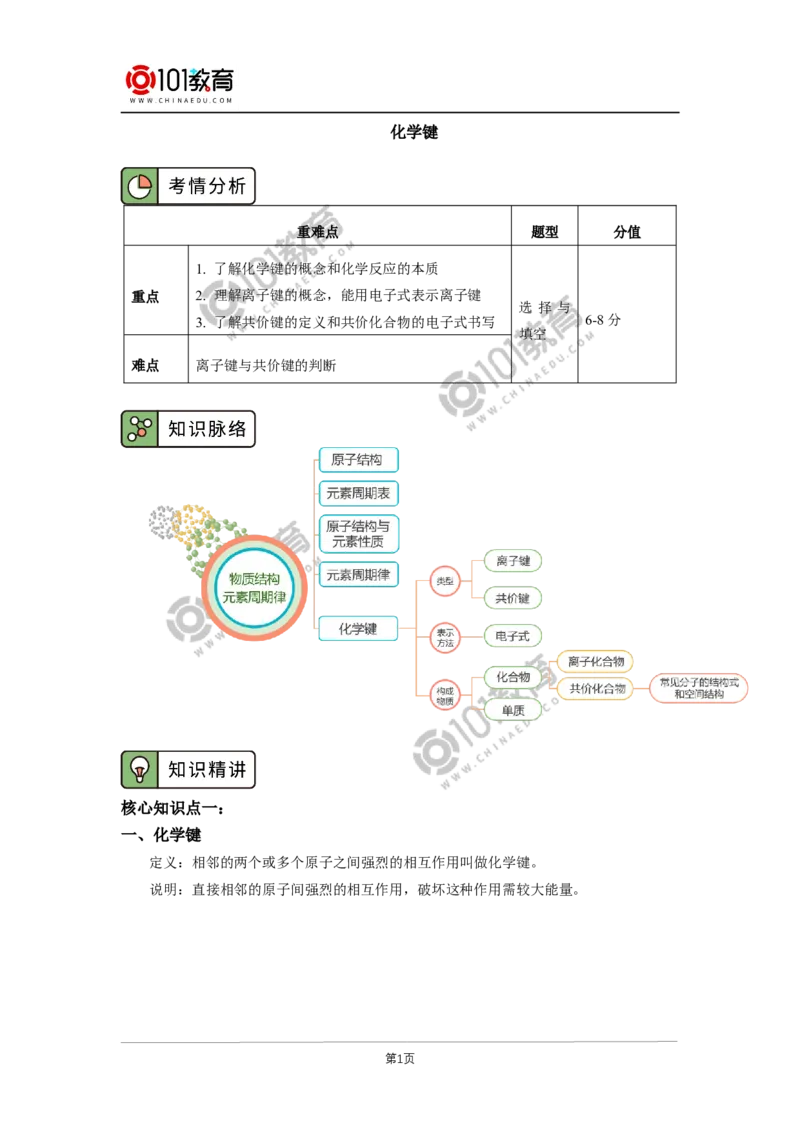
文档内容
化学键
重难点 题型 分值
1. 了解化学键的概念和化学反应的本质
重点 2. 理解离子键的概念,能用电子式表示离子键
选 择 与
3. 了解共价键的定义和共价化合物的电子式书写 6-8分
填空
难点 离子键与共价键的判断
核心知识点一:
一、化学键
定义:相邻的两个或多个原子之间强烈的相互作用叫做化学键。
说明:直接相邻的原子间强烈的相互作用,破坏这种作用需较大能量。
第1页二、离子键
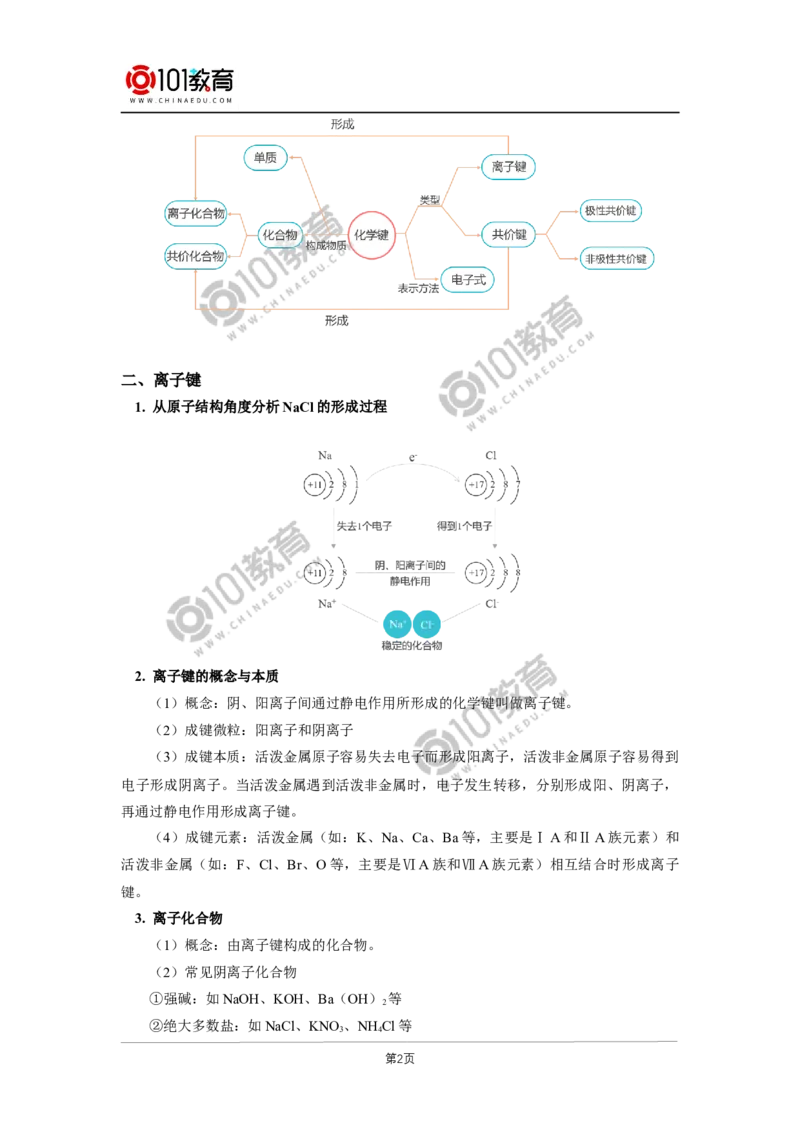
1. 从原子结构角度分析NaCl的形成过程
2. 离子键的概念与本质
(1)概念:阴、阳离子间通过静电作用所形成的化学键叫做离子键。
(2)成键微粒:阳离子和阴离子
(3)成键本质:活泼金属原子容易失去电子而形成阳离子,活泼非金属原子容易得到
电子形成阴离子。当活泼金属遇到活泼非金属时,电子发生转移,分别形成阳、阴离子,
再通过静电作用形成离子键。
(4)成键元素:活泼金属(如:K、Na、Ca、Ba等,主要是ⅠA和ⅡA族元素)和
活泼非金属(如:F、Cl、Br、O等,主要是ⅥA族和ⅦA族元素)相互结合时形成离子
键。
3. 离子化合物
(1)概念:由离子键构成的化合物。
(2)常见阴离子化合物
①强碱:如NaOH、KOH、Ba(OH) 等
2
②绝大多数盐:如NaCl、KNO、NH Cl等
3 4
第2页③金属氧化物:如NaO、CaO、MgO等
2
4. 电子式的几种表示方法
(1)离子
单核阳离子符号,即为阳离子的电子式,如H+、K+、Na+、Mg2+;原子团的阳离子;
复杂阴、阳离子。
(2)离子化合物
KS、CaC 、CaO、CaF 、NaO、NH Cl
2 2 2 2 2 4
5. 离子键与离子化合物的关系
(1)三个“一定”
①含有离子键的化合物一定是离子化合物
②离子化合物中一定含有离子键
③离子化合物中一定含有阴离子和阳离子
(2)两个“不一定”
①离子化合物中不一定含有金属元素
②含有金属元素的化合物不一定是离子化合物
核心知识点二:
一、共价键
定义:原子间通过共用电子对所形成的化学键叫共价键。
说明:①成键元素:通常为非金属元素的原子间。②成键原因:同种或不同种元素的
原子之间结合成分子时并不发生电子的完全得失,而是通过共用电子对而结合的。③共价
键可以形成单质也可形成化合物。
非极性键:同种元素的原子之间形成的共价键称非极性共价键,简称非极性键。
极性键:不同元素的原子之间形成的共价键称极性共价键,简称极性键。
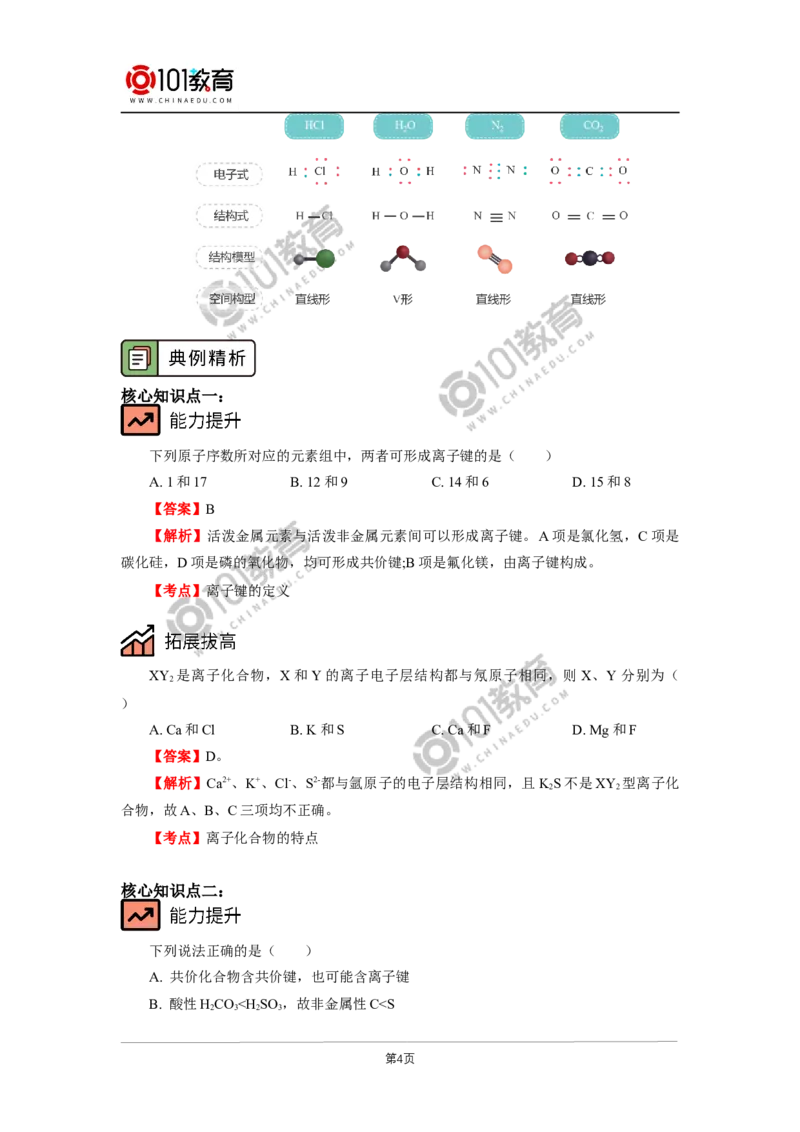
二、常见共价化合物
三、共价化合物的几种表现形式。
第3页核心知识点一:
下列原子序数所对应的元素组中,两者可形成离子键的是( )
A. 1和17 B. 12和9 C. 14和6 D. 15和8
【答案】B
【解析】活泼金属元素与活泼非金属元素间可以形成离子键。A项是氯化氢,C项是
碳化硅,D项是磷的氧化物,均可形成共价键;B项是氟化镁,由离子键构成。
【考点】离子键的定义
XY 是离子化合物,X和Y的离子电子层结构都与氖原子相同,则 X、Y分别为(
2
)
A. Ca和Cl B. K和S C. Ca和F D. Mg和F
【答案】D。
【解析】Ca2+、K+、Cl-、S2-都与氩原子的电子层结构相同,且KS不是XY 型离子化
2 2
合物,故A、B、C三项均不正确。
【考点】离子化合物的特点
核心知识点二:
下列说法正确的是( )
A. 共价化合物含共价键,也可能含离子键
B. 酸性HCO