文档内容
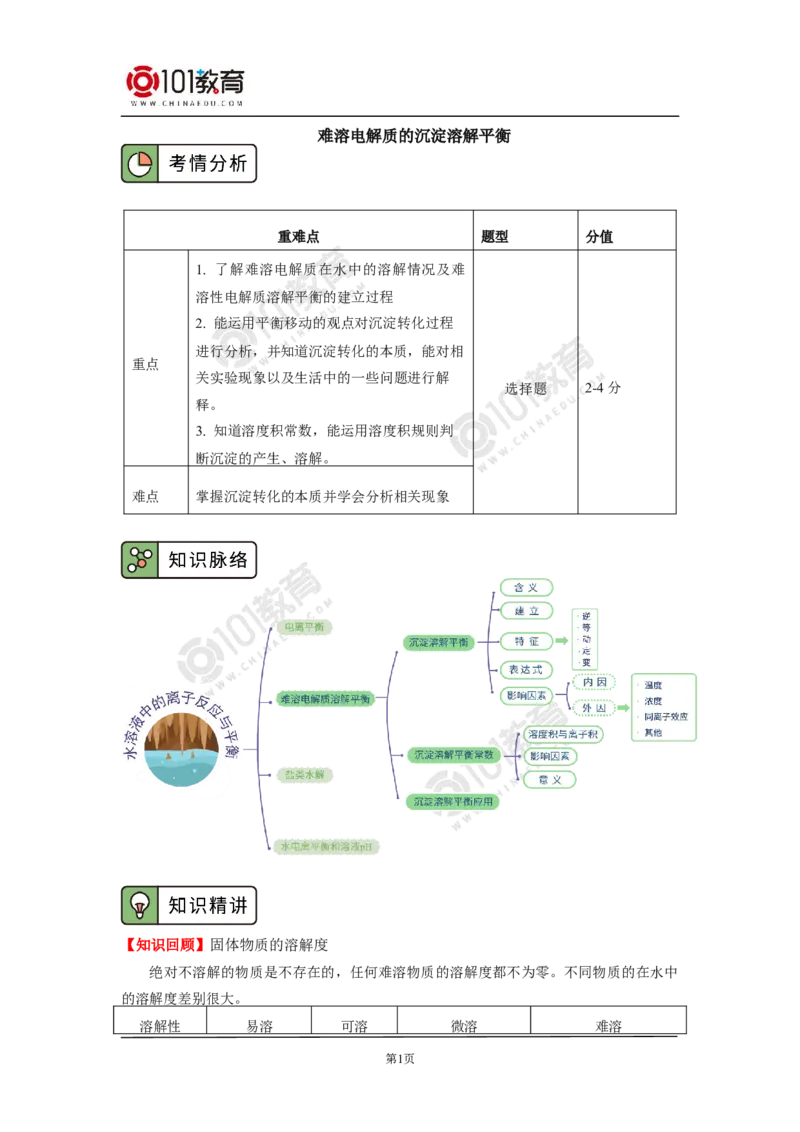
难溶电解质的沉淀溶解平衡
重难点 题型 分值
1. 了解难溶电解质在水中的溶解情况及难
溶性电解质溶解平衡的建立过程
2. 能运用平衡移动的观点对沉淀转化过程
进行分析,并知道沉淀转化的本质,能对相
重点
关实验现象以及生活中的一些问题进行解
选择题 2-4分
释。
3. 知道溶度积常数,能运用溶度积规则判
断沉淀的产生、溶解。
难点 掌握沉淀转化的本质并学会分析相关现象
【知识回顾】固体物质的溶解度
绝对不溶解的物质是不存在的,任何难溶物质的溶解度都不为零。不同物质的在水中
的溶解度差别很大。
溶解性 易溶 可溶 微溶 难溶
第1页溶解度 >10g 1~10g 0.01~1g <0.01g
实例 AgNO、NaCl NaHCO CaSO 、Ca(OH) AgCl、CaCO 、BaSO
3 3 4 3 4
2
一、沉淀溶解平衡
1. 沉淀溶解平衡的含义
在一定温度下,难溶电解质溶解的速率和沉淀的生成速率相等时,形成饱和溶液,达
到平衡状态,即达到沉淀溶解平衡状态。
如AgCl沉淀体系中的溶解平衡可表示为 AgCl(s) Cl - ( aq )+ Ag + ( aq ) 。
由于沉淀、溶解之间的这种动态平衡的存在,决定了Ag+和Cl-的反应不能完全进行到底。
2. 沉淀溶解平衡的建立(还是以AgCl为例)
从固体溶解平衡的角度,AgCl在溶液中存在下述两个过程:一方面,在水分子作用下,
少量 Ag + 与 C l - 脱离 AgC l 的表面进入 H O 中 ;另一方面,溶液中的Ag+和Cl-受AgCl表
2
面阴、阳离子的吸引, 回到 AgC l 的表面析出沉淀 。
3. 沉淀溶解平衡的特征
【归纳1】v 与v 的相对大小与沉淀溶解、生成的关系
溶解 沉淀
(1)v >v 沉淀溶解
溶解 沉淀
(2)v =v 溶解平衡
溶解 沉淀
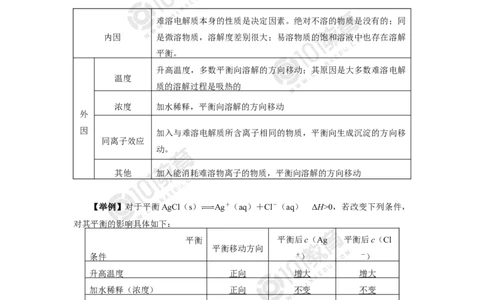
(3)v 0,若改变下列条件,
对其平衡的影响具体如下:
平衡 平衡后c(Ag 平衡后c(Cl
平衡移动方向
条件 +) -)
升高温度 正向 增大 增大
加水稀释(浓度) 正向 不变 不变
加NaCl(s)(同离子效应) 逆向 减小 增大
加少量AgNO(同离子效应) 逆向 增大 减小
3
通入HS(其他) 正向 减小 增大
2
【注意】(1)升高温度,少数平衡向生成沉淀的方向移动,如Ca(OH) 的溶解平衡。
2
(2)沉淀溶解平衡遵循勒夏特列原理,如将难溶电解质溶液加水稀释,相当于“对有
气体参与的化学平衡体系增大反应容器的容积”,所以溶解平衡向生成离子数目增多的方
向(即溶解的方向)移动。
第3页二、沉淀溶解平衡常数
与电离平衡、水解平衡一样,难溶电解质的沉淀总结平衡也存在平衡常数,称为溶度
积常数,简称溶度积,符号为Ksp。
1. 溶度积与离子积
以A B (s) mAn+(aq)+nBm-(aq)为例:
m n
溶度积 离子积
在一定温度下,沉淀达溶解平衡后的溶
液为饱和溶液,其离子浓度不再发生变
概念 溶液中有关离子浓度幂的乘积
化,溶液中各离子浓度幂之积为常数,
叫做溶度积常数(简称溶度积),
符号 K Q
sp
K = c m ( A n + ) · c n ( B m - ) 式中的浓度 Q = c m ( A n + ) · c n ( B m - )式中的
sp sp
表达式
是平衡浓度 浓度是任意时刻的浓度 【注意 2 】
通过比较溶度积和离子积的相对大小,
判断在一定条件下沉淀能否生成或溶解
①Q>Ksp:溶液过饱和,有沉淀析出
应用
②Q = Ksp:溶液饱和,处于平衡状
态
③Q<Ksp:溶液未饱和,无沉淀析出
【注意】2离子积Q与溶度积Ksp的表达式相同,但意义不同。Q表达式中的离子浓度可
以是任意时刻的浓度,其数值不定;K 表达式中的离子浓度是指平衡时的浓度,在一定温
sp
度下,K 为定值。
sp
【问题探究】1
影响PbI (s) Pb2+(aq)+2I-(aq)平衡的因素:
2
(1)你预测一下将观察到什么现象?
提示:产生黄色沉淀。
第4页(2)请你用平衡移动的理论和K 与Q之间的关系,解释你的预测。
sp
提示:平衡移动理论方面:滴加KI浓溶液,I-的浓度增大,使平衡PbI (s) Pb2+
2
(aq)+2I-(aq)向左移动,产生PbI 沉淀。
2
2
利用K 与Q之间的关系:K =c (Pb2+)·c平(I-),滴加KI浓溶液,I-的浓度增
sp sp 平
大,Q>K ,平衡向左移动,产生PbI 固体。
sp 2
【问题探究】2
在T ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知 T ℃时AgCl的K =
sp
4×10-10。
[问题1] T ℃时,K (AgBr)等于多少?
sp
提示:K (AgBr)=c(Ag+)·c(Br-)=7×10-7×7×10-7=4.9×10-13。
sp
[问题2] 相同温度下,AgCl和AgBr的溶解度相对大小关系如何?
提示:Q(AgCl)>Q(AgBr)
[问题3] a点是否有沉淀析出?b点是否有沉淀析出?
提示:a点:QK ,溶液过饱和,有沉淀
sp sp
析出。
[问题4] 采取什么措施可以使溶液由c点到d点?该过程中K (AgBr)是否变化?
sp
提示:增大c(Br-);不变化。
2. 溶度积的影响因素
(1)内因
难溶电解质本身的性质,这是主要决定因素。
(2)外因
K 只受温度的影响(通常随温度的升高而增大),在一定温度下,K 是一个常数。
sp sp
【注意】溶度积的大小只与难溶电解质本身的性质和温度有关,与浓度无关。
3. 溶度积的意义
(1)K 的大小反映难溶电解质的溶解能力,通常K 越小,说明难溶物越难溶解。
sp sp
(2)相同类型的物质,溶度积越小,其溶解度越小。
【易错】2 溶度积与溶解度都可用于表示物质的溶解能力,利用 K 大小判断难溶电
sp
第5页解质在溶液中溶解能力的大小时需注意:
①对于同类型的物质(难溶电解质化学式所表示的组成中阴、阳离子个数比相同),
K 越小,则难溶电解质在水中的溶解能力就越弱。
sp
如由K 数值可知,溶解能力:AgCl>AgBr>AgI,Cu(OH)<Mg(OH)。
sp 2 2
②对于不同类型的物质,K 不能直接用于判断溶解能力的强弱,而应通过计算将 K
sp sp
转化为饱和溶液中溶质的物质的量浓度进而确定溶解能力的强弱。
如(25 ℃):AgCl(s) Ag+(aq)+Cl-(aq) K =1.8×10-10
sp
Mg(OH)(s) Mg2+(aq)+2OH-(aq) K =1.8×10-11
2 sp
虽然Mg(OH) 的K 较小,但不能认为Mg(OH) 比AgCl更难溶。
2 sp 2
例题1 石灰乳中存在下列平衡:Ca(OH) (s) Ca2+(aq)+2OH-(aq)。
2
加入下列溶液,可使Ca(OH) 减少的是( )
2
①NaCO 溶液 ②KCl溶液 ③NaOH溶液 ④CaCl 溶液
2 3 2
A. ①② B. ③④
C. ①③ D. ②④
【答案】A
2−
【解析】加入NaCO ,Ca2++CO3 =CaCO ↓,c(Ca2+)减小,平衡右移,使 Ca
2 3 3
(OH) 减少;加入KCl溶液相当于加水稀释,Ca(OH) 减少;加入NaOH,c(OH-)
2 2
增大,加入CaCl ,c(Ca2+)增大,平衡均左移,Ca(OH) 增多。
2 2
例题2 已知K (AgCl)=1.56×10-10,K (AgBr)=7.7×10-13,K (Ag CrO )=9×10
sp sp sp 2 4
2−
-11。某溶液中含有Cl-、Br-和CrO4 ,浓度均为0.010 mol·L-1,向该溶液中逐滴加入0.010
mol·L-1的AgNO 溶液时,三种阴离子产生沉淀的先后顺序为( )
3
2− 2−
A. Cl-、Br-、CrO4 B. CrO4 、Br-、Cl-
2− 2−
C. Br-、Cl-、CrO4 D. Br-、CrO4 、Cl-
【答案】C
2−
【解析】根据三种难溶物的溶度积数据,在Cl-、Br-和CrO4 的浓度均为0.010 mol·L-1
时,氯离子沉淀时银离子的最小值是(1.56×10-10/0.010)mol·L-1=1.56×10-8 mol·L-1,溴
2−
离子沉淀时银离子的最小值是(7.7×10-13/0.010)mol·L-1=7.7×10-11 mol·L-1,CrO4 沉淀
1
2
时银离子的最小值是[(9×10-11/0.010)] mol·L-1=3×10-4.5 mol·L-1,沉淀所需银离子浓
2−
度小的先沉淀,所以三种离子沉淀的先后顺序是Br-、Cl-、CrO4 。
第6页例题3 在0.1 mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化
铜沉淀生成,当溶液的pH=8时,c(Cu2+)=________ mol·L-1{K [Cu(OH) ]=2.2×10
sp 2
-20}。若在0.1 mol·L-1硫酸铜溶液中通入过量HS气体,使Cu2+完全沉淀为CuS,此时溶
2
液中的H+浓度是________mol·L-1。
【答案】2.2×10-8 0.2
【解析】pH=8时,c(OH-)=10-6 mol·L-1,由氢氧化铜的溶度积常数可知:K =
sp
2.2×10-20=10-12×c(Cu2+),得c(Cu2+)=2.2×10-8 mol·L-1;使Cu2+沉淀完全,已知c
(Cu2+)=0.1 mol·L-1,根据反应关系式:Cu2+~2H+得c(H+)=0.2 mol·L-1。
(答题时间:40分钟)
一、选择题
1. 下列有关溶度积常数K 的说法正确的是( )
sp
A. 常温下,向BaCO 饱和溶液中加入NaCO 固体,BaCO 的K 减小
3 2 3 3 sp
B. 溶度积常数K 只受温度影响,温度升高K 减小
sp sp
C. 溶度积常数K 只受温度影响,温度升高K 增大
sp sp
D. 常温下,向Mg(OH) 饱和溶液中加入NaOH固体,Mg(OH) 的K 不变
2 2 sp
2. 在一定温度下,当Mg(OH) 固体在水溶液中达到下列平衡时:Mg(OH) (s)
2 2
Mg2+(aq)+2OH-(aq),要使Mg(OH) 固体减少而c(Mg2+)不变,可采取的
2
措施是( )
A. 加MgSO 固体 B. 加HCl溶液
4
C. 加NaOH固体 D. 加少量水
3. 已知:K (AgCl)=1.8×10-10,K (AgI)=1.5×10-16,K (Ag CrO )=2.0×10-
sp sp sp 2 4
12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( )
A. AgCl>AgI>Ag CrO
2 4
B. AgCl>Ag CrO>AgI
2 4
C. Ag CrO>AgCl>AgI
2 4
D. Ag CrO>AgI>AgCl
2 4
*4. 在t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t ℃时AgCl的K =4×10-
sp
10,下列说法不正确的是( )
第7页A. 在t ℃时,AgBr的K 为4.9×l0-13
sp
B. 在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点
C. 图中a点对应的是t ℃ AgBr的不饱和溶液
D. 在t ℃时,AgCl(s)+Br-(aq) ⇌AgBr(s)+Cl- (aq)的平衡常数K≈816
*5. 已知几种难溶电解质的溶度积常数K (25 ℃)见下表:
sp
难溶电解质 AgCl AgBr AgI Ag SO Ag CrO
2 4 2 4
K 1.8×10-10 5.4×10-13 8.5×10-17 1.4×10-5 1.12×10-12
sp
下列叙述不正确的是 ( )
A. 由溶度积常数可判断在相同条件下一些物质的溶解性大小
B. 将等体积的4×10-3 mol·L-1的AgNO 溶液和4×10-3 mol·L-1的KCrO 溶液混合,
3 2 4
有Ag CrO 沉淀产生
2 4
C. 向AgCl的悬浊液中滴加饱和NaBr溶液可以得到黄色AgBr悬浊液
D. 向100 mL 0.1 mol·L-1的NaSO 溶液中加入1 mL 0.1 mol·L-1的AgNO 溶液,有白
2 4 3
色沉淀生成
6. 在饱和Ca(OH)
2
溶液中存在溶解平衡:Ca(OH)
2
(s) ⇌Ca2+(aq)+2OH-
(aq),加入以下溶液,可使pH减小的是( )
A. Na S溶液 B. AlCl 溶液
2 3
C. NaOH溶液 D. Na CO
2 3
二、非选择题
*7. 某温度时,Ag SO 在水溶液中的沉淀溶解平衡曲线如图所示。
2 4
请回答下列问题:
(1)A点表示Ag SO 是________(填“饱和”或“不饱和”)溶液。
2 4
第8页(2)B点对应的K ________(填“>”、“<”或“=”)C点对应的K 。
sp sp
(3)现将足量的Ag SO 分别放入下列三种溶液中
2 4
a. 40 mL 0.01 mol·L-1 KSO 溶液
2 4
b. 10 mL蒸馏水
c. 10 mL 0.02 mol·L-1 HSO 溶液
2 4
则Ag SO 的溶解程度由大到小的排列顺序为________________(填字母)。
2 4
第9页1.【答案】D
【解析】温度不变,溶度积常数不变,A项不正确;大多数难溶物温度升高,K 增大,
sp
但也有少数物质相反,故B、C均不正确。
2.【答案】D
【解析】Mg(OH) (s) Mg2+(aq)+2OH-(aq),加MgSO 固体使该溶解
2 4
平衡左移,Mg(OH) 固体增多,c(Mg2+)变大;加HCl溶液使该溶解平衡右移,Mg
2
(OH) 固体减少,c(Mg2+)变大;加NaOH固体使该溶解平衡左移,Mg(OH) 固体
2 2
增多,c(Mg2+)变小。
3.【答案】C
【解析】因为AgCl和AgI的结构相似,由K 可知AgCl的c(Ag+)大于AgI的;
sp
2−
AgCl中的c2(Ag+)=K
sp
=1.8×10-10,Ag
2
CrO
4
(s) ⇌2Ag+(aq)+CrO4 (aq)的K
sp
=c2
1
2−
2
(Ag+)·c(CrO4 )= c3(Ag+)=2.0×10-12,所以Ag CrO 中c(Ag+)大于AgCl中
2 4
的c(Ag+)。
4.【答案】B
【解析】根据溶度积的定义,K =c(Ag+)×c(Br-)=7×10-7×7×10-7=4.9×10-13,
sp
故说法A正确;AgBr(s) ⇌Ag+(aq)+Br-(aq),加入溴化钠溶液中,c(Br-)增大,
促使平衡向逆反应方向进行,c(Ag+)减小,故说法B错误;此时的离子积a>c
【解析】(1)A点没有达到平衡状态。
(2)K 只与温度有关。
sp
2−
(3)c(SO4 )越大,难溶电解质的溶解平衡逆向移动程度越大,Ag SO 的溶解程度
2 4
越小。
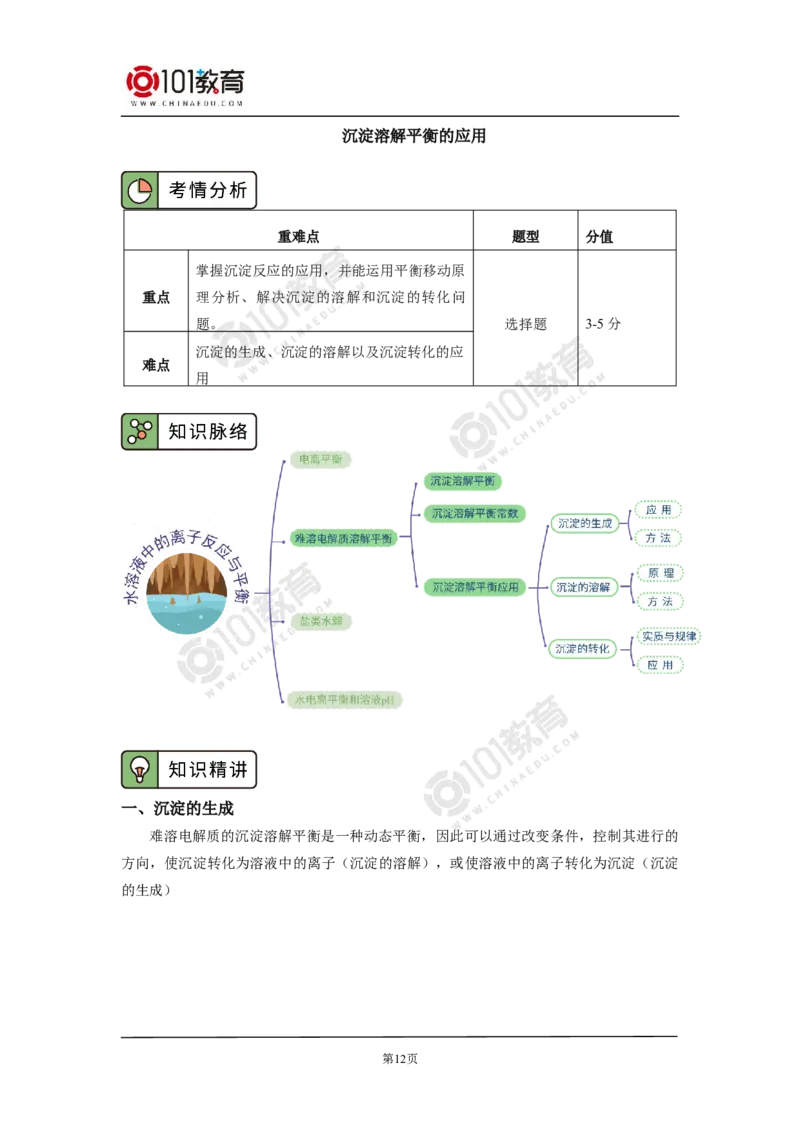
第10页第11页沉淀溶解平衡的应用
重难点 题型 分值
掌握沉淀反应的应用,并能运用平衡移动原
重点 理分析、解决沉淀的溶解和沉淀的转化问
题。 选择题 3-5分
沉淀的生成、沉淀的溶解以及沉淀转化的应
难点
用
一、沉淀的生成
难溶电解质的沉淀溶解平衡是一种动态平衡,因此可以通过改变条件,控制其进行的
方向,使沉淀转化为溶液中的离子(沉淀的溶解),或使溶液中的离子转化为沉淀(沉淀
的生成)
第12页1. 沉淀生成的应用
在涉及无机制备、提纯工艺的生产、科研、废水处理等领域中,常利用生成沉淀来达
到分离或去除某些离子的目的。例如,化学沉淀法废水处理工艺流程示意图如下:
(1)调节pH法
如工业原料氯化铵中含有杂质氯化铁,使其溶于水,再加入氨水调节pH至7~8,可
使Fe3+转变为 Fe ( OH ) 沉淀而除去。反应离子方程式: Fe 3 + + 3NH ·H O = Fe ( OH ) ↓ +
3 3 2 3
3NH 。
(2)加沉淀剂法
如以NaS、HS等作为沉淀剂,使某些金属离子如Cu2+、Hg2+等,生成极难溶的硫化
2 2
物CuS、HgS等沉淀,也是分离、除去杂质常用的方法。反应的离子方程式如下:
Cu2++S2-=CuS↓;
Cu2++HS= CuS↓ + 2H + ;
2
Hg2++HS= HgS↓ + 2H + 。
2
【注意】沉淀剂的选择
①要能除去溶液中的指定离子,又不能影响其他离子的存在,并且由沉淀剂引入溶液
的杂质离子要便于除去,如沉淀KNO 溶液中的Ag+,可用KCl作沉淀剂,而不能选用
3
NaCl。
②选用沉淀剂时,选用的沉淀剂应使沉淀生成的反应进行得越完全越好。例如,要除
去溶液中的SO 2-应选择加入钡盐而不是钙盐,因为BaSO 比CaSO 难溶,可使SO 2-沉淀更
4 4 4 4
完全。同理,除去Mg2+应加入OH-而不是CO2-因为Mg(OH) 难溶而MgCO 微溶。
3 2 3
③要注意沉淀剂的电离程度,如使Mg2+转化为Mg(OH) 沉淀时,用NaOH溶液作
2
第13页沉淀剂要比用氨水的效果好。
(3)同离子效应法
增大沉淀溶解平衡体系中某种离子的浓度,使平衡向生成沉淀的方向移动,如向
AgC1的饱和溶液中加入饱和食盐水可继续生成AgCl沉淀。
(4)氧化还原法
改变离子的存在形式,促使其转化为溶解度更小的难溶电解质,便于分离出来,例如
通过氧化还原反应将Fe2+氧化为Fe3+,从而生成更难溶的Fe(OH) 沉淀,常用的氧化剂
3
是HO,好处是不引入新杂质。【注意】4
2 2
【注意】4 反应完全的标志
化学上通常认为残留在溶液中的离子浓度小于 1×10-5 mol·L-1时,沉淀达到完全,即
视为将溶液中该离子除尽,此点在解题中时长以信息的形式给出。
二、沉淀的溶解
1. 原理:根据平衡移动原理,对于在水中难溶的电解质,只要不断减少溶解平衡体系中
的相应离子,平衡就向沉淀溶解的方向移动,从而使沉淀溶解。
2. 沉淀溶解的方法
(1)酸碱溶解法
加入酸或碱与沉淀溶解平衡体系中的相应离子反应,降低相应离子的浓度,使平衡向
沉淀溶解的方向移动。
例如,CaCO 溶于盐酸,离子方程式为CaCO + 2H + = C a 2 + + H O + CO ↑。
3 3 2 2
【知识拓展】溶洞里美丽的钟乳石和石柱的形成过程
石灰石里不溶性的碳酸钙与水及二氧化碳反应能转化为微溶性的碳酸氢钙[Ca(HCO )
3
]。溶有碳酸氢钙的水从溶洞顶向溶洞低落时,水蒸发、二氧化碳压强减小或温度的变化
2
都是二氧化碳的溶解度减小而析出碳酸钙沉淀。这些沉淀经过千百万年的积聚,渐渐形成
了钟乳石、石柱等。
如难溶于水的BaCO 沉淀可溶于盐酸中,其溶解原理可表示为:
3
第14页离子方程式为: BaCO + 2H + = B a 2 + + H O + CO ↑
3 2 2
【知识拓展】医疗上用BaSO 作“钡餐”的原因
4
BaCO 、BaSO 均难溶于水,但前者可溶于酸,而后者不溶于酸,因此医学上常将
3 4
BaSO 用于钡餐透视而不用 BaCO ,因为 BaCO 溶于胃酸(主要成分为盐酸)会产生
4 3 3
Ba2+,使人中毒。
(2)盐溶解法
+
如:Mg(OH) 溶于 NH Cl 溶液,离子方程式为 Mg ( OH ) + 2NH 4 = M g 2 + +
2 4 2
2NH ·H O。
3 2
(3)氧化还原法
某些金属硫化物(如CuS、HgS),其溶度积特别小,在其饱和溶液中c(S2-)特别小。
这些金属硫化物能溶于氧化性酸(如硝酸、王水等),不溶于非氧化性酸,则可通过减小
c(S2-)来达到使沉淀溶解的目的。
例如:CuS溶于稀HNO:3CuS+8 HNO(稀)=3Cu(NO )+3S+2NO↑+4H O
3 3 3 2 2
【注意】此法适用于那些具有明显氧化性或还原性的难溶物。
(4)生成配合物法
向沉淀溶解平衡体系中加入适当的配位剂,使溶液中某种离子生成稳定的配合物,以
减小其离子浓度,从而使沉淀溶解。
如AgCl沉淀可溶于氨水,其溶解原理为AgCl电离出的Ag+与NH ·H O 作用生成可溶
3 2
性但难电离的配离子 [A g ( NH ) ] + ,则 AgCl 溶解平衡体系中 c ( Ag+)减小,溶解平衡向
3 2
右直至AgCl完全溶解,反应的离子方程式为 AgCl + 2NH ·H O = [Ag ( NH ) ] + + Cl - +
3 2 3 2
2HO。
2
三、沉淀的转化
1. 沉淀转化的实质与规律
(1)实质:沉淀溶解平衡的移动
(2)规律:一般来说,溶解度小的沉淀容易转化成溶解度更小的沉淀;沉淀的溶解度
第15页差别越大,转化越容易。
溶解度小的沉淀转化成溶解度更小的沉淀。两种沉淀的溶解度差别越大,沉淀越容易
转化。
如:AgNO 溶液
⃗NaClAgCl(白色沉淀) ⃗NaBrAgBr(浅黄色沉淀) ⃗NaI
3
⃗Na S
AgI(黄色沉淀) 2 Ag S(黑色沉淀)。
2
【易错】2 溶解度较小的沉淀在一定条件下也可以转化成溶解度较大的沉淀,如
BaSO 的饱和溶液中加入高浓度的NaCO 溶液,可以生成溶解度较大的BaCO 沉淀。
4 2 3 3
2. 应用
(1)锅炉除水垢:
将水垢中含有的难溶于酸的CaSO 转化为易溶于酸的CaCO 。
4 3
水垢[CaSO(s)]
⃗Na
2
CO
3CaCO (s)
⃗盐酸
Ca2+(aq)
4 3
其离子反应方程式:CaSO(s)+ CO2-(aq) CaCO (s)+ SO 2 - ( aq ) :
4 3 3 4
具体反应过程: CaSO ( s )+ N aCO ( a q ) = CaCO ( s )+ N aSO ( a q ) 、
4 2 3 3 2 4
CaCO + 2HC l = CaC l + CO ↑ + H O。
3 2 2 2
(2)自然界中矿物的转化:
如 ZnS 遇 CuSO 溶液转化为 CuS ,离子反应: C u 2 + ( aq )+ ZnS ( s ) CuS ( s )+ Zn 2 +
4
( a q ) ;
如 PbS 遇 CuSO 溶液转化为 CuS ,离子反应: C u 2 + ( aq )+ PbS ( s )= CuS ( s )+ P b 2 +
4
( a q ) 。
【知识点睛】沉淀转化的一般原则
(1)溶解度较小的沉淀易转化成溶解度更小的沉淀。
(2)当一种试剂能沉淀溶液中的几种离子时,生成沉淀时所需试剂离子浓度越小的越
先沉淀。
例题1 下列现象不能用沉淀溶解平衡移动原理解释的是( )
第16页A. 相同温度下,AgCl在水中的溶解度大于在氯化钠溶液中的溶解度
B. 浓FeCl 溶液滴入沸水中继续加热形成红褐色透明液体
3
C. 自然界地表层原生铜矿变成CuSO 溶液向下层渗透,遇到难溶的ZnS或PbS,慢慢
4
转变为铜蓝(CuS)
D. 加入少量AgCl固体可以除去氯化钠溶液中的少量硫化钠杂质
【答案】B
【解析】B项为胶体的形成,不能用沉淀溶解平衡移动原理解释。
例题2 实验:①0.1 mol·L-1 MgCl 溶液和0.2 mol·L-1 NaOH溶液等体积混合得到浊
2
液a,取少量浊液a过滤得到滤液b和白色沉淀c;②向浊液a中滴加0.1 mol·L-1 FeCl 溶
3
液,出现红褐色沉淀。下列分析不正确的是( )
A. 滤液b的pH=7
B. ②中颜色变化说明Mg(OH) 转化为Fe(OH)
2 3
C. 滤液b的pH>7
D. 浊液a中存在沉淀溶解平衡:Mg(OH)(s) Mg2+(aq)+2OH-(aq)
2
【答案】A
【解析】根据题意,发生的反应为Mg2++2OH-=Mg(OH) ↓;3Mg(OH) (s)
2 2
+2Fe3+(aq)=3Mg2+(aq)+2Fe(OH) (s)。由于存在Mg(OH) (s) Mg2+
3 2
(aq)+2OH-(aq),所以滤液b的pH应大于7,A项错误。
例题3
化合物 Zn(OH) Fe(OH) Fe(OH)
2 2 3
K 近似值 10-17 10-17 10-39
sp
用废电池的锌皮制备ZnSO·7H O的过程中,需除去锌皮中的少量杂质铁,其方法是
4 2
加稀HSO 和HO 溶解,铁变为________,加碱调节至pH为________时,铁刚好沉淀完
2 4 2 2
全(离子浓度小于1×10-5 mol·L-1时,即可认为该离子沉淀完全);继续加碱至pH为
________时,锌开始沉淀(假定Zn2+浓度为0.1 mol·L-1)。若上述过程不加HO 后果是
2 2
____________,原因是______________________。
【答案】Fe3+ 2.7 6 Zn2+和Fe2+分离不开 Fe(OH) 和Zn(OH) 的K 相近
2 2 sp
【解析】Fe与稀HSO 反应生成FeSO ,再被HO 氧化转化为Fe (SO ) 。Fe(OH)
2 4 4 2 2 2 4 3 3
√ K
3 sp
的K =c(Fe3+)·c3(OH-),则有c(OH-)=
c(Fe3+)
≈10-11.3mol·L-1,则溶液的
sp
第17页√ K
sp
pH=2.7。Zn(OH) 的K =c(Zn2+)·c2(OH-),则有c(OH-)=
c(Zn2+)
=10-
2 sp
8mol·L-1,则溶液的pH=6。Fe(OH) 和Zn(OH) 的K 相近,不加入HO 将Fe2+转化
2 2 sp 2 2
为Fe3+,很难将Zn2+和Fe2+分开。
(答题时间:40分钟)
一、选择题
1. 25 ℃时,K [Mg(OH) ]=5.61×10-12,K [MgF ]=7.42×10-11。下列说法正确的是(
sp 2 sp 2
)
A. 25 ℃时,饱和Mg(OH) 溶液与饱和MgF 溶液相比,前者的c(Mg2+)大
2 2
B. 25 ℃时,在Mg(OH) 的悬浊液中加入少量的NH Cl固体,c(Mg2+)增大
2 4
C. 25 ℃时,Mg(OH) 固体在20 mL 0.01 mol·L-1氨水中的K 比在20 mL 0.01 mol·L-1
2 sp
NH Cl溶液中的K 小
4 sp
D. 25 ℃时,在Mg(OH) 的悬浊液加入NaF溶液后,Mg(OH) 不可能转化成为
2 2
MgF
2
2. 25 ℃时,已知下列三种金属硫化物的溶度积常数(K )分别为K (FeS)=6.3×10-
sp sp
18;K (CuS)=1.3×10-36;K (ZnS)=1.6×10-24。下列关于常温时的有关叙述正确的是
sp sp
( )
A. 硫化锌、硫化铜、硫化亚铁的溶解度依次增大
B. 将足量的ZnSO 晶体加入到0.1 mol·L-1的NaS溶液中,Zn2+的浓度最大只能达到
4 2
1.6×10-23 mol·L-1
C. 除去工业废水中含有的Cu2+,可采用FeS固体作为沉淀剂
D. 向饱和的FeS溶液中加入FeSO 溶液后,混合液中c(Fe2+)变大、c(S2-)变小,
4
但K (FeS)变大
sp
3. 实验:①向盛有1 mL 0.1 mol·L-1 MgCl 溶液试管中加1 mL 0.2 mol·L-1 NaOH溶液,
2
得到浊液a,过滤得到滤液b和白色沉淀c。②向沉淀c中滴加0.1 mol·L-1 FeCl 溶液,沉
3
淀变为红褐色。下列分析不正确的是( )
A. 浊液a中存在沉淀溶解平衡:Mg(OH)
2
(s) ⇌Mg2+(aq)+2OH-(aq)
B. 滤液b中不含有Mg2+
C. ②中颜色变化说明Mg(OH) 转化为Fe(OH)
2 3
D. 实验可以证明Fe(OH) 比Mg(OH) 更难溶
3 2
*4. 下列说法正确的是( )
第18页A. 根据K (AgCl)=1.77×10-10,K (Ag CrO )=2.0×10-12,可以推知AgCl的溶
sp sp 2 4
解度比Ag CrO 的溶解度大
2 4
B. 0.1 mol·L-1的ZnCl 溶液中通入足量硫化氢气体最终得不到ZnS沉淀是因为溶液中c
2
(Zn2+)·c(S2-)>K (ZnS)
sp
C. 向碳酸钡沉淀中加入稀硫酸,沉淀发生转化,可推知硫酸钡的K 比碳酸钡的大
sp
D. AgCl在10 mL 0.01 mol·L-1的KCl溶液中比在10 mL 0.05 mol·L-1的AgNO 溶液中
3
溶解的质量多
5. 锅炉水垢是一种安全隐患,除去水垢中的CaSO,可先用NaCO 溶液处理,使之转化
4 2 3
为易溶于酸的CaCO ,而后用酸除去。下列说法不正确的是( )
3
A. CaCO 的溶解度小于CaSO 的
3 4
B. 沉淀转化的实质是沉淀溶解平衡的移动
C. 沉淀转化的难易与溶解度差别的大小无关
D. CaSO 到CaCO 的沉淀转化中并存着两个沉淀溶解平衡
4 3
*6. 实验:①0.1 mol·L-1 AgNO 溶液和0.1 mol·L-1NaCl溶液等体积混合得到浊液a,过
3
滤得到滤液b和白色沉淀c;
②向滤液b中滴加0.1 mol·L-1 KI溶液,出现浑浊;
③向沉淀 c 中滴加 0.1 mol·L-1 KI 溶液,沉淀变为黄色。下列分析不正确的是
( )
A. 浊液a中存在沉淀溶解平衡:AgCl(s) ⇌Ag+(aq)+Cl-(aq)
B. 滤液b中不含有Ag+
C. ③中颜色变化说明AgCl转化为AgI
D. 实验可以证明AgI比AgCl更难溶
7. 下列事实不能用平衡移动原理解释的是( )
A. Mg(OH) 不溶于水,但能溶于浓NH Cl溶液中
2 4
B. 水垢中含有的 CaSO ,先用 NaCO 溶液处理,使之转化为疏松、易溶于酸的
4 2 3
CaCO ,再用酸除去
3
C. 洗涤BaSO 沉淀时,用稀硫酸洗涤BaSO 沉淀比用蒸馏水洗涤损失少
4 4
D. FeCl 溶液中混有FeCl ,常加入少量的HO,使Fe2+氧化为Fe3+
3 2 2 2
二、非选择题
*8. 高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫
化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
第19页相关金属离子[c(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
0
金属离子 Mn2+ Fe2+ Fe3+ Al3+ Mg2+ Zn2+ Ni2+
开始沉淀的pH 8.1 6.3 1.5 3.4 8.9 6.2 6.9
沉淀完全的pH 10.1 8.3 2.8 4.7 10.9 8.2 8.9
(1)“滤渣1”含有S和 ;写出“溶浸”中二氧化锰与硫化锰反应
的化学方程式 。
(2)“氧化”中添加适量的MnO 的作用是 。
2
(3)“调pH”除铁和铝,溶液的pH范围应调节为 ~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是 。
(5)“除杂2”的目的是生成MgF 沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,
2
原因是 。
(6)写出“沉锰”的离子方程式 。
第20页1.【答案】B
【解析】由于Mg(OH) 的溶度积小,所以其电离出的Mg2+浓度要小一些,A项错
2
+
误;由于NH4可以直接结合Mg(OH) 电离出的OH-,从而促使Mg(OH) 的电离平衡
2 2
正向移动,c(Mg2+)增大,B项正确;由于K 仅与温度有关,与溶液中离子浓度的大小、
sp
难溶电解质量的多少等无关,C项错误;因为K [Mg(OH) ]和K (MgF )相差不大,
sp 2 sp 2
在Mg(OH) 悬浊液中加入NaF,若溶液中c(Mg2+)·
2
c2(F-)>7.42×10-11时,也可以生成MgF 沉淀,即由Mg(OH) 转化为MgF ,D项
2 2 2
错误。
2.【答案】C
【解析】化学式所表示的组成中阴、阳离子个数比相同时,K 数值越大的难溶电解质
sp
在水中的溶解能力越强,由K 可知,常温下,CuS的溶解度最小,故A错;将足量的
sp
ZnSO 晶体加入到0.1 mol·L-1的NaS溶液中,c(S2-)将减至非常小,而Zn2+的浓度远远
4 2
大于1.6×10-23 mol·L-1;因CuS比FeS更难溶,FeS沉淀可转化为CuS沉淀;温度不变,
K (FeS)不变。
sp
3.【答案】B
【解析】绝对不溶的物质是不存在的,B选项错误。
4.【答案】D
√1.77
【解析】A 项,c(Ag+)= ×10-5mol·L-1,1 L 水中溶解的 AgCl 的质量为
√1.77 2−
×10-5×143.5 g,由Ag
2
CrO
4
(s) ⇌2Ag+(aq)+CrO4 (aq),可知,
2− 2− 2− √ 3 0.5
c2(Ag+)·c(CrO4 )=4c3(CrO4 ),所以c(CrO4 )= ×10-4 mol·L-1,1 L
√ 3 0.5
水中溶解的Ag CrO 的质量为 ×10-4×332 g,A错误。
2 4
5.【答案】C
【解析】沉淀转化的方向是难溶物向更难溶的方向转化,所以沉淀的溶解度差别越大,
越易转化,C选项错误。
6.【答案】B
【解析】注意“0.1 mol·L-1 AgNO 溶液和0.1 mol·L-1 NaCl溶液等体积混合”,即二
3
者恰好完全反应,是分析、解答本题的关键。
A. 向二者恰好反应后的滤液b中滴加0.1 mol·L-1 KI溶液出现碘化银沉淀,则说明浊
液a中存在沉淀溶解平衡,A正确。B.向滤液b中加入0.1 mol·L-1 KI溶液,出现浑浊,则
说明b中含有Ag+,B错误。C.③中颜色变化是沉淀进行了转化,即AgCl转化为AgI,C
正确。D.因AgCl沉淀能转化为AgI沉淀,所以K (AgI)