文档内容
第一章 原子结构与性质
第二节 原子结构与元素的性质
1.2.1 原子结构与元素周期表
1.熟知原子结构与元素周期表的关系,进一步熟悉元素周期表的结构。
2.能够从原子结构的角度认识元素周期表中区的划分。
教学重点:原子核外电子排布与元素周期表分区的关系
教学难点:原子核外电子排布与元素周期表分区的关系
【旧知回顾】
一、元素周期表的结构
周期
短周期 长周期
第一周期 第二周期 第三周期 第四周期 第五周期 第六周期 第七周期 第八周期
种元素 种元素 种元素 种元素 种元素 种元素 种元素 种元素
注意:镧 La–镥 Lu共15种元素称镧系元素;锕 Ac–铹 Lr共15种元素称锕系元素
57 71 89 103
族
主族 副族 第VIII族 零族
【新知学习】
一、元素周期系
(1)含义:元素按其原子 排列的序列称为元素周期系。这个序列中的元素性质随着核
电荷数的递增发生 的重复
(2)特点:各周期元素原子的核外电子排布重复出现从 到 (除第一周期)的周期性变化。
二、构造原理与元素周期表
1、原子核外电子排布与周期的关系
(1)根据构造原理得到的核外电子排布,可以解释元素周期系的基本结构。
①第一周期从 开始,以 结束,只有两种元素。
②其余各周期总是从 能级开始,以 能级结束,
③而从 能级开始以 能级结束递增的核电荷数(或电子数)就等于每个周期里的
。具体数据如下:
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s……
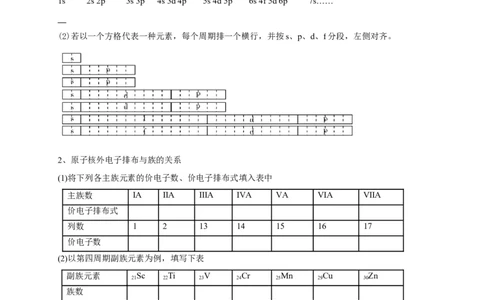
(2)若以一个方格代表一种元素,每个周期排一个横行,并按s、p、d、f分段,左侧对齐。
2、原子核外电子排布与族的关系
(1)将下列各主族元素的价电子数、价电子排布式填入表中
主族数 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
价电子排布式
列数 1 2 13 14 15 16 17
价电子数
(2)以第四周期副族元素为例,填写下表
副族元素 Sc Ti V Cr Mn Cu Zn
21 22 23 24 25 29 30
族数
价电子排布式
价电子数目
[总结归纳]
① 同主族元素原子的 完全相同,价电子全部排布在
或
轨道上。价电子数与 相同。
②稀有气体的价电子排布为 或 。
② 过渡元素(副族和Ⅷ族)同一纵行原子的价层电子排布基本相同。价电子排布为,
的价电子数与族序数相同,第 族和第 族不相同。
3、元素周期表的分区
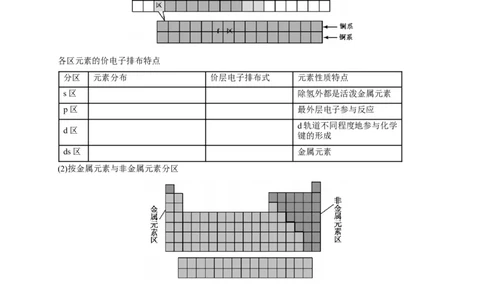
(1)按电子排布分区
各区元素的价电子排布特点
分区 元素分布 价层电子排布式 元素性质特点
s区 除氢外都是活泼金属元素
p区 最外层电子参与反应
d轨道不同程度地参与化学
d区
键的形成
ds区 金属元素
(2)按金属元素与非金属元素分区
沿着周期表中 与 之间画一条线,线的左边是金属元素(氢除外),线的
右边是非金属元素。
金属与非金属交界处元素的性质特点:在元素周期表中位于金属和非金属分界线上的元素兼有金属
和非金属的性质,位于此处的元素(如硼、硅、锗、砷、锑等)常被称为半金属或类金属(一般可
用作半导体材料)。
[思考交流]
(1) 为什么副族元素又称为过渡元素?(2) 为什么在元素周期表中非金属元素主要集中在右上角三角区内?处于非金属三
角区边缘的元素常被称为半金属或准金属。为什么?
(3) 在周期表里找出Cr和Cu的价层电子,它们的电子排布符合构造原理吗?此外还有哪些元素的
基态原子电子排布不符合构造原理?
(4) 预言119号元素基态原子最外层电子排布;预言第八周期有多少种元素?
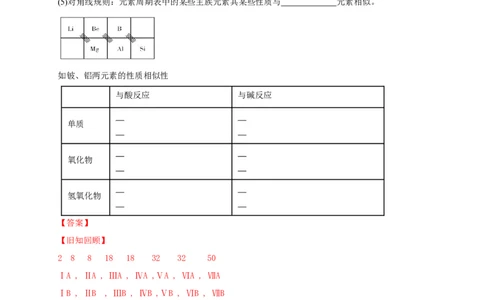
(5)对角线规则:元素周期表中的某些主族元素其某些性质与 元素相似。
如铍、铝两元素的性质相似性
与酸反应 与碱反应
单质
氧化物
氢氧化物
【答案】
【旧知回顾】
2 8 8 18 18 32 32 50
ⅠA , ⅡA , ⅢA , ⅣA ,ⅤA , ⅥA , ⅦA
ⅠB , ⅡB , ⅢB , ⅣB ,ⅤB , ⅥB , ⅦB
三个纵行(8、9、10),位于Ⅶ B 与ⅠB中间 稀有气体元素
【新知学习 】
一、核电荷数递增 周期性 ns1 ns2np6
二、构造原理与元素周期表
1、1s1 1s2 ns np ns np 元素数 2 8 8 18 18 32
2、(1)ns1 ns2 ns2np1 ns2np2 ns2np3 ns2np4 ns2np5
1 2 3 4 5 6 7(2)ⅢB ⅣB ⅤB ⅥB ⅦB ⅠB ⅡB
3d14s2 3d24s2 3d34s2 3d54s1 3d54s2 3d104s1 3d104s2
3 4 5 6 7 11 12
[总结归纳]
① 价电子 ns ns、np 原子的最外层电子数。
② ns2np6 1s2
③ (n-1)d1~10ns1~2 ⅢB~ⅦB族 第ⅠB、ⅡB族 第Ⅷ族
3、(1) ⅠA族、ⅡA族 ns1~2 ⅢA族~ⅦA族、0族 ns2np1~6
ⅢB族~ⅦB族、Ⅷ族 (n-1)d1~9ns1~2 ⅠB族、ⅡB族 (n-1)d10ns1~2
(2)金属 非金属
[思考交流]
(1)副族元素处于金属元素向非金属元素过渡的区域,因此,又把副族元素称为过渡元素
(2) 由元素的价电子结构和元素周期表中元素性质递变规律可知,在元素周期表中,同周期的元素
从左到右非金属性渐强,同主族元素从上到下非金属性渐弱,结果使元素周期表右上角的元素主要
呈现非金属性。处于非金属三角区边缘的元素既能表现出一定的非金属性,又能表现出一定的金属
性,因此,这些元素常被称之为半金属或准金属。
(3) Cr和Cu的价层电子,它们的电子排布不符合构造原理,Mo、Ag、Au基态原子电子排布不符
合构造原理。
(4)119号元素基态原子最外层电子排布8s1,第八周期有50中元素。
(5)右下方的主族元素
与酸反应 与碱反应
单质 2Al6H2Al33H2Al2OH2HO2AlO3H
2 2 22
Be2HBe2HBe2OHBeO2H
2 2 2
氧化物 AlO6H=2Al33HOAlO2OH2AlOHO
23 2 23 22
BeO2HBe2HOBeO2OHBeO2HO
2 2 2
氢氧化物 Al(OH)3H=Al33HOAl(OH)OHAlO2HO
3 2 3 2 2
Be(OH)2H=Be22HOBe(OH)2OHBeO22HO
2 2 2 2 21. 下列有关元素周期表及元素周期律的说法错误的是
A. N能层的能级数最多为3个
B. Cu元素在元素周期表的ds区
C. F元素在同周期中电负性最大
D. 根据对角线规则,铍和铝的化学性质具有相似性
【答案】A
【解析】
A.N能层的能级数为4个,故A错误;
B.根据Cu元素在元素周期表位置判断,Cu元素在元素周期表的ds区,故B正确;
C.F元素的非金属性最强,所以F元素在同周期中电负性最大,故C正确;
D.对角线规则为:沿周期表中金属与非金属分界线方向对角的两主族元素性质相似,铍和铝位置关
系符合对角线规则,物质的化学性质相似,故D正确。
故选A。
2. 元素的分区及在元素周期表中的位置与元素原子的结构密不可分,下列说法正确的是
A. 所有非金属元素都分布在p区
B. s区元素的最后一个电子进入p轨道或者s轨道
C. 元素周期表中ⅢB族到ⅡB族10个纵行的元素都是金属元素
D. 所有金属元素都是过渡元素
【答案】C
【解析】
A.周期表中大部分非金属都分布在p区,但氢元素分布在s区,故A错误;
B.s区元素最后一个电子都进入s轨道,故B错误;
C.元素周期表中ⅢB族到ⅡB族10个纵行的元素都是金属元素,故C正确;
D.周期表中主族中的金属元素不属于过渡元素,故D错误。
故选C。
3. 已知某基态原子的电子排布式为 ,该元素在周期表中的位置和区分别是A. 第四周期ⅡB族;s区 B. 第四周期ⅧB族;d区
C. 第四周期Ⅷ族;d区 D. 第四周期Ⅷ族;ds区
【答案】C
【解析】
由原子的电子排布式为 可知共有4个电子层,为第四周期元素,价电子排布
式为 ,为d区元素,位于第四周期Ⅷ族。
故选C。
4.元素周期表中,铍 与铝处于对角线的位置,它们的性质相似。试回答:
元素在周期表的位置______________________。
比较 、 、 微粒半径的大小_______________________。
下列有关Be性质的推断正确的是_______________________。
是一种轻金属,能与冷水反应
氧化铍具有高熔点
常温时, 溶液的
已 知 : , 写 出 与 水 反 应 的 方 程 式
__________________。
【答案】 第二周期第ⅡA族
【解析】
铍 与铝处于对角线的位置,Al位于第三周期ⅢA族,可知Be位于第二周期第ⅡA族;
故答案为:第二周期第ⅡA族;
具有相同电子层结构的离子中原子序数大的离子半径小,电子层越多,离子半径越大,则离子半径为 ;
故答案为: ;
与冷水不反应,可知Be是一种轻金属,但不能与冷水反应,故a错误;
的熔点高,可知氧化铍具有高熔点,故b正确;
氯化铝溶液显酸性,可知常温时, 溶液的 ,故c正确;
故答案为:bc;
由 可知, ,则
与水反应的方程式为: ,
故答案为: 。
5.元素周期表的形式多种多样,如图是扇形元素周期表的一部分,对比中学常见元素周期表,思考
扇形元素周期表的填充规律,回答下列问题:
写出 在长式周期表中的位置:________________。
在 元素中,金属性最强的是________ 填元素符号 ,元素 形成的简单离子半径由小到大的顺序是________________ 用离子符号表示 。
中元素的最高价氧化物对应水化物的酸性最强的是________ 填化学式 。写出 和
的最高价氧化物对应的水化物反应的离子方程式:________________________。
表中元素 和 可以形成一种淡黄色物质X, 与水反应转移的电子数为_____。
表中元素 和 可形成一种相对分子质量为66的共价化合物Y,Y分子中各原子均达到8电
子稳定结构,Y的电子式为________________________。
【答案】 第四周期第Ⅷ族
;
;
【解析】
由元素在周期表中的位置可知, 元素分别为H、C、N、O、F、Na、Mg、Al、S、Cl、Fe。
为Fe元素,在长式周期表中的位置第四周期第Ⅷ族;
在元素 中,金属性最强的是Na;离子电子层数越多,其离子半径越大,电子层结构相同
的离子,离子半径随着原子序数增大而减小,离子半径由小到大的顺序是 ;
非金属性越强最高价氧化物对应水化物的酸性越强,氯的非金属性强于硫,所以酸性较强的是
;氢氧化铝与氢氧化钠反应的离子方程式为 ;
表中元素 和 可以形成一种淡黄色物质X为过氧化钠, ,
反应 转移 , 与水反应转移电子数为 ;
表中元素 元素 和 元素 可形成一种相对分子质量为66的共价化合物Y为 ,Y分子中各原子均达到8电子稳定结构,Y的电子式为 。