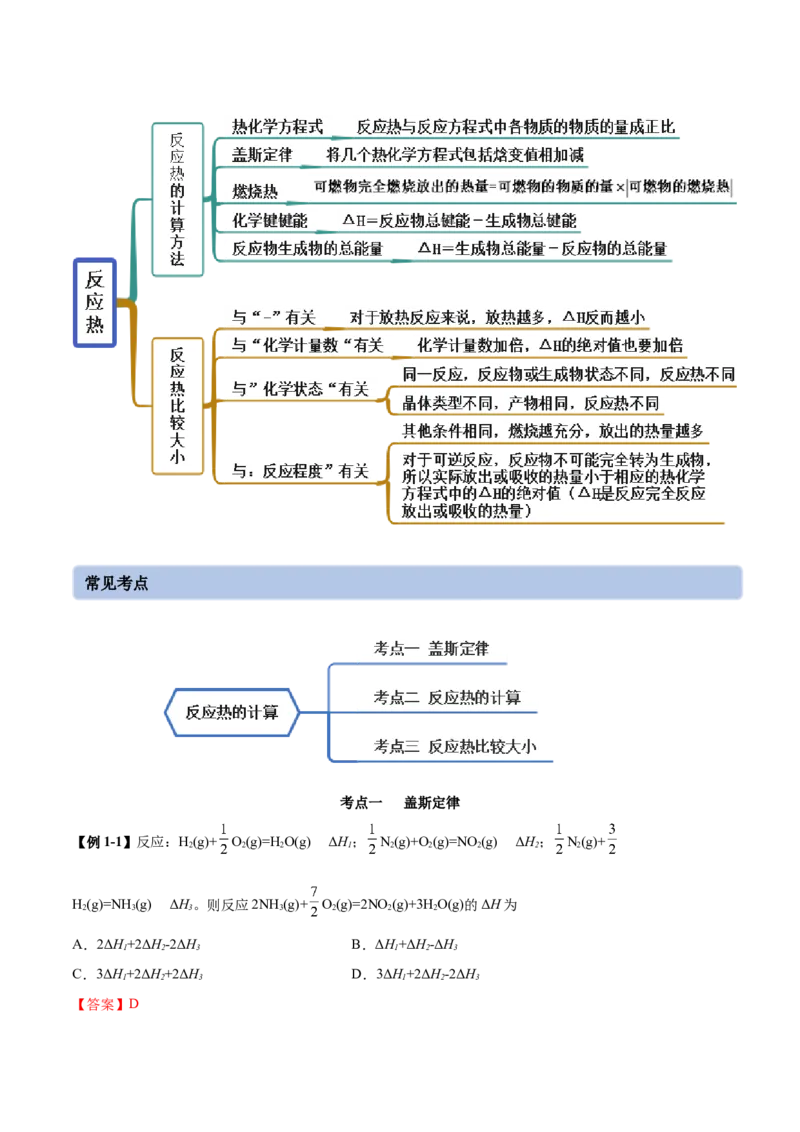
文档内容
1.2 反应热的计算(精讲)
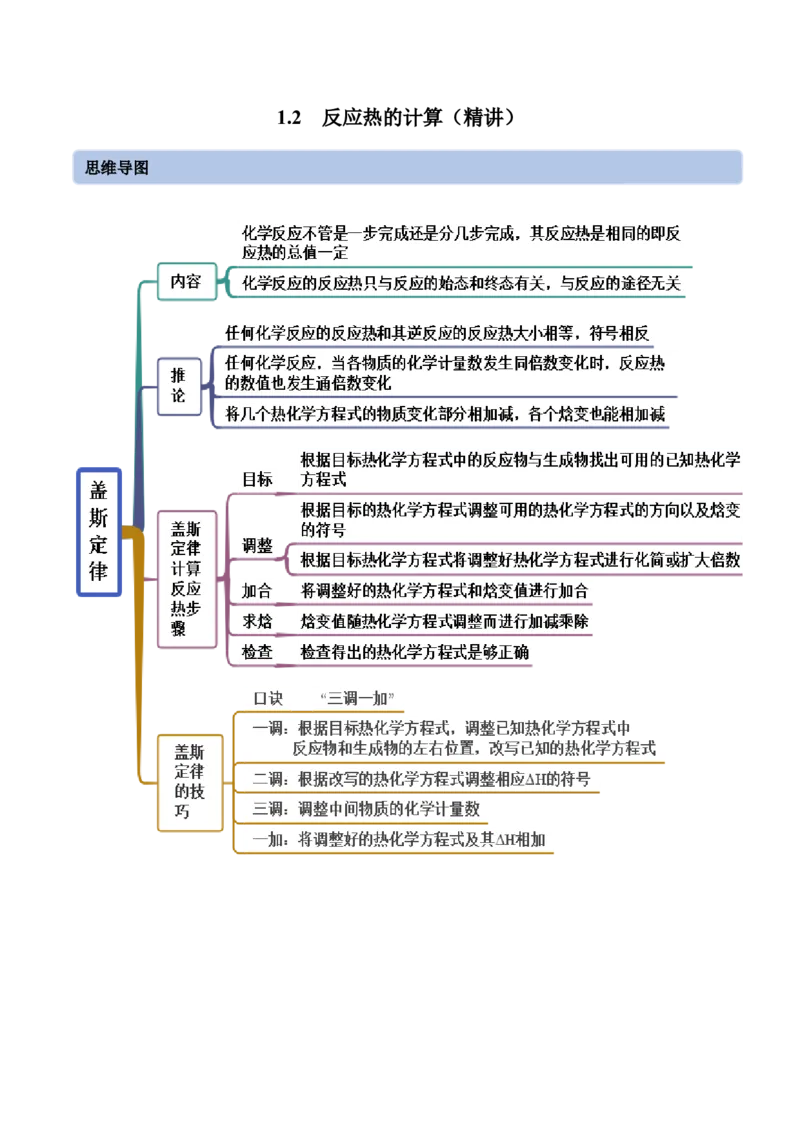
思维导图常见考点
考点一 盖斯定律
【例1-1】反应:H(g)+ O(g)=HO(g) ΔH; N(g)+O(g)=NO (g) ΔH; N(g)+
2 2 2 1 2 2 2 2 2
H(g)=NH (g) ΔH。则反应2NH (g)+ O(g)=2NO (g)+3HO(g)的ΔH为
2 3 3 3 2 2 2
A.2ΔH+2ΔH-2ΔH B.ΔH+ΔH-ΔH
1 2 3 1 2 3
C.3ΔH+2ΔH+2ΔH D.3ΔH+2ΔH-2ΔH
1 2 3 1 2 3
【答案】D【解析】将已知反应依次编号为①、②、③,热化学方程式①×3+②×2-③×2可得2NH (g)+
3
O(g)=2NO (g)+3HO(g),根据盖斯定律,ΔH=3ΔH+2ΔH-2ΔH;故选D。
2 2 2 1 2 3
【例1-2】已知下列热化学方程式:
①Fe O(s)+3CO(g)=2Fe(s)+3CO(g) ΔH=-24.8kJ·mol-1
2 3 2 1
②3Fe O(s)+CO(g)=2Fe O(s)+CO(g) ΔH=-47.19kJ·mol-1
2 3 3 4 2 2
③Fe O(s)+CO(g)=3FeO(s)+CO(g) ΔH=640.4kJ·mol-1
3 4 2 3
则14gCO气体还原足量FeO固体得到Fe单质和CO 气体时对应的ΔH约为
2
A.-218kJ·mol-1 B.-109kJ·mol-1 C.109kJ·mol-1 D.218kJ·mol-1
【答案】B
【解析】根据盖斯定律,由①-[②+③×2]× ,把结果除以2化简后,得FeO(s)+CO(g)=Fe(s)+CO (g)
2
ΔH=-218kJ·mol-1,14gCO的物质的量为0.5mol,反应放热为218kJ×0.5=109kJ,即ΔH=-109kJ·mol-1。
答案选B。
【一隅三反】
1.(2022·内蒙古·阿拉善盟第一中学高二期末)已知下列两个热化学方程式:
①
② 。
下列结论正确的是
A.①的反应热为221 kJ/mol
B.碳的燃烧热大于110.5 kJ/mol
C.由②可知氢气的燃烧热为
D.已知 ,则
【答案】B
【解析】A.反应热需带符号,①的反应热为-221kJ/mol,A错误;
B.燃烧热是指1 mol可燃物完全燃烧生成稳定的氧化物所放出的热量,由反应①不完全燃烧,可推出碳的
燃烧热大于110.5 kJ/mol,B正确;
C.由B选项的分析可知,燃烧热为正值,C错误;
D.设2H(g)+O(g)=2HO(l)为式①,HO(l)= H O(g)为式②,根据盖斯定律,①+2×②可得热化学方程式,
2 2 2 2 2
2H(g)+O(g)=2HO(g) ∆H=-571.6 kJ/mol+44 kJ/mol×2=-483.6 kJ/mol,D错误;故选B。
2 2 22.(2022·云南·昆明一中高二期末)二氧化碳加氢制甲醇一般认为通过如下两步反应来实现:
①CO(g)+H(g)=CO(g)+HO(g) H=+41kJ·mol-1
2 2 2 1
②C(s)+2H
2
(g)=CH
3
OH(g) H
2
=△-90kJ·mol-1
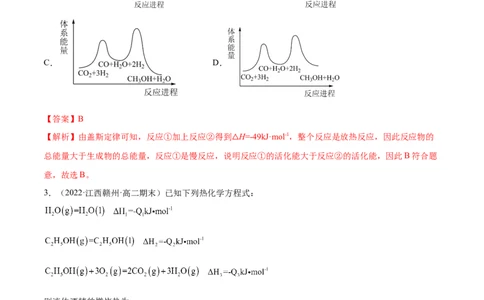
若反应①为慢反应,下列示△意图中能体现上述反应能量变化的是
A. B.
C. D.
【答案】B
【解析】由盖斯定律可知,反应①加上反应②得到 H=-49kJ·mol-1,整个反应是放热反应,因此反应物的
总能量大于生成物的总能量,反应①是慢反应,说△明反应①的活化能大于反应②的活化能,因此B符合题
意,故选B。
3.(2022·江西赣州·高二期末)已知下列热化学方程式:
则液体酒精的燃烧热为
A. B.
C. D.
【答案】C
【解析】燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量,由盖斯定律,3×反应1-反应2+反应3可得液体酒精的燃烧热化学方程式为 ∆H=
,故选:C。
4.(2022·四川达州·高二期末)已知:①
②
③
则: 的反应热 为
A. B. C. D.
【答案】C
【解析】由盖斯定律,2×反应②+反应①-反应③可得反应 ,
=2×(-393.5)+(-571.6)-(-870.3)= -488.3kJ/mol,故选:C。
考点二 反应热的计算
【例2】(2022·河北石家庄·高二期末)化学反应中均伴随有能量变化。
(1)下列反应中,反应物的总能量小于生成物的总能量的为____(填选项字母)。
A.Na与水反应 B.甲烷的燃烧反应 C.CaCO 受热分解 D.锌与盐酸反应
3
(2)已知25℃时,相关物质的相对能量如表所示;
物质 H(g) O(g) HO(g) HO(l)
2 2 2 2
相对能量(kJ·mol-1) 0 0 -242 -286
①表示H(g)燃烧热的热化学方程为____。
2
②0.5molHO(g)转化为HO(l)需要____(填“吸收”或“放出”)____kJ的热量。
2 2
(3)已知:
Ⅰ.2C(s)+O (g)=2CO(g) H=-221kJ·mol-1
2
Ⅱ.C(s)+O
2
(g)=CO
2
(g) △H=-393.5kJ·mol-1
△
根据盖斯定律计算CO(g)+ O(g)=CO (g) H=____kJ·mol-1。
2 2
△
【答案】(1)C(2) H(g)+ O(g)=HO(g) H=-286kJ·mol-1 放出 22
2 2 2
△
(3)-283
【解析】(1)反应物的总能量小于生成物的总能量则是吸热反应,
A.Na与HO反应,生成NaOH和H,化学方程式为2Na+2HO=2NaOH+H ↑,是放热反应,故A错误;
2 2 2 2
B.甲烷的燃烧反应,生成CO 和HO,化学方程式为:CH+2O =CO +2H O,是放热反应,故B错误;
2 2 4 2 2 2
C.CaCO 受热分解,生成CaO和CO,化学方程式为:CaCO CaO+CO ↑,属于分解反应,是吸热反
3 2 3 2
应,故C正确;
D.锌与盐酸反应,生成氯化锌和H,化学方程式为:Zn+2HCl=ZnCl +H ↑,是放热反应,故D错误;
2 2 2
故答案为:C;
(2)①燃烧热指1mol可燃物完全燃烧生成稳定氧化物放出的热量,H(g)燃烧反应方程式为H(g)+
2 2
O(g)=HO(g),由表数据可得, H=生成物的总能量-反应物的总能量=-286-(0+0)= -286 kJ·mol-1,则H(g)
2 2 2
△
燃烧热的热化学方程为H(g)+ O(g)=HO(g) H=-286kJ·mol-1;
2 2 2
△
②由HO(g) = H O(l) H=生成物的总能量-反应物的总能量=-286-(-242)= -44 kJ·mol-1,则0.5molHO(g)转
2 2 2
化为HO(l)需要放出2△2 kJ的热量;
2
(3)根据盖斯定律反应II- 反应I可得CO(g)+ O(g)=CO (g) H=-393.5- ×(-221)= -283 kJ·mol-1。
2 2
△
【一隅三反】
1.已知H—H键、N≡N键、N—H键键能如下表所示:
化学键 H—H N≡N N—H
键能/kJ·mol-1 436 946 391
则在一定条件下进行反应N(g)+3H(g)=2NH (g),生成1 mol NH 时的反应热Q=_______。
2 2 3 3
【答案】-46 kJ
【解析】断开反应物的化学键吸收能量为946 kJ+436 kJ×3 = 2254 kJ,形成生成物的化学键放出能量为391
kJ×6 = 2346 kJ,生成2 mol NH 时放出的热量=2346 kJ -2254 kJ = 92 kJ,所以1 mol NH 时的放出的热量为
3 3
46 kJ,即反应热Q=-46kJ,故答案为:-46kJ;
2.回答下列问题:
(1)在一 定条件下,氢气在氯气中燃烧的热化学方程式: H(g)+C1 (g) =2HCl(g) ΔH= - 184.6 kJ•mol-1;该
2 2
反应属于___________(填“热吸”或“放热”)反应 。(2)常温常压下,1 mol乙醇完全燃烧生成CO 气体和液态水放出的热量为1367 kJ,写出乙醇燃烧热的热化
2
学方程式:___________
(3)根据盖斯定律计算
P(白磷,s)+5O (g)= H=-2983.2 kJ·mol-1 ①
4 2
△
P(红磷,s)+ O(g)= H=-738.5 kJ·mol-1 ②
2
△
则白磷转化为红磷的热化学方程式为___________
(4)已知破坏1 mol H-H 键、1 mol I-I键、1 mol H-I键分别需要吸收的能量为436 kJ、151 kJ、299 kJ 。则
由氢气和碘单质反应生成2molHI 需要放出___________ kJ 的热量。
【答案】(1)放热
(2)C HOH(l)+3O (g)=2CO (g)+3HO(l) H=-1367kJ·mol-1
2 5 2 2 2
(3)P
4
(白磷,s)= 4P(红磷,s) H=-29.2△ kJ·mol-1
(4)11 △
【解析】(1)该反应的焓变小于零,为放热反应;
(2)常温常压下,1 mol乙醇完全燃烧生成CO 气体和液态水放出的热量为1367 kJ,则乙醇燃烧热的热化学
2
方程式:C HOH(l)+3O (g)=2CO (g)+3HO(l) H=-1367kJ·mol-1;
2 5 2 2 2
(3)由盖斯定律可知,①-4×②即为:P
4
(白磷,△s)= 4P(红磷,s) H=-2983.2 kJ·mol-1-4×(-738.5 kJ·mol-1)
=-29.2 kJ·mol-1; △
(4)氢气和碘单质反应为H+I =2HI,则由氢气和碘单质反应生成2molHI 需要放出299×2-(436+151)=11
2 2
kJ。
3.I.金刚石和石墨燃烧,氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示。
(1)在通常状况下,金刚石和石墨中____(填“金刚石”或“石墨”)更稳定,石墨的燃烧热ΔH为____。
(2)已知:N、O 分子中化学键的键能分别是946kJ·mol-1、497kJ·mol-1;N(g)+O(g)=2NO(g)
2 2 2 2ΔH=+180.0kJ·mol-1。NO分子中化学键的键能为____kJ·mol-1。
(3)综合上述有关信息,请写出CO和NO反应的热化学方程式:____。
II.2SO(g)+O(g) 2SO (g) ΔH=akJ·mol-1,反应过程的能量变化如图所示,已知1molSO (g)完全转化为
2 2 3 2
lmolSO (g)放热99kJ。请回答:
3
(4)a=____kJ·mol-1。
(5)E 的大小对该反应的ΔH____(填“有”或“无”)影响。该反应常用VO 作催化剂,加入VO 会使图中
a 2 5 2 5
B点____(填“升高”、“降低”或“不变”)。
(6)III.由盖斯定律结合下述反应方程式,回答问题:
已知:①C(s)+O(g)=CO (g) ΔH ;
2 2 1
②2CO(g)+O(g)=2CO (g) ΔH ;
2 2 2
③TiO(g)+2Cl (g)=TiCl (s)+O(g) ΔH ;
2 2 4 2 3
则TiO(s)+2Cl (g)+2C(s)=TiCl (s)+2CO(g)的ΔH=____。(列出关于ΔH、ΔH、ΔH 的表达式)
2 2 4 1 2 3
【答案】(1) 石墨 -393.5kJ·mol-1
(2)631.5
(3)2NO(g)+2CO(g)=N (g)+2CO (g)ΔH=-746.0kJ·mol-1
2 2
(4)-198
(5) 无 降低
(6)2ΔH -ΔH +ΔH
1 2 3
【解析】(1)图中金刚石能量高于石墨,能量越低越稳定,所以石墨稳定;1mol石墨完全燃烧生成1mol二
氧化碳放出的热量为11.05kJ+283.0kJ=393.5kJ,则石墨的燃烧热为ΔH=-393.5kJ·mol-1;
(2)ΔH=反应物键能之和-生成物键能之和,设NO分子中化学键的键能为X,则有:
946kJ·mol-1+497kJ·mol-1-2X=180kJ·mol-1解得:X=631.5kJ·mol-1;
(3)CO和NO反应的化学方程式为2NO(g)+2CO(g)=N (g)+2CO (g);
2 2
已知①C(石墨,s)+O(g)=CO (g)ΔH=-393.5 kJ·mol-1;
2 2
②C(石墨,s)+ O(g)=CO(g)ΔH=-110.5 kJ·mol-1;
2③N(g)+O(g)=2NO(g)ΔH=+180kJ·mol-1;
2 2
由盖斯定律:方程式①×2-②×2-③得2NO(g)+2CO(g)=N (g)+2CO (g)ΔH=-746.0kJ·mol-1;
2 2
(4)因1mol SO (g)氧化为1mol SO 的ΔH=-99kJ·mol-1,所以2molSO (g)氧化为2molSO 的ΔH=-198kJ•mol-1,
2 3 2 3
则2SO (g)+O(g)=2SO(g)ΔH=-198kJ·mol-1,即a=-198kJ·mol-1;
2 2 3
(5)E 为正反应活化能,据图可知ΔH为正逆反应活化能之差,所以E 的大小对该反应的ΔH无影响;催化
a a
剂可以降低反应活化能,使图中B点降低;
(6)根据盖斯定律③+①×2-②得到TiO(s)+2Cl (g)+2C(s)=TiCl (s)+2CO(g) ΔH=2ΔH-ΔH +ΔH 。
2 2 4 1 2 3
考点三 反应热比较大小
【例3-1】下列焓变比较正确的是
A.
B.
C.
D.
【答案】B
【解析】A.基态的气态原子失去最外层的1个电子所需能量叫做第一电离能,同一主族元素自上而下第
一电离能逐渐减小,原子序数Na ΔH >0,A错误;
1 2
B.非金属元素原子得电子释放能量,非金属性越强,得电子形成的阴离子越稳定,释放出来能量越多,
因为非金属性Cl>Br,所以0<ΔH <ΔH ,B正确;
1 2
C.构成离子晶体的阴、阳离子半径越小,电荷数越多,离子键越牢固,电离断键时吸收能量越多,
r(Cl-)ΔH >0,C错误;
1 2
D.物质不同聚集状态能量通常是气态>液态>固态,氢气与氯气反应放热,故生成HCl(l)放出热量更多,
0>ΔH >ΔH ,D错误;
1 2
答案选B。
【例3-2】(2022·浙江·效实中学高一期中)已知强酸与强碱在稀溶液里反应的中和热可表示为H+(aq)+
OH-(aq)=H O(l) ΔH=-57.3kJ·mol-1。现有下列反应:
2
NH ·H O(aq)+HCl(aq)=NHCl(aq)+HO(l) ΔH
3 2 4 2 1
HSO (浓)+NaOH(aq)= NaSO (aq)+HO(l) ΔH
2 4 2 4 2 2
HNO(aq)+NaOH(aq)=NaNO (aq)+HO(l) ΔH
3 3 2 3上述反应均在溶液中进行,则下列ΔH、ΔH、ΔH 的关系正确的是
1 2 3
A.ΔH>ΔH >ΔH B.ΔH>ΔH >ΔH
2 3 1 1 3 2
C.ΔH=ΔH =ΔH D.ΔH=ΔH >ΔH
1 2 3 2 3 1
【答案】B
【解析】由于CHOOH为弱电解质,与NaOH反应过程中CHOOH继续电离要吸收一部分热量,故最终
3 3
生成1 mol H O时放出热量小于57.3 kJ,浓硫酸遇水放出大量热量,故浓硫酸与NaOH反应生成1 mol H O
2 2
时放出热量大于57.3 kJ,HNO 与NaOH反应生成1 mol H O时放出热量等于57.3 kJ,由于中和反应为放热
3 2
反应,故放热越多,反应热数值越小,故ΔH>ΔH >ΔH ,所以答案选B。
1 3 2
【一隅三反】
1.(2022·江苏淮安·高二期中)已知:(1)CO(g)+ O(g)= CO (g) ΔH=-a kJ·mol-1
2 2 1
(2)2CO(g)+O(g)=2CO (g) ΔH=-bkJ·mol-1
2 2 2
(3)CO(g)+ O(g)= CO (s) ΔH=-c kJ·mol-1
2 2 3
(4)2CO(g)+ O(g)=2CO (s) ΔH=-d kJ·mol-1
2 2 4
下列关系式中不正确的是
A.ab/2,D选项错误;
答案选D。
2.下列各组热化学方程式中,化学反应的 前者小于后者的有
A. ;
B. ;
C.
D. ;【答案】A
【解析】A.S(g)+O(g)═SO (g) H S(s)+O (g)═SO (g) H,固体硫转变为气态硫需要吸收热量,所以固
2 2 1 2 2 2
体硫完全燃烧放出的热量偏小,△但放热反应 H<0,所△以化学反应的 H前者小于后者,A符合题意;
B.CaCO
3
(s)═CaO(s)+CO
2
(g) H
3
CaO(s)+H△2 O(1)═Ca(OH)
2
(s) H
4
,Ca△CO
3
分解吸热, H
3
>0,CaO(s)
+H O(1)═Ca(OH) (s)放热, △H<0,所以化学反应的 H前者△大于后者,B不符合题意△;
2 2 4
△ △
C.HCl(aq)+NaOH(aq)═NaCl(aq)+H O(1) H HSO (浓)+NaOH(aq)═ NaSO (aq)+H O(l) H,浓硫酸溶
2 5 2 4 2 4 2 6
△ △
于水放热,前者大于后者,C不符合题意;
D.一氧化碳是碳单质不完全燃烧的产物,完全燃烧时生成二氧化碳,完全燃烧放热更多,所以 H前者
大于后者,D不符合题意;故选A。 △
3.(2022·广东揭阳·高二期末)已知:2H(g)+O(g)=2HO(g) ΔH
2 2 2 1
3H(g)+ Fe O(s)=2Fe(s)+ 3H O(g) ΔH
2 2 3 2 2
2Fe(s)+ 1.5O(g)=Fe O(s) ΔH
2 2 3 3
2Al(s)+ 1.5O(g)=A1 O(S) ΔH
2 2 3 4
2Al(s)+ Fe O(s)=Al O(s)+ 2Fe(s) ΔH
2 3 2 3 5
下列关于上述反应恰变的判断正确的是
A.ΔH<0,ΔH>0 B.ΔH<0,ΔH<ΔH
1 3 5 4 3
C.ΔH=ΔH+ΔH D.ΔH=ΔH+ΔH
1 2 3 3 4 5
【答案】B
【解析】A.2Fe(s)+ 1.5O(g)=Fe O(s)为化合反应,属于放热反应,所以ΔH<0,A不正确;
2 2 3 3
B.2Al(s)+ Fe O(s)=Al O(s)+ 2Fe(s)为铝热反应,属于放热反应,ΔH<0,由于Al的金属活动性比Fe强,
2 3 2 3 5
所以燃烧放出的热量更多,但由于放热反应的ΔH<0,所以ΔH<ΔH,B正确;
4 3
C.ΔH 为2H(g)+O(g)=2HO(g)放出的热量,ΔH+ΔH 为3H(g)+1.5O (g)=3HO(g)放出的热量,所以
1 2 2 2 2 3 2 2 2
ΔH≠ΔH+ΔH,C不正确;
1 2 3
D.依据盖斯定律,ΔH=ΔH-ΔH,D不正确;
3 4 5
故选B。
4.甲烷燃烧的热化学方程式,可用下列两种方程式表示: ,
, 与 的关系为
A. B. C. D.【答案】C
【解析】液态水转化为气态水要吸收能量,因此甲烷燃烧生成液态水比生成气态水放热多,而反应放出的
热量与化学计量数成比例关系,因此 ,答案选C。
5.回答下列问题:
(1)已知:2H(g)+O(g)=2HO(l) ΔH=-571.6 kJ·mol-1
2 2 2
CH(g)+2O(g)=CO (g)+2HO(l) ΔH=-890 kJ·mol-1
4 2 2 2
现有H 与CH 的混合气体112 L(标准状况),使其完全燃烧生成CO 和HO(l),若实验测得反应放热3695
2 4 2 2
kJ,则原混合气体中CH 与H 的物质的量之比是___________。
4 2
(2)25 ℃、101 kPa时,14 g CO在足量的O 中充分燃烧,放出141.3 kJ热量,则能表示CO燃烧热的热化学
2
方程式为___________。
(3)嫦娥”五号预计在海南文昌发射中心发射,火箭的第一、二级发动机中,所用的燃料为偏二甲肼和四氧
化二氮,偏二甲肼可用肼来制备。用肼(N H)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。
2 4
已知:
①N(g)+2O(g)=NO(g) ΔH=+10.7 kJ·mol-1
2 2 2 4
②NH(g)+O(g)=N(g)+2HO(g) ΔH=-543 kJ·mol-1
2 4 2 2 2
写出气态肼和NO 反应的热化学方程式:___________。
2 4
(4)已知:2Fe(s)+ O(g)=Fe O(s) ΔH 2Al(s)+ O(g)=Al O(s) ΔH
2 2 3 1 2 2 3 2
计算2Al(s)+Fe O(s)=Al O(s)+2Fe(s) ΔH=___________(用上述有关ΔH表示);ΔH_____ΔH(填<或=或
2 3 2 3 3 1 2
>符号)
(5)下面列举了一些化学键的键能数据,供计算使用。
化学键 Si-O Si-Cl H-H H-Cl Si-Si Si-C
键能/kJ·mol-1 460 360 436 431 176 347
工业上的高纯硅可通过下列反应制取:SiCl (g)+H(g)→Si(s)+HCl(g),该反应的反应热化学方程式为为
4 2
___________。
【答案】(1)3 ∶1
(2)CO(g)+ O(g)=CO (g) ΔH=-282.6 kJ·mol-1
2 2
(3)2N H(g)+NO(g)=3N(g)+4HO(g) ΔH=-1 096.7 kJ·mol-1
2 4 2 4 2 2
(4) ΔH-ΔH, >
2 1(5)SiCl (g)+2H(g)=Si(s)+4HCl(g) ΔH=+236 kJ·mol-1
4 2
【解析】(1)H 与CH 的混合气体112 L(标准状况),物质的量为 ,设H 的物质的量是
2 4 2
xmol,使其完全燃烧生成CO 和HO(l),若实验测得反应放热3695 kJ,
2 2
,x=1.25mol,则原混合气体中CH 与H 的物质的
4 2
量之比是(5-1.25):1.25=3 ∶1;
(2)CO的燃烧热是1molCO完全燃烧生成二氧化碳放出的能量,25 ℃、101 kPa时,14 g CO在足量的O 中
2
充分燃烧,放出141.3 kJ热量,则1molCO完全燃烧生成二氧化碳放出282.6 kJ,能表示CO燃烧热的热化
学方程式为CO(g)+ O(g)=CO (g) ΔH=-282.6 kJ·mol-1;
2 2
(3)①N(g)+2O(g)=NO(g) ΔH=+10.7 kJ·mol-1
2 2 2 4
②NH(g)+O(g)=N(g)+2HO(g) ΔH=-543 kJ·mol-1
2 4 2 2 2
根据盖斯定律②×2-①得气态肼和NO 反应的热化学方程式是2NH(g)+NO(g)=3N(g)+4HO(g) ΔH
2 4 2 4 2 4 2 2
=-543 kJ·mol-1×2-10.7 kJ·mol-1=-1 096.7 kJ·mol-1;
(4)①2Fe(s)+ O(g)=Fe O(s) ΔH
2 2 3 1
②2Al(s)+ O(g)=Al O(s) ΔH
2 2 3 2
根据盖斯定律②-①得2Al(s)+Fe O(s)=Al O(s)+2Fe(s) ΔH=ΔH -ΔH;铝热反应放热,ΔH-ΔH<0,
2 3 2 3 3 2 1 2 1
ΔH>ΔH ;
1 2
(5)焓变=反应物总键能-生成物总键能,工业上的高纯硅可通过下列反应制取:SiCl (g)+2H(g)=Si(s)+
4 2
4HCl(g)反应的反应热化学方程式为为SiCl (g)+2H(g)=Si(s)+4HCl(g) ΔH=360×4+436×2-176×2-431×4=+
4 2
236 kJ·mol-1。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育