文档内容
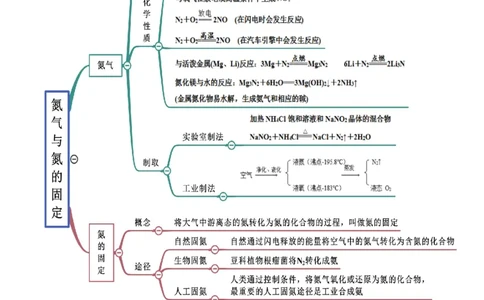
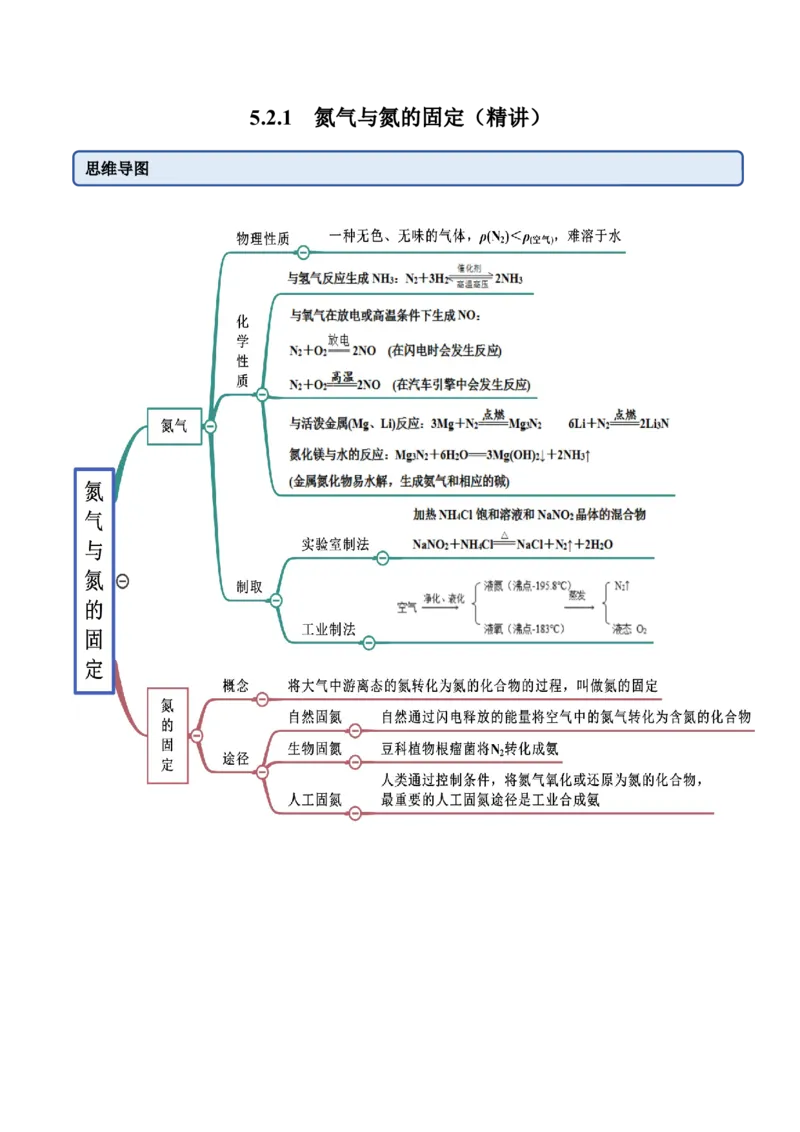
5.2.1 氮气与氮的固定(精讲)
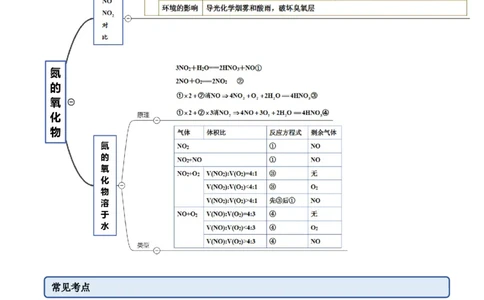
思维导图常见考点考点一 氮的固定
【例1-1】(2021·吉林·汪清县汪清第四中学高一月考)下列过程不属于固氮的是
A.雷电时生成氮的氧化物
B.工业上用氢气与氮气合成氨
C.豆科植物的根瘤菌把空气中的氮气转化为硝酸盐
D.植物的根从土壤中吸收铵根离子和硝酸
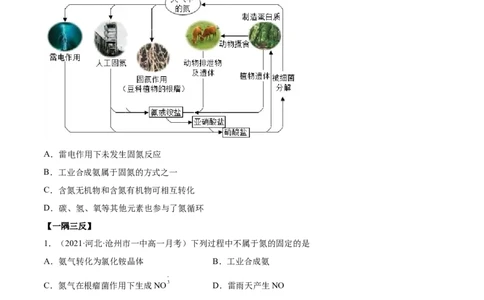
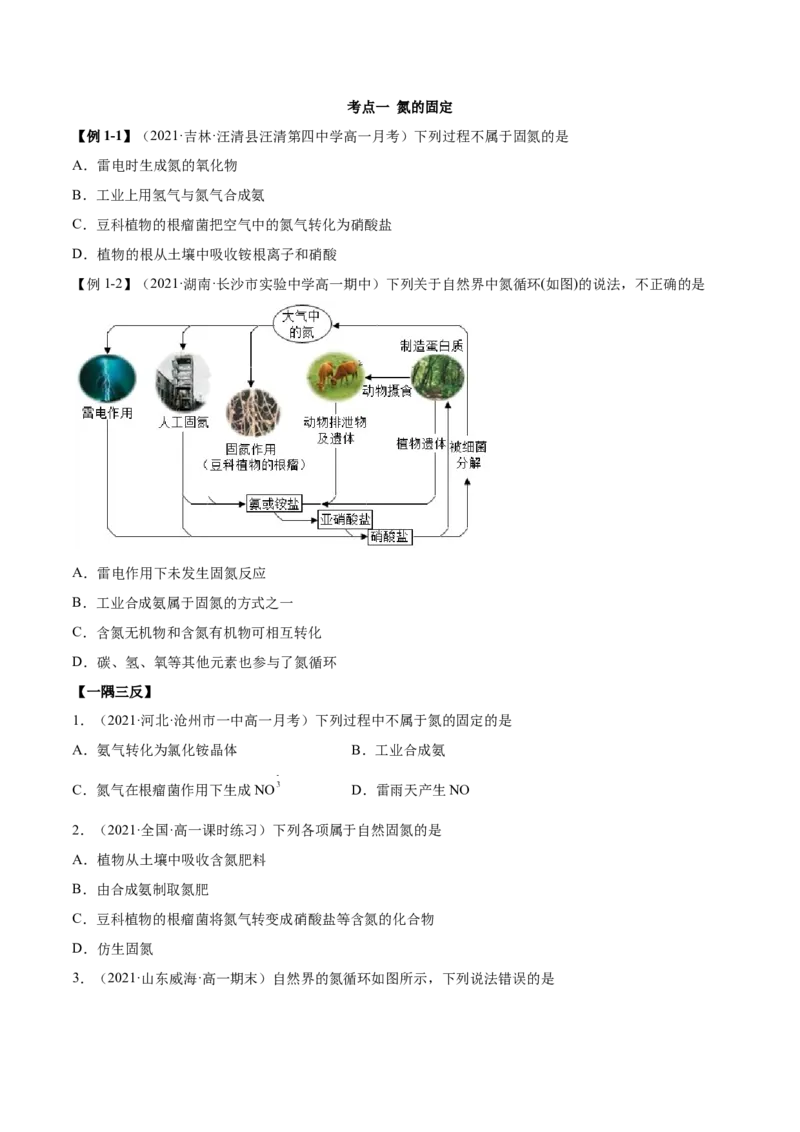
【例1-2】(2021·湖南·长沙市实验中学高一期中)下列关于自然界中氮循环(如图)的说法,不正确的是
A.雷电作用下未发生固氮反应
B.工业合成氨属于固氮的方式之一
C.含氮无机物和含氮有机物可相互转化
D.碳、氢、氧等其他元素也参与了氮循环
【一隅三反】
1.(2021·河北·沧州市一中高一月考)下列过程中不属于氮的固定的是
A.氨气转化为氯化铵晶体 B.工业合成氨
C.氮气在根瘤菌作用下生成NO D.雷雨天产生NO
2.(2021·全国·高一课时练习)下列各项属于自然固氮的是
A.植物从土壤中吸收含氮肥料
B.由合成氨制取氮肥
C.豆科植物的根瘤菌将氮气转变成硝酸盐等含氮的化合物
D.仿生固氮
3.(2021·山东威海·高一期末)自然界的氮循环如图所示,下列说法错误的是A.氮的固定主要有自然固氮和人工固氮两种方式
B.氧元素参与了氮循环
C.①中N 与O 反应直接生成NO ,NO 与水反应生成HNO
2 2 2 2 3
D.②中的合成氨反应中N 为氧化剂
2
考点二 氮气
【例2-1】(2021·北京市第五中学高一期中)下列关于氮气的性质,叙述错误的是
A.氮气在通常条件下化学性质稳定
B.氮气在高温、放电等条件下可以发生化学反应
C.氮气在化学反应中只能做氧化剂
D.氮气在发生化学反应过程中发生了化学键的断裂
【例2-2】(2021·广东·中山市第二中学高一月考)下列关于氮气的说法中,正确的是
A.通常情况下,氮气性质比较稳定
B.可在氧气中燃烧,生成一氧化氮
C.1molN 与3molH 完全反应生成2molNH
2 2 3
D.氮元素是活泼的非金属元素,氮气在化学反应中作氧化剂
【一隅三反】
1.(2021·吉林·长春市榆树高级中学高一期中)下列关于N 的叙述错误的是
2
A.N 既可以做氧化剂又可以做还原剂
2
B.1molN 可与3molH 完全反应生成2molNH
2 2 3
C.氮的固定是将N 转化成含氮的化合物
2
D.在雷雨天,空气中的N 与氧气可反应生成NO
2
2.(2021·广东·忠信中学高一月考)下列关于氮气的说法中不正确的是
A.固氮菌能把空气中的游离氮转化为化合物形态的铵态氮B.反应N+O 2NO是汽车尾气造成空气污染的主要因素之一
2 2
C.大气、陆地和水体中的氮元素在不停地进行着氮的循环
D.在反应3Mg+N MgN 中,N 作还原剂
2 3 2 2
3.(2021·吉林·大安市第六中学校高一期中)下列关于氮气的说法错误的是
A.氮气在通常情况下不燃烧,也不支持燃烧,不能供给呼吸
B.液氮可用于医学和高科技领域,制造低温环境
C.利用氮气的稳定性,工业上用来替代稀有气体作焊接金属的保护气
D.在高温高压、催化剂条件下与氢气反应时,氮气作还原剂
4.(2021·辽宁·盘锦市第二高级中学高一月考)下列关于N 的叙述错误的是
2
A.N 既可作氧化剂又可作还原剂
2
B.雷雨天,空气中的N 和O 可反应生成NO
2 2
C.氮的固定是将N 转化成含氮化合物的过程
2
D.氮气的化学性质比较活泼,通常情况下可以与很多物质发生反应
考点三 一氧化氮和二氧化氮的性质
【例3】(2021·山东济南·高一期末)下列对 和 的描述正确的是
A. 与水的反应中, 既是氧化剂又是还原剂
B. 是无色气体,可用向上排空气法收集
C. 可由 和 直接化合得到
D.实验室制取 ,可以通过金属铜与浓硝酸反应制得
【一隅三反】
1.(2021·全国·高一课时练习)下列关于 及氮的氧化物的说法正确的是
A. 化学性质稳定,可用作保护气
B. 、 均为大气污染气体,在大气中可稳定存在C. 、 均易溶于水
D. 能与水直接化合
2.(2021·福建·文博中学高一期中)下列说法正确的是
A.实验室能用排空气法收集N、NO和NO
2 2
B.NO为红棕色气体,NO 为无色气体
2
C.除去NO中的NO 气体可以使混合气体通过蒸馏水
2
D.NO、NO 、NO、NO 都属于酸性氧化物
2 2 4 2 5
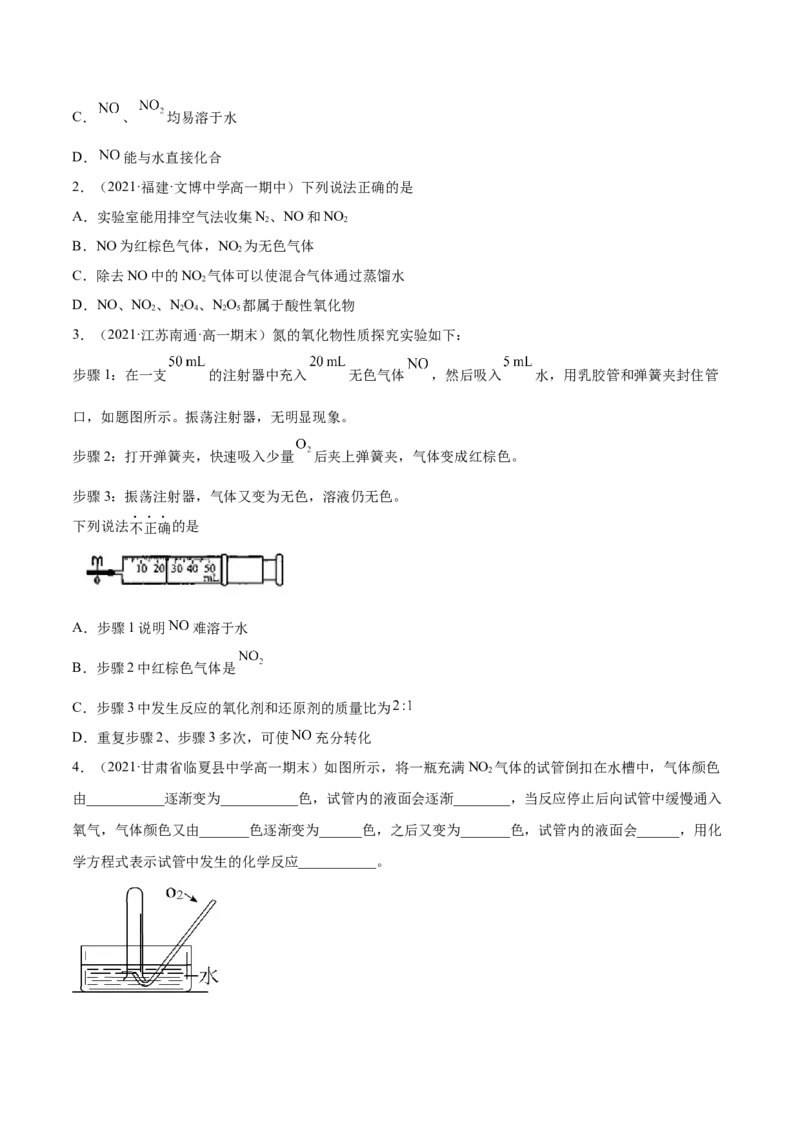
3.(2021·江苏南通·高一期末)氮的氧化物性质探究实验如下:
步骤1:在一支 的注射器中充入 无色气体 ,然后吸入 水,用乳胶管和弹簧夹封住管
口,如题图所示。振荡注射器,无明显现象。
步骤2:打开弹簧夹,快速吸入少量 后夹上弹簧夹,气体变成红棕色。
步骤3:振荡注射器,气体又变为无色,溶液仍无色。
下列说法不正确的是
A.步骤1说明 难溶于水
B.步骤2中红棕色气体是
C.步骤3中发生反应的氧化剂和还原剂的质量比为
D.重复步骤2、步骤3多次,可使 充分转化
4.(2021·甘肃省临夏县中学高一期末)如图所示,将一瓶充满NO 气体的试管倒扣在水槽中,气体颜色
2
由___________逐渐变为___________色,试管内的液面会逐渐________,当反应停止后向试管中缓慢通入
氧气,气体颜色又由_______色逐渐变为______色,之后又变为_______色,试管内的液面会______,用化
学方程式表示试管中发生的化学反应___________。考点四 一氧化氮和二氧化氮的相关计算
【例4-1】(2021·湖北·鄂州市鄂东高级中学高一月考)NO、NO 、O 按照一定比例通入水中,能被完全
2 2
吸收,无剩余气体。若NO、NO 、O 的气体体积分别为x、y、z,则x:y:z可能为
2 2
A.1:9:3 B.5:1:2 C.1:2:5 D.3:6:2
【例4-2】(2021·湖北·华中师大一附中高一期中)I.如图所示:在B水槽中装有500mL水,容积为a mL
的试管A充满了NO 和NO的混合气体(标准状况),将试管A倒插入B水槽的水中。充分反应后,试管A
2
中余下气体的体积为0.5a mL。
(1)通过导气管C向余下0.5a mL气体的试管A中持续通入氧气,A中可能观察到的现象是___________。
(2)当试管A中充满气体时停止通入氧气,然后将试管取出水槽,水槽B中溶液的物质的量浓度为
___________mol·L−1(设溶液的体积仍为500mL)。
II.将一定量铁粉和铜粉混合均匀后分为四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成
NO的体积和剩余金属的质量如表所示(设HNO 的还原产物只有NO):
3
实验序号 I II III IV
稀硝酸的体积/mL 50 100 150 175
剩余金属的质量/g 9.0 4.8 0 0
NO的体积(标准状况)/mL 1120 2240 3360 V
(3)每等份混合物的质量为___________g。
(4)稀硝酸的物质的量的浓度为___________mol/L。
(5)V=___________。
【一隅三反】
1.(2021·全国·高一期末)在标准状况下将3.84g铜粉投入一定量浓HNO 中,随着铜粉的溶解,反应生
3
成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由NO 和NO组成的混合气体1.12L,则反应消耗
2
HNO 的物质的量为
3
A.0.17mol B.0.15mol C.0.12mol D.无法计算
2.(2021·四川·三台县芦溪中学高一开学考试)盛有总体积为18mL的NO 、O 混合气体的试管倒立于水
2 2槽中,充分反应后剩余3mLO ,则O 原体积可能为
2 2
A.6mL B.4.5mL C.2mL D.1.8mL
3.(2021·浙江舟山·)常温常压下,将盛有20 mL NO 和O 的混合气体的大试管倒立在水槽中,水面上升
2 2
至一定位置后不再变化,此时还有3 mL气体,则原混合气体中的NO 的体积可能是
2
A.17.8 mL B.14.8 mL C.12.6 mL D.12.4 mL
4.(2021·吉林·白城一中高一期中)将气体体积分别为VmL、VmL、VmL的NO、NO 、O 混合于一支
1 2 3 2 2
大试管中,将此大试管倒立于水槽中,最终大试管内充满水。则V、V、V 之比可能是
1 2 3
A.3:4:5 B.5:1:4 C.4:2:3 D.3:2:6
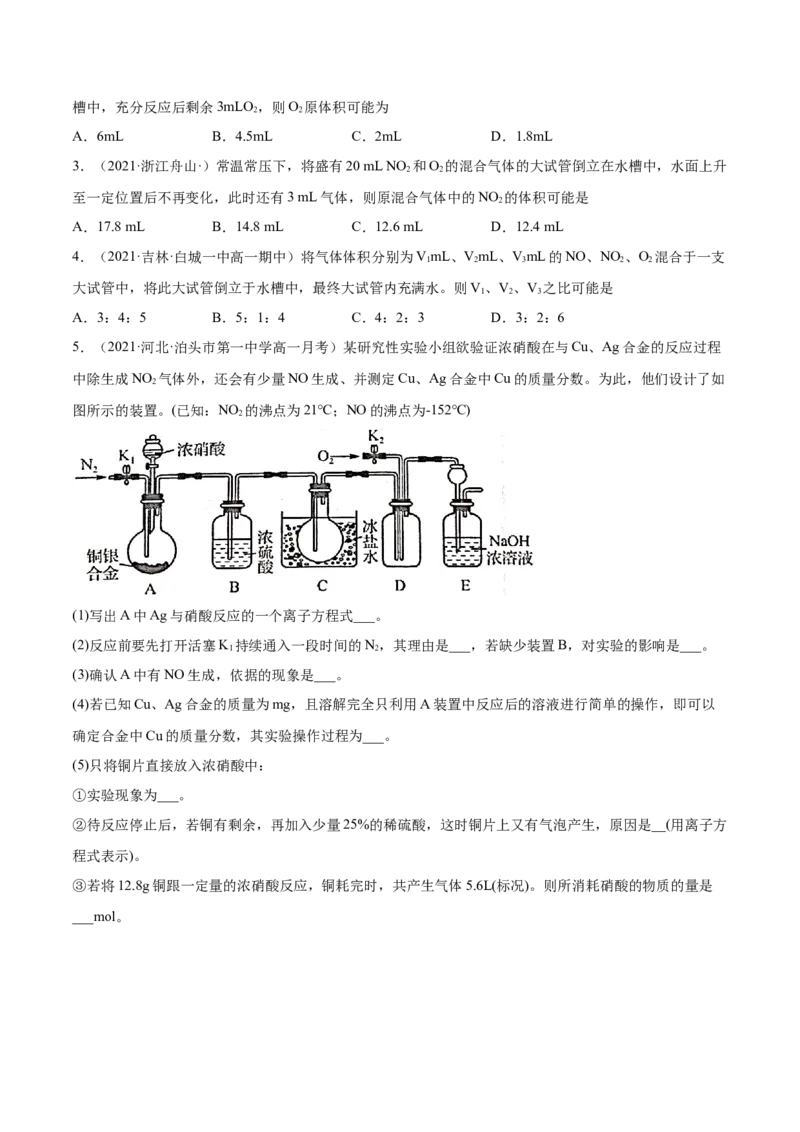
5.(2021·河北·泊头市第一中学高一月考)某研究性实验小组欲验证浓硝酸在与Cu、Ag合金的反应过程
中除生成NO 气体外,还会有少量NO生成、并测定Cu、Ag合金中Cu的质量分数。为此,他们设计了如
2
图所示的装置。(已知:NO 的沸点为21℃;NO的沸点为-152℃)
2
(1)写出A中Ag与硝酸反应的一个离子方程式___。
(2)反应前要先打开活塞K 持续通入一段时间的N,其理由是___,若缺少装置B,对实验的影响是___。
1 2
(3)确认A中有NO生成,依据的现象是___。
(4)若已知Cu、Ag合金的质量为mg,且溶解完全只利用A装置中反应后的溶液进行简单的操作,即可以
确定合金中Cu的质量分数,其实验操作过程为___。
(5)只将铜片直接放入浓硝酸中:
①实验现象为___。
②待反应停止后,若铜有剩余,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,原因是__(用离子方
程式表示)。
③若将12.8g铜跟一定量的浓硝酸反应,铜耗完时,共产生气体5.6L(标况)。则所消耗硝酸的物质的量是
___mol。倒卖拉黑不更新,淘宝唯一免费更新店铺:知二教育