文档内容
1、 氧化还原反应的判断方法
(1)判断反应是否为氧化还原反应,要抓住两个关键:一是
准确判断各反应物、生成物中各元素的化合价及其变化;
二是牢记“凡是有元素化合价升降的化
学反应都是氧化还原反应”。
(2)氧化反应和还原反应同时发生,有氧化必有还原,化合
价有升必有降。
对点练习1.有关氧化还原反应的叙述正确的是( )
A.氧化还原反应的判断是看有无元素化合价的升降
B.氧化还原反应的判断是看有无氧元素的得失
C.化合反应肯定不是氧化还原反应
D.氧化还原反应中一定有两种元素的价态发生改变
【答案】A
【详解】
A.有无化合价的变化是判断是否为氧化还原反应依据,故正确;
B.有的氧化还原反应中没有氧元素参与,故B错误;
C.化合反应不一定有化合价变化,故不一定是氧化还原反应,
故错误;D.氧化还原反应中一定有元素的化合价变化,
但不一定有两种元素化合价改变,故错误。故选A2、 氧化还原反应与四种基本反应类型
(1)氧化还原反应与四种基本反应类型之间的关系
①两个可能:化合反应和分解反应可能是氧化还原反应。
②两个一定:置换反应一定是氧化还原反应,复分解反应一
定是非氧化还原反应。
③有单质参加的化合反应或有单质生成的分解反应一定是氧
化还原反应。
(2)四种基本反应类型不包括所有的反应,有些反应属于氧
化还原反应,但不属于四种基本反应类型。
例如:4HCl(浓)+MnO =====MnCl +Cl ↑+2H O不属于四种
2 2 2 2
基本反应类型中的任何一种反应类型,但属于氧化还原反应。
(3)有单质参加或生成的反应不一定是氧化还原反应。如同
素异形体之间的相互转化(如3O =2O )不属于氧化还原反应。
2 3
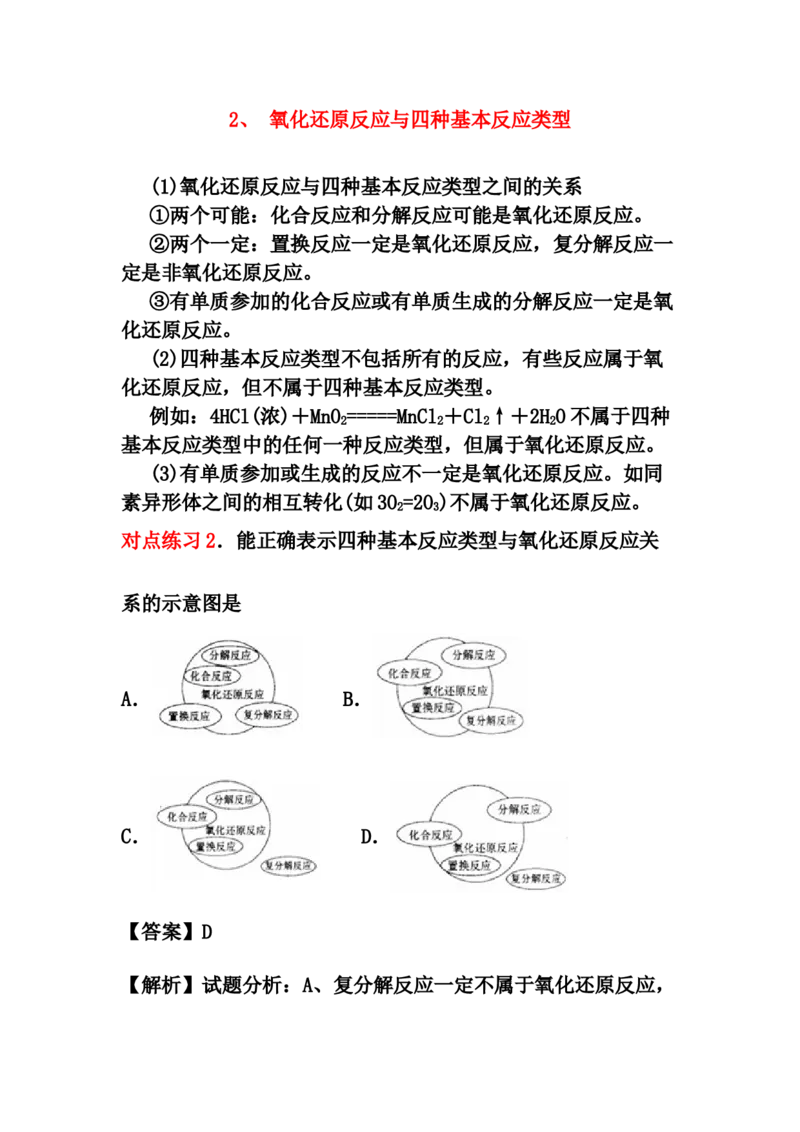
对点练习2.能正确表示四种基本反应类型与氧化还原反应关
系的示意图是
A. B.
C. D.
【答案】D
【解析】试题分析:A、复分解反应一定不属于氧化还原反应,则不会出现交叉,置换反应一定属于氧化还原反应,则应为包
含,部分的化合与分解反应属于氧化还原反应,则不能是包含,
应为交叉关系,故A错误;B、复分解反应一定不属于氧化还原
反应,则不会出现交叉,故B错误;C、有单质生成的分解反应
属于氧化还原反应,则分解反应与氧化还原反应的关系为交叉,
不是全包含,故C错误;D、置换反应一定属于氧化还原反应,
则是包含关系,复分解反应一定不属于氧化还原反应,则不是
包含也不是交叉关系,有单质生成的分解反应属于氧化还原反
应,有单质参加的化合反应属于氧化还原反应,则化合、分解
反应与氧化还原反应都是交叉关系,故D正确;故选D。
考点:考查了氧化还原反应与四种基本反应类型的关系的相关
知识。
3、 氧化还原反应过程中的得失电子守恒
氧化还原反应遵循得失电子守恒,即发生氧化反应的物质失
去的电子总数与发生还原反应的物质得到的电子总数相等。同时,化合价升高的总价数与化合价降低的总价数相等。
对点练习3.离子间发生氧化还原反应时存在质量守恒、电子
守恒、电荷守恒等规律。在一定条件下,RO n-和I-发生如下反
3
应:RO n-+6I-+6H+=R-+3I +3H O。则
3 2 2
(1)RO n-中n的值为______________,利用原理是
3
___________________
(2)RO n-中R的化合价为_________,利用原理是
3
_____________________
【答案】1 电荷守恒 +5 电子守恒
【解析】
【详解】
(1)根据电荷守恒可知RO n−+6I−+6H+=R−+3I +3H O中, −n+
3 2 2
(−6)+(+6)=−1,解得n=1;答案:1; 电荷守恒。
(2)设RO n-中R的化合价为+x,可见R元素的化合价由+x降
3
至-1价,I元素的化合价由-1价升至0价,根据电子守恒可知,
+x-(-1)=6×[0-(-1)],解得x=5;故答案为: +5;电子守恒。
【点睛】
根据电荷守恒、电子守恒来解答此题。在RO n-+6I-+6H+=R-
3
+3I +3H O中,也可利用RO n-中正负化合价的代数和为-n计算其
2 2 3
中R的化合价。
4、理解氧化还原反应的相关概念,要抓住两条线
(1)还原剂化合价升高→失去电子→发生氧化反应(被氧
化)→生成氧化产物。
(2)氧化剂化合价降低→得到电子→发生还原反应(被还
原)→生成还原产物。
对点练习4、在5NH NO =4N +2HNO +9H O的反应中,(1)氧化剂
4 3 2 3 2
是 ,(2)还原剂是 ,(3)氧化产物是
,(4)还原产物是 ,(5)被氧化的元素是 ,
(6)被还原的元素是 (7)氧化产物与还原产物的物质
的量之比是 。
【答案】(1)NH NO (2)NH NO (3)N (4)N (5)N (6)N
4 3 4 3 2 2(7)5:3
【解析】
【分析】
判断氧化还原反应中的氧化剂与还原剂需先标注变价元素原子
的化合价。本反应中变价的为N元素,因此标注化合价为:
。从产物中看出有两个NO -未变价,剩
3
余反应物中NH +和NO -均变为0价,据此解题。
4 3
【详解】
(1)氧化剂是反应中化合价降低的物质,因此为NH NO 中
4 3
的硝酸根离子,答案应写:NH NO ;(2)还原剂是反应中化合
4 3
价升高的物质,因此为NH NO 中的铵根离子,答案应写:
4 3
NH NO ;(3)氧化产物是反应物通过升高价态所得,因此为
4 3
N ;(4)还原产物是反应物通过降低价态所得,因此为N ;
2 2
(5)被氧化的元素是氮元素;(6)被还原的元素是氮元素
(7)由5mol铵根离子生成的氧化产物N 为2.5mol;由3mol硝
2
酸根离子生成的还原产物N 为1.5mol,因此氧化产物与还原产
2
物的物质的量之比是5:3。
5、 单、双线桥法表示氧化还原反应时注意的问题
(1)双线桥法书写注意事项
①箭头、箭尾指向有化合价变化的同种元素。
②必须注明“得”或“失”。
③失去的电子总数与得到的电子总数相等。转移电子数目以m×n e-的形式表示,m表示发生氧化还原反应的原子或离子数,
n表示每个原子或离子得到或失去电子的数目,m=1或n=1时,
要省去。
④箭头方向不代表电子转移的方向,仅表示电子转移前后的
变化。
(2)单线桥法书写注意事项
①箭头表明电子转移的实际情况,箭头的方向从还原剂中失
去电子(或共用电子对偏离)的元素指向氧化剂中得到电子(或共
用电子对偏向)的元素。
②只标明电子转移的数目,不需注明“得”“失”。
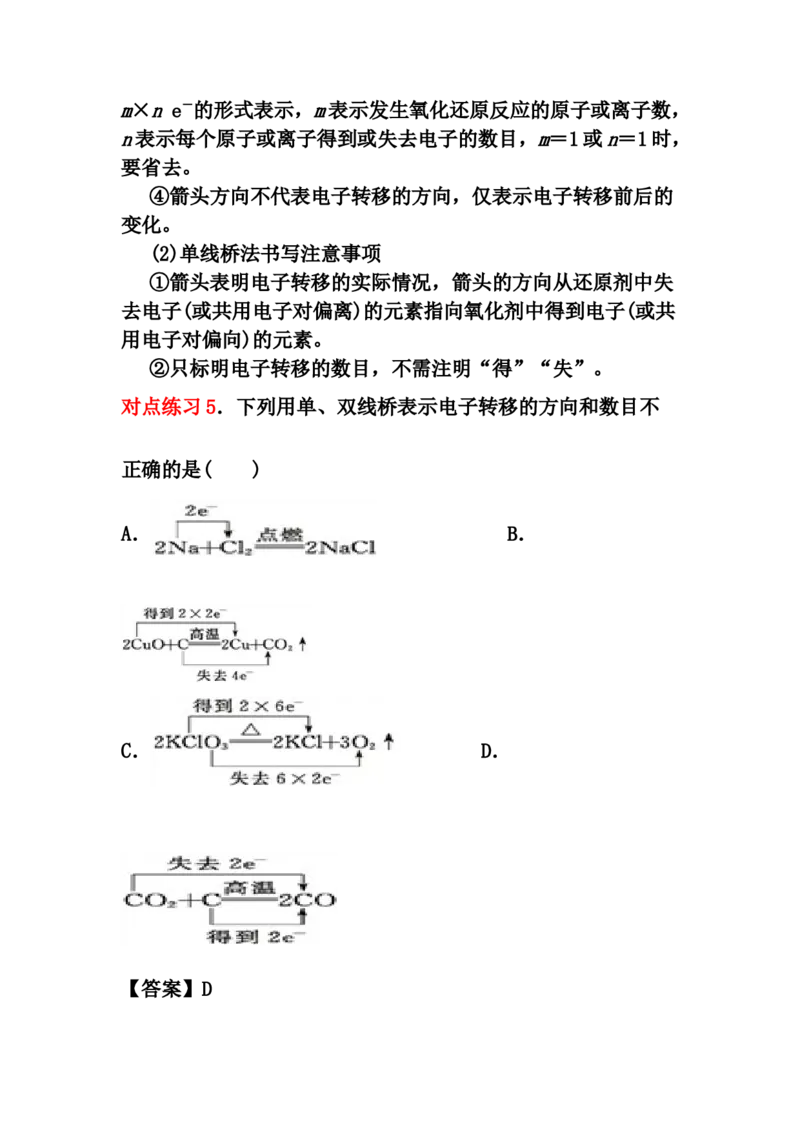
对点练习5.下列用单、双线桥表示电子转移的方向和数目不
正确的是( )
A. B.
C. D.
【答案】D【解析】
A、转移电子为2×[5-(-1)]=12,故A错误,B、得失电子数目
正确,以及双线桥的表示正确,故B正确;C:C的化合价升高,
C应是失去电子,Cu应是得到电子,故C错误;D:1mol氧气得
到4mole-,得失电子数目应守恒,故D错误。
点睛:本题的易错点是选项C和D,一是忘记氧化剂和还原剂的
概念,失去电子、化合价升高的物质为还原剂,反之为氧化剂,
二应注意得失电子数目守恒。
6、 应用化合价判断元素的氧化性和还原性
氧化性和还原性的确定:元素处于最高价时,只有氧化性;
元素处于最低价时,只有还原性;元素处于中间价态时,既有
氧化性又有还原性。
对点练习 6.从元素化合价和物质类别两个角度学习、研究
物质的性质,是一种行之有效的方法。以下是氯元素形成物质
的二维图的部分信息。(1)根据图中信息,写出任意两种氯的氧化物的化学式
_____________。
(2)写出高氯酸(HClO )与 NaOH 反应的化学方程式
4
__________。
(3)HCl既具有氧化性,又具有还原性。
①请任意写出一个体现HCl氧化性的离子方程式__________。
②浓 HCl 可作为还原剂在加热条件下与 MnO 发生反应制备
2
Cl ,写出该反应的化学方程式___________。
2
(4)Cl 既具有氧化性,又具有还原性,请结合上图说明原
2
因_________。潮湿的 Cl 与 Na CO 混合制取少量 Cl O 的反应中,
2 2 3 2
Cl 既体现了氧化性,也体现了还原性。写出反应的化学方程式
2
_________。
【答案】 Cl O、Cl O 、ClO 、Cl O 、Cl O 等中任意两种
2 2 3 2 2 5 2 7
HClO +NaOH=NaClO +H O Zn+2H+=Zn2++H ↑ Fe+2H+=Fe2++H ↑
4 4 2 2 2
MnO +4HCl(浓 MnCl +Cl ↑+2H O Cl 中 Cl 元素化合价为 0
2 2 2 2 2
价,氯元素还有-1 价以及+1 等价态,因此氯元素化合价可以升
高,氯气体现还原性;氯元素化合价可以降低,氯气体现氧化
性。 2Cl +2Na CO +H O=2NaHCO +2NaCl+Cl O
2 2 3 2 3 2
【解析】(1)根据图中信息可知氯元素的常见正化合价有
+1、+3、+4、+5、+7 等,因此氯的氧化物的化学式有 Cl O、
2
Cl O 、ClO 、Cl O 、Cl O 等。(2)高氯酸(HClO )是一元强
2 3 2 2 5 2 7 4
酸,与 NaOH 反应的化学方程式为 HClO +NaOH=NaClO +H O。
4 4 2
(3)①金属与盐酸反应生成氢气体现氯化氢的还原性,例如
Zn+2H+=Zn2++H ↑、Fe+2H+=Fe2++H ↑等。②浓 HCl 可作为还原剂
2 2在加热条件下与 MnO 发生反应制备 Cl ,该反应的化学方程式为
2 2
MnO +4HCl(浓 MnCl +Cl ↑+2H O。(4)Cl 中 Cl 元素化合
2 2 2 2 2
价为 0 价,氯元素还有-1 价以及+1 等价态,因此氯元素化合价
可以升高,氯气体现还原性;氯元素化合价可以降低,氯气体
现氧化性,即 Cl 既具有氧化性,又具有还原性;潮湿的 Cl 与
2 2
Na CO 混合制取少量 Cl O 的反应中,Cl 既体现了氧化性(还原
2 3 2 2
产物是氯化钠),也体现了还原性(氧化产物是 Cl O),因此
2
根据原子守恒以及电子得失守恒可知反应的化学方程式为
2Cl +2Na CO +H O=2NaHCO +2NaCl+Cl O。
2 2 3 2 3 2
7、应用氧化还原反应判断物质氧化性、还原性强弱
(1)氧化性:氧化剂>氧化产物。
(2)还原性:还原剂>还原产物。
对点练习 7、有 A、B、C、D 四种物质,已知它们能发生下列变
化:
①A2++B=B2++A ②A2++C=C2++A
③B2++C=C2++B ④C2++D=D2++C
由此可推知,各物质的氧化性、还原性强弱顺序正确的是
①氧化性:A2+>B2+>C2+>D2+
②氧化性:D2+>C2+>B2+>A2+
③还原性:A>B>C>D
④还原性:D>C>B>AA.①③ B.①④ C.②④ D.②③
【答案】B
【解析】
试题分析:同一氧化还原反应中氧化剂的氧化性大于氧化产物
的氧化性;还原剂的还原性大于还原产物的还原性;① A2++
B=B2++A,氧化性 A2+>B2+;还原性 B>A;② A2++C=C2++A,氧
化性 A2+>C2+;还原性 C>A;③ B2++C=C2++B,氧化性 B2+>C2
+;还原性 C>B;④ C2++D=D2++C,氧化性 C2+>D2+;还原性
D>C,故B正确。
考点:本题考查氧化性、还原性比较。
8、. 条件不同,反应不同
钠与氧气反应的条件不同,则反应产物不同。钠在常温下与
氧气反应生成氧化钠,在加热条件下与氧气反应生成过氧化钠。
对点练习8、下列反应物质间发生反应, 在不同条件下可制得
不同产物的是( )
A.铁与氯气 B.稀HCl与硝酸银溶液 C.钠与氧气
D.钠与水【答案】C
【解析】A项,铁与氯气反应只能生成FeCl ;B项,稀HCl与
3
硝酸银溶液反应只能生成AgCl和HNO ;C项,钠与氧气常温反
3
应生成Na O,点燃反应生成Na O ;D项,钠与水反应生成NaOH
2 2 2
和氢气;在不同条件下可制得不同产物的是C,答案选C。
【点睛】易错提醒:铁与氯气反应时,由于氯气具有强氧化性,
只能生成FeCl ,即使铁过量也不会生成FeCl 。
3 2