文档内容
2.2.1 化学平衡状态 化学平衡常数(学案)
1.理解化学平衡的概念以及可逆反应。
2.能用平衡状态的特征来判断可逆反应是否达到平衡状态。
3.知道化学平衡常数的含义并能利用化学平衡常数进行简单的计算。
1.化学平衡状态的判定。
2.利用化学平衡常数进行简单的计算。
达到化学反应限度的特征是________________________________。
一、可逆反应与不可逆反应
1.可逆过程
(1)可逆过程
当温度一定时,饱和溶液中的固体溶质溶解和溶质分子回到固体表面的结晶过程一直在进行,而
且两种过程的速率____,于是饱和溶液的浓度和固体溶质的质量都____。
(2)表述
约定采用“____”来代替反应式中原来用的“____”,把从左向右的过程称作_______________;
由右向左的反应称作_______________。
2.可逆反应与不可逆反应
(1)可逆反应
在________下,既能向__________同时又能向____________进行的反应。
(2)不可逆反应
在一定条件下,几乎所有的反应都具有不同程度的可逆性,但有些反应的逆反应进行程度太小因
而可忽略。如Ag++Cl- AgCl↓
二、化学平衡的建立
1.化学平衡的建立
以CO+HO(g) CO+H 反应为例。
2 2 2
在一定条件下,将0.01molCO和0.01molHO(g)通入1L密闭容器中,开始反应:
2(1)反应刚开始时:
反应物的浓度为_______,正反应速率为_______。
生成物的浓度为______, 逆反应速率为________。
(2)反应进行中:
反应物的浓度___________,正反应速率____________。
生成物的浓度_____________,逆反应速率_______________。
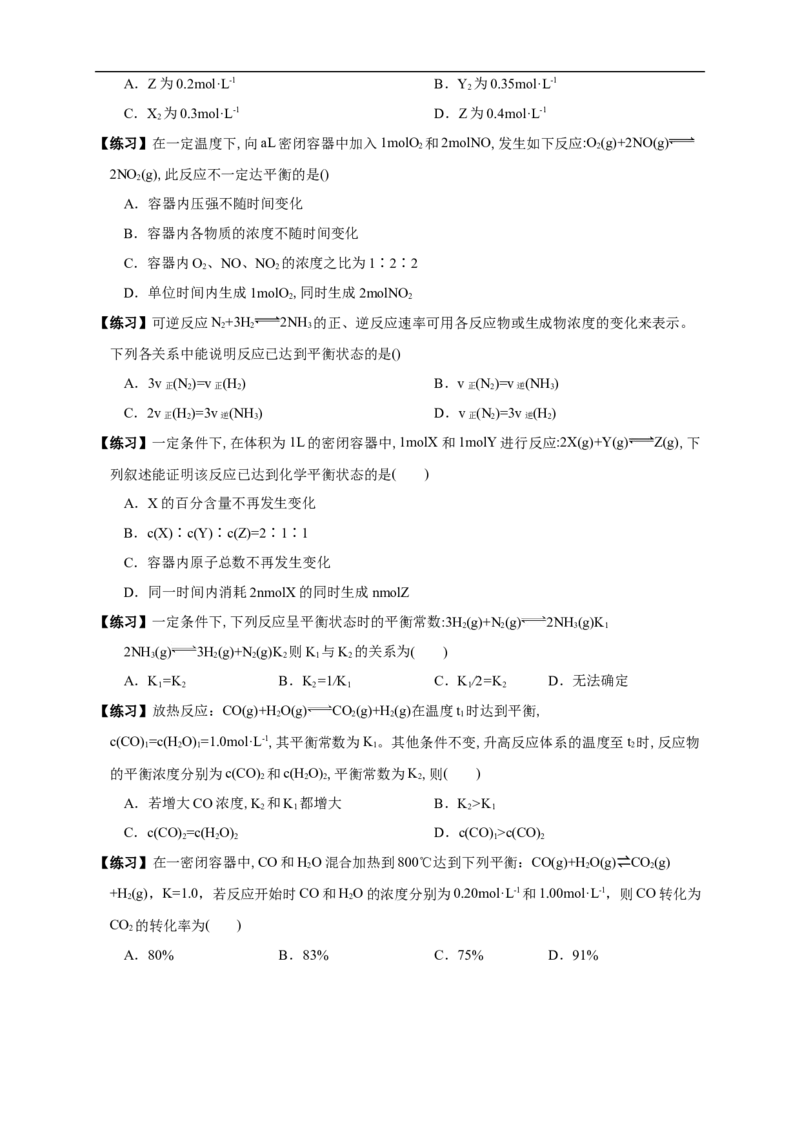
(3)肯定最终有一时刻,正反应速率与逆反应速率___________,此时,反应物的浓度___________,
生成物的浓度也____________。如图所示。
2.化学平衡状态
(1)定义:___________________________________________________________。
(2)特征:
①逆:________________________
②动:________________________
③等:________________________
④定:________________________
⑤变:________________________
(3)特点:化学平衡的建立与建立的途径无关。
【思考】相同条件(温度、浓度、压强等)时,一个反应从正反应开始与从逆反应开始,最终所达
到的平衡状态是否相同?
(4)达到平衡的标志:以mA(g)+nB(g)⇌pC(g)为例
直接标志:①速率关系:正反应速率与逆反应速率相等,即A的消耗速率与A的生成速率相等,A
的消耗速率与C的消耗速率之比等于m∶p,B的生成速率与C的生成速率之比等于n∶p。
②各物质的百分含量保持不变。
间接标志:①混合气体的总压强、总体积、总物质的量不随时间的改变而改变。(注:m+n≠p)
②各物质的浓度不随时间的改变而改变。
③各物质的物质的量不随时间的改变而改变。
③各气体的体积、分压不随时间的改变而改变。
三、对于密闭容器中的可逆反应:mA(g)+nB(g)⇌pC(g)+qD(g),根据对化学平衡的理解,判断下列各情况下,是否达到平衡。
可能的情况举例 是否能判断已达平衡
①各物质的物质的量或物质的量分数一定
1.混合物体系中各 ②各物质的质量或质量分数一定
成分的含量 ③各气体的体积或体积分数一定
④总体积、总压强、总物质的量一定
①单位时间内消耗了mmolA,同时生成mmolA
2.正、逆反应速率
②单位时间内消耗了nmolB,同时消耗了pmolC
的关系 ③v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q
④单位时间内生成nmolB,同时消耗qmolD
①其他条件不变,m+n≠p+q时,总压强一定
3.压强
②其他条件不变,m+n=p+q时,总压强一定
4.平均相对分子质
①当m+n≠p+q时,M一定
量M
②当m+n=p+q时,M一定
5.温度 其他条件一定时,体系温度一定
6.体系密度 其他条件一定时,体系密度一定
7.其他 组成成分有颜色时,体系颜色不再变化
四、化学平衡常数
1.定义:在____下,当一个可逆反应达到______时,生成物____________与反应物____________
的比值是一个常数,这个常数就是该反应的化学平衡常数,简称平衡常数,用符号____表示。
2 . 表 达 式 : 对 于 一 般 的 可 逆 反 应 ,mA(g)+nB(g) pC(g)+qD(g), 在 一 定 温 度 下 ,
K=___________。该式中(1)c(A)、c(B)、c(C)、c(D)是各物质处于____时的浓度;(2)标准平衡常数的
单位为1。
3.书写平衡常数关系式的原则:
请写出下表中各反应的平衡常数表达式并总结规律:
反应 K
1 1/2N (g)+3/2H (g) NH (g)
2 2 3
2 N(g)+3H(g) 2NH (g)
2 2 3
3 2NH (g) N(g)+3H(g)
3 2 2
4 FeO(s)+CO(g) Fe(s)+CO2(g)
5 AgCl(s) Ag+(aq)+Cl-(aq)
6 Cr O2-(aq)+H O CrO2-(aq)+2H+(aq)
2 7 2 4
规律:(1)同一化学反应,可以用不同的化学反应方程式来表示,每个化学方程式都有自己的平衡
常数关系式及相应的平衡常数。
(2)对于同一可逆反应,正反应的平衡常数等于逆反应的平衡常数的倒数,即___________。
(3)化学平衡关系式中只包括____物质和____中各溶质的浓度。4.特点:K只受____影响,与反应物或生成物的____无关。
五、平衡常数K的应用
1.判断反应的热效应:
若正反应是吸热反应,升高温度,K____;
若正反应是放热反应,升高温度,K____。
2.判断某时刻反应进行的方向:
可用该时刻产物浓度幂之积与反应物浓度幂之积的比即浓度商Q与K比较大小来判断。
即Q=K体系处于__________________;
c
QK反应___________________进行。
c
3.判断反应进行的程度:
K值越大,说明平衡体系中生成物所占的比例____,它的正向反应进行的程度____,即该反应进
行得越____,反应物转化率____;反之,就越____,转化率就____。一般地说,____时,该反应进行得就
基本完全了。
【练习】在一定条件下,使NO和O 在一密闭容器中进行反应,下列说法中不正确的是()
2
A.反应开始时,正反应速率最大,逆反应速率为零
B.随着反应的进行,正反应速率逐渐减小,最后为零
C.随着反应的进行,逆反应速率逐渐增大,最后不变
D.随着反应的进行,正反应速率逐渐减小,最后不变
【练习】哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容
器中充入1molN 和3molH ,在一定条件下使该反应发生:N +3H 2NH ,下列有关说法正
2 2 2 2 3
确的是()
A.达到化学平衡时,N 将完全转化为氨
2
B.达到化学平衡时,N、H 和NH 的物质的量浓度一定相等
2 2 3
C.达到化学平衡时,N、H 和NH 的物质的量浓度不再变化
2 2 3
D.达到化学平衡时,正、逆反应速率都为零
【练习】14CO 与碳在高温条件下发生反应:14CO+C 2CO,达到平衡后,平衡混合物中含14C的粒
2 2
子有()
A.14CO B.14CO、14CO
2 2
C.14CO、14CO、14C D.14CO
2
【练习】在密闭容器中进行反应X(g)+Y(g) 2Z(g),已知X、Y、Z的起始浓度分别为
2 2 2 2
0.1mol·L-1、0.2mol·L-1、0.2mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是()A.Z为0.2mol·L-1 B.Y 为0.35mol·L-1
2
C.X 为0.3mol·L-1 D.Z为0.4mol·L-1
2
【练习】在一定温度下,向aL密闭容器中加入1molO 和2molNO,发生如下反应:O (g)+2NO(g)
2 2
2NO (g),此反应不一定达平衡的是()
2
A.容器内压强不随时间变化
B.容器内各物质的浓度不随时间变化
C.容器内O、NO、NO 的浓度之比为1∶2∶2
2 2
D.单位时间内生成1molO ,同时生成2molNO
2 2
【练习】可逆反应N+3H 2NH 的正、逆反应速率可用各反应物或生成物浓度的变化来表示。
2 2 3
下列各关系中能说明反应已达到平衡状态的是()
A.3v (N )=v (H ) B.v (N )=v (NH )
正 2 正 2 正 2 逆 3
C.2v (H )=3v (NH ) D.v (N )=3v (H )
正 2 逆 3 正 2 逆 2
【练习】一定条件下,在体积为1L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g) Z(g),下
列叙述能证明该反应已达到化学平衡状态的是( )
A.X的百分含量不再发生变化
B.c(X)∶c(Y)∶c(Z)=2∶1∶1
C.容器内原子总数不再发生变化
D.同一时间内消耗2nmolX的同时生成nmolZ
【练习】一定条件下,下列反应呈平衡状态时的平衡常数:3H (g)+N(g) 2NH (g)K
2 2 3 1
2NH (g) 3H(g)+N(g)K 则K 与K 的关系为( )
3 2 2 2 1 2
A.K=K B.K=1/K C.K/2=K D.无法确定
1 2 2 1 1 2
【练习】放热反应:CO(g)+HO(g) CO(g)+H(g)在温度t 时达到平衡,
2 2 2 1
c(CO) =c(H O) =1.0mol·L-1,其平衡常数为K。其他条件不变,升高反应体系的温度至t 时,反应物
1 2 1 1 2
的平衡浓度分别为c(CO) 和c(HO) ,平衡常数为K,则( )
2 2 2 2
A.若增大CO浓度,K 和K 都增大 B.K>K
2 1 2 1
C.c(CO) =c(H O) D.c(CO) >c(CO)
2 2 2 1 2
【练习】在一密闭容器中,CO和HO混合加热到800℃达到下列平衡:CO(g)+HO(g)⇌CO(g)
2 2 2
+H (g),K=1.0,若反应开始时CO和HO的浓度分别为0.20mol·L-1和1.00mol·L-1,则CO转化为
2 2
CO 的转化率为( )
2
A.80% B.83% C.75% D.91%【练习】在容积为1L的密闭容器中,加入5molA物质,在一定条件下同时发生下列两个反应:
(1)2A(g) 2B(g)+C(g);(2)A(g) C(g)+D(g)。当达到平衡时,测得c(A)=2.5mol·L-1,
c(C)=2.0mol·L-1。则下列说法中正确的是( )
A.达到平衡时A的总转化率为40% B.达到平衡时c(B)=2c(D)
C.达到平衡时c(B)为1.0mol·L-1 D.达到平衡时c(D)=2c(B)
1.在密闭容器中有如下反应:X (g)+Y (g) 2Z(g)。已知:X 、Y 、Z的起始浓度分别为
2 2 2 2
0.1mol•L﹣1、0.3mol•L﹣1、0.2mol•L﹣1,在一定⇌条件下,当反应达到平衡时,各物质的浓度(单
位mol•L﹣1)可能是( )
A.X 为0.2 B.Y 为0.2 C.Z为0.3 D.Z为0.4
2 2
2.对于工业合成氨反应:N +3H 2NH ,下列说法正确的是( )
2 2 3
A.反应到达平衡时,v(正)=v(逆)=0
B.该反应是可逆反应,N 、H 、NH 一定共存,且浓度之比为1:3:2
2 2 3
C.增大H 的浓度可以增大化学反应速率
2
D.加入足够多的N 可以使H 的转化率达到100%
2 2
3 . 在 373K 时 , 密 闭 容 器 中 充 入 一 定 物 质 的 量 的 NO 和 SO , 发 生 如 下 反 应 :
2 2
NO +SO NO+SO ,达到平衡时,下列叙述正确的是( )
2 2 3
A.SO
2
、⇌NO
2
、NO、SO
3
的物质的量一定相等
B.NO 和 SO 的物质的量一定相等
2 2
C.平衡体系中总物质的量一定等于反应开始时总物质的量
D.NO 和 SO 的物质的量一定相等
3
4.已知:N
2
(g)+3H
2
(g) 2NH
3
△H=﹣92.4kJ•mol﹣1.在恒容密闭容器内,投入2molN
2
和
6molH 发生反应,当反应达⇌到平衡状态时,下列说法不正确的是( )
2
A.其他条件不变,升高温度,平衡被破坏,逆反应速率增大,正反应速率减小
B.一定存在2v(H
2
)
正
=3v(NH
3
)
正
C.若容器内有 1mol NH 生成,则放出热量46.2kJ
3
D.容器内混合气体压强不再发生变化
5.下列关于平衡常数K的说法正确的是( )
A.平衡常数K与反应本身及温度有关
B.改变反应物浓度能改变平衡常数KC.加入催化剂可能会改变平衡常数K
D.K越大,反应物的转化率越小
6.某温度下,反应2A(g)+B(g) 2C(g)的平衡常数K =50,在同一温度下,反应2C(g)
1
2A(g)+B(g)的平衡常数K 为⇌( )
2
⇌A.2500 B.50 C.0.02 D.0.002
7.E和F加入密闭容器中,在一定条件下发生反应:E(s)+4F(g) G(g),已知该反应的平
衡常数值如下表所示.下列说法正确的是( ) ⇌
温度℃ 25 80 230
平衡常数值 5×104 2 1.9×10﹣5
A.上述反应是熵增反应
B.25℃时,反应G(g) E(s)+4F(g)的平衡常数值是0.5
C.在80℃时,测得某时刻⇌,F、G浓度均为0.5 mol•L﹣1,则此时v(正)>v(逆)
D.恒温恒容下,向容器中再充入少量G(g),达新平衡时,G的体积百分含量将增大
8.在2L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g) M(g)+N(s),所
得实验数据如表:下列说法不正确的是( ) ⇌
起始时物质的量/mol 平衡时物质的量/mol
实验编号 温度/℃
n(X) n(Y) n(M) n(N)
800 0.10 0.15 0.05 0.05
① 800 0.20 0.30 a a
② 900 0.10 0.15 0.04 0.04
A.正反应③为放热反应
B.实验 5min达平衡,平均反应速率v(X)=0.005mol/(L•min)
C.实验①中,该反应的平衡常数K=0.1(mol/L)﹣1
D.实验②中,达到平衡时,a大于0.10
9.在一固定②体积的密闭容器中,进行着下列化学反应:CO
2
(g)+H
2
(g) CO(g)+H
2
O
(g),其化学平衡常数K和温度T的关系如下表: ⇌
T(℃) 700 800 830 1000 1200
K 0.6 0.9 1.0 1.7 2.6
则下列有关的叙述正确的是( )
A.该反应为放热反应
B.可测量容器总压变化来判定化学反应是否达到平衡
C.若在某平衡状态时,c(CO )×c(H )=c(CO)×c(H O),此时的温度为830℃
2 2 2D.达平衡时,浓度:c(CO )=c(CO)
2
【知识点填空答案】
各物质的浓度不再改变
【知识点填空答案】
相等;不变;⇌;==;正反应;逆反应;同一条件;正反应方向;逆反应方向;最大;最大;0;
0;逐渐减小;逐渐减小;;逐渐增大;逐渐增大;相等;不变;不变;化学平衡状态是指在一定
条件下的可逆反应里,当正反应速率和逆反应速率相等,反应混合物中各组分的百分含量(浓度、质
量、质量分数、体积分数等)保持不变的状态;可逆反应;动态平衡(正、逆反应仍在进行);v(正)、
v(逆)不为0;v(正)=v(逆);体系中所有反应物和生成物的百分含量(混合物各组分的浓度、质量、质
量分数、体积分数等)保持不变;条件改变,原平衡被破坏,在新的条件下建立新的平衡;相同,因为
化学平衡的建立与反应进行的方向无关,而与反应时的条件有关,只要条件(温度、浓度、压强等)相
同,最终就会达到相同的平衡状态;平衡;平衡;平衡;不一定平衡;平衡;平衡;不一定平衡;
不一定平衡;平衡;;不一定平衡;平衡;不一定平衡;平衡;不一定平衡;平衡
【练习答案】BCCACCABCBC
【检测反馈答案】CCCAACDCC